В реакции каким веществом сера проявляет восстановительные свойства

Сера – элемент VIa группы 3 периода периодической таблицы Д.И. Менделеева. Относится к
группе халькогенов – элементов VIa группы.
Сера – S – простое вещество имеет светло-желтый цвет. Использовалась еще до нашей эры в составе священных курений при
религиозных обрядах.

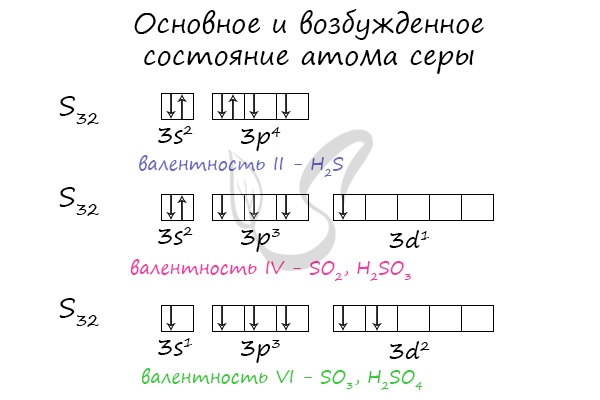
Основное и возбужденное состояние атома серы
Электроны s- и p-подуровня способны распариваться и переходить на d-подуровень. Как и всегда, количество валентных
электронов отражает количество возможных связей у атома.
В разных электронных конфигурациях сера способна принимать валентности: II, IV и VI.
Природные соединения
- FeS2 – пирит, колчедан
- ZnS – цинковая обманка
- PbS – свинцовый блеск (галенит), Sb2S3 – сурьмяный блеск, Bi2S3 – висмутовый блеск
- HgS – киноварь
- CuFeS2 – халькопирит
- Cu2S – халькозин
- CuS – ковеллин
- BaSO4 – барит, тяжелый шпат
- CaSO4 – гипс
В местах вулканической активности встречаются залежи самородной серы.

Получение
В промышленности серу получают из природного газа, который содержит газообразные соединения серы: H2S,
SO2.
H2S + O2 = S + H2O (недостаток кислорода)
SO2 + C = (t) S + CO2
Серу можно получить разложением пирита
FeS2 = (t) FeS + S
В лабораторных условиях серу можно получить слив растворы двух кислот: серной и сероводородной.
H2S + H2SO4 = S + H2O
Химические свойства
- Реакции с неметаллами
- Реакции с металлами
- Реакции с кислотами
- Реакции с щелочами
- Реакции с солями
На воздухе сера окисляется, образуя сернистый газ – SO2. Реагирует со многими неметаллами, без нагревания –
только со фтором.
S + O2 = (t) SO2
S + F2 = SF6
S + Cl2 = (t) SCl2
S + C = (t) CS2

При нагревании сера бурно взаимодействует со многими металлами с образованием сульфидов.
K + S = (t) K2S
Al + S = Al2S3
Fe + S = (t) FeS
При взаимодействии с концентрированными кислотами (при длительном нагревании) сера окисляется до сернистого газа или серной кислоты.
S + H2SO4 = (t) SO2 + H2O
S + HNO3 = (t) H2SO4 + NO2 + H2O
Сера вступает в реакции диспропорционирования с щелочами.
S + KOH = (t) K2S + K2SO3 + H2O
Сера вступает в реакции с солями. Например, в кипящем водном растворе сера может реагировать с сульфитами с образованием тиосульфатов.
Na2SO3 + S → (t) Na2S2O3
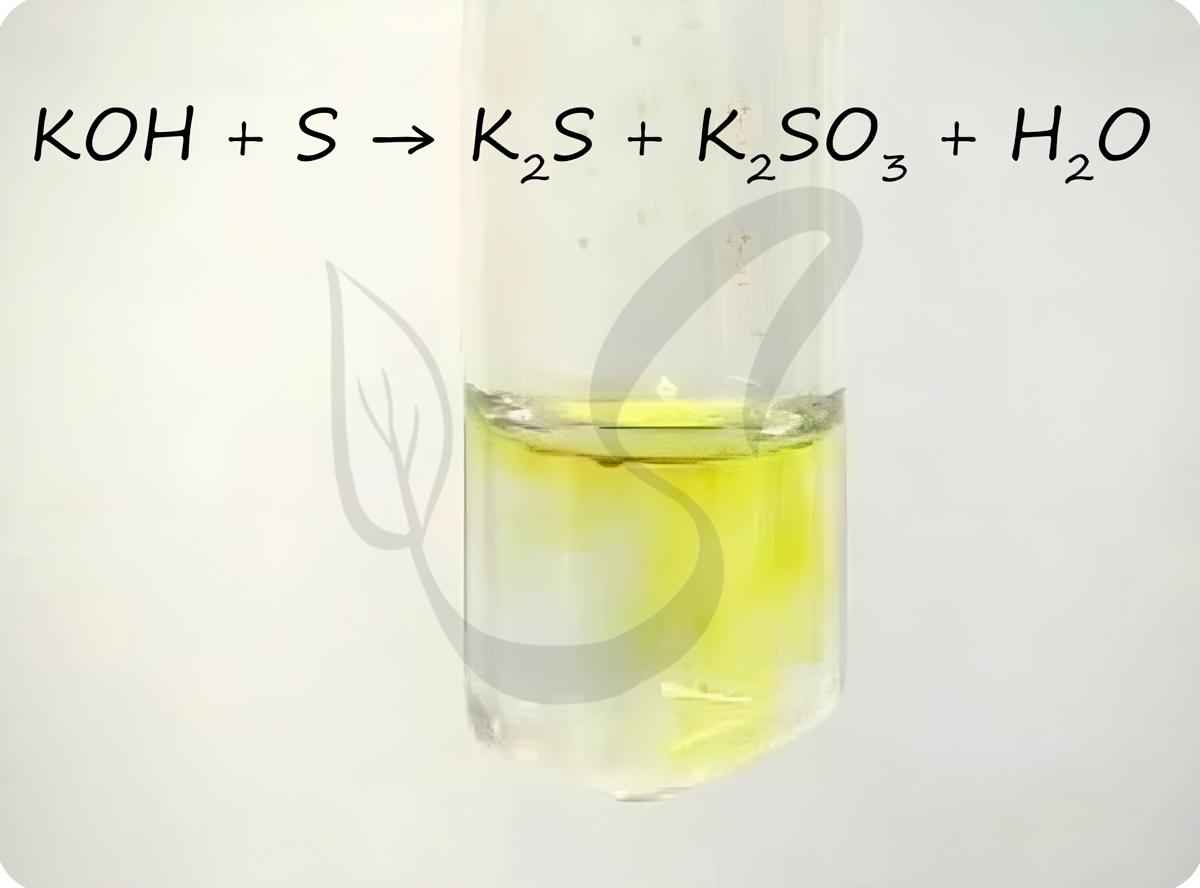
Сероводород – H2S
Бесцветный газ с характерным запахом тухлых яиц. Огнеопасен. Используется в химической промышленности и в лечебных целях (сероводородные
ванны).

Получение
Сероводород получают в результате реакции сульфида алюминия с водой, а также взаимодействия разбавленных кислот с сульфидами.
Al2S3 + H2O = (t) Al(OH)3↓ + H2S↑
FeS + HCl = FeCl2 + H2S↑

Химические свойства
- Кислотные свойства
- Восстановительные свойства
- Качественная реакция
Сероводород плохо диссоциирует в воде, является слабой кислотой. Реагирует с основными оксидами, основаниями с образованием средних и кислых солей (зависит
от соотношения основания и кислоты).
MgO + H2S = (t) MgS + H2O
KOH + H2S = KHS + H2O (гидросульфид калия, избыток кислоты)
2KOH + H2S = K2S + 2H2O
Металлы, стоящие в ряду напряжений до водорода, способны вытеснить водород из кислоты.
Ca + H2S = (t) CaS + H2
Сероводород – сильный восстановитель (сера в минимальной степени окисления S2-). Горит в кислороде синим пламенем, реагирует с кислотами.
H2S + O2 = H2O + S (недостаток кислорода)
H2S + O2 = H2O + SO2 (избыток кислорода)
H2S + HClO3 = H2SO4 + HCl

Качественной реакцией на сероводород является реакция с солями свинца, при котором образуется сульфид свинца.
H2S + Pb(NO3)2 = PbS↓ + HNO3
Оксид серы – SO2
Сернистый газ – SO2 – при нормальных условиях бесцветный газ с характерным резким запахом (запах загорающейся
спички).

Получение
В промышленных условиях сернистый газ получают обжигом пирита.
FeS2 + O2 = (t) FeO + SO2
В лаборатории SO2 получают реакцией сильных кислот на сульфиты. В ходе подобных реакций образуется сернистая кислота,
распадающаяся на сернистый газ и воду.
K2SO3 + H2SO4 = (t) K2SO4 + H2O + SO2↑
Сернистый газ получается также в ходе реакций малоактивных металлов с серной кислотой.
Cu + H2SO4(конц.) = (t) CuSO4 + SO2 + H2O
- Кислотные свойства
- Восстановительные свойства
- Как окислитель
С основными оксидами, основаниями образует соли сернистой кислоты – сульфиты.
K2O + SO2 = K2SO3
NaOH + SO2 = NaHSO3
2NaOH + SO2 = Na2SO3 + H2O

Химически сернистый газ очень активен. Его восстановительные свойства продемонстрированы в реакциях ниже.
Fe2(SO4)3 + SO2 + H2O = FeSO4 + H2SO4
SO2 + O2 = (t, кат. – Pt) SO3
В присутствии сильных восстановителей SO2 способен проявлять окислительные свойства (понижать степень окисления).
CO + SO2 = CO2 + S
H2S + SO2 = S + H2O
Сернистая кислота
Слабая, нестойкая двухосновная кислота. Существует лишь в разбавленных растворах.
Получение
SO2 + H2O ⇄ H2SO3
Химические свойства
- Диссоциация
- Кислотные свойства
- Окислительные свойства
- Восстановительные свойства
Диссоциирует в водном растворе ступенчато.
H2SO3 = H+ + HSO3-
HSO3- = H+ + SO32-
В реакциях с основными оксидами, основаниями образует соли – сульфиты и гидросульфиты.
CaO + H2SO3 = CaSO3 + H2O
H2SO3 + 2KOH = 2H2O + K2SO3 (соотношение кислота – основание, 1:2)
H2SO3 + KOH = H2O + KHSO3 (соотношение кислота – основание, 1:1)
С сильными восстановителями сернистая кислота принимает роль окислителя.
H2SO3 + H2S = S↓ + H 2O
Как и сернистый газ, сернистая кислота и ее соли обладают выраженными восстановительными свойствами.
H2SO3 + Br2 = H2SO4 + HBr

Оксид серы VI – SO3
Является высшим оксидом серы. Бесцветная летучая жидкость с удушающим запахом. Ядовит.
Получение
В промышленности данный оксид получают, окисляя SO2 кислородом при нагревании и присутствии катализатора
(оксид ванадия – Pr, V2O5).
SO2 + O2 = (кат) SO3
В лабораторных условиях разложением солей серной кислоты – сульфатов.
Fe2(SO4)3 = (t) SO3 + Fe2O3
Химические свойства
- Кислотные свойства
- Окислительные свойства
Является кислотным оксидом, соответствует серной кислоте. При реакции с основными оксидами и основаниями образует ее соли – сульфаты и
гидросульфаты. Реагирует с водой с образованием серной кислоты.
SO3 + 2KOH = K2SO4 + 2H2O (основание в избытке – средняя соль)
SO3 + KOH = KHSO4 + H2O (кислотный оксид в избытке – кислая соль)
SO3 + Ca(OH)2 = CaSO4 + H2O

SO3 + Li2O = Li2SO4
SO3 + H2O = H2SO4
SO3 – сильный окислитель. Чаще всего восстанавливается до SO2.
SO3 + P = SO2 + P2O5
SO3 + H2S = SO2 + H2O
SO3 + KI = SO2 + I2 + K2SO4

© Беллевич Юрий Сергеевич 2018-2020
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение
(в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов
без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования,
обратитесь, пожалуйста, к Беллевичу Юрию.
Источник
Сера,
её физические и химические свойства. Биологическое значение серы, её применение
(демеркуризация).СЕРА S
Cера в природе
Самородная сера
Сульфиды
PbS – свинцовый блеск
Cu2S – медный блеск
ZnS – цинковая обманка
FeS2 – пирит, серный колчедан, кошачье золото
H2S – сероводород (в минеральных источниках и природном газе)
Белки
Сульфаты
CaSO4 * 2H2O – гипс
MgSO4 * 7H2O – горькая соль (английская)
Na2SO4 *10H2O – глауберова соль (мирабилит)
Физические свойства
Твердое кристаллическое вещество желтого цвета, нерастворима в воде, водой не смачивается (плавает на поверхности), t°кип = 445°С.
Одно из особенных физических свойств серы – флотация, способность мелкого порошка серы всплывать, тогда, как ее крупные кристаллы тонут в воде. Дело в том, что сера не смачивается водой, и ее частички держатся на поверхности воды за счет прилипших к ним мелких пузырьков воздуха. Это свойство используют при отделении самородной серы от примесей. Руду размалывают, заливают водой, а снизу продувают воздухом, сера всплывает, а примеси остаются на дне.
Аллотропия
Для серы характерны несколько аллотропных модификаций, но наиболее известные видоизменения: ромбическая (кристаллическая), моноклинная (игольчатая) и пластическая.
Ромбическая (a – сера) – S8
t°пл. = 113°C; ρ = 2,07 г/см3. Наиболее устойчивая модификация.
Моноклинная (b – сера) – S8
темно-желтые иглы, t°пл. = 119°C; ρ = 1,96 г/см3. Устойчивая при температуре более 96°С; при обычных условиях превращается в ромбическую.
Пластическая Sn
коричневая резиноподобная (аморфная) масса. Неустойчива, при затвердевании превращается в ромбическую.
ПОЛУЧЕНИЕ ПЛАСТИЧЕСКОЙ СЕРЫ
Взаимопревращение аллотропных модификаций серы
Строение атома серы
Размещение электронов по уровням и подуровням
Основное состояние
1s22s22p63s23p4
Размещение электронов по
орбиталям (последний слой)Степень
окисленияВалентность
-2
В основном состоянии
II
+4
Первое возбуждённое состояние
IV
+6
Второе возбуждённое состояние
VI
Получение серы
1. Промышленный метод – выплавление из руды с помощью водяного пара.
2. Неполное окисление сероводорода (при недостатке кислорода).
2H2S + O2 = 2S + 2H2O
3. Реакция Вакенродера
2H2S + SO2 = 3S + 2H2O
Химические свойства серы
Сера – окислитель S0 + 2ē→ S-2 | Сера – восстановитель: S – 4ē → S+4; S – 6ē →S+6 |
1. Взаимодействие серы со всеми щелочными и щелочноземельными металлами, медью, ртутью, серебром без нагревания: 2Na + S → Na2S ОПЫТ S + Hg = HgS Ртуть обладает высокой летучестью. Её пары ядовиты. Эта реакция лежит в основе удаления и обезвреживания ртути, например из разбитого медицинского термометра. Места, из которых нельзя извлечь капельки ртути, засыпают порошком серы. Сера и ртуть вступают в реакцию при соприкосновении. В результате образуется химически инертное и безвредное вещество. Этот процесс называется демеркуризацией 2. Взаимодействие серы c остальными металлами (кроме Au,Pt) при повышенной t°: 2Al + 3S t→ Al2S3 Zn + S t°→ ZnS ОПЫТ Cu + S t→ CuS ОПЫТ 3.Взаимодействие серы с некоторыми неметаллами с образованием бинарных соединений: H2 + S → H2S 2P + 3S→ P2S3 C + 2S → CS2 | 1. Взаимодействие серы c кислородом: S + O2 t°→ S+4O2 2S + 3O2 t°;pt→ 2S+6O3 2. Взаимодействие серы c галогенами (кроме йода): S + Cl2 → S+2Cl2 **Взаимодействие серы с кислотами – окислителями: S + 2H2SO4(конц) → 3S+4O2 + 2H2O S + 6HNO3(конц) → H2S+6O4 + 6NO2 + 2H2O **Реакции диспропорционирования: 4. 3S0 + 6KOH→ K2S+4O3 + 2K2S-2 + 3H2O |
Тренажёр №1 – Характеристика серы по её положению в периодической системе Д. И. Менделеева
Тренажёр №2 – Химические свойства серы
Тренажёр №3 – Взаимодействие серы с металлами
Применение
Вулканизация каучука, получение эбонита, производство спичек, пороха, в борьбе с вредителями сельского хозяйства, для медицинских целей (серные мази для лечения кожных заболеваний), для получения серной кислоты и т.д.
Применение серы и её соединений
Домашнее задание параграф 21; упражнения 1, 3, 4 стр. 99-100.
Дополнительные зхадания
Закончите уравнения реакций, расставьте коэффициенты методом электронного баланса, укажите окислитель, восстановитель.
- S + O2
- S + Na
- S + H2
№2. Осуществите превращения по схеме:
Это интересно…
- Содержание серы в организме человека массой 70 кг – 140 г.
- В сутки человеку необходимо 1 г серы.
- Серой богаты горох, фасоль, овсяные хлопья, пшеница, мясо, рыба, плоды и сок манго.
- Сера входит в состав гормонов, витаминов, белков, она есть в хрящевой ткани, в волосах, ногтях. При недостатке серы в организме наблюдается хрупкость ногтей и костей, выпадение волос.
Следите за своим здоровьем!
Знаете ли вы..
- Соединения серы могут служить лекарственными препаратами;
- Сера – основа мази для лечения грибковых заболеваний кожи, для борьбы с чесоткой. Тиосульфат натрия Na2S2O3 используется для борьбы с нею.
- Многие соли серной кислоты содержат кристаллизационную воду: ZnSO4×7H2O и CuSO4×5H2O. Их применяют как антисептические средства для опрыскивания растений и протравливания зерна в борьбе с вредителями сельского хозяйства.
- Железный купорос FeSO4×7H2O используют при анемии.
- BaSO4 применяют при рентгенографическом исследовании желудка и кишечника.
- Алюмокалиевые квасцы KAI(SO4)2×12H2O – кровоостанавливающее средство при порезах.
- Минерал Na2SO4×10H2O носит название «глауберова соль» в честь открывшего его в VIII веке немецкого химика Глаубера И.Р.Глаубер во время своего путешествия внезапно заболел. Он ничего не мог есть, желудок отказывался принимать пищу. Один из местных жителей направил его к источнику. Как только он выпил горькую соленую воду, сразу стал есть. Глаубер исследовал эту воду, из нее выкристаллизовалась соль Na2SO4×10H2O. Сейчас ее применяют как слабительное в медицине, при окраске хлопчато- бумажных тканей. Соль также находит применение в производстве стекла.
- Тысячелистник обладает повышенной способностью извлекать из почвы серу и стимулировать поглощение этого элемента с соседними растениями.
- Чеснок выделяет вещество – альбуцид, едкое соединение серы. Это вещество предотвращает раковые заболевания, замедляет старение, предупреждает сердечные заболевания.
Источник
Сера
Элемент сера 16S, как и кислород 8О, находится в главной подгруппе VI группы периодической системы элементов. Однако химия серы существенно отличается от химии кислорода. Это обусловлено следующими причинами:
1. В отличие от кислорода сера проявляет и окислительные, и восстановительные свойства.
2. В отличие от кислорода, имеющего постоянную валентность II и степень окисления в соединениях -2, сера – элемент с переменной валентностью и с переменной степенью окисления.
Характеристика элемента
16S1s22s22p63s23p4
Аr = 32,066
ЭО – 2,5
Изотопы: 32S (95,084 %); 34S (4,16 %); 33S и 36S (
Кларк в земной коре 0,05 % по массе. Формы нахождения:
1) самородная сера (свободная S);
2) S2- (H2S и сульфиды металлов);
3) S+6 (сульфаты Ва и Са);
4) в составе белков, витаминов.
Сера – типичный неметалл, р-элемент. Устойчивые С.О. в соединениях -2, +4, +6.
Отличительное свойство – способность образовывать прочные гомоатомные связи-S-S-S- что приводит к существованию линейных и циклических цепей.
Важнейшие S-содержащие вещества
S-2 | S0 | S+4 | S+6 |
восстановители | окислительно – восстановительная двойственность | окислители | |
H2S сероводород CS2 – сероуглерод | S, свободная сера, большое число аллотропов | SO2 сернистый ангидрид | SO3 |
Свободная сера
Аллотропные модификации серы: ромбическая – S8. Твердое кристаллическое вещество ли монно-желтого цвета; нерастворимо в воде, хорошо растворимо в сероуглероде, ацетоне, бензоле.
Моноклинная – S8. Существует при температуре около 950С. Отличается от ромбической взаимной ориентацией октаэдров в кристаллической решетке.
Пластическая. Длинные зигзагообразные цепи.
Получение серы
1. Извлечение самородной серы из ее месторождений
2. Переработка природных газов, содержащих H2S (окисление при недостатке О2).
3. В лаборатории серу получают взаимодействием SО2 и H2S в водном растворе:
SО2 + 2H2S = 3S↓ + 2H2О
Химические свойства серы
При обычной температуре твердофазная сера малореакционноспособна. Однако при нагревании, и особенно в расплавленном состоянии, сера ведет себя как очень химически активное вещество
Сера – окислитель:
S + 2e- = S2-
Для завершения октета на внешнем слое атомы серы принимают недостающие 2 электрона и в состоянии S2- образуют ионные и ковалентные связи с водородом, металлами и некоторыми неметаллами.
1) Сера непосредственно соединяется с большинством Me (кроме Pt, Au), образуя сульфиды. С некоторыми Me реакция протекает при обычной температуре, например:
S + Сu = CuS
S + 2Ag = Ag2S
S + Hg = HgS
С железом и многими другими Me сера реагирует при нагревании:
S + Fe = FeS
S + Н2 = H2S сероводород
2S + С = CS2 сероуглерод
3S + 2Р = P2S3 сульфид фосфора (III)
Сера – восстановитель:
S – 4e- = S+4; S – 6e- = S+6
В соединениях с более ЭО элементами атомы серы находятся в положительно заряженном состоянии.
Непосредственно сера не взаимодействует с азотом и йодом.
Практически важными являются реакции соединения серы с кислородом. При обычных условиях сера горит на воздухе, окисляясь кислородом до диоксида серы:
S + O2 = SO2
Высший оксид SO3 образуется при окислении серы или SO2 кислородом в присутствии катализаторов:
2S + 3O2 = 2SO3 триоксид серы (оксид серы (VI)).
Сера непосредственно соединяется с фтором (при обычной температуре) и с хлором (расплавленная сера):
S + 3F2 = SF6 гексафторид серы
2S + Cl2 = S2CI2 дитиодихлорид серы
S2Cl2 + Cl2 = 2SCI2 дихлорид серы
Сильные окислители (HNO3, H2SO4 конц., К2Сr2O7 и др.) окисляют свободную серу до SO2 или H2SO4:
S + 2HNO3(разб.) = H2SO4 + 2NO↑
S + 6HNO3(конц.) = H2SO4 + 6NO2↑ + 2Н2O
S + 2H2SO4(конц.) = 3SO2↑ + 2Н2O
S + К2Сr2O7 = Сr2O3 + K2SO4
Диспропорционирование серы в растворах щелочей
3S+ 6NaOH = 2Na2S + Na2SO3 + 3Н2O
Источник
2. Химические свойства соединений серы с точки зрения изменения степеней окисления
В данном разделе реакции выходят за рамки ЕГЭ, но также являются полезными.
Правило 2.1. Соединения S+4 преимущественно проявляют восстановительные свойства при взаимодействии с большинством окислителей, т.е. довольно легко окисляются до S+6 :
С такими окислителями как кислород, пероксид водорода и оксиды азота:
2SO2 + O2 → 2SO3 (t, kt = V2O5)
SO2 + H2O2 → H2SO4
С солями Fe+3 и Cu+2:
SO2 + 2FeCl3 + 2H2O → 2FeCl2 + H2SO4 + 2HCl
SO2 + 2CuCl2 + 2H2O → 2CuCl + H2SO4+ 2HCl
С растворами галогенов (кроме F2):
SO2 + Cl2 + H2O → H2SO4 + 2HCl
SO2 + Br2 + H2O → H2SO4 + 2HBr
SO2 + I2 + H2O → H2SO4 + 2HI
С раствором перманганата калия в различных средах:
5SO2 + 2KMnO4 +2H2O → 2MnSO4 + K2SO4 + 2H2SO4
SO2 + 2KMnO4 + 4KOH → 2K2MnO4 +K2SO4 + 2H2O
Примеры реакций окисления сульфита натрия до сульфата различными окислителями:
Na2SO3 + Cl2 + H2O → Na2SO4 + 2HCl
Na2SO3 + H2O2 → Na2SO4 + H2O
Na2SO3 + H2SO4(к) → Na2SO4 + SO2 + H2O
5Na2SO3 + 2KMnO4 + 3H2SO4 → 5Na2SO4 + 2MnSO4 + K2SO4 + 3H2O
3Na2SO3 + 2KMnO4 + H2O → 2Na2SO4 + 2MnO2 + 2KOH
Na2SO3 + 2KMnO4 + 2KOH → Na2SO4 + 2K2MnO4 + H2O
3Na2SO3 + K2Cr2O7 + 4H2SO4 → 3Na2SO4 + Cr2(SO4)3 + K2SO4 + 4H2O
3Na2SO3 + K2Cr2O7 + 4H2O → 3Na2SO4 + 2Cr(OH)3 + 2KOH
Только очень сильными восстановителями S+4 восстанавливается до S0:
SO2 + 2H2S → 3S + 2H2O
SO2 + 2C → S + 2CO2
SO2 + 4HI → S + 2I2 + 2H2O
SO2 + 2CO → S + 2CO2 (Al2O3, 500°C)
Серная кислота (конц.)
Правило 2.2.
- При взаимодействии H2SO4(к) со слабыми восстановителями (неметаллами: S, P, C, средне- и малоактивными металлами: Fe, Cu, Ag, сложными веществами: H2S, сульфидами металлов, солями Fe2+ и т.д.) образуются SO2 и H2O.
- При взаимодействии H2SO4(к) с сильными восстановителями (активными металлами: Li-Zn, некоторыми сложными веществами: HI, KI) образуются H2S или S.
4Zn + 5H2SO4(конц.) → 4ZnSO4 + H2S + 4H2O (возможно образование SO2 и S, так как Zn – хороший восстановитель)
+ 4H2O (возможно образование SO2 и S, так как Zn – хороший восстановитель)
2Fe + 6H2SO4(конц.) → Fe2(SO4)3 + 3SO2 + 6H2O (только при нагревании)
+ 6H2O (только при нагревании)
Al, Cr, Fe пассивируются холодной концентрированной серной кислотой (т.е. покрываются оксидной пленкой, препятствующей дальнейшей реакции). Реакции идут только при нагревании.
C + H2SO4(конц.) → CO2 + 2SO2 + 2H2O (t)
+ 2H2O (t)
S + H2SO4(конц.) → 3SO2 + 2H2O (t)
+ 2H2O (t)
2P + 5H2SO4(конц.) → 2H3PO4 + 5SO2 + 2H2O (t)
+ 2H2O (t)
Из галогеноводородов концентрированная серная кислота может окислить только ионы Br– и I– :
HF + H2SO4(конц.) → реакция не идет
HCl + H2SO4(конц.) → реакция не идет
2HBr + H2SO4(конц.) → Br2 + SO2 + 2H2O
+ 2H2O
8HI + H2SO4(конц.) → 4I2 + H2S + 4H2O
+ 4H2O
2CuI + 4H2SO4(конц.) → 2CuSO4 + I2 + 2SO2 + 4H2O
+ 4H2O
2CrCl2 + 4H2SO4(конц.) → Cr2(SO4)3 + SO2 + 4HCl + 2H2O
+ 4HCl + 2H2O
Соли меди восстанавливают кислоту до SO2, тогда как соли активных металлов до H2S:
2CuI + 4H2SO4(конц.) → 2CuSO4 + I2 + 2SO2 + 4H2O
+ 4H2O
8KI + 5H2SO4(конц.) → 4K2SO4 + 4I2 + H2S + 4H2O
+ 4H2O
Примеры реакций с солями (окисляем анион):
4H2SO4(конц., гор.) + CuS → CuSO4 + 4SO2 + 4H2O
+ 4H2O
Примеры реакций с солями (окисляем катион):
2H2SO4(к) + 2FeSO4 → Fe2(SO4)3 + SO2 + 2H2O
+ 2H2O
4H2SO4 + 2CrCl2 → Cr2(SO4)3 + SO2 + 4HCl + 2H2O
+ 4HCl + 2H2O
Правило 2.3. Окисление соединений S–2 до S+6 происходит под действием следующих окислителей: H2O2, Cl2(водн.), HNO3(конц.):
H2S + Cl2 + 4H2O → H2SO4 + 8HCl
PbS + 4H2O2 → PbSO4 + 4H2O (черный сульфид свинца превращается в белый сульфат)
H2S + 8HNO3(конц.) → H2SO4 + 8NO2 + 4H2O (образование S будет считаться ошибкой!)
+ 4H2O (образование S будет считаться ошибкой!)
CuS + 8HNO3(конц., гор.) → CuSO4 + 8NO2 + 4H2O
Na2S + 8HNO3(конц, гор.) → Na2SO4 + 8NO2 + 4H2O
С H2SO4(к) при нагревании сероводород и сульфиды реагируют с образованием SO2, аналогично реакции кислоты с серой:
S + H2SO4(конц.) → 3SO2 + 2H2O (t)
+ 2H2O (t)
H2S + 3H2SO4(конц.) → 4SO2 + 4H2O (t)
+ 4H2O (t)
CuS + 4H2SO4(конц., гор.) → CuSO4 + 4SO2 + 4H2O
+ 4H2O
K2S + 4H2SO4(конц.) → K2SO4 + 4SO2 + 4H2O
+ 4H2O
В этой реакции сульфид-ион окисляется до SO2: S–2 -6e → S+4.
Часть сульфат-ионов восстанавливается также до SO2 и часть остается для образования соли K2SO4.
Без нагревания возможна реакция:
K2S + 2H2SO4 → S + SO2
+ SO2 + K2SO4 + 2H2O
+ K2SO4 + 2H2O
Источник: лекция на youtube.com от разработчиков экзамена “Методические рекомендации по подготовке ЕГЭ по химии”, время 49:52.
Правило 2.4. Сера в степени окисления -2 может быть окислена до простого вещества галогенами (Cl2, Br2, I2) или солями Fe+3, Mn+7 и Cr+6 :
1. Реакции с Cl2, Br2 и I2:
H2S + Cl2 (газ) → S + 2HCl
H2S + Br2 → S + 2HBr
H2S + I2 → S + 2HI
2. Реакции с солями Fe+3, Mn+7 и Cr+6:
3H2S + 2FeCl3 → S + 2FeCl2 + 2HCl
5H2S + 2KMnO4 + 3H2SO4 → 5S + 2MnSO4 + K2SO4 + 8H2O
3H2S + 2KMnO4 → 3S + 2MnO2 + 2KOH + 2H2O
3H2S + 2KMnO4 + 2CO2 → 3S + 2MnO2 + 2KHCO3 + 2H2O
3H2S + K2Cr2O7 + 4H2SO4 → 3S + Cr2(SO4)3 + K2SO4 + 7H2O
3H2S + 2K2CrO4 + 2H2O → 3S + 2Cr(OH)3 + 4KOH
3H2S + 2HMnO → 3S + 2MnO2+ 4H2O
3K2S + 2KMnO4 + 4H2O → 3S + 2MnO2 + 8KOH
3H2S + Na2Cr2O7 + 4H2SO4 → 3S + Cr2(SO4)3 + Na2SO4 + 7H2O
3Na2S + K2Cr2O7 + 7H2SO4 → 3S + Cr2(SO4)3 + K2SO4 + 3Na2SO4 + 7H2O
3(NH4)2S + K2Cr2O7 + 7H2SO4 → 3S + Cr2(SO4)3 + K2SO4 + 3(NH4)2SO4 + 7H2O.
Согласно разработчикам экзамена (Вебинар “Методические рекомендации по подготовке к ЕГЭ по химии от разработчиков“, время 33:41, ссылка естьв разделе “О проекте”), окисление сульфид-ионов протекает с образованием S0, но образование сульфат-иона (в реакциях с такими сильными окислителями, как KMnO4, K2Cr2O7) также будет засчитано как правильный ответ.
Источник
