В каких соединениях содержится азот

Азот – неметаллический элемент Va группы периодической таблицы Д.И. Менделеева. Составляет 78% воздуха. Входит в состав
белков, являющихся важной частью живых организмов.
Температура кипения азота составляет -195,8 °C. Однако быстрого замораживания объектов, которое часто демонстрируют в
кинофильмах, не происходит. Даже для заморозки растения нужно продолжительное время, это связано с низкой теплоемкостью
азота.
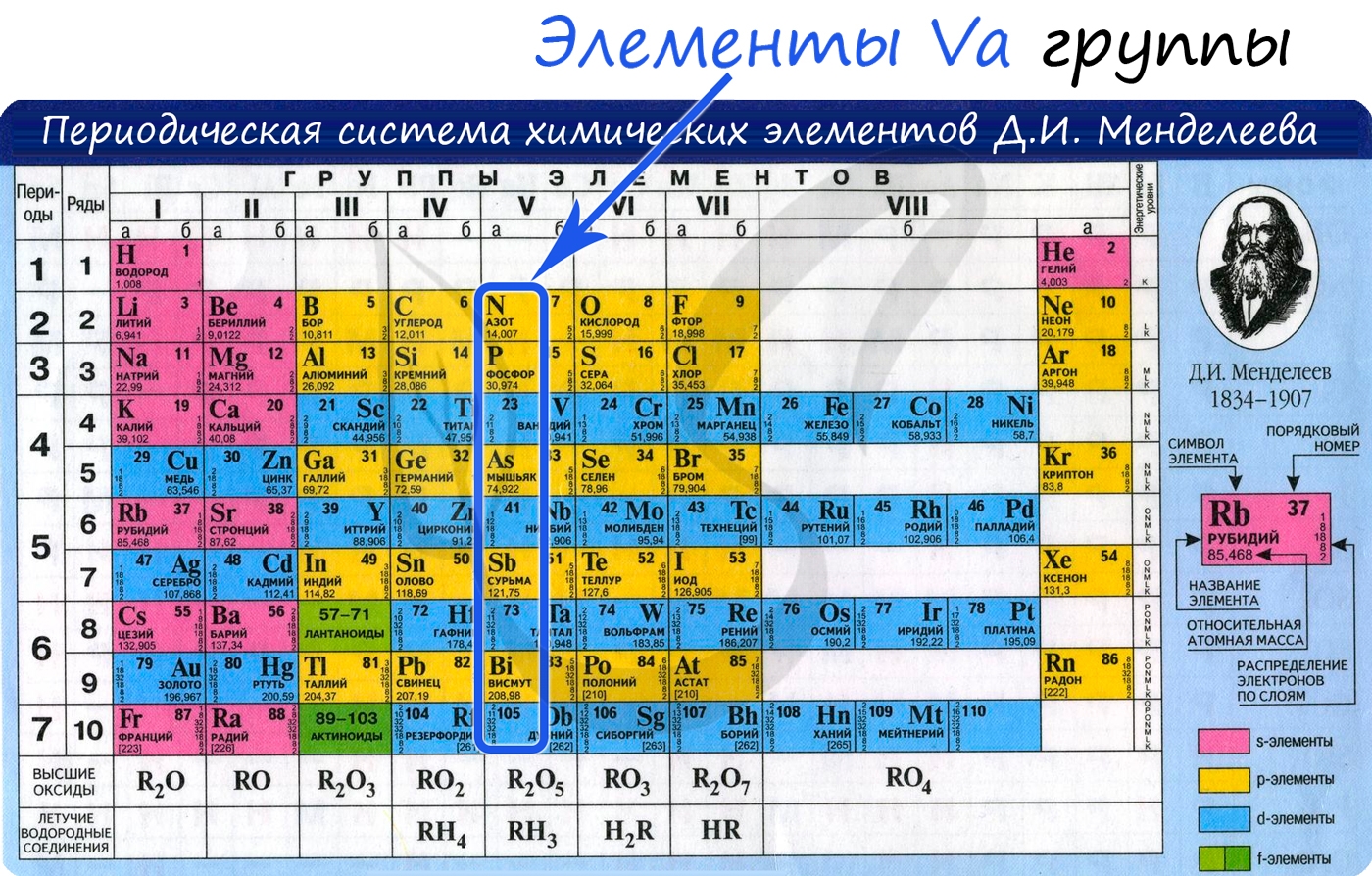
Общая характеристика элементов Va группы
От N к Bi (сверху вниз в периодической таблице) происходит увеличение: атомного радиуса, металлических, основных, восстановительных свойств.
Уменьшается электроотрицательность, энергия ионизация, сродство к электрону.
Азот, фосфор и мышьяк являются неметаллами, сурьма – полуметалл, висмут – металл.
Электронные конфигурации у данных элементов схожи, так как они находятся в одной группе (главной подгруппе!), общая формула ns2np3:
- N – 2s22p3
- P – 3s23p3
- As – 4s24p3
- Sb – 5s25p3
- Bi – 6s26p3
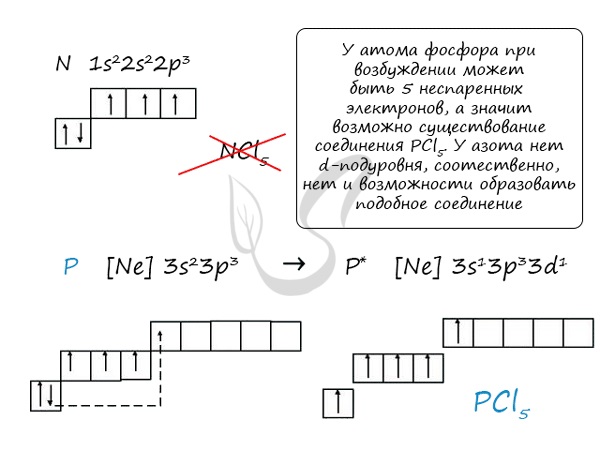
Основное и возбужденное состояние азота
При возбуждении атома азота электроны на s-подуровне распариваются и переходят на p-подуровень. Поскольку азот находится во втором периоде, то
3ий уровень у него отсутствует, что проявляется в особенностях электронной конфигурации возбужденного состояния.
Сравнивая возможности перемещения электронов у азота и фосфора, разница становится очевидна.
Природные соединения
В природе азот встречается в виде следующих соединений:
- Воздух – во вдыхаемом нами воздухе содержится 78% азота
- Азот входит в состав нуклеиновых кислот, белков
- KNO3 – индийская селитра, калиевая селитра
- NaNO3 – чилийская селитра, натриевая селитра
- NH4NO3 – аммиачная селитра (искусственный продукт, в природе не встречается)
Селитры являются распространенными азотными удобрениями, которые обеспечивают быстрый рост и развитие растений, повышают урожайность. Однако,
следует строго соблюдать правила их применения, чтобы не превысить допустимые концентрации.

Получение
В промышленности азот получают путем сжижения воздуха. В дальнейшем путем испарения их сжиженного воздуха получают азот.
Применяют и метод мембранного разделения, при котором через специальный фильтр из сжатого воздуха удаляют кислород.
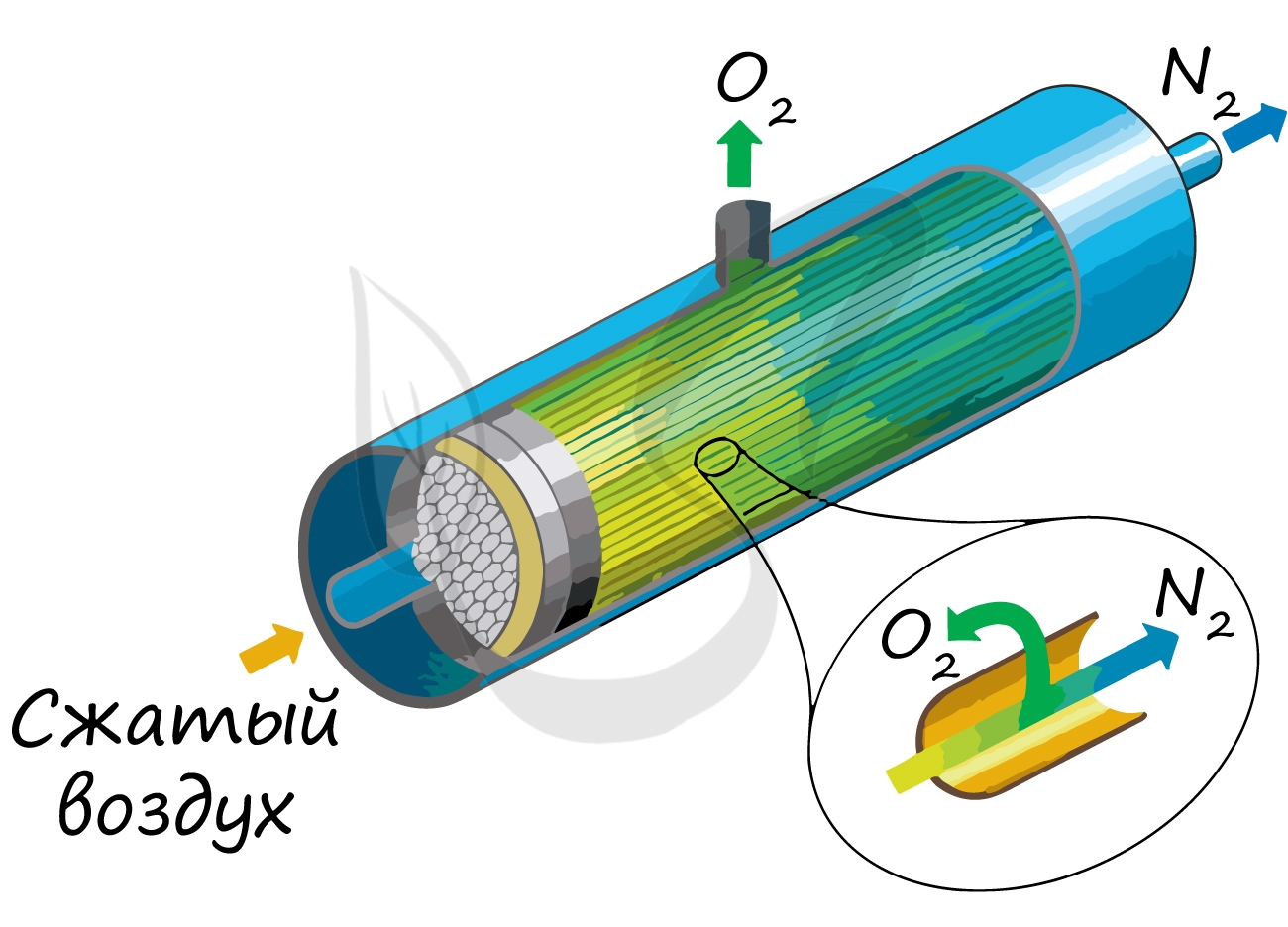
В лаборатории методы не столь экзотичны. Чаще всего получают азот разложением нитрита аммония
NH4NO2 → (t) N2 + H2O
Также азот можно получить путем восстановления азотной кислоты активными металлами.
HNO3(разб.) + Zn → Zn(NO3)2 + N2 + H2O

Химические свойства
Азот восхищает – он принимает все возможные для себя степени окисления от -3 до +5.

Молекула азота отличается большой прочностью из-за наличия тройной связи. Вследствие этого многие реакции эндотермичны: даже горение
азота в кислороде сопровождается поглощением тепла, а не выделением, как обычно бывает при горении.

- Реакция с металлами
- Реакция с неметаллами
Без нагревания азот взаимодействует только с литием. При нагревании реагирует и с другими металлами.
N2 + Li → Li3N (нитрид лития)
N2 + Mg → (t) Mg3N2
N2 + Al → (t) AlN
Важное практическое значение имеет синтез аммиака, который применяется в дальнейшим при изготовлении удобрений, красителей, лекарств.
N2 + H2 ⇄ (t, p) NH3
Аммиак
Бесцветный газ с резким едким запахом, раздражающим слизистые оболочки. Раствор концентрацией 10% аммиака применяется в медицинских целях,
называется нашатырным спиртом.
Получение
В промышленности аммиак получают прямым взаимодействием азота и водорода.
N2 + H2 ⇄ (t, p) NH3
В лабораторных условиях сильными щелочами действуют на соли аммония.
NH4Cl + NaOH → NH3 + NaCl + H2O
Химические свойства
Аммиак проявляет основные свойства, окрашивает лакмусовую бумажку в синий цвет.
- Реакция с водой
- Основные свойства
- Восстановительные свойства
Образует нестойкое соединение – гидроксид аммония, слабое основание. Оно сразу же распадается на воду и аммиак.
NH3 + H2O ⇄ NH4OH
Как основание аммиак способен реагировать с кислотами с образованием солей.
NH3 + HCl → NH4Cl (хлорид аммония)
NH3 + HNO3 → NH4NO3 (нитрат аммония)

Поскольку азот в аммиаке находится в минимальной степени окисления -3 и способен только ее повышать, то аммиак проявляет выраженные
восстановительные свойства. Его используют для восстановления металлов из их оксидов.
NH3 + FeO → N2↑ + Fe + H2O
NH3 + CuO → N2↑ + Cu + H2O
Горение аммиака без катализатора приводит к образованию азота в молекулярном виде. Окисление в присутствии катализатора сопровождается
выделением NO.
NH3 + O2 → (t) N2 + H2O
NH3 + O2 → (t, кат) NO + H2O

Соли аммония
Получение
NH3 + H2SO4 → NH4HSO4 (гидросульфат аммония, избыток кислоты)
3NH3 + H3PO4 → (NH4)3PO4
Химические свойства
Помните, что по правилам общей химии, если по итогам реакции выпадает осадок, выделяется газ или образуется вода – реакция идет.
- Реакции с кислотами
- Реакции с щелочами
- Реакции с солями
- Реакция гидролиза
- Реакции разложения
NH4Cl + H2SO4 → (NH4)2SO4 + HCl↑
В реакциях с щелочами образуется гидроксид аммония – NH4OH. Нестойкое основание, которое легко распадается на воду и аммиак.
NH4Cl + KOH → KCl + NH3 + H2O
(NH4)2SO4 + BaCl2 = BaSO4↓ + NH4Cl
В воде ион аммония подвергается гидролизу с образованием нестойкого гидроксида аммония.
NH4+ + H2O ⇄ NH4OH + H+
NH4OH ⇄ NH3 + H2O
NH4Cl → (t) NH3↑ + HCl↑
(NH4)2CO3 → (t) NH3↑ + H2O + CO2↑
NH4NO2 → (t) N2↑ + H2O
NH4NO3 → (t) N2O↑ + H2O
(NH4)3PO4 → (t) NH3↑ + H3PO4

Оксид азота I – N2O
Закись азота, веселящий газ – N2O – обладает опьяняющим эффектом. Несолеобразующий оксид. При н.у. является бесцветным газом с приятным
сладковатым запахом и привкусом. В медицине применяется в больших концентрациях для ингаляционного наркоза.

Получают N2O разложением нитрата аммония при нагревании:
NH4NO3 → N2O + H2O
Оксид азота I разлагается на азот и кислород:
N2O → (t) N2 + O2
Оксид азота II – NO
Окись азота – NO. Несолеобразующий оксид. При н.у. бесцветный газ, на воздухе быстро окисляется до оксида азота IV.
Получение
В промышленных масштабах оксид азота II получают при каталитическом окислении аммиака.
NH3 + O2 → (t, кат) NO + H2O
В лабораторных условиях – в ходе реакции малоактивных металлов с разбавленной азотной кислотой.
Cu + HNO3(разб.) → Cu(NO3)2 + NO + H2O
Химические свойства
На воздухе быстро окисляется с образованием бурого газа – оксида азота IV – NO2.
NO + O2 → NO2

Оксид азота III – N2O3
При н.у. жидкость синего цвета, в газообразной форме бесцветен. Высокотоксичный, приводит к тяжелым ожогам кожи.

Получение
Получают N2O3 в две стадии: сначала реакцией оксида мышьяка III с азотной кислотой, затем
охлаждением полученной смеси газов до температуры – 36 °C.
As2O3 + HNO3 → H3AsO4 + NO↑ + NO2↑
При охлаждении газов образуется оксид азота III.
NO + NO2 → N2O3
Химические свойства
Является кислотным оксидом. соответствует азотистой кислота – HNO2, соли которой называются нитриты (NO2-).
Реагирует с водой, основаниями.
H2O + N2O3 → HNO2
NaOH + N2O3 → NaNO2 + H2O
Оксид азота IV – NO2
Бурый газ, имеет острый запах. Ядовит.

Получение
В лабораторных условиях данный оксид получают в ходе реакции меди с концентрированной азотной кислотой. Также NO2 выделяется при
разложении нитратов.
Cu + HNO3(конц) → Cu(NO3)2 + NO2 + H2O

Cu(NO3)2 → (t) CuO + NO2 + O2
Pb(NO3)2 → (t) PbO + NO2 + O2
Химические свойства
Проявляет высокую химическую активность, кислотный оксид.
- Окислительные свойства
- Реакции с водой и щелочами
Как окислитель NO2 ведет себя в реакциях с фосфором, углеродом и серой, которые сгорают в нем.
NO2 + C → CO2 + N2
NO2 + P → P2O5 + N2
Окисляет SO2 в SO3 – на этой реакции основана одна из стадий получения серной кислоты.
SO2 + NO2 → SO3 + NO
Оксид азота IV соответствует сразу двум кислотам – азотистой HNO2 и азотной HNO3. Реакции с
водой и щелочами протекают по одной схеме.
NO2 + H2O → HNO3 + HNO2
NO2 + LiOH → LiNO3 + LiNO2 + H2O
Если растворение в воде оксида проводить в избытке кислорода, образуется азотная кислота.
NO2 + H2O + O2 → HNO3

© Беллевич Юрий Сергеевич 2018-2020
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение
(в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов
без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования,
обратитесь, пожалуйста, к Беллевичу Юрию.
Источник

Один из важнейших макроэлементов. Без его участия невозможно развитие растений. Он отвечает за обмен веществ. При этом находится в составе всех белков, цитоплазмы, ядер клеток, аминокислот, хлорофилла, гормонов, витаминов и других соединений. Все это – азот.

Растениям он необходим постоянно, так как отвечает за все процессы питания. Поэтому его недостаток задевает жизненно важные функции.
Особенно нуждаются в этом элементе молодые растения во время активного роста стеблей и листьев. Они содержат наибольшее количество азота. Но с развитием, его доля снижается.
Роль азота в жизни растения заключается еще в том, что он больше других элементов влияет на качество и количество урожая. Поэтому, чтобы вырастить богатый урожай нужно с ранней весны позаботиться о достатке азота.
Азот в природе
Растения используют азот в виде солей аммония (NH4+), и нитратов (NO3-):
- Аммоний называют “долгим” азотом, так как он неподвижен в почве, не вымывается и долго превращается в нитратную форму. Больше необходим на ранних стадиях развития растения.
- Нитраты – “быстрый” азот. Быстро действуют, но легко вымываются. В большинстве случаев азот поступает в растения именно в виде нитратов.
Обе формы полезны при разных условиях: когда нужно быстро подкормить растение, используют нитраты. А когда необходимо поступление азота только на определенной фазе роста, вносят аммонийные удобрения.
Нитраты не задерживаются в почве и могут вымываться со склонов, выноситься с урожаем:
- В водопроницаемых почвах (песчаных) вымывание азота происходит намного интенсивней, чем в почвах с низкой фильтрационной способностью (глинистых). Для уменьшения вымывания воды и соответственно азота, вносят перегной. Он имеет хорошую влагоемкость, склеивает частички почвы и заполняет собой пространство между ними.
- Также происходит потеря азота при денитрификации, когда почвенные бактерии перерабатывают нитрат, используя его для поддержания своей жизнедеятельности. В результате он становится недоступным.
- Так как азот накапливается в разных частях растения, то при уборке, уносится с урожаем. Разные культуры по-разному его используют. В зависимости от вида, в среднем выносится 100-200 кг/га органических веществ, содержащих азот.
- Также он выносится при улетучивании мочевины, когда уреаза превращает ее в аммиак.
Азот атмосферы – это единственный природный источник азота. В газообразном состоянии находится в неограниченном количестве. Но его могут использовать лишь некоторые растения. Свойство переводить такой азот в форму, доступную для усвоения имеют азотфиксирующие бактерии. Такие бактерии находятся на корнях бобовых (соя, люцерна, клевер). Поэтому для природного восполнения уровня азота, их высаживают на местах, где в будущем будут произрастать культурные растения. И после уборки бобовых, азот остается в почве.
Азот в гидропонике
В питательном растворе для гидропоники важно наличие обеих форм азота. С помощью контроля их соотношения, можно добиться стабильного значения рН. Потому что, если раствор имеет только аммоний – это приведет к понижению уровня рН раствора и его подкислению. И наоборот – при перевесе нитратов, повысится рН вокруг корней и раствор станет щелочным. В этом случае, если значение рН не соответствует нужному уровню, растение перестанет получать необходимые элементы для нормального развития. При значении рН 6,8 растения одинаково усваивают обе формы азота.
При одинаковых пропорциях аммоний больше понижает рН раствора, чем нитратный азот повышает его. Поэтому для стабилизации уровня рН аммония используют намного меньше, чем нитратов (в соотношении 1:3).
Еще одна важность правильного соотношения NH4+ и NO3- в том, что повышенное содержание аммония приводит к дефициту кальция и магния.
Соотношение нитратов и аммония очень важно. Но оно может меняться в зависимости от сорта растения, температуры раствора, стадии роста, освещения:
- 1. Если при образовании плодов у некоторых растений в питательном растворе присутствует аммоний – это снижает урожайность и может привести к заболеваниям. Поэтому лучше использовать аммоний только на начальной стадии развития. 2. При повышении температуры увеличивается потребление сахара и уменьшается обмен веществ аммония с ним. Поэтому при повышенных температурах недопустимо содержание высокого уровня аммония. 3. Наоборот, при низкой температуре нитраты транспортируются медленнее, поэтому использование их в растворе негативно сказывается на росте растения.
Нехватка азота у растений
Чтобы понять, как выглядит растение с недостатком азота N2 не нужно иметь специальных знаний. Главный признак – это прекращение роста и общая слабость. Растение с нормальным его содержанием выглядит здоровым, с насыщенным зеленым цветом листьев. Даже на начальной стадии азотное голодание может привести к потере половины урожая.
Недостаток азота у растений проявляет себя по таким признакам:
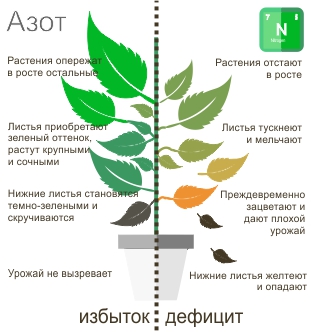
- растут слабые, короткие побеги;
- недостаток листьев, а те, что есть, теряют яркую окраску;
- новые листья мелкие, узкие, бледно-зеленые с красноватыми оттенками, рано опадают;
- пожелтение жилок с расположенными возле них частями листа. Сначала желтеть начинают нижние, старые листья;
- слабое ветвление деревьев;
- слабое цветение;
- плоды вырастают мелкие, рано осыпаются.
Как восполнить дефицит азота у растений
В почве
Азот для подкормки растений вносят в виде: калиевой, натриевой селитры, аммиачных, органических и других удобрений. Они повышают урожайность практически всех культур.
Почву удобряют ранней весной и в начале лета. За это время растение наиболее активно развивается. Своевременная подкормка стимулирует обмен веществ и активизирует рост.
Положительно удобрения влияют после весенних заморозков и понижений температуры. А вносить их после середины лета не рекомендуется. Это продлит рост, и существенно снизит зимостойкость растений. Также возможно накопление нитратов в плодах.
В гидропонике
Для гидропоники используют минеральные удобрения. Обычные органические удобрения (навоз) не используют, потому что они могут привести к загниванию. Это происходит из-за того, что органические удобрения расщепляются организмами, которые находятся только в почве. А удобрения для гидропоники содержат все готовые для использования элементы.
Раньше, чтобы получить питательный раствор, нужно было самому смешивать химические реактивы. Но это очень сложно. Сейчас раствор для гидропоники можно приготовить самому с помощью готовых удобрений:

Минеральное удобрение Plagron Hydro A/B 5 л. Двухкомпонентные азотсодержащие удобрения идеально подходят для профессионалов с большим опытом выращивания. Они содержат все необходимые питательные вещества даже для самых капризных растений. Используют эти подкормки во время развития, цветения и плодоношения. Они предназначены для гидропонного метода выращивания.

Стимулятор корнеобразования Plagron Power Roots 1 л. Это удобрение обеспечивает рост сильной, развитой корневой системы. В результате увеличивается усвоение питательных веществ, ускоряется рост молодых побегов. Используется во время вегетации и после пересадки для укрепления иммунитета. Подходит для любого способа выращивания.

Минеральное удобрение FloraGro 500 мл. Стимулирует активное развитие и укрепление корневой системы за счет обеспечения растения главными элементами. Используется на стадии вегетации для гидропонного способа, выращивания в почве, субстратах.
Источник
Азот входит в состав земной атмосферы в молекулярном виде, на него приходится 76% атмосферы по массе.
В связанном состоянии элемент встречается в почве и воде в виде химических соединений.
В живых организмах (растениях и животных) азот представлен в составе органических соединений, входит в аминокислоты в количестве от 15% до 18%.
к оглавлению ↑
Как влияет на организм
В начале 20 века было установлено, что для обеспечения жизнедеятельности живых организмов необходимо регулярное поступление в них некоторых химических соединений, включая азот.

В теле мужчины содержится в среднем 1,8 кг элемента, а женщины – 1,3 кг. Такая разница обусловлена тем, что белки входят в состав мышечной ткани, а у мужчин мышцы развиты сильнее, чем у женщин.
Для человека атмосферный азот является биологически неактивным веществом, поступающим в легкие с вдыхаемым воздухом и выводимым с выдыхаемым.
Потребность человека в белке складывается из 2 компонентов – удовлетворение потребности в общем азоте и в незаменимых аминокислотах.
Белковые соединения для синтеза своих тканей человек получает из пищи, которая должна содержать достаточное их количество.
Из необходимых организму аминокислот некоторые (называемые заменимыми) синтезируются в организме из аммиака и иных веществ, а несинтезируемые (называемые незаменимыми) должны поступать с пищей (растительной и животной).
Чтобы атмосферный азот оказался в составе белков, он должен претерпеть ряд превращений. Использовать его напрямую способны лишь живущие в почве бактерии рода Азотобактер с дальнейшим синтезом органических азотистых соединений.
Все остальные живые организмы не способны использовать атмосферный азот. У них азотистый обмен начинается с использования аммиака или аминокислот.
Аммиак образуют высшие растения путем восстановления содержащихся в почве нитратов с конечным биосинтезом аминокислот и белков.
Травоядные животные питаются растениями и превращают аминокислоты растений в собственные белки. Человек потребляет растительные и животные продукты и также превращает их в собственные ткани.
После смерти живых организмов микроорганизмы расщепляют органические вещества, азот поступает в почву, где ассимилируется азотфиксирующими бактериями и вновь превращается в органические вещества. Это и есть кругооборот азота в природе.
к оглавлению ↑
Потребность человека в белке, симптомы дефицита
В конце 19 века было окончательно установлено, что при нормальных условиях организм человека находится в состоянии азотистого равновесия, т. е. поступление азота с пищей равняется количеству элемента в выделяемых с мочой азотистых веществах (мочевине).

Количество выделяемой взрослым человеком мочевины зависит от количества потребляемой белковой пищи и обычно составляет 25-35 г в сутки.
Азотистый баланс нарушается при голодании или недостатке в пище белков. Длительное состояние отрицательного азотистого баланса (когда азота выводится больше, чем поступает) ведет к гибели организма.
Положительный азотистый баланс наблюдается в период восстановления после голодания или истощения. Нормальным является положительный азотистый баланс у растущих детей и подростков до периода прекращения их роста.
Для поддержания азотистого равновесия человеку, по нормам Всемирной организации здравоохранения, достаточно потреблять ежесуточно 0,8 г полноценного по аминокислотному составу белка на каждый килограмм своего веса.
При смешанном растительно-животном питании потребность в связи со снижением усвояемости возрастает и доходит до 1,0 г/кг. Под весом при данном расчете понимается нормальный (идеальный) вес без учета избыточной жировой ткани, например, по формуле «Рост минус 105».
При перечисленных ниже состояниях потребность в белке (и в азоте) увеличивается:
- стрессы;
- заболевания и травмы;
- после хирургических операций;
- беременность;
- грудное вскармливание;
- интенсивная физическая нагрузка.

При избыточном весе и похудении на сниженном по калорийности рационе также необходимо увеличить норму белка до 1,2-1,3 г/кг.
Но здесь нужна мера – потребление белка в количестве свыше 1,5 г/кг нежелательно, а свыше 2 г/кг — вредно.
Рекомендации по потреблению больших доз отдельных аминокислот или их комбинаций в виде добавки для спортсменов силовых видов спорта и бодибилдеров не подтверждаются, а применение чистых аминокислот считается неблагоприятным для здоровья, тем более, если они поступают взамен белковой пищи.
В чистом виде белковая недостаточность встречается редко. Это следствие общего недоедания, т. е. недостаточности калорийности рациона. Состояние при одновременном глубоком дефиците белка и энергии называется маразмом.
К социальным причинам недостаточности питания относятся:
- стихийные бедствия;
- войны;
- терроризм.
Поражает белково-энергетическая недостаточность беднейшие слои населения.
В развитых странах белково-калорийная недостаточность может наступать, как следствие заболеваний, хронического алкоголизма и наркомании, со снижением потребления пищи и нарушением ее усвоения.
Симптомы белково-калорийной недостаточности:
- задержка роста детей;
- слабость и потеря мышечной массы, что ведет к снижению веса тела;
- развитие обширных отеков;
- сухость и шелушение кожных покровов;
- образование медленно заживающих гноящихся язв;
- выпадение и обесцвечивание волос;
- потеря аппетита, тошнота;
- рвота с последующим обезвоживанием;
- анемия;
- снижение иммунитета.

к оглавлению ↑
Где его содержание больше всего, рекомендации по употреблению
Наиболее полноценные по аминокислотному составу белки содержатся в животных продуктах – мясе, рыбе, молочных продуктах, яйцах.
Достаточно белка и в крупах, макаронных изделиях, хлебе, бобовых (сое, чечевице, фасоли, бобах), в орехах и семечках.
Ниже в таблице приведена информация о том, в чем (в каких продуктах питания) содержится белок (азот).
| Продукт | Содержание белка, г/100 г продукта |
| Говядина | 20-22 |
| Свинина | 14-19 |
| Яйца | 12,7 |
| Колбасы, сосиски, сардельки | 9-14 |
| Рыба | 13-23 |
| Молоко и кисломолочные продукты | 2,6-4,3 |
| Творог | 14-18 |
| Сыр | 23-31 |
| Крупы | 7-13 |
| Хлеб | 5-8 |
| Бобовые | 22-23 |
| Овощи | 0,6-4 |
| Картофель | 2 |
| Фрукты | 0,2-2 |
| Орехи | 12-25 |
Еще больше информации о продуктах, богатых белком (азотом) в этом видео:
к оглавлению ↑
Допустимо ли сочетать белковые продукты с углеводными
Следующий из системы раздельного питания запрет на совместное употребление белковых и углеводных продуктов теорией рационального питания не обосновывается, да и эволюционно человек приспособлен к потреблению смешанной пищи.
Для полноценного усвоения белка необходимо оптимальное соотношение в нем аминокислот; этому условию отвечает смешанное растительно-животное питание.
Соблюдая рекомендации по разнообразному питанию и нормам потребления белка, удается обеспечить организм достаточным количеством белка и аминокислот без приема пищевых добавок.
к оглавлению ↑
Дополнительные рекомендации и советы
Помимо белков, азот включен и в состав азотсодержащих экстрактивных веществ и пуриновых оснований.

Содержащие азот экстрактивные вещества возбуждают железы желудка и способствуют лучшему усвоению белков и жиров в продуктах питания и еде.
Однако эти вещества оказывают и неблагоприятное воздействие на нервную систему, что осложняет течение болезней органов кровообращения, желудочно-кишечного тракта, почек и нервной системы.
Поэтому из диетического питания исключаются первые блюда на мясных и рыбных бульонах, жареные или тушеные вторые блюда.
Пуриновые основания нарушают обменные процессы в организме, что приводит к задержке мочевой кислоты и отложениям ее солей в тканях — основной причине подагры.
Но пуриновые основания являются также обязательным компонентом питания, и их оптимальный уровень в организме поддерживается употреблением хорошо вываренного мяса.
На Земле химический элемент азот присутствует в атмосфере, составляя большую ее часть. Азот входит в состав белков живых организмов, но они не способны усваивать атмосферный азот напрямую.
Азот поступает к ним с белковой пищей или из содержащихся в почве нитратов. В начале цепи превращения атмосферного азота в белки стоят живущие в почве бактерии рода Азотобактер.
Источник
