В каких реакциях проявляются амфотерные свойства аминокислот
Амофтерные – значит проявляют и свойства кислоты, и свойства основания.
У аминокислот есть кислотная группа -COOH, значит, они проявляют свойства кислот и реагируют с основаниями:
H2N – CH2 – COOH + NaOH = H2N – CH2 – COONa + H2O
У аминокислот есть основная аминогруппа, поэтому они проявляют свойства оснований и реагируют с кислотами:
H2N – CH2 – COOH + HCl = (H3N – CH2 – COOH)Cl + H2O
В этой реакции образуется соль – солянокислый глицин.
Таким образом, аминокислоты амфотерны.
(не те реакции)
65. Заменимые и незаменимые аминокислоты. Приведите примеры. Напишите уравнения реакции образования цистина и цистеина.
1)HS-CH2-CH(NH2)-COOH (цистеин) –(O2, -H2O)–> HOOC-CH(NH2)-CH2-S-S-CH2-CH(NH2)-COOH (цистин)
2)CH2=CH-CN (акрилонитрил) –(S, t)–>
–(NH3)–> HS-CH2-CH(NH2)-CN –(H2O)–> HS-CH2-CH(NH2)-COOH (цистеин)
Заменимые аминокислоты:
Аланин способствует восстановлению после травм. Регулирует уровень сахара в крови. Участвует в энергообразовании. Способствует запасанию гликогена мышцами и печенью.
Аспарагин участвует в метаболизме нервной системы. Участвует в синтезе аминокислот в печени. Способствует выработке аспарагиновой кислоты, которая участвует в синтезе ДНК и РНК.
Аспарагиновая кислота активизирует иммунную систему. Снижает утомляемость. Способствует превращению углеводов в мышечную энергию. Образует лизин и метионин.
Глутамин стимулирует память и мышление. Участвует в синтезе протеина. Повышает выносливость. Нейтрализует токсические соединения в организме. Снижает тягу к алкоголю и сладостям.
Глицин – антидепрессант. Повышает умственную работоспособность. Ослабляет влечение к алкоголю. Снижает кислотность желудка. Участвует в образовании заменимых аминокислот.
Глутаминовая кислота участвует в метаболизме аминокислот. Выполняет функции нейромедиатора в ЦНС. Играет важную роль в углеводном обмене.
Пролин укрепляет суставы и связки. Участвует в выработке энергии. Способствует заживлению ран.
Серин укрепляет иммунную систему. Необходим для нормального обмена жиров и жирных кислот. Участвует в биосинтезе глицина, метионина, цистеина, и триптофана.
Тирозин – антидепрессант. Подавляет аппетит. Способствует функционированию надпочечников и щитовидной железы. Участвует в биосинтезе адреналина, гормонов щитовидной железы.
Цистеин ускоряет заживление тканей. Стимулирует рост волос. Активизирует иммунную систему. Улучшает мозговую деятельность. Переносит аминокислоты по организму. Антиоксидант.
Незаменимые аминокислоты:
Валин содержится в моркови, свекле, зерновых, мясе, грибах, молочных продуктах, арахисе. Валин метаболизируется в мышечную ткань, стимулирует умственную деятельность. Валин необходим организму для поддержания нужного уровня обмена азота.
Изолейцин содержится в рыбе, курином мясе, печени, миндале, кешью, в соевых белках. Изолейцин регулирует уровень сахара в крови. Участвует в синтезе гемоглобина. Повышает выносливость организма. Участвует в синтезе метаболизма в мышцах. Расщепляет холестерин.
Лейцин содержится в бобах, буром рисе, пшеничной муке и орехах. Лейцин является источником энергии, способствует восстановлению мышц и костей. Снижает повышенный уровень сахара в крови при диабетах.
Лизин содержат сельдерей, зеленые овощи, молоко, яйца, дрожжевые продукты, мясо. Лизин необходим для роста костной ткани, поддержания женской половой функции. Поддерживает обмен азота в организме. Оказывает противовирусное действие. Стимулирует умственную деятельность.
Метионин содержат в себе яйца, бобовые, лук, чеснок, мясо, йогурты. Метионин улучшает пищеварение, помогает перерабатывать жир. Расщепляет холестерин. Предотвращает выпадение волос. Антиоксидант.
Треонин содержится в листовых овощах, моркови. Треонин активизирует иммунную систему. Детоксикатор. Способствует росту тканей. Помогает усваивать пищевой белок.
Триптофан есть в бананах, помидорах, редьке, фенхеле.
Триптофан регулирует функции иммунной и центральной нервной системы. Способствует хорошему сну. Стимулирует рост кожи и волос. Улучшает пищеварение.
Фенилаланин можно найти в свекле, моркови, яблоках и шпинате. Фенилаланин стимулирует ЦНС. Антидепрессант. Улучшает память и внимание. Повышает работоспособность. Снижает аппетит.
Источник
Физические свойства
a-Аминокислоты – кристаллические вещества белого или сероватого цвета. Они хорошо растворяются в воде с образованием электролитов, плохо – в спирте, не растворяются в эфире. Аминокислоты в твердом и растворенном состоянии имеют биполярное строение, на что указывает отсутствие в ИК-спектрах отдельных полос поглощения, характерных для – NН2 и –СООН групп, они обладают высокой температурой плавления (См. Приложение 3).
Амфотерность
– способность a-аминокислот диссоциировать в водном растворе по типу кислоты и основания из-за наличия в их составе групп кислотного (-СООН) и основного (-NH2) характера. Аминокислоты существует в виде равновесной смеси биполярного иона (цвиттериона) катионной и анионнойформ, равновесие которых зависит от рН среды:
+H+ +OH–
NH3+ – СH – COOH NH3+ – CH – COO– NH2 – CH – COO– + H2O
ï – H+ ï – OH– ï
R R R
Катионная форма Биполярный ион Анионная форма
Сильнокислая среда Сильнощелочная среда
рН 1,0 рН 7,0 рН 11,0
Катионные формы пребладают в сильнокислых средах, анионные – в сильнощелочных. Катионная форма a-аминокислоты, с позиций теории Бренстеда, является двухосновной кислотой, содержащей две кислотные группы: недиссоциированную карбоксильную группу и протонированную аминогруппу. Характеризуется кислота соответствующими значениями рКа1и рКа2. Отдавая один протон, двухосновная кислота превращается в слабую одноосновную – диполярный ион с одной кислотной +NH3-группой. Депротонирование диполярного иона приводит к получению анионной формы a-аминокислоты – карбоксилат-аниона (основание Бренстеда).
Значения рКа1, характеризующие кислотные свойства – СООН группы a-аминокислот, лежат в интервале от 1 до 3; значения рКа2, характеризующие кислотность аммониевой группы, – от 9 до 10. Положение равновесия (соотношение различных форм a-аминокислоты) в водном растворе при определенных значениях рН зависит от наличия в радикале R ионогенных групп, которые играют роль дополнительных кислотных и основных центров.
Значение рН, при котором концентрация диполярных ионов максимальна, а минимальные концентрации катионных и анионных форм a-аминокислоты равны, называется изоэлектрической точкой (pI).
pI = 1/2 . (рКа n + рКа n+1),где
n – максимальное число положительных зарядов в протонированной a-аминокислоте
В изоэлектрической точке суммарный заряд молекулы a-аминокислоты равен нулю. Биполярные ионы не перемещаются в электрическом поле. При значениях рН ниже рI катион a-аминокислоты (аммониевая форма) движется к катоду; при рН выше, чем pI, карбоксилат-анион аминокислоты перемещается к аноду. На этом основано разделение аминокислот методом электрофореза.
Нейтральные а-аминокислоты имеют рI несколько ниже 7,0 (5,5—6,3) из-за большей ионизации карбоксильной группы под влиянием -Iэфф+NH3 –группы:
катион биполярный ион анион
pKa 1 = 2,3 СOOH-группы pI = 6,0 рКа2 = 9,6 +NH3-группы
Кислые а-аминокислоты, имеющие в радикале дополнительную карбоксильную группу, в сильнокислой среде находятся в полностью протонированной форме. Они являются трехосновными кислотами (по Бренстеду), характеризующимися тремя значениями рКа, как это видно на примере глутаминовой кислоты (рI = 3,2):
катион биполярный ион анион дианион
рКа1= 2,2 (a-СOOH) pI=3,2 pKa2=4,3 (COOH в pKa3=9,7 +NH3- радикале группы
Основные а-аминокислоты имеют изоэлектрическую точку выше рН 7. В сильнокислой среде они также представляют собой трехосновные кислоты, этапы ионизации которых выглядят следующим образом:
Дикатион катион биполярный ион анион
лизина pKa1=2,2 (COOH) pKa2=9,0 (a-+NH3) pKa3=10,5 ( +NH3 в радикале)
Свойство аминокислот диссоциировать на ионы в кислой или щелочной среде лежит в основе методов разделения и идентификации их ионообменной хроматографией и электрофорезом (см. главу 6 ).
Источник
Аминокислоты являются амфотерными соединениями, для них характерны кислотно-основные свойства. Это обусловлено наличием в их молекулах функциональных групп кислотного (-СООН) и основного (-NH2) характера.
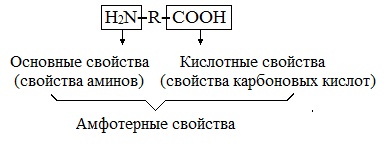
Кислотно-основное равновесие в водных растворах
В водных растворах и твердом состоянии аминокислоты существуют в виде внутренних солей.
Ионизация молекул аминокислот в водных растворах зависит от кислотного или щелочного характера среды:
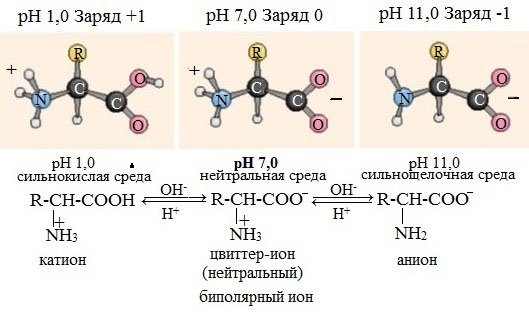
В кислой среде молекулы аминокислот представляю собой катион. В щелочной среде молекулы аминокислот представляют собой анион. В нейтральной среде аминокислоты представляют собой цвиттер-ион или биполярный ион.
Аминокислоты в твердом состоянии всегда существуют в виде биполярного, двухзарядного иона — цвиттер-иона.
Водные растворы аминокислот в кислой и щелочной среде проводят электрический ток.
1. Взаимодействие внутри молекулы – образование внутренних солей (биполярных ионов)
Молекулы аминокислот существуют в виде внутренних солей, которые образуются за счет переноса протона от карбоксила к аминогруппе.
Карбоксильная группа аминокислоты отщепляет ион водорода, который затем присоединяется к аминогруппе той же молекулы по месту неподеленной электронной пары азота. В результате действие функциональных групп нейтрализуется, образуется так называемая внутренняя соль.
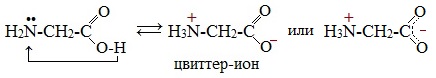
Водные растворы аминокислот в зависимости от количества функциональных групп имеют нейтральную, кислую или щелочную среду.
Аминокислоты с одной карбоксильной группой и одной аминогруппой имеют нейтральную реакцию.
Видеоопыт «Свойства аминоуксусной кислоты»
а) моноаминомонокарбоновые кислоты (нейтральные кислоты)
Внутримолекулярная нейтрализация — образуется биполярный цвиттер-ион.
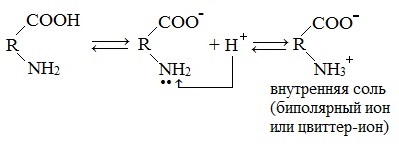
Водные растворы моноаминомонокарбоновых кислот нейтральны (рН≈7).
б) моноаминодикарбоновые кислоты (кислые аминокислоты)
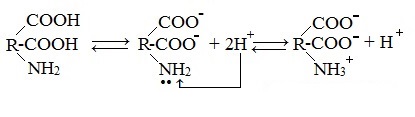
Водные растворы моноаминодикарбоновых кислот имеют рН<7 (кислая среда), так как в результате образования внутренних солей этих кислот в растворе появляется избыток ионов водорода Н+.
в) диаминомонокарбоновые кислоты (основные аминокислоты)
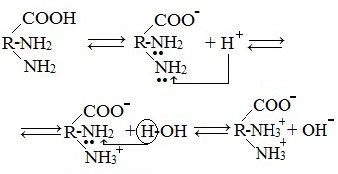
Водные растворы диаминомонокарбоновых кислот имеют рН>7 (щелочная среда), так как в результате образования внутренних солей этих кислот в растворе появляется избыток гидроксид-ионов ОН— .
2. Взаимодействие с основаниями и кислотами
Аминокислоты как амфотерные соединения образуют соли как с кислотами (по группе NH2), так и со щелочами (по группе СООН).
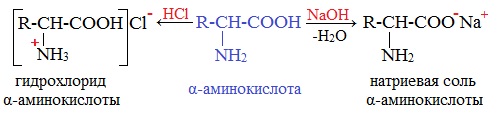
Как кислота (участвует карбоксильная группа)
Как карбоновые кислоты α-аминокислоты образуют функциональные производные: соли, сложные эфиры, амиды.
а) взаимодействие с основаниями
Образуются соли:
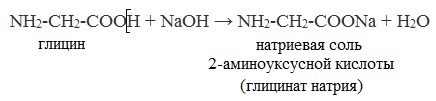
б) взаимодействие со спиртами (р. этерификации)
Аминокислоты могут реагировать со спиртами в присутствии газообразного хлороводорода, превращаясь в сложный эфир. Сложные эфиры аминокислот не имеют биполярной структуры и являются летучими соединениями.
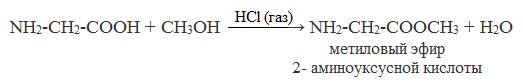
в) взаимодействие с аммиаком
Образуются амиды:
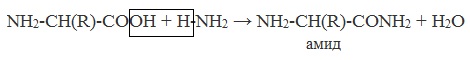
Как основание (участвует аминогруппа)
а) взаимодействие с сильными кислотами
Подобно аминам, аминокислоты реагируют с сильными кислотами с образованием солей аммония:
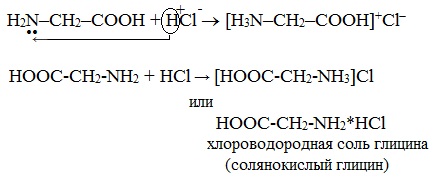
б) взаимодействие с азотистой кислотой (р. дезаминирования)
Подобно первичным аминам, аминокислоты реагируют с азотистой кислотой, при этом аминогруппа превращается в гидроксогруппу, а аминокислота – в гидроксикислоту:
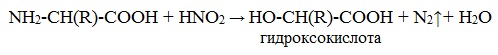
Измерение объёма выделившегося азота позволяет определить количество аминокислоты (метод Ван-Слайка).
3. Внутримолекулярное взаимодействие функциональных групп ε-аминокапроновой кислоты, в результате которого образуется ε-капролактам (полупродукт для получения капрона).
4. Межмолекулярное взаимодействие α-аминокислот – образование пептидов (р. поликонденсации)
При взаимодействии карбоксильной группы одной молекулы аминокислоты и аминогруппы другой молекулы аминокислоты образуются пептиды. При взаимодействии двух α-аминокислот образуется дипептид.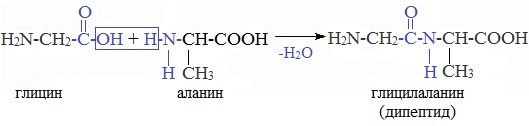
Межмолекулярная реакция с участием трех α-аминокислот приводит к образованию трипептида и т.д.
Важнейшие природные полимеры – белки (протеины) – относятся к полипептидам, т.е представляют собой продукт поликонденсации a-аминокислот.
5. Качественные реакции!
а) нингидриновая реакция
Все аминокислоты окисляются нингидрином с образованием продуктов сине-фиолетового цвета:
Иминокислота пролин дает с нингидрином желтое окрашивание.
б) с ионами тяжелых металлов α-аминокислоты образуют внутрикомплексные соли. Комплексы меди (II), имеющие глубокую синюю окраску, используются для обнаружения α-аминокислот.
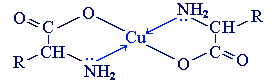
Видеоопыт «Образование медной соли аминоуксусной кислоты»
Аминокислоты
Источник
Среди
азотсодержащих органических веществ имеются соединения с двойственной функцией.
Особенно важными из них являются аминокислоты.
В клетках и тканях живых организмов
встречается около 300 различных аминокислот, но только 20 (α-аминокислоты) из них служат звеньями (мономерами), из которых построены пептиды и
белки всех организмов (поэтому их называют белковыми аминокислотами).
Последовательность расположения этих аминокислот в белках закодирована в
последовательности нуклеотидов соответствующих генов. Остальные аминокислоты
встречаются как в виде свободных молекул, так и в связанном виде. Многие из
аминокислот встречаются лишь в определенных организмах, а есть и такие, которые
обнаруживаются только в одном из великого множества описанных организмов.
Большинство микроорганизмов и растения синтезируют необходимые им аминокислоты;
животные и человек не способны к образованию так называемых незаменимых
аминокислот, получаемых с пищей. Аминокислоты участвуют в обмене белков и
углеводов, в образовании важных для организмов соединений (например, пуриновых
и пиримидиновых оснований, являющихся неотъемлемой частью нуклеиновых кислот),
входят в состав гормонов, витаминов, алкалоидов, пигментов, токсинов,
антибиотиков и т. д.; некоторые аминокислоты служат посредниками при передаче
нервных импульсов.
Аминокислоты — органические амфотерные соединения, в состав
которых входят карбоксильные группы – СООН и аминогруппы -NH2.
Аминокислоты можно рассматривать как
карбоновые кислоты, в молекулах которых атом водорода в радикале замещен
аминогруппой.
КЛАССИФИКАЦИЯ

Аминокислоты классифицируют по структурным признакам.
1.
В
зависимости от взаимного расположения амино- и карбоксильной групп аминокислоты
подразделяют на α-, β-, γ-, δ-, ε- и
т. д.
2.
В
зависимости от количества функциональных групп различают кислые, нейтральные и
основные.
3.
По
характеру углеводородного радикала различают алифатические (жирные), ароматические,
серосодержащие и гетероциклические
аминокислоты. Приведенные выше аминокислоты относятся к жирному ряду.
Примером
ароматической аминокислоты может служить пара-аминобензойная
кислота:
Примером
гетероциклической аминокислоты может служить триптофан – незаменимая α- аминокислота
НОМЕНКЛАТУРА
По систематической номенклатуре названия
аминокислот образуются из названий соответствующих кислот прибавлением
приставки амино- и указанием места расположения аминогруппы по отношению
к карбоксильной группе. Нумерация углеродной цепи с атома углерода карбоксильной группы.
Например:
Часто используется также другой способ
построения названий аминокислот, согласно которому к тривиальному названию
карбоновой кислоты добавляется приставка амино- с указанием положения
аминогруппы буквой греческого алфавита.
Пример:
Для α-аминокислот R-CH(NH2)COOH

, которые играют исключительно важную
роль в процессах жизнедеятельности животных и растений, применяются тривиальные
названия.
Таблица. Некоторые важнейшие α-аминокислоты
Аминокислота | Сокращённое обозначение | Строение радикала ( R ) |
Глицин | Gly (Гли) | H – |
Аланин | Ala (Ала) | CH3 – |
Валин | Val (Вал) | (CH3)2CH – |
Лейцин | Leu (Лей) | (CH3)2CH – CH2 – |
Серин | Ser (Сер) | OH- CH2 – |
Тирозин | Tyr (Тир) | HO – C6H4 – CH2 – |
Аспарагиновая кислота | Asp (Асп) | HOOC – CH2 – |
Глутаминовая кислота | Glu (Глу) | HOOC – CH2 – CH2 – |
Цистеин | Cys (Цис) | HS – CH2 – |
Аспарагин | Asn (Асн) | O = C – CH2 – │ NH2 |
Лизин | Lys (Лиз) | NH2 – CH2- CH2 – CH2 – |
Фенилаланин | Phen (Фен) | C6H5 – CH2 – |
Если
в молекуле аминокислоты содержится две аминогруппы, то в ее названии
используется приставка диамино-, три группы NH2 – триамино-
и т.д.
Пример:
Наличие
двух или трех карбоксильных групп отражается в названии суффиксом –диовая
или -триовая кислота:
ИЗОМЕРИЯ
1. Изомерия углеродного скелета
2. Изомерия положения функциональных
групп
3. Оптическая изомерия
α-аминокислоты, кроме глицина NН2-CH2-COOH.
ФИЗИЧЕСКИЕ СВОЙСТВА
Аминокислоты представляют собой
кристаллические вещества с высокими (выше 250°С) температурами плавления,
которые мало отличаются у индивидуальных аминокислот и поэтому нехарактерны.
Плавление сопровождается разложением вещества. Аминокислоты хорошо растворимы в
воде и нерастворимы в органических растворителях, чем они похожи на
неорганические соединения. Многие аминокислоты обладают сладким вкусом.
ПОЛУЧЕНИЕ
3. Микробиологический синтез. Известны микроорганизмы, которые
в процессе жизнедеятельности продуцируют α – аминокислоты белков.
ХИМИЧЕСКИЕ СВОЙСТВА
Аминокислоты
амфотерные органические соединения, для них характерны кислотно-основные
свойства.
I.Общие свойства
1. Внутримолекулярная нейтрализация → образуется биполярный цвиттер-ион:
Водные
растворы электропроводны. Эти свойства объясняются тем, что молекулы
аминокислот существуют в виде внутренних солей, которые образуются за счет
переноса протона от карбоксила к аминогруппе:
цвиттер-ион
Водные растворы аминокислот имеют нейтральную, кислую
или щелочную среду в зависимости от количества функциональных групп.
Видео-опыт «Свойства аминоуксусной кислоты»
2. Поликонденсация→ образуются полипептиды (белки):
При взаимодействии двух
α-аминокислот образуется дипептид.
3. Разложение → Амин +
Углекислый газ:
NH2-CH2-COOH → NH2-CH3 + CO2↑
II. Свойства карбоксильной группы
(кислотность)
1. С основаниями → образуются соли:
NH2-CH2-COOH
+ NaOH → NH2-CH2-COONa + H2O
NH2-CH2-COONa – натриевая соль 2-аминоуксусной кислоты
2. Со спиртами → образуются сложные
эфиры – летучие вещества (р.
этерификации): NH2-CH2-COOH
+ CH3OH HCl(газ)→ NH2-CH2-COOCH3
+ H2O
NH2-CH2-COOCH3 – метиловый эфир 2- аминоуксусной кислоты
3. С аммиаком → образуются
амиды:
NH2-CH(R)-COOH + H-NH2 →
NH2-CH(R)-CONH2 + H2O
4. Практическое значение имеет
внутримолекулярное взаимодействие функциональных групп ε-аминокапроновой
кислоты, в результате которого образуется ε-капролактам (полупродукт для
получения капрона):
III. Свойства аминогруппы (основность)
1. С сильными кислотами → соли:
HOOC-CH2-NH2 + HCl → [HOOC-CH2-NH3]Cl
или HOOC-CH2-NH2*HCl
2. С азотистой кислотой (подобно
первичным аминам):
NH2-CH(R)-COOH +
HNO2 → HO-CH(R)-COOH + N2↑+ H2O
гидроксокислота
Измерение
объёма выделившегося азота позволяет определить количество аминокислоты (метод
Ван-Слайка)
IV.Качественная реакция
1. Все аминокислоты окисляются
нингидрином с образованием продуктов сине-фиолетового цвета!
2. С ионами тяжелых металлов α-аминокислоты
образуют внутрикомплексные соли. Комплексы меди (II), имеющие глубокую
синюю окраску, используются для обнаружения α-аминокислот.
Видео-опыт “Образование медной соли аминоуксусной кислоты”.
Генетическая связь аминокислот с другими классами органических соединений
ПРИМЕНЕНИЕ
1) аминокислоты широко
распространены в природе;
2) молекулы аминокислот – это те
кирпичики, из которых построены все растительные и животные белки;
аминокислоты, необходимые для построения белков организма, человек и животные
получают в составе белков пищи;
3) аминокислоты прописываются при
сильном истощении, после тяжелых операций;
4) их используют для питания
больных;
5) аминокислоты необходимы в
качестве лечебного средства при некоторых болезнях (например, глутаминовая
кислота используется при нервных заболеваниях, гистидин – при язве желудка);
6) некоторые аминокислоты
применяются в сельском хозяйстве для подкормки животных, что положительно
влияет на их рост;
7) имеют техническое значение:
аминокапроновая и аминоэнантовая кислоты образуют синтетические волокна –
капрон и энант.
О РОЛИ АМИНОКИСЛОТ
Нахождение в природе и биологическая роль аминокислот
Источник
