В каких химических реакциях сера проявляет восстановительные свойства

Сера – элемент VIa группы 3 периода периодической таблицы Д.И. Менделеева. Относится к
группе халькогенов – элементов VIa группы.
Сера – S – простое вещество имеет светло-желтый цвет. Использовалась еще до нашей эры в составе священных курений при
религиозных обрядах.

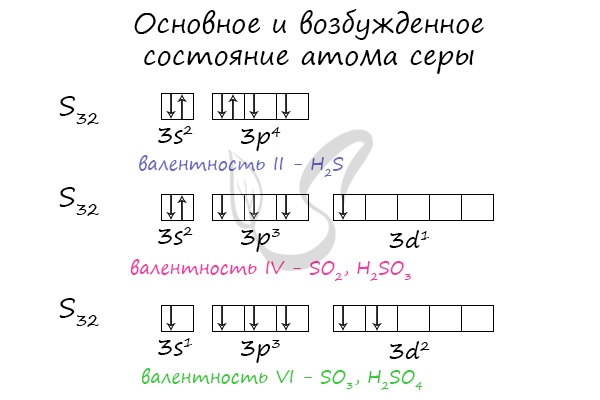
Основное и возбужденное состояние атома серы
Электроны s- и p-подуровня способны распариваться и переходить на d-подуровень. Как и всегда, количество валентных
электронов отражает количество возможных связей у атома.
В разных электронных конфигурациях сера способна принимать валентности: II, IV и VI.
Природные соединения
- FeS2 – пирит, колчедан
- ZnS – цинковая обманка
- PbS – свинцовый блеск (галенит), Sb2S3 – сурьмяный блеск, Bi2S3 – висмутовый блеск
- HgS – киноварь
- CuFeS2 – халькопирит
- Cu2S – халькозин
- CuS – ковеллин
- BaSO4 – барит, тяжелый шпат
- CaSO4 – гипс
В местах вулканической активности встречаются залежи самородной серы.

Получение
В промышленности серу получают из природного газа, который содержит газообразные соединения серы: H2S,
SO2.
H2S + O2 = S + H2O (недостаток кислорода)
SO2 + C = (t) S + CO2
Серу можно получить разложением пирита
FeS2 = (t) FeS + S
В лабораторных условиях серу можно получить слив растворы двух кислот: серной и сероводородной.
H2S + H2SO4 = S + H2O
Химические свойства
- Реакции с неметаллами
- Реакции с металлами
- Реакции с кислотами
- Реакции с щелочами
- Реакции с солями
На воздухе сера окисляется, образуя сернистый газ – SO2. Реагирует со многими неметаллами, без нагревания –
только со фтором.
S + O2 = (t) SO2
S + F2 = SF6
S + Cl2 = (t) SCl2
S + C = (t) CS2

При нагревании сера бурно взаимодействует со многими металлами с образованием сульфидов.
K + S = (t) K2S
Al + S = (t) Al2S3
Fe + S = (t) FeS
При взаимодействии с концентрированными кислотами (при длительном нагревании) сера окисляется до сернистого газа или серной кислоты.
S + H2SO4 = (t) SO2 + H2O
S + HNO3 = (t) H2SO4 + NO2 + H2O
Сера вступает в реакции диспропорционирования с щелочами.
S + KOH = (t) K2S + K2SO3 + H2O
Сера вступает в реакции с солями. Например, в кипящем водном растворе сера может реагировать с сульфитами с образованием тиосульфатов.
Na2SO3 + S → (t) Na2S2O3
Сероводород – H2S
Бесцветный газ с характерным запахом тухлых яиц. Огнеопасен. Используется в химической промышленности и в лечебных целях (сероводородные
ванны).

Получение
Сероводород получают в результате реакции сульфида алюминия с водой, а также взаимодействия разбавленных кислот с сульфидами.
Al2S3 + H2O = (t) Al(OH)3↓ + H2S↑
FeS + HCl = FeCl2 + H2S↑

Химические свойства
- Кислотные свойства
- Восстановительные свойства
- Качественная реакция
Сероводород плохо диссоциирует в воде, является слабой кислотой. Реагирует с основными оксидами, основаниями с образованием средних и кислых солей (зависит
от соотношения основания и кислоты).
MgO + H2S = (t) MgS + H2O
KOH + H2S = KHS + H2O (гидросульфид калия, избыток кислоты)
2KOH + H2S = K2S + 2H2O
Металлы, стоящие в ряду напряжений до водорода, способны вытеснить водород из кислоты.
Ca + H2S = (t) CaS + H2
Сероводород – сильный восстановитель (сера в минимальной степени окисления S2-). Горит в кислороде синим пламенем, реагирует с кислотами.
H2S + O2 = H2O + S (недостаток кислорода)
H2S + O2 = H2O + SO2 (избыток кислорода)
H2S + HClO3 = H2SO4 + HCl

Качественной реакцией на сероводород является реакция с солями свинца, при котором образуется сульфид свинца.
H2S + Pb(NO3)2 = PbS↓ + HNO3
Оксид серы – SO2
Сернистый газ – SO2 – при нормальных условиях бесцветный газ с характерным резким запахом (запах загорающейся
спички).

Получение
В промышленных условиях сернистый газ получают обжигом пирита.
FeS2 + O2 = (t) FeO + SO2
В лаборатории SO2 получают реакцией сильных кислот на сульфиты. В ходе подобных реакций образуется сернистая кислота,
распадающаяся на сернистый газ и воду.
K2SO3 + H2SO4 = (t) K2SO4 + H2O + SO2↑
Сернистый газ получается также в ходе реакций малоактивных металлов с серной кислотой.
Cu + H2SO4(конц.) = (t) CuSO4 + SO2 + H2O
- Кислотные свойства
- Восстановительные свойства
- Как окислитель
С основными оксидами, основаниями образует соли сернистой кислоты – сульфиты.
K2O + SO2 = K2SO3
NaOH + SO2 = NaHSO3
2NaOH + SO2 = Na2SO3 + H2O

Химически сернистый газ очень активен. Его восстановительные свойства продемонстрированы в реакциях ниже.
Fe2(SO4)3 + SO2 + H2O = FeSO4 + H2SO4
SO2 + O2 = (t, кат. – Pt) SO3
В присутствии сильных восстановителей SO2 способен проявлять окислительные свойства (понижать степень окисления).
CO + SO2 = CO2 + S
H2S + SO2 = S + H2O
Сернистая кислота
Слабая, нестойкая двухосновная кислота. Существует лишь в разбавленных растворах.
Получение
SO2 + H2O ⇄ H2SO3
Химические свойства
- Диссоциация
- Кислотные свойства
- Окислительные свойства
- Восстановительные свойства
Диссоциирует в водном растворе ступенчато.
H2SO3 = H+ + HSO3-
HSO3- = H+ + SO32-
В реакциях с основными оксидами, основаниями образует соли – сульфиты и гидросульфиты.
CaO + H2SO3 = CaSO3 + H2O
H2SO3 + 2KOH = 2H2O + K2SO3 (соотношение кислота – основание, 1:2)
H2SO3 + KOH = H2O + KHSO3 (соотношение кислота – основание, 1:1)
С сильными восстановителями сернистая кислота принимает роль окислителя.
H2SO3 + H2S = S↓ + H 2O
Как и сернистый газ, сернистая кислота и ее соли обладают выраженными восстановительными свойствами.
H2SO3 + Br2 = H2SO4 + HBr

Оксид серы VI – SO3
Является высшим оксидом серы. Бесцветная летучая жидкость с удушающим запахом. Ядовит.
Получение
В промышленности данный оксид получают, окисляя SO2 кислородом при нагревании и присутствии катализатора
(оксид ванадия – Pr, V2O5).
SO2 + O2 = (кат) SO3
В лабораторных условиях разложением солей серной кислоты – сульфатов.
Fe2(SO4)3 = (t) SO3 + Fe2O3
Химические свойства
- Кислотные свойства
- Окислительные свойства
Является кислотным оксидом, соответствует серной кислоте. При реакции с основными оксидами и основаниями образует ее соли – сульфаты и
гидросульфаты. Реагирует с водой с образованием серной кислоты.
SO3 + 2KOH = K2SO4 + 2H2O (основание в избытке – средняя соль)
SO3 + KOH = KHSO4 + H2O (кислотный оксид в избытке – кислая соль)
SO3 + Ca(OH)2 = CaSO4 + H2O

SO3 + Li2O = Li2SO4
SO3 + H2O = H2SO4
SO3 – сильный окислитель. Чаще всего восстанавливается до SO2.
SO3 + P = SO2 + P2O5
SO3 + H2S = SO2 + H2O
SO3 + KI = SO2 + I2 + K2SO4

© Беллевич Юрий Сергеевич 2018-2020
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение
(в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов
без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования,
обратитесь, пожалуйста, к Беллевичу Юрию.
Источник
Химические свойства кислорода
Химический элемент кислород может существовать в виде двух аллотропных модификаций, т.е. образует два простых вещества. Оба этих вещества имеют молекулярное строение. Одно из них имеет формулу O2 и имеет название кислород, т.е. такое же, как и название химического элемента, которым оно образовано.
Другое простое вещество, образованное кислородом, называется озон. Озон в отличие от кислорода состоит из трехатомных молекул, т.е. имеет формулу O3.
Поскольку основной и наиболее распространенной формой кислорода является молекулярный кислород O2, прежде всего мы рассмотрим именно его химические свойства.
Химический элемент кислород находится на втором месте по значению электроотрицательности среди всех элементов и уступает лишь фтору. В связи с этим логично предположить высокую активность кислорода и наличие у него практически только окислительных свойств. Действительно, список простых и сложных веществ, с которыми может реагировать кислород огромен. Однако, следует отметить, что поскольку в молекуле кислорода имеет место прочная двойная связь, для осуществления большинства реакций с кислородом требуется прибегать к нагреванию. Чаще всего сильный нагрев требуется в самом начале реакции (поджиг) после чего многие реакции идут далее уже самостоятельно без подвода тепла извне.
Среди простых веществ не окисляются кислородом лишь благородные металлы (Ag, Pt, Au), галогены и инертные газы.
Сера сгорает в кислороде с образованием диоксида серы:
Фосфор в зависимости от избытка или недостатка кислорода может образовать как оксида фосфора (V), так и оксид фосфора (III):
Взаимодействие кислорода с азотом протекает в крайне жестких условиях, в виду того что энергии связи в молекулах кислорода и особенно азота очень велики. Также свой вклад в сложность протекания реакции делает высокая электроотрицательность обоих элементов. Реакция начинается лишь при температуре более 2000 oC и является обратимой:
Не все простые вещества, реагируя с кислородом образуют оксиды. Так, например, натрий, сгорая в кислороде образует пероксид:
а калий – надпероксид:
Чаще всего, при сгорании в кислороде сложных веществ образуется смесь оксидов элементов, которыми было образовано исходное вещество. Так, например:
Однако, при сгорании в кислороде азотсодержащих органических веществ вместо оксида азота образуется молекулярный азот N2. Например:
При сгорании в кислороде хлорпроизводных вместо оксидов хлора образуется хлороводород:
Химические свойства озона:
Озон является более сильным окислителем, чем кислород. Обусловлено это тем, что одна из кислород-кислородных связей в молекуле озона легко рвется и в результате образуется чрезвычайно активный атомарный кислород. Озон в отличие от кислорода не требует для проявления своих высоких окислительных свойств нагревания. Он проявляет свою активность при обычной и даже низкой температурах:
PbS + 4O3 = PbSO4 + 4O2
Как было сказано выше, серебро с кислородом не реагирует, однако, реагирует с озоном:
2Ag + O3 = Ag2O + O2
Качественной реакцией на наличие озона является то, что при пропускании исследуемого газа через раствор иодида калия наблюдается образование йода:
2KI + O3 + H2O = I2↓ + O2 + 2KOH
Химические свойства серы
Сера как химический элемент может существовать в нескольких аллотропных модификациях. Различают ромбическую, моноклинную и пластическую серу. Моноклинная сера может быть получена при медленном охлаждении расплава ромбической серы , а пластическая напротив получается при резком охлаждении расплава серы, предварительно доведенного до кипения. Пластическая сера обладает редким для неорганических веществ свойством эластичности – она способна обратимо растягиваться под действием внешнего усилия, возвращаясь в исходную форму при прекращении этого воздействия. Наиболее устойчива в обычных условиях ромбическая сера и все иные аллотропные модификации со временем переходят в нее.
Молекулы ромбической серы состоят из восьми атомов, т.е. ее формулу можно записать как S8. Однако, поскольку химические свойства всех модификаций достаточно схожи, чтобы не затруднять запись уравнений реакций любую серу обозначают просто символом S.
Сера может взаимодействовать и с простыми и со сложными веществами. В химических реакциях проявлет как окислительные, так и восстановительные свойства.
Окислительные свойства серы проявляются при ее взаимодействии с металлами, а также неметаллами, образованными атомами менее электроотрицательного элемента (водород, углерод, фосфор):
Как восстановитель сера выступает при взаимодействии с неметаллами, образованными более электроотрицательными элементами (кислород, галогены), а также сложными веществами с ярко выраженной окислительной функцией, например, серной и азотной концентрированной кислотами:
Также сера взаимодействует при кипячении с концентрированными водными растворами щелочей. Взаимодействие протекает по типу диспропорционирования, т.е. сера одновременно и понижает, и повышает свою степень окисления:
Источник
Сера
Элемент сера 16S, как и кислород 8О, находится в главной подгруппе VI группы периодической системы элементов. Однако химия серы существенно отличается от химии кислорода. Это обусловлено следующими причинами:
1. В отличие от кислорода сера проявляет и окислительные, и восстановительные свойства.
2. В отличие от кислорода, имеющего постоянную валентность II и степень окисления в соединениях -2, сера – элемент с переменной валентностью и с переменной степенью окисления.
Характеристика элемента
16S1s22s22p63s23p4
Аr = 32,066
ЭО – 2,5
Изотопы: 32S (95,084 %); 34S (4,16 %); 33S и 36S (
Кларк в земной коре 0,05 % по массе. Формы нахождения:
1) самородная сера (свободная S);
2) S2- (H2S и сульфиды металлов);
3) S+6 (сульфаты Ва и Са);
4) в составе белков, витаминов.
Сера – типичный неметалл, р-элемент. Устойчивые С.О. в соединениях -2, +4, +6.
Отличительное свойство – способность образовывать прочные гомоатомные связи-S-S-S- что приводит к существованию линейных и циклических цепей.
Важнейшие S-содержащие вещества
S-2 | S0 | S+4 | S+6 |
восстановители | окислительно – восстановительная двойственность | окислители | |
H2S сероводород CS2 – сероуглерод | S, свободная сера, большое число аллотропов | SO2 сернистый ангидрид | SO3 |
Свободная сера
Аллотропные модификации серы: ромбическая – S8. Твердое кристаллическое вещество ли монно-желтого цвета; нерастворимо в воде, хорошо растворимо в сероуглероде, ацетоне, бензоле.
Моноклинная – S8. Существует при температуре около 950С. Отличается от ромбической взаимной ориентацией октаэдров в кристаллической решетке.
Пластическая. Длинные зигзагообразные цепи.
Получение серы
1. Извлечение самородной серы из ее месторождений
2. Переработка природных газов, содержащих H2S (окисление при недостатке О2).
3. В лаборатории серу получают взаимодействием SО2 и H2S в водном растворе:
SО2 + 2H2S = 3S↓ + 2H2О
Химические свойства серы
При обычной температуре твердофазная сера малореакционноспособна. Однако при нагревании, и особенно в расплавленном состоянии, сера ведет себя как очень химически активное вещество
Сера – окислитель:
S + 2e- = S2-
Для завершения октета на внешнем слое атомы серы принимают недостающие 2 электрона и в состоянии S2- образуют ионные и ковалентные связи с водородом, металлами и некоторыми неметаллами.
1) Сера непосредственно соединяется с большинством Me (кроме Pt, Au), образуя сульфиды. С некоторыми Me реакция протекает при обычной температуре, например:
S + Сu = CuS
S + 2Ag = Ag2S
S + Hg = HgS
С железом и многими другими Me сера реагирует при нагревании:
S + Fe = FeS
S + Н2 = H2S сероводород
2S + С = CS2 сероуглерод
3S + 2Р = P2S3 сульфид фосфора (III)
Сера – восстановитель:
S – 4e- = S+4; S – 6e- = S+6
В соединениях с более ЭО элементами атомы серы находятся в положительно заряженном состоянии.
Непосредственно сера не взаимодействует с азотом и йодом.
Практически важными являются реакции соединения серы с кислородом. При обычных условиях сера горит на воздухе, окисляясь кислородом до диоксида серы:
S + O2 = SO2
Высший оксид SO3 образуется при окислении серы или SO2 кислородом в присутствии катализаторов:
2S + 3O2 = 2SO3 триоксид серы (оксид серы (VI)).
Сера непосредственно соединяется с фтором (при обычной температуре) и с хлором (расплавленная сера):
S + 3F2 = SF6 гексафторид серы
2S + Cl2 = S2CI2 дитиодихлорид серы
S2Cl2 + Cl2 = 2SCI2 дихлорид серы
Сильные окислители (HNO3, H2SO4 конц., К2Сr2O7 и др.) окисляют свободную серу до SO2 или H2SO4:
S + 2HNO3(разб.) = H2SO4 + 2NO↑
S + 6HNO3(конц.) = H2SO4 + 6NO2↑ + 2Н2O
S + 2H2SO4(конц.) = 3SO2↑ + 2Н2O
S + К2Сr2O7 = Сr2O3 + K2SO4
Диспропорционирование серы в растворах щелочей
3S+ 6NaOH = 2Na2S + Na2SO3 + 3Н2O
Источник
2. Химические свойства соединений серы с точки зрения изменения степеней окисления
В данном разделе реакции выходят за рамки ЕГЭ, но также являются полезными.
Правило 2.1. Соединения S+4 преимущественно проявляют восстановительные свойства при взаимодействии с большинством окислителей, т.е. довольно легко окисляются до S+6 :
С такими окислителями как кислород, пероксид водорода и оксиды азота:
2SO2 + O2 → 2SO3 (t, kt = V2O5)
SO2 + H2O2 → H2SO4
С солями Fe+3 и Cu+2:
SO2 + 2FeCl3 + 2H2O → 2FeCl2 + H2SO4 + 2HCl
SO2 + 2CuCl2 + 2H2O → 2CuCl + H2SO4+ 2HCl
С растворами галогенов (кроме F2):
SO2 + Cl2 + H2O → H2SO4 + 2HCl
SO2 + Br2 + H2O → H2SO4 + 2HBr
SO2 + I2 + H2O → H2SO4 + 2HI
С раствором перманганата калия в различных средах:
5SO2 + 2KMnO4 +2H2O → 2MnSO4 + K2SO4 + 2H2SO4
SO2 + 2KMnO4 + 4KOH → 2K2MnO4 +K2SO4 + 2H2O
Примеры реакций окисления сульфита натрия до сульфата различными окислителями:
Na2SO3 + Cl2 + H2O → Na2SO4 + 2HCl
Na2SO3 + H2O2 → Na2SO4 + H2O
Na2SO3 + H2SO4(к) → Na2SO4 + SO2 + H2O
5Na2SO3 + 2KMnO4 + 3H2SO4 → 5Na2SO4 + 2MnSO4 + K2SO4 + 3H2O
3Na2SO3 + 2KMnO4 + H2O → 2Na2SO4 + 2MnO2 + 2KOH
Na2SO3 + 2KMnO4 + 2KOH → Na2SO4 + 2K2MnO4 + H2O
3Na2SO3 + K2Cr2O7 + 4H2SO4 → 3Na2SO4 + Cr2(SO4)3 + K2SO4 + 4H2O
3Na2SO3 + K2Cr2O7 + 4H2O → 3Na2SO4 + 2Cr(OH)3 + 2KOH
Только очень сильными восстановителями S+4 восстанавливается до S0:
SO2 + 2H2S → 3S + 2H2O
SO2 + 2C → S + 2CO2
SO2 + 4HI → S + 2I2 + 2H2O
SO2 + 2CO → S + 2CO2 (Al2O3, 500°C)
Серная кислота (конц.)
Правило 2.2.
- При взаимодействии H2SO4(к) со слабыми восстановителями (неметаллами: S, P, C, средне- и малоактивными металлами: Fe, Cu, Ag, сложными веществами: H2S, сульфидами металлов, солями Fe2+ и т.д.) образуются SO2 и H2O.
- При взаимодействии H2SO4(к) с сильными восстановителями (активными металлами: Li-Zn, некоторыми сложными веществами: HI, KI) образуются H2S или S.
4Zn + 5H2SO4(конц.) → 4ZnSO4 + H2S + 4H2O (возможно образование SO2 и S, так как Zn – хороший восстановитель)
2Fe + 6H2SO4(конц.) → Fe2(SO4)3 + 3SO2 + 6H2O (только при нагревании)
Al, Cr, Fe пассивируются холодной концентрированной серной кислотой (т.е. покрываются оксидной пленкой, препятствующей дальнейшей реакции). Реакции идут только при нагревании.
C + H2SO4(конц.) → CO2 + 2SO2 + 2H2O (t)
S + H2SO4(конц.) → 3SO2 + 2H2O (t)
2P + 5H2SO4(конц.) → 2H3PO4 + 5SO2 + 2H2O (t)
Из галогеноводородов концентрированная серная кислота может окислить только ионы Br– и I– :
HF + H2SO4(конц.) → реакция не идет
HCl + H2SO4(конц.) → реакция не идет
2HBr + H2SO4(конц.) → Br2 + SO2 + 2H2O
8HI + H2SO4(конц.) → 4I2 + H2S + 4H2O
2CuI + 4H2SO4(конц.) → 2CuSO4 + I2 + 2SO2 + 4H2O
2CrCl2 + 4H2SO4(конц.) → Cr2(SO4)3 + SO2 + 4HCl + 2H2O
Соли меди восстанавливают кислоту до SO2, тогда как соли активных металлов до H2S:
2CuI + 4H2SO4(конц.) → 2CuSO4 + I2 + 2SO2 + 4H2O
8KI + 5H2SO4(конц.) → 4K2SO4 + 4I2 + H2S + 4H2O
Примеры реакций с солями (окисляем анион):
4H2SO4(конц., гор.) + CuS → CuSO4 + 4SO2 + 4H2O
Примеры реакций с солями (окисляем катион):
2H2SO4(к) + 2FeSO4 → Fe2(SO4)3 + SO2 + 2H2O
4H2SO4 + 2CrCl2 → Cr2(SO4)3 + SO2 + 4HCl + 2H2O
Правило 2.3. Окисление соединений S–2 до S+6 происходит под действием следующих окислителей: H2O2, Cl2(водн.), HNO3(конц.):
H2S + Cl2 + 4H2O → H2SO4 + 8HCl
PbS + 4H2O2 → PbSO4 + 4H2O (черный сульфид свинца превращается в белый сульфат)
H2S + 8HNO3(конц.) → H2SO4 + 8NO2 + 4H2O (образование S будет считаться ошибкой!)
CuS + 8HNO3(конц., гор.) → CuSO4 + 8NO2 + 4H2O
Na2S + 8HNO3(конц, гор.) → Na2SO4 + 8NO2 + 4H2O
С H2SO4(к) при нагревании сероводород и сульфиды реагируют с образованием SO2, аналогично реакции кислоты с серой:
S + H2SO4(конц.) → 3SO2 + 2H2O (t)
H2S + 3H2SO4(конц.) → 4SO2 + 4H2O (t)
CuS + 4H2SO4(конц., гор.) → CuSO4 + 4SO2 + 4H2O
K2S + 4H2SO4(конц.) → K2SO4 + 4SO2 + 4H2O
В этой реакции сульфид-ион окисляется до SO2: S–2 -6e → S+4.
Часть сульфат-ионов восстанавливается также до SO2 и часть остается для образования соли K2SO4.
Без нагревания возможна реакция:
K2S + 2H2SO4 → S + SO2 + K2SO4 + 2H2O
Источник: лекция на youtube.com от разработчиков экзамена “Методические рекомендации по подготовке ЕГЭ по химии”, время 49:52.
Правило 2.4. Сера в степени окисления -2 может быть окислена до простого вещества галогенами (Cl2, Br2, I2) или солями Fe+3, Mn+7 и Cr+6 :
1. Реакции с Cl2, Br2 и I2:
H2S + Cl2 (газ) → S + 2HCl
H2S + Br2 → S + 2HBr
H2S + I2 → S + 2HI
2. Реакции с солями Fe+3, Mn+7 и Cr+6:
3H2S + 2FeCl3 → S + 2FeCl2 + 2HCl
5H2S + 2KMnO4 + 3H2SO4 → 5S + 2MnSO4 + K2SO4 + 8H2O
3H2S + 2KMnO4 → 3S + 2MnO2 + 2KOH + 2H2O
3H2S + 2KMnO4 + 2CO2 → 3S + 2MnO2 + 2KHCO3 + 2H2O
3H2S + K2Cr2O7 + 4H2SO4 → 3S + Cr2(SO4)3 + K2SO4 + 7H2O
3H2S + 2K2CrO4 + 2H2O → 3S + 2Cr(OH)3 + 4KOH
3H2S + 2HMnO → 3S + 2MnO2+ 4H2O
3K2S + 2KMnO4 + 4H2O → 3S + 2MnO2 + 8KOH
3H2S + Na2Cr2O7 + 4H2SO4 → 3S + Cr2(SO4)3 + Na2SO4 + 7H2O
3Na2S + K2Cr2O7 + 7H2SO4 → 3S + Cr2(SO4)3 + K2SO4 + 3Na2SO4 + 7H2O
3(NH4)2S + K2Cr2O7 + 7H2SO4 → 3S + Cr2(SO4)3 + K2SO4 + 3(NH4)2SO4 + 7H2O.
Согласно разработчикам экзамена (Вебинар “Методические рекомендации по подготовке к ЕГЭ по химии от разработчиков“, время 33:41, ссылка естьв разделе “О проекте”), окисление сульфид-ионов протекает с образованием S0, но образование сульфат-иона (в реакциях с такими сильными окислителями, как KMnO4, K2Cr2O7) также будет засчитано как правильный ответ.
Источник
