Составить кроссворд о свойствах и применении какого либо вещества
Часть I
1. Химия изучает:
– вещества
– их строение
– их свойства
2. Вещество – это то, из чего сделаны физические тела.
3. Признаки, по которым одни вещества отличаются от других, – это свойства, например: водород – газ, лёгкий, без запаха, цвета, вкуса.
4. Существует взаимосвязь: свойство вещества – применение вещества.
Например, для стекла:
1) прозрачное – используют в качестве оконных стёкол
2) изготовление хрусталя
3) витражное стекло
5. Вещества состоят из молекул, которые, в свою очередь, образованы из атомов. Определённый вид атомов называют химическим элементом. Всего известно 119 химических элементов.
6. Химический элемент существует в трёх формах.
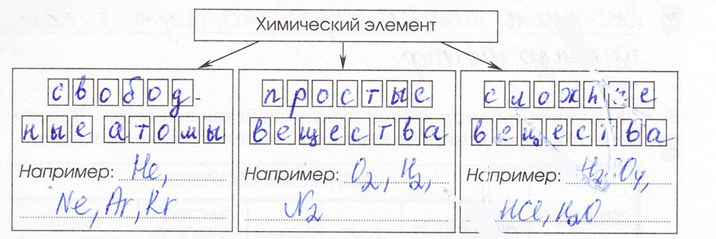
Простые вещества – это вещества, образованные атомами одного и того же химического элемента.
Вещества, образованные из двух и более химических элементов, называются сложными.
Часть II
1. Установите соответствие между понятием и примером.

Ответ:
А – 1, 3, 5.
Б – 2, 4, 6.
2. Вычеркните «лишнее»:
Колба, пробирка, химический стакан, мензурка, ступка, мерный цилиндр, кристаллизатор.
Укажите признак, общий для оставшихся объектов.
Химическая посуда, сделанная из стекла.
3. Составьте задание, аналогичное предыдущему.
Вычеркнуть лишнее: пипетка, пробирка, резиновая груша, фильтровальная бумага, мерная колба, мензурка.
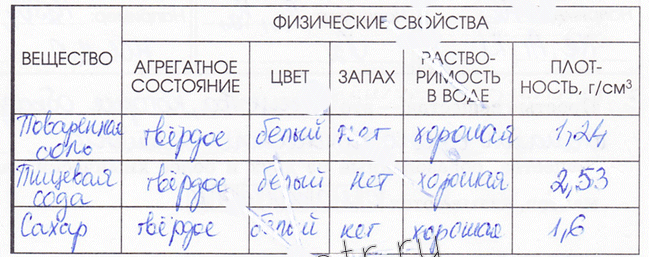
4. Заполните таблицу «Физические свойства веществ». В качестве примеров опишите вещества, используемые на кухне.
5. Укажите прилагательные, которые характеризуют свойства воды.
1) жидкая
3) бесцветная
4) прозрачная
6. Заполните таблицу «Сравнение физических свойств газообразных веществ».

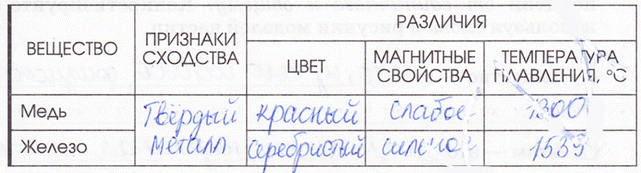
7. Заполните таблицу «Сравнение физических свойств меди и железа».
8. Составьте кроссворд о свойствах и применении какого-либо вещества (по своему выбору).
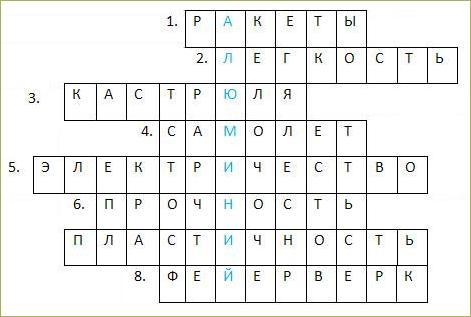
1. Аппарат, при производстве которого используются сплавы алюминия.
2. Физическое свойство алюминия, которое позволяет использовать его сплавы в самолетостроении.
3. Емкость для приготовления пищи методом варки, сделанная из алюминия.
4. Воздушное судно, предназначенное для полетов в атмосфере, при производстве которого используются сплавы алюминия.
5. Благодаря теплопроводности и способности проводить это, алюминий используется для изготовления электрических проводов.
6. Физическое свойство алюминия, которое наряду с легкостью, позволяет использовать его сплавы в ракето- и самолетостроении.
7. Это физическое свойство металла позволяет делать из алюминия фольгу.
8. Свойство алюминия гореть ослепительным пламенем применяется для получения этих декоративных праздничных огней.
9. На примере химического элемента водорода укажите правильную последовательность (1-2-3) перечисленных понятий от единичного к общему. Конкретизируйте её, используя слова и рисунки моделей частиц.
3) Вещество – это то, из чего состоят физические тела.
1) Атом – это химически неделимая частица.
2) Молекула – это наименьшая частица вещества, обладающая его свойствами.
10. Выражения, являющиеся синонимами понятия «химический элемент».
1) вид одинаковых атомов
3) вид атомов, имеющих одинаковые свойства.
11. Установите соответствие между формой существования химического элемента и рисунками моделей частиц.
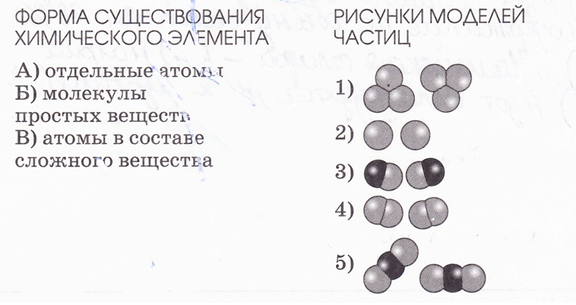
Ответ:
А-2;
Б-1, 4;
В-3, 5.
12. Проанализируйте рисунки и впишите пропущенные слова.
На рисунках изображено две молекулы сложных веществ, образованных из двух химических элементов.
13. Отметьте фразы, в которых говорится о сере как о химическом элементе. Из букв, соответствующих правильным ответам, вы составите название химического элемента, соединения которого используют для обеззараживания воды: хлор.
2) сера входит в состав молекул серной кислоты – Х
3) некоторые белки содержат серу – Л
5) молекулы сероводорода образованы серой и водородом – О
7) молекулы серы состоят из 8 атомов – Р
В тех фразах, которые вы не выбрали, речь идёт о сере как о простом веществе.
Сохраните или поделитесь с одноклассниками:
Источник
Генератор титульных листовТаблица истинности ONLINE |
|
Источник
Составление кроссворда по химии
Кроссворд – одна из форм самостоятельной работы обучающихся во внеурочное время, которая предполагает работу с дополнительной научной литературой.
Дидактические задачи:
– повышение интереса обучающихся к изучаемой дисциплине;
– активизация мыслительной деятельности обучающихся;
– закрепление специальной терминологии и частичное решение проблемы грамотного написания используемых слов: обучающихся заучивают или проговаривают сложные и непонятные слова, а все термины в кроссворде должны писаться без грамматических ошибок;
– расширение кругозора обучающихся;
– раскрытие творческого потенциала обучающихся.
Можно использовать разные виды кроссворда:
· Классический. Разгадывания кроссворда по заданиям.
· Кроссворд заполненный. Обучающийся дает краткие формулировки предложенных терминов и понятий.
· Кроссворд обучающихся составляют сами по заданной теме (индивидуально, в паре или в малой группе).
· Кроссворд с ключевым словом.
Кроссворды применяются для обучения, контроля и коррекции знаний.
Рекомендации к составлению и оформлению тематического кроссворда
I. Составление кроссворда:
1. Получить тему кроссворда от учителя.
2. В библиотеке подобрать литературу по данной теме.
3. Составить вопросы, чтобы они имели правильную формулировку (можно проконсультироваться с учителем).
4. Распределить вопросы по горизонтали и вертикали, т.е. составить кроссворд графически таким образом, чтобы количество клеток соответствовало количеству букв в слове – ответе.
5. После составления кроссворда необходимо осуществить проверку, т. е. составитель сам отвечает на вопросы кроссворда и заполняет его (для этого делают кроссворд-черновик).
II. Оформление кроссворда:
1. Первый лист: по середине листа – тема кроссворда, в нижнем правом углу – Ф.И.О. автора.
2. Второй лист: вопросы по горизонтали и вертикали.
3. Третий лист: графическое изображение кроссворда.
4. Четвертый лист: приложение с ответами.
Все листы формата А 4.
Кроссворд по разделу «Органическая химия» по теме «Углеводороды»
По горизонтали: 1.Способность атомов химического элемента образовывать связи с другими атомами. 2. Процесс присоединения водорода. 3. Процесс отщепления водорода 4. Предельные углеводороды, молекулы которых способны замещать один или несколько атомов водорода. 5. Вещества, сходные по составу, но отличающиеся по строению и свойствам 6. Явление, при котором могут существовать несколько веществ, имеющих один и тот же состав и одну и ту же молекулярную массу, но отличающихся строением молекул. 7. Ароматические углеводороды. 8. Процесс смешивания электронных облаков. 9. Вещество, из которого образуется бензол (по доказательству Земского) | По вертикали: 10. Разновидность ковалентной связи, образующаяся при перекрывании электронных облаков по линиям, связывающих центры атомов. 11. Вещества, имеющие сходное строение и свойства, но отличаются по составу на СН2- группу. 12. Органические соединения, в молекулах которых присутствуют атомы углерода и водорода. 13. Реакции характерные для алканов. 14. Процесс соединения многих одинаковых молекул в одну более крупную. 15. Частицы, имеющие один неспаренный электрон. 16. Непредельные углеводороды, в молекулах которых содержится одна тройная связь. 17. Непредельные углеводороды, молекулы которых содержат одну двойную связь. 18. Бесцветная, нерастворимая в воде жидкость со своеобразным запахом 19. Учёный, создавший теорию химического строения органических веществ. 20. Форма молекулы метана в пространстве. |
Источник
Генератор титульных листовТаблица истинности ONLINE |
|
Источник
