Сколько молекул содержится в 1 л воды и какой объем при нормальных условиях
Молекулы вступают в реакцию в определённых соотношениях, и это описывают химические реакции. Например, из этого уравнения
2Н2 + О2 = 2Н2О
видно, что в реакции приняли участие 2 молекулы водорода и 1 молекула кислорода, образовав при этом 2 молекулы воды. Но молекула так малы, что увидеть их невозможно, и уж тем более нельзя взять их в руки. Поэтому в учебнике химии и появляется понятие моль – количество вещества, в котором содержится число Авогадро частиц (6,02*10 в двадцать третьей степени). Рядом с этим понятием стоит другое – молярная масса, то есть масса 1 моля частиц. Молярная масса совпадает с атомной или молекулярной, рассчитывается по таблице Менделеева и выражается в граммах на моль (г/моль).
Фото: pixabay.com
Но мы прекрасно знаем, что не все вещества в обычных условиях находятся в твёрдом или жидком состоянии. Например, кислород, азот, хлор, неон – это газы. Резонно спросить: а как же их взвешивать? На этот случай химии для 8 класса припасено ещё одно понятие – молярный объём.
Что такое молярный объём
Тут следует запомнить, что в обычных условиях 1 моль любого газа занимает одинаковый объём. То есть молярный объём – это объём 1 моля любого газа. Сейчас советую на всякий случай вспомнить, что в 1 моле любого вещества (в том числе газа) содержится число Авогадро частиц. Старайтесь не забывать об этом факте.
Теперь надо обязательно упомянуть следующее. Все знают, что при изменении температуры и давления объём газов меняется. Так вот чтобы все расчёты вести правильно, то есть в одинаковых условиях, говорят о нормальных условиях: температуре 0 градусов Цельсия и давлении в 1 атмосферу (или 101,3 кПа). Это нужно просто запомнить:
нормальные условия в химии: температура – 0 градусов Цельсия, давление – 1 атм.
Экспериментально было доказано, что в нормальные условиях 1 моль любого газа занимает объем 22,4 литра.
То есть молярный объём любого газа в н.у. составляет 22,4 л/моль.
И это число тоже нужно запомнить! Оно даже важнее, чем сами нормальные условия, потому используется это число в решениях по химии намного чаще, чем н.у. (нормальные условия).
Как найти молярный объём
Очень просто. Если молярную массу для каждого вещества нужно рассчитывать по таблице Менделеева, то
молярный объём для всех газов одинаков.
Пример 1.
Молярная масса воды Н2О 18 г/моль (2*1+16, всё берем из периодической таблицы), молярная масса оксида кальция СаО 56 г/моль (40+16), молярная масса серной кислоты Н2SO4 98 г/моль (2*1+32+4*16).
Зато в нормальных условиях молярный объём кислорода О2 22,4 л/моль, молярный объём фтора P2 22,4 л/моль, молярный объём ксенона 22,4 г/моль. Приятно, не правда ли?
Другое дело, если речь идёт о химических реакциях. Но для начала просто потренируемся с цифрами.
Пример 2.
Определите объём, который занимают 10 моль кислорода в н.у.
Решение:
Молярный объём кислорода 22,4 л/моль, то есть 1 моль занимает 22,4 л. Следовательно, 10 моль будут занимать в 10 раз больше 22,4*10=224 литра. Это и есть ответ: 10 моль кислорода займут объём 224 литра.
Пример 3.
Известно, что неон в н.у. занял объём 5,6 литра. В каком количестве взят неон (в молях)?
Решение:
1 моль занимает объём 22,4 литра, а вот неизвестное число моль заняло объём 5,6 литра. Можно составить пропорцию:
1 моль – 22,4 литра
Х моль – 5,6 литра
Отсюда Х=1*5,6/22,4=0,25. Значит ответ такой: неон взяли в количестве 0,25 моль.
Пример 4.
Это уже расчёт по химической реакции, поэтому будьте внимательны. Итак, хлор прореагировал с водородом с образованием хлорида водорода:
Н2 + Cl2 = 2HCl
Для реакции взяли 11,2 литра водорода. Сколько понадобилось хлора (н.у.)?
Решение:
Посмотрим, сколько нам дано водорода по условию задачи. 1 моль водорода занимает объём 22,4 литра. Но у нас всего 11,2 литра водорода, то есть Х моль. Составим пропорцию:
1 моль – 22,4 литра
Х моль – 11,2 литра
Отсюда Х=1*11,2/22,4=0,5 моль водорода. Значит, по условию задачи у нас водорода 0,5 моль.
Из уравнения химической реакции Н2 + Cl2 = 2HCl видно, что нам нужно по 1 молю водорода и хлора (об этом говорят коэффициенты в уравнении). То есть, 1 моль водорода реагирует с 1 молем хлора. Но нам дали всего 0,5 моль водорода, сколько нам нужно хлора? Составим ещё одну пропорцию:
1 моль водорода реагирует с 1 молем хлора
0,5 моль водорода реагирует с Х молями хлора.
Отсюда получаем: Х=0,5*1/1=0,5 моль. Таким образом, нам нужно 0,5 моль хлора. А это количество занимает объём 22,4*0,5=11,2 литра.
Ответ: понадобилось 11,2 литра хлора.
В следующий раз мы научимся делать расчёты по реакциям, в которых участвуют и твёрдые вещества, и газы, то есть одновременно будем использовать молярную массу и молярный объём.
Пишите, пожалуйста, в комментариях, что осталось непонятным, и я обязательно дам дополнительные пояснения. Жалуйтесь на сложности в изучении школьного курса и говорите, что вас испугало в учебнике химии. И тогда следующая статья будет рассказывать именно об этой проблеме.
Источник
Решениие задач по химии на закон Авогадро
Задача 53.
Сопоставить числа молекул, содержащихся в 1г NH3 и в 1г N2. В каком случае и во сколько раз число молекул больше?
Решение:
В одном моле любого вещества содержится 6,02 . 1023 молекул этого вещества.
Рассчитаем содержание количества вещества в 1г NH3 и N2 по формуле:
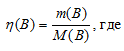
 (B) – количество вещества (В);
(B) – количество вещества (В);
m(B)- масса вещества (В);
M(B) – Молярная масса вещества (В).
М(NH3) = 17г/моль, M(N2) = 28г/моль.
Тогда
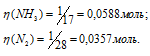
Число молекул NH3 больше числа молекул N2, так как  (NH3) >
(NH3) > (N2) . Теперь рассчитаем, во сколько раз число молекул NH3 больше числа молекул N2:
(N2) . Теперь рассчитаем, во сколько раз число молекул NH3 больше числа молекул N2:
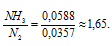
Ответ: в 1,65 раз число молекул NH3 больше числа молекул N2.
Задача 54.
Выразить в граммах массу одной молекулы диоксида серы.
Решение:
Находим молекулярную массу диоксида серы:
M(SO2) = 32 + (16 . 2) = 64г/моль.
Молекулярная масса численно составляет массу одного моля вещества, а значит, вес одного моля численно равен молекулярной массе и составляет 64г. Известно, что в одном моле любого вещества содержится 6,02 . 1023 молекул данного вещества. Исходя из этого, рассчитаем массу в граммах одной молекулы диоксида серы:
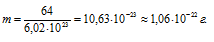
Ответ: масса одной молекулы диоксида серы равна.
Задача 55.
Одинаково ли число молекул в 0,001кг Н2 и в 0,001кг О2? В 1 моле Н2 и в 1 моле 02? В 1л Н2 и в 1л О2 при одинаковых условиях?
Решение:
Молекулярные массы водорода и кислорода равны соответственно 2г/моль и 32г/моль. Отсюда находим количество водорода и кислорода, зная их массы:
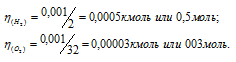
Один моль любого вещества содержит 6,02 .1023 молекул. Следовательно, в 0,001кг водорода и в 0,001кг кислорода содержится разное число молекул:

Так как имеется по одному молю водорода и кислорода, то количество молекул веществ будет одинаково:
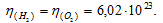
Согласно закону Авогадро в равных объёмах любых газов, взятых при одинаковых условиях, содержится одинаковое число молекул, Один моль любого газа занимает 22,4л, В которых содержится 6,02 . 1023 молекул. Отсюда рассчитаем количество молекул вещества, содержащихся в 1л водорода и в 1л кислорода:
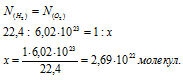
Ответ: а) в 0,001кг водорода и в 0,001кг кислорода содержится разное число молекул; б) в одном моле водорода и в одном моле кислорода содержится одинаковое число молекул: в) в одном литре водорода и в одном литре кислорода содержится одинаковое число молекул.
Задача 56.
Сколько молекул содержится в 1,00 мл водорода при нормальных условиях?
Решение:
Согласно закону Авогадро в равных объёмах любых газов, взятых при одинаковых условиях, содержится одинаковое число молекул, Один моль любого газа занимает 22,4л, В которых содержится 6,02 .1023 молекул. Отсюда рассчитаем количество молекул вещества, содержащихся в 1мл водорода из пропорции:
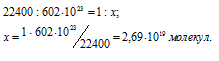
Ответ: 2,69 .1019 молекул.
Задача 57.
Какой объем при нормальных условиях занимают 27 .1021 молекул газа?
Решение:
Согласно закону Авогадро в равных объёмах любых газов, взятых при одинаковых условиях, содержится одинаковое число молекул, Один моль любого газа занимает 22,4л, В которых содержится 6,02 . 1023 молекул. Отсюда находим какой объём при нормальных условиях занимают 27 .1021 молекул газа, составив пропорцию:
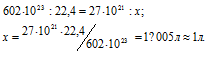
Ответ: V=1л.
Задача 58.
Каково соотношение объемов, занимаемых 1 молем О2 и 1 молем О3 (условия одинаковые)?
Решение:
Согласно закону Авогадро в равных объёмах любых газов, взятых при одинаковых условиях, содержится одинаковое число молекул, Один моль любого газа занимает 22,4л. Следовательно соотношение объёмов, занимаемых одним молем О2 и одним молем О3 иметь вид:
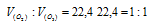
Ответ: 1:1
Задача 59.
Взяты равные массы кислорода, водорода и метана при одинаковых условиях. Найти отношение объемов взятых газов.
Решение:
Согласно закону Авогадро в равных объёмах любых газов, взятых при одинаковых условиях, содержится одинаковое число молекул, Один моль любого газа занимает 22,4л. Мольные массы кислорода, водорода и метана, соответственно равны 32 г/моль; 2г/моль; 16 г/моль.
Так как массы кислорода, водорода и метана одинаковы при одинаковых условиях, то отношение объёмов взятых газов находим из пропорции:
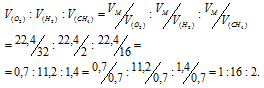
Ответ: 1:16:2.
Задача 60.
На вопрос, какой объем займет 1моль воды при нормальных условиях, получен ответ: 22,4л. Правильный ли это ответ?
Решение:
Согласно закону Авогадро в равных объёмах любых газов, взятых при одинаковых условиях, содержится одинаковое число молекул, Один моль любого газа занимает 22,4л. Так как вода при нормальных условиях находится в жидкой, а не в газообразной фазе, то ответ, что 1моль воды займёт 22,4л не правильный. Учитывая, что молярная масса воды равна 18г/моль, а плотность равна единице, то правильный ответ будет равен:
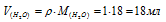
Ответ: 18мл.
Задача 61.
Сколько молекул диоксида углерода находится в 1л воздуха, если объемное содержание СО2 составляет 0,03% (условия нормальные)?
Решение:
При нормальных условиях углекислый газ, содержащийся в 1л воздуха, занимает объём 0,0003л. Зная, что мольный объём любого газа занимает 22,4л, рассчитаем число молей углекислого газа в 0,0003л из пропорции:
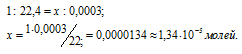
Учитывая, что в одном моле вещества содержится 6,02 . 1023 молекул, находим число молекул в 0,0003л газа:

Ответ: 8,07 .1018 молекул.
Источник
Анонимный вопрос
10 января 2018 · 5,9 K
Книги, звери и еда – это хобби навсегда.
1 моль любого вещества содержит Na=6*10^23 молекул. Формула воды H2O, ее молярная масса составляет М=18 г, следовательно, в m=180 мг=0.18 г содержится N=Na*m/M=6*10^23*0.18/18=6*10^21 молекул.
Примерно сколько атомов гелия содержится в 4 кг гелия?
Молодой-исследовать в области химии и ядерной физики ускорителей частиц, г. Падуя, Италия. · tele.click/real_italy
К уже правильному ответу предложу свое решение, для тех кто предпочитает формульные решения.
n = m/M = N / Na = V / Vm
где n – кол моль вещества
m – масса вещества – в г
M – молекулярная масса (в нашем случаи атомная масса) в г/моль
N – колл. составляющих (атомов или молекул)
Na – число Авгодаро 6,022 * 10^23
V – обьем в л
Vm – молекулярный обьем 22,4 л/моль
С помощью этой формулы можно решить очень много задач школьной химии
Подставляем известные и выражаем неизвестную величины:
N = (m * Na)/M = 4000г * 6,022 * 10^23 ) / 4 г/моль = 6,022 * 10^26
Прочитать ещё 2 ответа
Сколько весят 150 молекул воды?
Чтобы найти массу 150 молекул воды, найдём сперва массу одной молекулы, а затем умножим её на 150. Молекула воды состоит из двух атомов водорода и одного атома кислорода (это видно по формуле — H₂O). Атом водорода имеет массу 1 а. е. м. (атомная единица массы), кислорода — 16 а. е. м. (эти значения приведены в таблице Менделеева). Тогда масса целой молекулы воды составит 18 а. е. м., а 150 молекул — 150 × 18 а. е. м. = 2700 а. е. м., что, к слову, приблизительно равно 4,48 × 10⁻²¹ г (т. е. 0,00000000000000000000448 г).
Почему атомы кислорода активнее, чем молекулы кислорода?
Молекула кислорода появляется по очень простоя причине. – Активные атомы кислорода объединяются в эту молекулу и получается значительно менее активная конструкция. Если кислород (уже молекулярный) объединить с водородом, получится еще менее активная конструкция типа Н2О. Ей можно даже реакцию окисления остановить. Такая вот жизнь у молекул и атомов. – Активные чаще превращаются в не активных, чем наоборот. Обратный процесс идет уже с использованием энергии. Можно сказать, накачка энергии в молекулу расщепляет её на атомы. Каковые несут в себе ту закачанную энергию и рвутся её использовать для соединений с другими атомами, или молекулами. При этом энергию еще и выделяют. В частности, в виде тепла и света. Например, накачка энергии в уже существующие молекулы в процессе фотосинтеза, в котором свет используется для расщепления ранее сформированных молекул. Так что ответ простой – молекула кислорода активна меньше, чем отдельный атом потому, что она образована за счет активности атома. Она как бы ту активность уже скушала. Здесь примерно такая же история как с бизонами в Северной Америке и тем, что осталось от них.
Другими словами, можно было сказать наоборот. – Это не атом активен больше, чем молекула. А просто молекулы менее активны чем атомы. Потому и возникают. Но могут быть расщеплены на атомы. Атомы же существуют вечно. Вместе со свойственной им активностью. Потому и образуют множество молекул, минералов… Которые снова распадаются на атомы, давая начало другим многоатомным соединениям. Исключение составляют атомы инертных газов. Но, это не принципиально. И инертные газы тоже вступают в различные соединения. Только реже. Есть еще благородные металлы. Они меньше вступают в реакцию именно с кислородом. Однако, водку любят все. Если она царская. Потому и получили общее название “благородных”. 🙂
Сколько молекул содержится в 2,5 моль кислорода?
Инженер по профессии, люблю спорт, музыку, кино.
В одном моле любого вещества всегда содержится одно и тоже число молекул, называемое числом Авогадро:
Na = 6.02*10^23
Тогда в n=2,5 моль кислорода содержится молекул:
N = n*Na = 2.5*6.02*10^23 = 15.05*10^23
Источник
![]()
сколько молекул содержится в 1 л воды
1 ответ:
![]()
2
0
Рассчитывать эту цифру следует исходя из химической формулы воды (аш два о) Н2О, у водорода 1 моль будет равен одному грамму, а у кислорода 16 граммов, следовательно, у воды 18 граммов (2 водорода и один кислород) и вода имеет 18 граммов молярной массы на 1 моль.
В одном литре воды 1000 граммов, их разделить на 18 граммов, результат = 55,56 моль, эту цифру умножить на число Авогадро, равное 6, 22 х 10 в 23 степени, перемножив получим:
3,3336 х 10 в 25 степени – количество молекул в 1 литре воды
Конечно, самый простой расчёт всегда для воды, потому что самое знакомое, понятное каждому вещество и не только тем, что более всего используется человеком, ещё потому, что всякий знает её формулу…
Читайте также
![]()
Плотность воды изменяется в зависимости от температкры. Наибольшую плотность вода имеет при температуре 4 градуса по Цельсию, при этом один литр воды весит 999,972 граима. Вода дистиллированная и деаэрированная. При 100 градусах литр воды весит на 41 грамм легче, а именно 958,365 грамма.
В практическом плане важнее не вес одного литра, а объем одного килограмма воды. Вода практически несжимаема и при охлаждении или нагревании ее в замкнутом объеме она может разрушить сосуд.
![]()
Ванны бывают разных размеров, например стандартные ванны размером 650х1500 вмещает 155 литров воды, а ванны 750х1700 вмещают 245 литров воды, но есть ванны и побольше туда входит 250-255 литров воды.
Сейчас очень много в продаже нестандартных ванн в форме ракушки, овальные, круглые, лотоса, там объем воды подсчитать невозможно, т.к. у каждого из этих товаров имеются свои документы, там и указывается количество вмещаемости воды, но везде по разному.

Джакузи также бывают разные, поэтому воду туда надо заливать выше верхнего ряда форсунок на 5 см.

![]()
Казалось бы – раз банка объемом в один литр, то и воды в ней (если наполнить ее полностью) будет тоже ровно столько же. Но, это далеко не так 1-литровая (и еще 0,5-литровая тоже) банка имеет так называемую каёмку – специальная линия, чуть ниже рифленых ободков для закручивания крышки:

Вода, налитая “в аккурат” по этой линии и дает объем в 1000 мл. Все, что свыше будет излишком, величина которого незначительна – примерно 25-30 мл.
![]()
Из восьми литровой банки 1 литр воды переливаем в трехлитровую банку. Из трехлитровой банки два литра переливаем в пятилитровую банку. В трехлитровой банке остается 1 литр.
![]()
Сначала нужно взять трех литровую банку и вылить воду в пяти литровое ведро. Затем налить еще трехлитровую банку и вылить из нее недостающие до пяти литров в ведре два литра. В банке останется 1 литр.
Выливаем из ведра всю воду и переливает в него этот один литр. А затем добавляем целую трехлитровую банку воды и в ведре получается 4 литра.
Источник
Жамалбек Ш.
31 января · 2,3 K
1 моль газа при н.у. занимает около 22 литров. Значит в 2 литрах содержится 1/11 моля, а так как в 1 моле содержится 6х10^23 молекул, то 1/11 от этого количества это ~5,5х10^22 молекул.
Почему атомы кислорода активнее, чем молекулы кислорода?
Молекула кислорода появляется по очень простоя причине. – Активные атомы кислорода объединяются в эту молекулу и получается значительно менее активная конструкция. Если кислород (уже молекулярный) объединить с водородом, получится еще менее активная конструкция типа Н2О. Ей можно даже реакцию окисления остановить. Такая вот жизнь у молекул и атомов. – Активные чаще превращаются в не активных, чем наоборот. Обратный процесс идет уже с использованием энергии. Можно сказать, накачка энергии в молекулу расщепляет её на атомы. Каковые несут в себе ту закачанную энергию и рвутся её использовать для соединений с другими атомами, или молекулами. При этом энергию еще и выделяют. В частности, в виде тепла и света. Например, накачка энергии в уже существующие молекулы в процессе фотосинтеза, в котором свет используется для расщепления ранее сформированных молекул. Так что ответ простой – молекула кислорода активна меньше, чем отдельный атом потому, что она образована за счет активности атома. Она как бы ту активность уже скушала. Здесь примерно такая же история как с бизонами в Северной Америке и тем, что осталось от них.
Другими словами, можно было сказать наоборот. – Это не атом активен больше, чем молекула. А просто молекулы менее активны чем атомы. Потому и возникают. Но могут быть расщеплены на атомы. Атомы же существуют вечно. Вместе со свойственной им активностью. Потому и образуют множество молекул, минералов… Которые снова распадаются на атомы, давая начало другим многоатомным соединениям. Исключение составляют атомы инертных газов. Но, это не принципиально. И инертные газы тоже вступают в различные соединения. Только реже. Есть еще благородные металлы. Они меньше вступают в реакцию именно с кислородом. Однако, водку любят все. Если она царская. Потому и получили общее название “благородных”. 🙂
Какой объем кислорода требуется для сжигания 56 л пропана?
Книги, звери и еда – это хобби навсегда.
Запишем уравнение горения пропана
С3H8+5*O2->3CO2+4*H2O
Из уравнения видно, что для сжигания 1 моль пропана требуется 5 моль кислорода. Поскольку оба вещества являются газами, то 56 л пропана составляет 56/22.4=2.5 моль, а требуемое количество кислорода составляет 2.5*5 = 12.5 моль, которое будет занимать 12.5*22.4=280 л.
Примерно сколько атомов гелия содержится в 4 кг гелия?
Молодой-исследовать в области химии и ядерной физики ускорителей частиц, г. Падуя, Италия. · tele.click/real_italy
К уже правильному ответу предложу свое решение, для тех кто предпочитает формульные решения.
n = m/M = N / Na = V / Vm
где n – кол моль вещества
m – масса вещества – в г
M – молекулярная масса (в нашем случаи атомная масса) в г/моль
N – колл. составляющих (атомов или молекул)
Na – число Авгодаро 6,022 * 10^23
V – обьем в л
Vm – молекулярный обьем 22,4 л/моль
С помощью этой формулы можно решить очень много задач школьной химии
Подставляем известные и выражаем неизвестную величины:
N = (m * Na)/M = 4000г * 6,022 * 10^23 ) / 4 г/моль = 6,022 * 10^26
Прочитать ещё 2 ответа
Сколько молекул содержится в 180 мг воды?
Книги, звери и еда – это хобби навсегда.
1 моль любого вещества содержит Na=6*10^23 молекул. Формула воды H2O, ее молярная масса составляет М=18 г, следовательно, в m=180 мг=0.18 г содержится N=Na*m/M=6*10^23*0.18/18=6*10^21 молекул.
Источник

