Сколько и каких орбиталей содержится в атоме углерода на внешнем электронном уровне

Углерод (С) – шестой элемент периодической таблицы Менделеева с атомным весом 12. Элемент относится к неметаллам и имеет изотоп 14С. Строение атома углерода лежит в основе всей органической химии, т. к. все органические вещества включают молекулы углерода.

Атом углерода
Положение углерода в периодической таблице Менделеева:
- шестой порядковый номер;
- четвёртая группа;
- второй период.
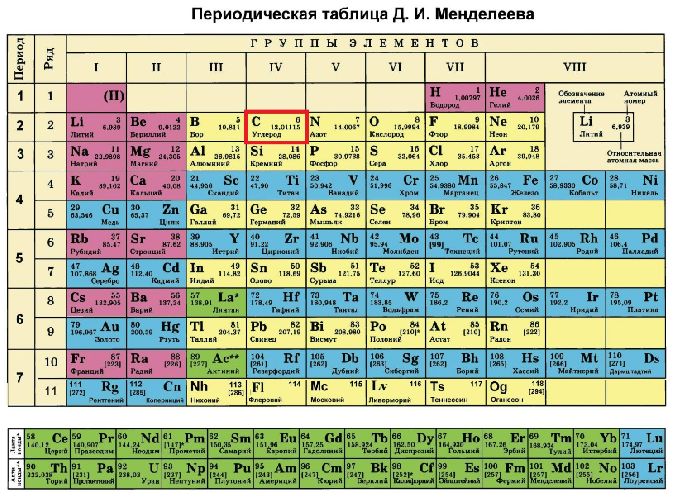
Рис. 1. Положение углерода в таблице Менделеева.
Опираясь на данные из таблицы, можно заключить, что строение атома элемента углерода включает две оболочки, на которых расположено шесть электронов. Валентность углерода, входящего в состав органических веществ, постоянна и равна IV. Это значит, что на внешнем электронном уровне находится четыре электрона, а на внутреннем – два.
Из четырёх электронов два занимают сферическую 2s-орбиталь, а оставшиеся два – 2p-орбиталь в виде гантели. В возбуждённом состоянии один электрон с 2s-орбитали переходит на одну из 2p-орбиталей. При переходе электрона с одной орбитали на другую затрачивается энергия.
Таким образом, возбуждённый атом углерода имеет четыре неспаренных электрона. Его конфигурацию можно выразить формулой 2s12p3. Это даёт возможность образовывать четыре ковалентные связи с другими элементами. Например, в молекуле метана (СН4) углерод образует связи с четырьмя атомами водорода – одна связь между s-орбиталями водорода и углерода и три связи между p-орбиталями углерода и s-орбиталями водорода.
Схему строения атома углерода можно представить в виде записи +6C)2)4 или 1s22s22p2.
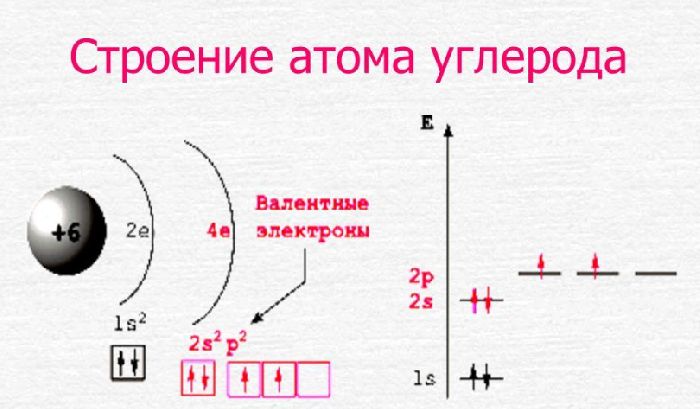
Рис. 2. Строение атома углерода.
Физические свойства
Углерод встречается в природе в виде горных пород. Известно несколько аллотропных модификаций углерода:
- графит;
- алмаз;
- карбин;
- уголь;
- сажа.
Все эти вещества отличаются строением кристаллической решётки. Наиболее твёрдое вещество – алмаз – имеет кубическую форму углерода. При высоких температурах алмаз превращается в графит с гексагональной структурой.
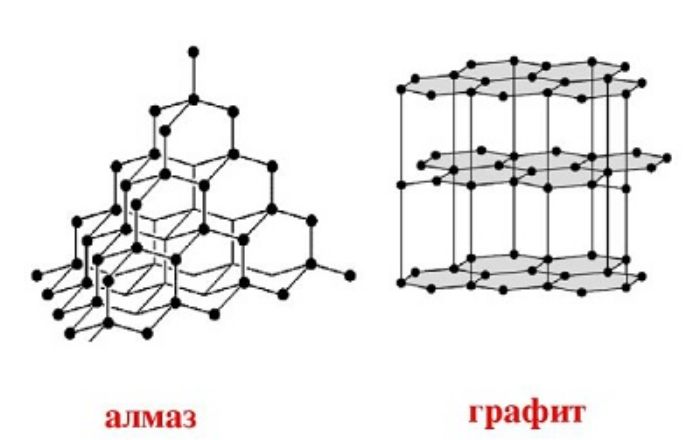
Рис. 3. Кристаллические решётки графита и алмаза.
Химические свойства
Атомное строение углерода и его способность присоединять четыре атома другого вещества определяют химические свойства элемента. Углерод реагирует с металлами, образуя карбиды:
- Са + 2С → СаС2;
- Cr + C → CrC;
- 3Fe + C → Fe3C.
Также реагирует с оксидами металлов:
- 2ZnO + C → 2Zn + CO2;
- PbO + C → Pb + CO;
- SnO2 + 2C → Sn + 2CO.
При высоких температурах углерод реагирует с неметаллами, в частности с водородом, образуя углеводороды:
С + 2Н2 → СН4.
С кислородом углерод образует углекислый газ и угарный газ:
- С + О2 → СО2;
- 2С + О2 → 2СО.
Угарный газ также образуется при взаимодействии с водой:
C + H2O → CO + H2.
Концентрированные кислоты окисляют углерод, образуя углекислый газ:
- 2H2SO4 + C → CO2 + 2SO2 + 2H2O;
- 4HNO3 + C → CO2 + 4NO2 + 2H2O.
Активность углерода возрастает при нагревании. При низких температурах элемент относительно стабилен.
Что мы узнали?
Углерод – типичный неметалл с шестью электронами на s- и р-орбиталях. В активном состоянии приобретает валентность IV и способен присоединять четыре атома вещества. Углерод может быть представлен в виде угля, сажи, графита, алмаза. Элемент реагирует с металлами, неметаллами, кислотами, кислородом, оксидами.
Тест по теме
Оценка доклада
Средняя оценка: 4.1. Всего получено оценок: 265.
Источник
Атом углерода — основа органических веществ, поэтому его электронное строение представляет особый интерес при изучении органической химии.
Углерод — первый элемент IV группы периодической системы элементов Д.И.Менделеева. Два его электрона (в состоянии Is2) находятся на внутреннем Д-у ровне, а на внешнем, Д-уровне, — четыре электрона (в состоянии 2s22p2).
Потеря четырех электронов с Д-уровня (с образованием катиона С4+) энергетически невыгодна, так как при этом каждый из электронов должен преодолеть притяжение положительно заряженного ядра. Приобретение же четырех электронов для образования октета на внешнем Д-уровне также маловероятно (образование С4′). Для этого необходимо преодолеть отталкивание между электронами, что также связано с очень большой затратой энергии. Итак, на внешнем энергетическом уровне атом углерода сохраняет четыре электрона. Как они распределяются по подуровням и орбиталям?
Электронная конфигурация изолированного атома углерода в основном (невозбужденном) состоянии выглядит так:

В этой схеме число неспаренных электронов на р-подуровне не совпадает с его обычной четырехвалентностью (известно, что валентность атома связывают с числом неспаренных электронов на его внешнем энергетическом уровне). Согласно же приведенной схеме распределения электронов по орбиталям может показаться, что у углерода валентность равна двум. Это противоречие можно устранить, если принять во внимание, что атом углерода (как и любой другой) .во время химической реакции возбуждается — меняет свое электронное состояние (условно обозначается как С*). При этом происходит распаривание 2s-электронов и переход одного из них на свободную 2р-орби- таль:

В результате такого перехода электронов на внешнем энергетическом уровне атома углерода оказываются четыре неспаренных электрона — один 2s и три 2р. Это, естественно, требует определенной энергии, но она затем с избытком компенсируется при образовании четырех ковалентных связей.
Таким образом, атом углерода о органических соединениях находится в возбужденном состоянии и его валентность равна четырем.
Четыре неспаренных электрона, которые находятся на //-уровне атома углерода, различны по своему состоянию (один 2s и три 2р). Это предполагало, что неравноценными могут быть и четыре связи, которые образует углеродный атом с любым другим атомом (например, водородом). Например, в молекуле метана одна из связей будет образована только s-электронами (s—s-связь), а три других—s- и р-электронами (s—p-связи). В действительности же, в симметрично построенных органических соединениях (например, в СН4 и CCI4) все четыре связи (С~С

или С—С1) одинаковы. Для объяснения этого факта было введено понятие о гибридизации (смешении) орбиталей. Согласно этой гипотезе электроны в молекулах распределяются не на “чистых” s- и р-орбиталях, а на усредненных, обладающих одинаковой
Рис.4. Схема гибридной ip-орбитали энергией. Такие электронные
орбитали называют гибридными. Их форма отличается от форм исходных 2s- и 2р-орбиталей и представляет собой неправильную “восьмерку”, один из “лепестков” которой значительно вытянут и имеет бблыпую электронную плотность (рис. 4). Такие гибридные орбитали в ббльшей степени, чем обычные, могут перекрываться с орбиталями других атомов.
Для атома углерода возможны три типа гибридизации (три валентных состояния).
5р3-Гибридизадия — смешение одной 2s- и трех 2р-орбиталей. Все четыре гибридные орбитали строго ориентированы в пространстве под углом 109°28′ друг к другу, создавая утолщенными “лепестками” геометрическую фигуру — тетраэдр (рис. 5). Поэтому э^-гибридизо- ванный атом углерода часто называют “тетраэдрическим”. Состояние углеродного атома с врЗ-гибридными орбиталями (первое валентное состояние) характерно для предельных углеводородов — алканов.

Рис. 5. Схема образования четырех зр3-гибридных орбиталей: а – негибридизованные орбитали атома углерода; б – орбитали атома углерода в состоянии $р3-гибридизации
лр2-Гибридизация — смешение одной 2 s- и двух 2р-орбиталей. Три гибридные орбитали расположены в одной плоскости под углом 120° друг к другу (форма трехлопастного пропеллера) (рис. 6). Оставшаяся 2р-орбиталь не гибридизована и перпендикулярна плоскости, в которой расположены три эрЗ-гибридные орбитали. Состояние атома углерода с врЗ-гибридными орбиталями (второе валентное состояние) характерно для непредельных углеводородов ряда этилена — алкенов.

Рис. 6. Схема образования трех зрЗ-рибридных орбиталей: а – негибридизованные орбитали атома углерода; б – орбитали1 атома углерода в состоянии sp2-rvfipидизации
sp-Гибридизация — смешение одной 2s- и одной 2р-орбитали. Две гибридные орбитали расположены на одной прямой линии под углом 180° друг к другу (рис. 7). Остальные две негибридизованные 2р- орбитали расположены во взаимно перпендикулярных плоскостях. Состояние атома углерода с sp-гибридными орбиталями (третье валентное состояние) характерно для непредельных углеводородов ацетиленового ряда — алкинов.

Рис.7. Схема образования двух sp-гибридных орбиталей: а – негибридизованные орбитали атома углерода; б – орбитали атома углерода в состоянии зр-гибридизации
Связь между типом гибридизации орбиталей и характером углеродных атомов показана в табл. 3.
Таблица 3. Гибридные орбитали и характер углеродных атомов
Состояние углеродного атома | Орбитали | Валентное состояние атома углерода | Тип гибридизации и строение молекулы | |||
Возбужденное, исходное состояние | 2s | 2рж | 2Py | 2pz | – | – |
Возбужденное, в алканах | 2 sp3 | 2 sp3 | 2 sp3 | 2 sp3 | i | (sp3) Тетраэдрическое |
Возбужденное, в алке- нах | 2 sp2 | 2 sp2 | 2 sp2 | 2P | ii | (sp2) Тригональное (плоскостное) |
Возбужденное, в алки- нах | 2 sp | 2 sp | 2P | 2V | ш | (sp) Дигональное (линейное) |
Однако гибридизация — всего лишь гипотеза, не подтвержденная экспериментально. Но она является настолько плодотворной, что позволяет судить о химической связи в органических соединениях и об их пространственном строении.
Источник
| Я не химик, а медсестра. Зашла на ваш сайт потому, что он называется: “химия и жизнь” и надеюсь получить ответ на свой вопрос из лечебной практики: Скажите пожалуйста, почему при растворении препарата амбробене для ингаляций в мин. воде Есентуки №17, раствор побелел. Раньше этого не происходило!!! Видимо поменялся состав амбробене? Но состав в инструкции тот-же. Конечно, в инструкции прописано разводить физ. р-ром, но для усиления муколитиаза в бронхах все же использовали мин. воду – и было все хорошо. А сейчас, когда раствор побелел, я его боюсь и не могу использовать не зная можно ли? Здравствуйте,Наталья Владимировна! Не думаю, что поменялся состав препарата. А вот в состав минеральной воды “Ессентуки” входят соли калия, кальция, магния, натрия и др. Возможно при взаимодействии с препаратом образовался небольшой осадок, за счет нерастворимых кальциевых солей. Думаю нужно проконтролировать качество минеральной воды. Добавил: Наталья Владимировна является ли 2-этилбутан изомером гексана Молекула 2-этилбутана теоретически является изомером гексана, т.к. имеет одинаковый качественный и количественный состав. Но правильно эту молекулу называть 2-метилпентан, исходя из правил номенклатуры ИЮПАК, согласно которой сначала выбирают самую длинную углеводородную цепь, затем нумеруют ее с того края ,где ближе расположен заместитель(радикал). Радикал в этой молекуле СН3 – метил и длинная углеводородная цепь насчитывает 5 атомов углерода, поэтому пентан. Добавил: marina Здравствуйте. Вопрос по электролизу фосфата калия (электроды графитовые): анод не растворим, соль кислородсожержащей кислоты, а калий в ряду напряжений до алюминия, значит, на катоде выделяется водород, а на аноде кислород. Но как ведут себя ионы калия в р-ре (образуется ли KOH) и тогда какое молекулярное уравнение? Или рассуждение неверное? Я прикрепила решение. Заранее спасибо) При электролизе фосфата калия электролизу подвергается вода. На катоде разряжается вода и образуется Н2. На аноде разряжается вода и образуется О2. Фосфат калия остается в растворе в виде соли. Гидроксида калия не образуется. Добавил: марина В нашей фирме обслуживает скважины, производит Канализация загородного дома. В Сервисе имеется к продаже ОБЕЗВОЖИВАТЕЛИ ОСАДКА И УТИЛИЗАЦИЯ, Силосы для хранения сыпучих продуктов, Промышленные смесители, Сжигание осадков сточных вод, Водоприемный колодец, Ершовая загрузка, Канализационные насосные станции (КНС), ОДЪЕМНЫЕ УСТРОЙСТВА И МЕТАЛЛОКОНСТРУКЦИИ Ангары, Павильоны, ВОДООЧИСТНОЕ ОБОРУДОВАНИЕ Биологическая очистка хоз.бытовых сточных вод, ПОДЪЕМНЫЕ УСТРОЙСТВА И МЕТАЛЛОКОНСТРУКЦИИ Ангары, Павильоны, ОЧИСТКА ЛИВНЕВЫХ СТОЧНЫХ ВОД Маслобензотделители, НАСОСНОЕ И КОМПРЕССОРНОЕ ОБОРУДОВАНИЕ (Грунфос, КСБ, Вило, КИТ, Взлёт, ТВП) Запорная арматура, ВОДОПОДГОТОВКУ Сорбционная фильтрация, а также все для автомойки Автомойки на базе песчанно-гравийной фильтрации. У нас вы найдете ЛОС, а также Нефтеуловители, мы можем произвести Обустройство скважин под ключ. Бурение артезианских скважин, Оценка запасов подземных вод, Монтаж водоснабжения. Диагностика скважин : [url=https://cpdisa.ru ] Обслуживание скважин[/url] Еще нет ответа на этот вопрос. Добавил: HauplE |
Источник
Атомная орбиталь
Все химические свойства веществ, то есть способность вступать в химические реакции, определяются строением электронных оболочек атомов. Электрон — главная элементарная частица для химии, так как именно благодаря обмену электронами могут образовываться новые химические соединения. Электрон — уникальная элементарная частица: обладая свойствами, отличающими его от всех других частиц, он одновременно является и частицей, и волной. Говоря научным языком, имеет двойственную природу. С одной стороны, обладая малой массой (почти в 2 тыс. раз меньше, чем масса протона и нейтрона), электрон проявляет свойства частицы. С другой стороны, электрон движется с такой высокой скоростью, что фактически «размазан» по атому, он находится не в одной конкретной точке, а образует «электронное облако». В этой области пространства электронная плотность достаточно велика. Этим объясняются волновые свойства электрона. Дуализм электрона подтверждается экспериментально. Так, например, для потока электронов, как и для световых волн, характерны явления интерференции (наложения) и дифракции (огибание препятствия).

Определение
Атомная орбиталь — это область пространства, в которой вероятность нахождения электрона максимальна.

На каждой орбитали могут максимально размещаться два электрона, обладающие равной энергией, но отличающиеся особым свойством, спином.

Если очень условно уподобить электрон детской игрушке — волчку, то электроны с разными спинами будут соответствовать волчкам, вращающимся в разные стороны. Графически орбиталь принято изображать в виде квадрата, а электроны — в виде стрелок, направленных вверх или вниз. Стрелки, направленные в противоположные стороны, означают электроны с двумя противоположными спинами.
Электронные орбитали имеют определенную форму и энергию. Ряд орбиталей, обладающих равной или близкой энергией, образует энергетический уровень (слой). Номер уровня обозначают числом (n = 1, 2, 3…) или заглавной латинской буквой (K, L, M и дальше по алфавиту). Различают первый (n = 1 или K), второй (n = 2 или L), третий (n = 3 или M) и т. д. энергетические уровни, вплоть до бесконечности ($n =infty$ означает, что электрон улетает из атома, и атом превращается в ион). Уровень с номером n включает ровно $n^2$ орбиталей, на которых может разместиться максимально $2n^2$ электронов. Номер энергетического уровня $n$ называют главным квантовым числом.
Таким образом, на первом энергетическом уровне могут максимально находиться 2 электрона, на втором — 8, на третьем — 18 и т. д.
Формы атомных орбиталей
Каждый энергетический уровень делится на энергетические подуровни, которые образованы орбиталями, имеющими одинаковую форму и равную энергию. По форме различают s-, p-, d- и f-орбитали. s-орбитали имеют форму шара, иными словами, электрон, находящийся на такой орбитали (его называют s-электроном), большую часть времени проводит внутри сферы. s-орбиталь, находящуюся на первом энергетическом уровне, обозначают 1s, на втором — 2s и т. д.

р-орбитали имеют форму объемной восьмерки (см. рис. б и в). Следует подчеркнуть, что любая орбиталь является объемной. Они могут быть направлены по одной из трех координатных осей (обозначаются $p_x$,$ p_y$, $p_z$), поэтому на каждом энергетическом уровне (кроме первого, где есть только s-орбиталь) существуют три р-орбитали, обладающие одинаковой энергией. Формы d- и f-орбиталей намного сложнее. На рисунке видно, что существует 5 форм d-орбиталей и 7 форм f-орбиталей. На каждой из орбиталей, как вы помните, могут размещаться не более двух электронов, следовательно, s-подуровень максимально вмещает 2 электрона, p — 6, d — 10, f — 14.

Орбитали одной и той же формы, но находящиеся на разных энергетических уровнях (например, 1s, 2s и 3s-орбитали), отличаются по энергии. Чем больше номер уровня, тем выше энергия орбитали и тем больше ее размер.
Рассмотрим три первых энергетических уровня. На первом уровне (n = 1) есть только 1s-подуровень (одна 1s-орбиталь), на котором максимально могут находиться два электрона (2 = 2×1). Второй энергетический уровень включает два подуровня: 2s- подуровень (одна 2s- орбиталь) и 2p-подуровень (три 2p-орбитали), всего четыре орбитали, на которых может находиться до 8 электронов (8 = 2×22). В состав третьего уровня (максимально 18 электронов) входят три подуровня: 3s- (одна орбиталь), 3p- (три орбитали) и 3d- (пять орбиталей), всего 9 орбиталей, содержащих не более 18 электронов (18 = 2×32).
| Номер энергетического уровня (n) | Подуровни и их схематичное изображение | Максимальное число электронов на энергетическом уровне ($N = 2n^2$) | |||
|---|---|---|---|---|---|
| s- | p- | d- | f- | ||
| 1 | $Box 1s$ | 2 | |||
| 2 | $Box 2s$ | $Box Box Box 2p$ | 8 | ||
| 3 | $Box 3s$ | $Box Box Box 3p$ | $Box Box Box Box Box 3d$ | 18 | |
| 4 | $Box 4s$ | $Box Box Box 4p$ | $Box Box Box Box Box 4d$ | $Box Box Box Box Box Box Box 4f$ | 32 |
Электроны занимают уровни и орбитали последовательно, в порядке увеличения энергии. Сначала заполняется первый энергетический уровень, после его завершения — второй и т. д.
Принципы построения электронной конфигурации элемента
Количество электронов в атоме элемента равно его порядковому номеру.
Количество энергетических уровней атома равно номеру периода, в котором расположен элемент.
Количество электронов на внешнем (валентном) уровне равно номеру группы, в которой расположен элемент.
При более подробном описании электронной конфигурации рассматривают не только количество электронов на данном энергетическом уровне, но и их распределение по подуровням.

Разместим уже известные нам орбитали на энергетической диаграмме. Каждую незаполненную орбиталь мы обозначим пустым квадратиком (вертикальная ось показывает направление возрастания энергии).
Для полного описания электронного строения атома надо знать, как именно распределены электроны по энергетическим уровням. Перечень энергетических уровней, заполненных электронами, называют электронной конфигурацией атома.
При заполнении орбиталей электронами используют следующие правила.
Принцип минимума энергии
Орбитали заполняются в порядке увеличения энергии, снизу вверх. Каждый электрон располагается так, чтобы его энергия была минимальной, т. е. среди свободных орбиталей он выбирает орбиталь с самой низкой энергией.
Порядок заполнения энергетических подуровней (см. рис.) можно запомнить в виде ряда:
1s < 2s < 2p < 3s < 3p < 4s < 3d < 4p < 5s < 4d < 5p < 6s < 5d » 4f < 6p < 7s….
Принцип Паули
На каждой орбитали может находиться не более двух электронов. Если два электрона находятся на одной орбитали, то они обладают противоположными спинами (стрелки направлены в разные стороны). Такие электроны называют спаренными. Если на орбитали находится только один электрон, то его называют неспаренным.
Правило Хунда (Гунда)
Атом в основном состоянии должен иметь максимально возможное число неспаренных электронов в пределах определенного подуровня.
Обратите внимание, что 4s-орбиталь обладает меньшей энергией, чем 3d-орбиталь. Это означает, что в первую очередь электроны заполнят 4s-подуровень и лишь затем 3d-подуровень. Для удобства запоминания порядка заполнения энергетических подуровней лучше воспользоваться следующей схемой: в каждой отдельной строке написать возможные типы орбиталей для каждого уровня, провести стрелки под углом 45$^0$ и «расселять» электроны по подуровням, ориентируясь по стрелкам сверху вниз.

Запись электронной конфигурации атома
Подробные электронные конфигурации атомов изображают двумя способами:
графически, с помощью квадратиков со стрелками (часто называют энергетическими диаграммами);
в строчку, когда перечисляются все занятые энергетические подуровни с указанием общего числа электронов на каждом из них.


Рассмотрим порядок заполнения электронами энергетических уровней, воспользовавшись периодической системой. Число электронов в атоме элемента, как вы помните, равно заряду его ядра, а следовательно, и порядковому номеру элемента в периодической системе. Так, например, в атоме водорода (N = 1) содержится всего один электрон, а в атоме кислорода (N = 8) — восемь. В каждом периоде периодической системы электронная оболочка атома каждого последующего элемента повторяет строение электронной оболочки предыдущего элемента с добавлением одного электрона.
Число заполненных энергетических уровней в атоме равно номеру периода, в котором расположен элемент.
Электронные конфигурации некоторых элементов
Первый энергетический уровень вмещает максимально два электрона. Поэтому первый период состоит лишь из двух элементов — водорода и гелия. Простейший из атомов — водород, H. Он содержит один электрон, который занимает орбиталь с самой низкой энергией — 1s-орбиталь. Электронная конфигурация атома водорода. В атоме гелия первый энергетический уровень полностью завершен.


У элементов второго периода начинается заполнение второго энергетического уровня — он включает восемь электронов (n = 2, N = 8). Второй период содержит восемь элементов. У неона, элемента, завершающего второй период, первый и второй энергетические уровни оказываются целиком заполненными.

В третьем периоде происходит заполнение третьего энергетического уровня. Третий уровень (n = 3) может максимально вмещать 18 электронов. Однако элементов в третьем периоде всего восемь. К концу третьего периода (у аргона) полностью заполняются 3s- и 3p-подуровни, а 3d-подуровень остается пустым, поэтому третий уровень не заполняется до конца.

В четвертом периоде у первых двух элементов (калия и кальция) электроны идут на четвертый энергетический уровень (4s-подуровень), а затем у последующих десяти элементов (от скандия до цинка) завершается заполнение третьего энергетического уровня (3d-подуровня).

Определение
Элементы, в атомах которых происходит заполнение предвнешнего энергетического уровня, называют переходными.
Такие элементы расположены в побочных подгруппах периодической системы. Начиная с элемента галлия заполнение четвертого уровня продолжается.
Химические свойства элементов определяются не всеми электронами, а только внешними, обладающими наибольшей энергией.
Внешние электроны называют валентными, и их количество, как правило, равно номеру группы, в которой расположен элемент.
Их атом может отдавать в результате химических реакций, они обуславливают его химические свойства. У элементов главных подгрупп валентными являются электроны внешнего энергетического уровня. Число валентных электронов равно номеру группы, в которой находится элемент. Например, водород, натрий и калий, расположенные в первой группе, имеют по одному валентному электрону, а элементы четвертой группы — углерод и кремний — по четыре. Как вы помните, элементы, входящие в одну и ту же подгруппу, обладают сходными химическим свойствами. Это объясняется тем, что они имеют сходные электронные конфигурации, т. е. являются электронными аналогами. Полностью завершенные внутренние энергетические уровни не оказывают существенного влияния на химические свойства.
Элементы, в атомах которых валентные электроны расположены на s-подуровне, называют s-элементами, p-подуровне — p-элементами, d-подуровне — d-элементами, а f-подуровне — f-элементами.
s-элементы расположены в начале периодов, а р-элементы — в конце. В короткопериодном варианте периодической системы f-элементы (лантаноиды и актиноиды) вынесены за пределы таблицы. Малые периоды и главные подгруппы состоят лишь из s- и р-элементов. Все d- и f-элементы расположены в побочных подгруппах.
В длиннопериодном варианте s-, p-, d- и f-элементы занимают отдельные поля.
Именно конфигурация валентных электронов определяет то, является ли элемент металлом или неметаллом, с какими другими элементами он может взаимодействовать и какова его валентность. При заполнении орбиталей электронами конфигурация валентных электронов периодически повторяется, что приводит к периодическому изменению химических свойств элементов.
Пример
Записать электронную конфигурацию и энергетическую диаграмму атома серы, указав распределение электронов по уровням и подуровням.
Сера расположена в третьем периоде и VI (6) группе, порядковый номер — 16.

Значит, в атоме серы всего 16 электронов, которые расположены на трех энергетических уровнях (т. к. номер периода = 3), причем на последнем (валентном) уровне находится 6 электронов (т. к. номер группы = 6). В соответствии с принципом минимума энергии расположим электроны по подуровням.
Электронная конфигурация атома серы тогда выглядит следующими образом: $1S^22S^22P^63S^23P^4$.
«Проскок» или «провал» электрона
У атомов Cr, Cu, Nb, Mo, Ru, Rh, Pd, Ag, Pt, Au имеет место «провал» электрона с s-подуровня внешнего слоя на d-подуровень предыдущего слоя, что приводит к энергетически более устойчивому состоянию атома. Например, электронная формула атома меди, исходя из вышенаписанного, должна иметь вид: Cu $1s^2 2s^2 2p^6 3s^2 3p^6underline{4s^2 3d^9} $. Однако в действительности один из двух 4s-электронов «проваливается» на 3d-подуровень, и атом меди имеет следующую конфигурацию: $1s^2 2s^2 2p^6 3s^2 3p^6 underline{4s^1 3d^{10}} $.

Для элементов IБ-подгруппы характерна конфигурация внешнего слоя: $ns^1 (n-1)d^{10}$.
Для элементов Cr и Mo характерна конфигурация внешнего слоя: $ns^1 (n-1)d^5$.
Особо следует отметить палладий, у которого «проваливаются» два электрона:
$Pd hspace{1cm} 1s^2 2s^2 2p^6 3s^23p^6 4s^2 3d^{10} 4p^6 underline{5s^0 4d^{10}}.$
Возбужденное состояние атома
Все электронные конфигурации, о которых мы говорили выше, являются конфигурациями с наименьшей энергией и соответствуют основному состоянию атома.
Получив энергию извне (облучение или нагревание системы), один либо несколько электронов могут переходить на более высокий энергетический подуровень.
Определение
Состояние атома, при котором электрон из электронной пары с предыдущего подуровня «распаривается» и переходит на следующий подуровень, называется возбужденным состоянием атома.
Возбужденное состояние атома является неустойчивым, и через некоторое время электрон теряет энергию, перейдя на энергетическую орбиталь с меньшей энергией, испустив при этом квант света.
Определение
Состояние, которое требует для повышения энергии электрона наименьших энергетических затрат, называют первым возбужденным состоянием. Состояние, при котором все валентные электроны являются неспаренными, называют максимально возбужденным состоянием.
Например, для атома хлора возможны три возбужденных состояния, обозначенные на рисунке как Cl*, Cl**, Cl***, причем последнее является максимально возбужденным состоянием. У атомов в возбужденном состоянии меняется число валентных электронов и, соответственно, возможная степень окисления.

Источник
