На какое свойство элемента указывает водород

Элемент водород начинает Периодическую систему – он имеет порядковый номер 1. Это самый легкий из химических элементов. Обладая уникальными свойствами, частично напоминающими свойства галогенов, частично – щелочных металлов, он оказывается расположенным и в первой, и в VII группах Периодической системы.
Строение водорода
Атом водорода имеет очень простое строение – в нем содержится всего один протон и один электрон. Отдавая электрон, атом приобретает степень окисления +1, а принимая его – степень окисления –1. Относительная атомная масса атома водорода равна 1. Однако в природе существуют и более тяжелые атомы водорода – дейтерий (содержит один нейтрон, поэтому его масса равна 2) и тритий (содержит два нейтрона, атомная масса равна 3).

Водород – самый распространенный элемент во Вселенной. На Земле он уступает по распространенности кислороду, кремнию и некоторым другим элементам. Главное соединение водорода – вода. Также он содержится в природном газе, нефти, в некоторых минералах, в белках, жирах и углеводах.
Физические свойства
При обычных условиях водород – газ, состоящий из двухатомных молекул. Он не имеет ни цвета, ни запаха, мало растворим в воде (1,82 мл в 100 г воды при 20 $^circ C$). При сильном сжатии и охлаждении переходит в жидкое состояние. Жидкий водород кипит при –253°C, при этой температуре азот и кислород находятся в кристаллическом состоянии. Твердый водород образуется при охлаждении до –259°C.
Газообразный водород обладает рядом уникальных свойств. Благодаря маленькому радиусу атомы и молекулы водорода могут проникать через резину, стекло и даже через металлы. Некоторые металлы, например, платина и палладий, способны растворять значительные количества газообразного водорода. Водород в 14,5 раз легче воздуха, 100 л водорода при 0$^circ C$ весят всего 9 г. Это самый легкий из газов и самое легкое вещество.
Химические свойства
При комнатной температуре реагирует лишь с фтором, а на свету – с хлором, при нагревании – с кислородом, серой, азотом, углеродом:
H$_2$ + X$_2$ = 2HX (X = F, Cl)
2H$_2$ + O$_2$ = 2H$_2$O,
H$_2$ + S = H$_2$S,
3H$_2$ + N$_2$ = 2NH$_3$.
С кислородом и воздухом водород образует взрывчатые смеси. Особенно опасна смесь одного объема кислорода и двух объемов водорода. Ее называют гремучим газом.
При взаимодействии с щелочными и щелочноземельными металлами образует гидриды. Восстанавливает некоторые металлы из оксидов:
CuO + H$_2$ = Cu + H$_2$O
HgO + H$_2$ = Hg + H$_2$O
Получение водорода
В лаборатории получают действием цинка на разбавленные кислоты – серную или соляную:
Zn + H$_2$SO$_4$ = ZnSO$_4$ + H$_2$
Реакцию обычно проводят в аппарате Киппа.
Также образуется при действии растворов щелочей на цинк, кремний и алюминий, при реакции щелочных и щелочноземельных металлов и их гидридов с водой.
В промышленности водород получают электролизом воды, термическим разложением (пиролизом) углеводородов, в смеси с угарным газом взаимодействием угля и природного газа с перегретым водяным паром (водяной газ, синтез-газ).
Применяется водород в синтезе аммиака, хлороводорода и соляной кислоты, метилового спирта, получении некоторых металлов из оксидов, при гидрировании растительных жиров. В смеси с угарным газом (синтез-газ) используется для получения разнообразным органических веществ. Является перспективным топливом.
Источник
Атомная масса – 1 а.е.м. Молекула водорода двухатомна – Н2.
Электронная конфигурация атома водорода – 1s1. Водород относится к семейству s-элементов. В своих соединениях проявляет степени окисления -1, 0,
+1. Природный водород состоит из двух стабильных изотопов – протия 1Н (99,98%) и дейтерия 2Н (D) (0,015%) – и радиоактивного изотопа трития 3Н (Т) (следовые количества, период полураспада – 12,5 лет).
Химические свойства водорода
При обычных условиях молекулярный водород проявляет сравнительно низкую реакционную способность, что объясняется высокой прочностью связей в молекуле. При нагревании вступает во взаимодействие практически со всеми простыми веществами, образованными элементами главных подгрупп (кроме благородных газов, B, Si,
P, Al). В химических реакциях может выступать как в роли восстановителя (чаще), так и окислителя (реже).
Водород проявляет свойства восстановителя (Н20 -2е → 2Н+) в следующих реакциях:
1. Реакции взаимодействия с простыми веществами – неметаллами. Водород реагирует с галогенами, причем, реакция взаимодействия со фтором при обычных условиях, в темноте, со взрывом, с хлором – при освещении (или УФ-облучении) по цепному механизму, с бромом и йодом только при нагревании; кислородом (смесь кислорода и водорода в объемном отношении 2:1 называют «гремучим газом»), серой, азотом и углеродом:
H2 + Hal2 = 2HHal;
2H2 + O2 = 2H2O + Q (t);
H2 + S = H2S (t = 150 – 300C);
3H2 + N2 ↔ 2NH3 (t = 500C, p, kat = Fe, Pt);
2H2 + C ↔ CH4 (t, p, kat).
2. Реакции взаимодействия со сложными веществами. Водород реагирует с оксидами малоактивных металлов, причем он способен восстанавливать только металлы, стоящие в ряду активности правее цинка:
CuO + H2 = Cu + H2O (t);
Fe2O3 + 3H2 = 2Fe + 3H2O (t);
WO3 + 3H2 = W + 3H2O (t).
Водород реагирует с оксидами неметаллов:
H2 + CO2 ↔ CO + H2O (t);
2H2 + CO ↔ CH3OH (t = 300C, p = 250 – 300 атм., kat = ZnO, Cr2O3).
Водород вступает в реакции гидрирования с органическими соединениями класса циклоалканов, алкенов, аренов, альдегидов и кетонов и др. Все эти реакции проводят при нагревании, под давлением, в качестве катализаторов используют платину или никель:
CH2 = CH2 + H2 ↔ CH3-CH3;
C6H6 + 3H2 ↔ C6H12;
C3H6 + H2 ↔ C3H8;
CH3CHO + H2 ↔ CH3-CH2-OH;
CH3-CO-CH3 + H2 ↔ CH3-CH(OH)-CH3.
Водород в качестве окислителя (Н2 +2е → 2Н—) выступает в реакциях взаимодействия со щелочными и щелочноземельными металлами. При этом образуются гидриды – кристаллические ионные соединения, в которых водород проявляет степень окисления -1.
2Na +H2 ↔ 2NaH (t, p).
Ca + H2 ↔ CaH2 (t, p).
Физические свойства водорода
Водород – легкий бесцветный газ, без запаха, плотность при н.у. – 0,09 г/л, в 14,5 раз легче воздуха, tкип = -252,8С, tпл = — 259,2С. Водород плохо растворим в воде и органически растворителях, хорошо растворим в некоторых металлах: никеле, палладии, платине.
По данным современной космохимии водород является самым распространенным элементом Вселенной. Основная форма существования водорода в космическом пространстве – отдельные атомы. По распространенности на Земле водород занимает 9 место среди всех элементов. Основное количество водорода на Земле находится в связанном состоянии – в составе воды, нефти, природного газа, каменного угля и т.д. В виде простого вещества водород встречается редко – в составе вулканических газов.
Получение водорода
Различают лабораторные и промышленные способы получения водорода. К лабораторным способам относят взаимодействие металлов с кислотами (1), а также взаимодействие алюминия с водными растворами щелочей (2). Среди промышленных способов получения водорода большую роль играют электролиз водных растворов щелочей и солей (3) и конверсия метана (4):
Zn + 2HCl = ZnCl2 + H2↑ (1);
2Al + 2NaOH + 6H2O = 2Na[Al(OH)4] +3 H2↑ (2);
2NaCl + 2H2O = H2↑ + Cl2↑ + 2NaOH (3);
CH4 + H2O ↔ CO + H2 (4).
Примеры решения задач
Источник
Гидроген Н – химический элемент, один из самых распространённых в нашей Вселенной. Масса водорода как элемента в составе веществ составляет 75 % от общего содержания атомов другого типа. Он входит в наиважнейшее и жизненно необходимое соединение на планете – воду. Отличительной особенностью водорода также является то, что он первый элемент в периодический системе химических элементов Д. И. Менделеева.

Открытие и исследование
Первые упоминания о водороде в трудах Парацельса датируются шестнадцатым веком. Но его выделение из газовой смеси воздуха и исследование горючих свойств были произведены уже в семнадцатом веке учёным Лемери. Досконально изучил гидроген английский химик, физик и естествоиспытатель Генри Кавендиш, который опытным путём доказал, что масса водорода наименьшая в сравнении с другими газами. В последующих этапах развития науки многие учёные работали с ним, в частности Лавуазье, назвавший его «рождающим воду».
Характеристика по положению в ПСХЭ
Элемент, открывающий периодическую таблицу Д. И. Менделеева, – это водород. Физические и химические свойства атома проявляют некую двойственность, так как гидроген одновременно относят к первой группе, главной подгруппе, если он ведёт себя как металл и отдаёт единственный электрон в процессе химической реакции, и к седьмой – в случае полного заполнения валентной оболочки, то есть приёме отрицательной частицы, что характеризует его как подобный галогенам.

Особенности электронного строения элемента
Свойства атома водорода, сложных веществ, в состав которых он входит, и самого простого вещества Н2 в первую очередь определяются электронной конфигурацией гидрогена. Частица имеет один электрон с Z= (-1), который вращается по своей орбите вокруг ядра, содержащего один протон с единичной массой и положительным зарядом (+1). Его электронная конфигурация записывается как 1s1, что означает наличие одной отрицательной частицы на самой первой и единственной для гидрогена s-орбитали.
При отрыве или отдаче электрона, а атом этого элемента имеет такое свойство, что роднит его с металлами, получается катион. По сути ион водорода – это положительная элементарная частица. Поэтому лишенный электрона гидроген называют попросту протоном.
Физические свойства
Если описывать физические свойства водорода кратко, то это бесцветный, малорастворимый газ с относительной атомной массой равной 2, в 14,5 раза легче, чем воздух, с температурой сжижения, составляющей -252,8 градуса Цельсия.
На опыте можно легко убедиться в том, что Н2 самый легкий. Для этого достаточно наполнить три шара различными веществами – водородом, углекислым газом, обычным воздухом – и одновременно выпустить их из руки. Быстрее всех достигнет земли тот, который наполнен СО2, после него опустится надутый воздушной смесью, а содержащий Н2 вовсе поднимется к потолку.
Маленькая масса и размер частиц водорода обосновывают его способность проникать через различные вещества. На примере того же шара в этом легко убедиться, через пару дней он сам сдуется, так как газ просто пройдёт через резину. Также водород может накапливаться в структуре некоторых металлов (палладий или платина), а при повышении температуры испаряться из неё.
Свойство малорастворимости водорода используют в лабораторной практике для его выделения способом вытеснения воды. Физические свойства водорода (таблица, изображенная ниже, содержит основные параметры) определяют сферы его применения и методы получения.
| Параметр атома или молекулы простого вещества | Значение |
| Атомная масса (молярная масса) | 1,008 г/моль |
| Электронная конфигурация | 1s1 |
| Кристаллическая решётка | Гексагональная |
| Теплопроводность | (300 K) 0,1815 Вт/(м·К) |
| Плотность при н. у. | 0,08987 г/л |
| Температура кипения | -252,76 °C |
| Удельная теплота сгорания | 120,9·106 Дж/кг |
| Температура плавления | -259,2 °C |
| Растворимость в воде | 18,8 мл/л |
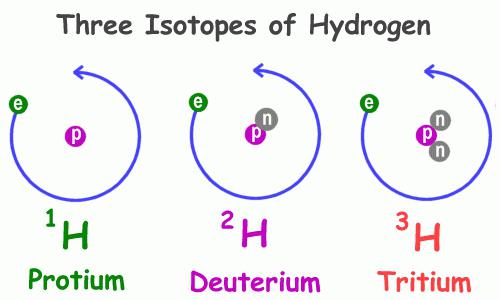
Изотопный состав
Как и многие другие представители периодической системы химических элементов, гидроген имеет несколько природных изотопов, то есть атомов с одинаковым числом протонов в ядре, но различным числом нейтронов – частиц с нулевым зарядом и единичной массой. Примеры атомов, обладающих подобным свойством – кислород, углерод, хлор, бром и прочие, в том числе радиоактивные.
Физические свойства водорода 1Н, самого распространённого из представителей данной группы, значительно отличаются от таких же характеристик его собратьев. В частности, разнятся особенности веществ, в состав которых они входят. Так, существует обычная и дейтерированная вода, содержащая в своём составе вместо атома водорода с одним-единственным протоном дейтерий 2Н – его изотоп с двумя элементарными частицами: положительной и незаряженной. Этот изотоп в два раза тяжелее обычного гидрогена, что и объясняет кардинальное различие в свойствах соединений, которые они составляют. В природе дейтерий встречается в 3200 раз реже, чем водород. Третий представитель – тритий 3Н, в ядре он имеет два нейтрона и один протон.
Способы получения и выделения
Лабораторные и промышленные методы получения водорода весьма отличаются. Так, в малых количествах газ получают в основном с помощью реакций, в которых участвуют минеральные вещества, а крупномасштабные производства в большей степени используют органический синтез.
В лаборатории применяют следующие химические взаимодействия:
- Реакция щелочных и щелочноземельных металлов с водой с образованием щёлочи и искомого газа.
- Электролиз водного раствора электролита, на аноде выделяется Н2↑, а на катоде – кислород.
- Разложение гидридов щелочных металлов водой, продуктами являются щёлочь и, соответственно, газ Н2↑.
- Взаимодействие разбавленных кислот с металлами с образованием солей и Н2↑.
- Действие щелочей на кремний, алюминий и цинк также способствует выделению водорода параллельно с образованием комплексных солей.
В промышленных интересах газ получают такими методами, как:
- Термическое разложение метана в присутствии катализатора до составляющих его простых веществ (350 градусов достигает значение такого показателя, как температура) – водорода Н2↑ и углерода С.
- Пропускание парообразной воды через кокс при 1000 градусов Цельсия с образованием углекислого газа СО2 и Н2↑ (самый распространённый метод).
- Конверсия газообразного метана на никелевом катализаторе при температуре, достигающей 800 градусов.
- Водород является побочным продуктом при электролизе водных растворов хлоридов калия или натрия.
Химические взаимодействия: общие положения
Физические свойства водорода во многом объясняют его поведение в процессах реагирования с тем или иным соединением. Валентность гидрогена равняется 1, так как он в таблице Менделеева расположен в первой группе, а степень окисления проявляет различную. Во всех соединениях, кроме гидридов, водород в с.о.= (1+), в молекулах типа ХН, ХН2, ХН3 – (1-).
Молекула газа водорода, образованная посредством создания обобщенной электронной пары, состоит из двух атомов и довольно устойчива энергетически, именно поэтому при нормальных условиях несколько инертна и в реакции вступает при изменении нормальных условий. В зависимости от степени окисления водорода в составе прочих веществ, он может выступать как в качестве окислителя, так и восстановителя.
Вещества, с которыми реагирует и которые образует водород
Элементные взаимодействия с образованием сложных веществ (часто при повышенных температурах):
- Щелочной и щелочноземельный металл + водород = гидрид.
- Галоген + Н2 = галогеноводород.
- Сера + водород = сероводород.
- Кислород + Н2 = вода.
- Углерод + водород = метан.
- Азот + Н2 = аммиак.
Взаимодействие со сложными веществами:
- Получение синтез-газа из монооксида углерода и водорода.
- Восстановление металлов из их оксидов с помощью Н2.
- Насыщение водородом непредельных алифатических углеводородов.
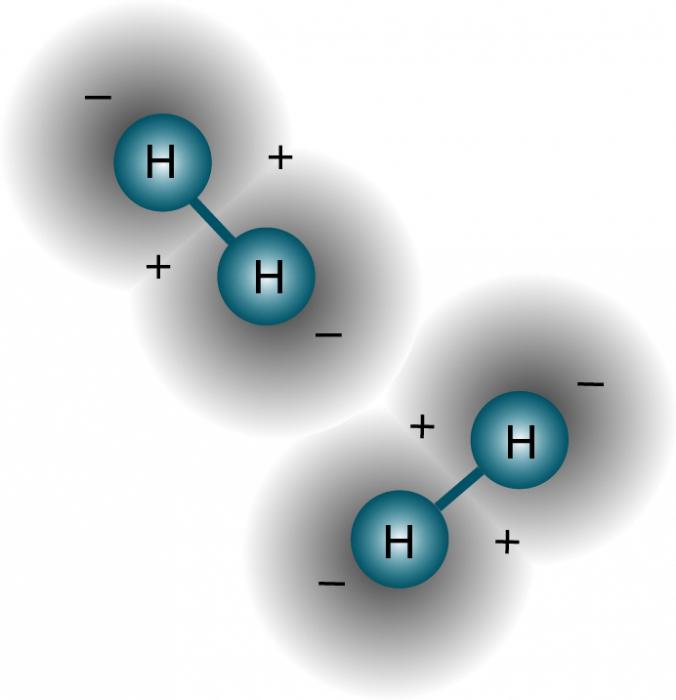
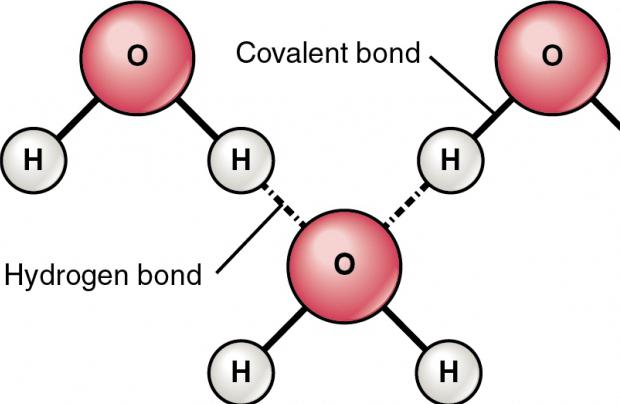
Водородная связь
Физические свойства водорода таковы, что позволяют ему, находясь в соединении с электроотрицательным элементом, образовывать особый тип связи с таким же атомом из соседних молекул, имеющих неподелённые электронные пары (например, кислородом, азотом и фтором). Ярчайший пример, на котором лучше рассмотреть подобное явление, – это вода. Она, можно сказать, прошита водородными связями, которые слабее ковалентных или ионных, но за счёт того, что их много, оказывают значительное влияние на свойства вещества. По сути, водородная связь – это электростатическое взаимодействие, которое связывает молекулы воды в димеры и полимеры, обосновывая её высокую температуру кипения.
Гидроген в составе минеральных соединений
В состав всех неорганических кислот входит протон – катион такого атома, как водород. Вещество, кислотный остаток которого имеет степень окисления больше (-1), называется многоосновным соединением. В нём присутствует несколько атомов водорода, что делает диссоциацию в водных растворах многоступенчатой. Каждый последующий протон отрывается от остатка кислоты всё труднее. По количественному содержанию водородов в среде определяется его кислотность.

Водород содержат и гидроксильные группы оснований. В них водород соединён с атомом кислорода, в результате степень окисления этого остатка щёлочи всегда равна (-1). По содержанию гидроксилов в среде определяется её основность.
Применение в деятельности человека
Баллоны с веществом, так же как и емкости с другими сжиженными газами, например кислородом, имеют специфический внешний вид. Они выкрашены в темновато-зелёный цвет с ярко-красной надписью «Водород». Газ закачивают в баллон под давлением порядка 150 атмосфер. Физические свойства водорода, в частности легкость газообразного агрегатного состояния, используют для наполнения им в смеси с гелием аэростатов, шаров-зондов и т.д.
Водород, физические и химические свойства которого люди научились использовать много лет назад, на сегодняшний момент задействован во многих отраслях промышленности. Основная его масса идёт на производство аммиака. Также водород участвует в получении металлов (гафния, германия, галлия, кремния, молибдена, вольфрама, циркония и прочих) из окислов, выступая в реакции в качестве восстановителя, синильной и соляной кислот, метилового спирта, а также искусственного жидкого топлива. Пищевая промышленность использует его для превращения растительных масел в твёрдые жиры.
Определили химические свойства и применение водорода в различных процессах гидрогенизации и гидрирования жиров, углей, углеводородов, масел и мазута. С помощью него производят драгоценные камни, лампы накаливания, проводят ковку и сварку металлических изделий под воздействием кислородно-водородного пламени.
Источник
Химические свойства
водорода
При обычных условиях молекулярный Водород сравнительно мало активен, непосредственно соединяясь лишь с наиболее активными из неметаллов (с фтором, а на свету и с хлором). Однако при нагревании он вступает в реакции со многими элементами.
Водород вступает в реакции с простыми и сложными веществами:

– Взаимодействие водорода с металлами приводит к образованию сложных веществ – гидридов, в химических формулах которых атом металла всегда стоит на первом месте:

При высокой температуре Водород непосредственно реагирует с некоторыми металлами (щелочными, щелочноземельными и другими), образуя белые кристаллические вещества – гидриды металлов (LiН, NaН, КН, СаН2 и др.):
Н2 + 2Li = 2LiH
Гидриды металлов легко разлагаются водой с образованием соответствующей щелочи и водорода:
СаH2 + 2Н2О = Са(ОН)2 + 2Н2↑
– При взаимодействии водорода с неметаллами образуются летучие водородные соединения. В химической формуле летучего водородного соединения, атом водорода может стоять как на первом так и на втором месте, в зависимости от местонахождения в ПСХЭ (см. табличку в слайде):

1). С кислородом
Водород образует воду:
Видео “Горение водорода”
2Н2 + О2 = 2Н2О + Q
При обычных температурах реакция протекает крайне
медленно, выше 550°С – со взрывом (смесь
2 объемов Н2 и 1 объема О2 называется гремучим газом).
Видео “Взрыв гремучего газа”
Видео “Приготовление и взрыв гремучей смеси”
2). С галогенами
Водород образует галогеноводороды, например:
Н2 + Cl2 = 2НСl
При этом с фтором Водород взрывается (даже в темноте и
при – 252°С), с хлором и бромом реагирует лишь при освещении или нагревании, а
с йодом только при нагревании.
3). С азотом
Водород взаимодействует с образованием аммиака:
ЗН2 + N2 = 2NН3
лишь на катализаторе и при повышенных температуpax и
давлениях.
4). При нагревании Водород энергично реагирует с серой:
Н2 + S = H2S (сероводород),
значительно труднее с селеном и теллуром.
5). С чистым
углеродом Водород может реагировать без катализатора только при высоких
температуpax:
2Н2 + С (аморфный) = СН4 (метан)
– Водород вступает в реакцию замещения с оксидами металлов, при этом образуются в продуктах вода и восстанавливается металл. Водород – проявляет свойства восстановителя:

Водород используется для восстановления многих металлов, так как отнимает кислород у их
оксидов:
CuO + H2 = Cu + H2O,
Fe3O4 + 4H2 = 3Fe +
4Н2О, и т. д.
Применение
водорода
Видео “Применение водорода”
В настоящее время водород получают в огромных
количествах. Очень большую часть его используют при синтезе аммиака,
гидрогенизации жиров и при гидрировании угля, масел и углеводородов. Кроме
того, водород применяют для синтеза соляной кислоты, метилового спирта,
синильной кислоты, при сварке и ковке металлов, а также при изготовлении ламп
накаливания и драгоценных камней. В продажу водород поступает в баллонах под
давлением свыше 150 атм. Они окрашены в тёмно-зелёный цвет и снабжаются красной
надписью “Водород”.
Водород используется для
превращения жидких жиров в твердые (гидрогенизация), производства жидкого
топлива гидрогенизацией углей и мазута. В металлургии водород используют как
восстановитель оксидов или хлоридов для получения металлов и неметаллов
(германия, кремния, галлия, циркония, гафния, молибдена, вольфрама и др.).
Практическое применение водорода
многообразно: им обычно заполняют шары-зонды, в химической промышленности он
служит сырьём для получения многих весьма важных продуктов (аммиака и др.), в
пищевой – для выработки из растительных масел твёрдых жиров и т. д. Высокая
температура (до 2600 °С), получающаяся при горении водорода в кислороде,
используется для плавления тугоплавких металлов, кварца и т. п. Жидкий водород
является одним из наиболее эффективных реактивных топлив. Ежегодное мировое
потребление водорода превышает 1 млн. т.
ТРЕНАЖЕРЫ
№1. Химические свойства водорода
№2. Водород
ЗАДАНИЯ ДЛЯ ЗАКРЕПЛЕНИЯ
Задание №1
Составьте уравнения реакций взаимодействия водорода со следующими веществами: F2, Ca, Al2O3, оксидом ртути (II), оксидом вольфрама (VI). Назовите продукты реакции, укажите типы реакций.
Задание №2
Осуществите превращения по схеме:
H2O -> H2 -> H2S -> SO2
Задание №3.
Вычислите массу воды, которую можно получить при сжигании 8 г водорода?
Источник
