На каких свойствах основано применения углерода
Углерод – важнейший химический элемент периодической таблицы Менделеева. Без него, как и без кислорода и водорода немыслимой была бы сама Жизнь. Можно без преувеличения сказать, что жизнь всех живых существ от амебы до человека построена именно из соединений углерода. Углерод – биогенный элемент составляющий основу жизни на нашей планете. Будучи структурной единицей огромного числа различных органических соединений, он участвует и в построении живых организмов и в обеспечении их жизнедеятельности. Даже возникновение самой Жизни рассматривается учеными как сложный процесс эволюции углеродных соединений. А какие химические и физические свойства этого чудесного элемента, история его открытие и современное применение в химии, читайте об этом далее.
История открытия углерода
На самом деле углерод был известен человеку еще с глубокой древности в виде своих аллотропных модификаций: алмаза и графита. Помимо этого углерод в виде древесного угля активно применялся при выплавке металлов. От угля происходит и само название углерода, как химического элемента.
Но в те далекие времена люди пользовались углеродом в виде угля, или любовались им же, в виде алмазов, неосознанно, без понимания того, какой важный химический элемент стоит за всем этим.
Научное открытие углерода произошло в 1791 году, когда английский химик Теннант впервые получил свободный углерод. Для получения углерода он пропускал пары фосфора над прокаленным мелом. В результате этой химической реакции образовались фосфат кальция и чистый углерод. Впрочем, этому опыту предшествовали и другие искания, например выдающийся французский химик Лавуазье поставил опыт по сжиганию алмаза при помощи большой зажигательной машины. Драгоценный алмаз сгорел без остатка, после чего ученый пришел к выводу, что алмаз представляет собой ничто иное как кристаллический углерод.

Интересно, что в этих опытах совместно с алмазом пробовали сжигать и другие драгоценные камни, к примеру, рубин. Но другие камни выдерживали высокую температуру, только алмаз сгорал без остатка, что и обратило внимание на его отличную химическую природу.
Углерод в таблице Менделеева
В основе расположения химических элементов в периодической системе Менделеева лежит их атомный вес, рассчитанный относительно атомного веса водорода. Атомная масса углерода составляет 12,011, согласно ней он занимает почетное 6-е место в таблице Менделеева и обозначается латинской литерой С.
Помимо этого следует обратить внимание на следующие характеристики углерода:
- Природный углерод состоит из смеси двух стабильных изотопов 12С (98,892%) и 13С (1,108%)
- Помимо этого известно 6 радиоактивных изотопов углерода. Один из них, изотоп 14С с периодом полураспада 5,73*103 лет в небольших количествах образуется в верхних слоях атмосферы нашей планеты под действием космического излучения.
Строение атома углерода
Атом углерода имеет 2 оболочки (как впрочем, и все элементы, расположенные во втором периоде) и 6 электронов: 1s22s22p2. Четыре валентных электрона находятся на внешнем электронном уровне атома углерода. А оставшиеся два электрона находятся на отдельных p-орбиталях, при этом они являются неспаренными.
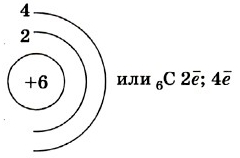
Так на картинке изображена схема электронного строения атома углерода.
Физические свойства углерода
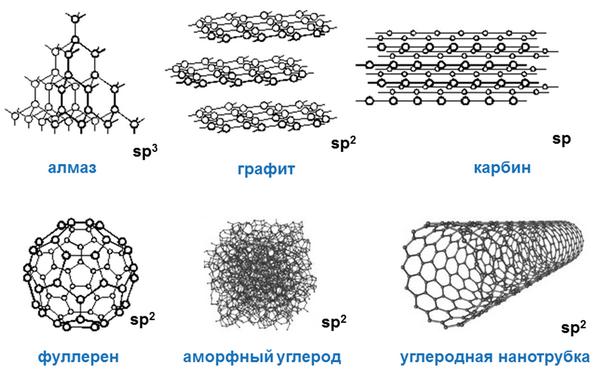
Своими физическими свойствами углерод типичный неметалл. При этом он образует множество аллотропных модификаций («аллотропные» означает существование двух и более разных веществ из одного химического элемента): наиболее популярными из них являются алмаз, графит, уголь, сажа. При этом алмаз – одно из самых твердых веществ, представляющих углерод.
Разумеется, разные аллотропные модификации углерода имеют и разные физические свойства. Если алмаз типичное твердое тело, то, к примеру, жидкий углерод, который можно получить только при определенном внешнем давлении, обладает совершенно иными физическими свойствами, нежели алмаз или графит.
Химические свойства углерода
В обычных условиях углерод, как правило, химически инертен, но при высоких температурах он может вступать в химические взаимодействия со многими другими элементами, обычно проявляя сильные восстановительные свойства. Приведем примеры химических реакций углерода как восстановителя с:
— с кислородом
C0 + O2 –t°= CO2 углекислый газ
при недостатке кислорода — неполное сгорание:
2C0 + O2 –t°= 2C+2O угарный газ
— со фтором
С + 2F2 = CF4
— с водяным паром
C0 + H2O –1200°= С+2O + H2 водяной газ
— с оксидами металлов. Таким образом, выплавляют металл из руды.
C0 + 2CuO –t°= 2Cu + C+4O2
— с кислотами – окислителями:
C0 + 2H2SO4(конц.) = С+4O2 + 2SO2 + 2H2O
С0 + 4HNO3(конц.) = С+4O2 + 4NO2 + 2H2O
— с серой образует сероуглерод:
С + 2S2 = СS2.
Порой углерод может выступать и как окислитель, образуя карбиды при вступлении в химические реакции с некоторыми металлами:
4Al + 3C0 = Al4C3
Ca + 2C0 = CaC2-4
Вступая в реакцию с водородом, углерод образует метан:
C0 + 2H2 = CH4
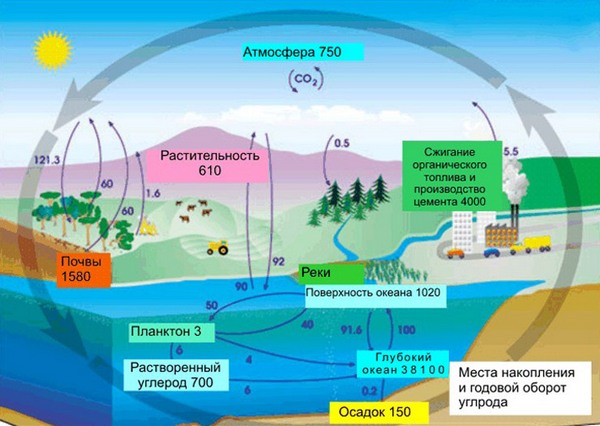
Углерод в природе
В земной коре содержание углерода составляет всего лишь 0,15%. Несмотря на эту кажущуюся маленькой цифру, стоит заметить, что углерод непрерывно участвует в природном круговороте из земной коры через биосферу в атмосферу и наоборот. Также именно из углерода состоят такие ценные ресурсы как нефть, уголь, торф, известняки и природный газ. И как мы писали в начале нашей статьи, углерод – основа жизни. Скажем, в теле взрослого человека с весом в 70 кг имеется около 13 кг углерода. Это только в одном человека, примерно в таких же пропорциях углерод содержится в телах всех других живых существ, растений и животных.

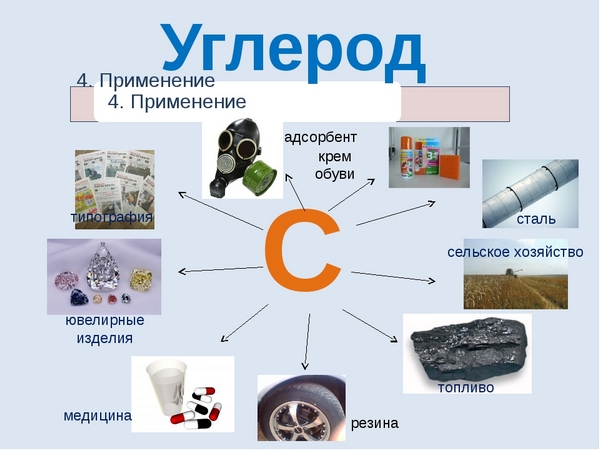
Применение углерода
Можно сказать, что углерод неразрывно связан с самим развитием человеческой цивилизации. Именно из соединений с участием углерода образованы основные топлива, благодаря которым ездят машины, летают самолеты, вы можете приготовить себе еду и обогреть свой дом в холодную пору – это нефть и газ. Помимо этого соединения углерода активно используются в химической и металлургической промышленности, в фармацевтике и строительстве. Алмазы, будучи аллотропной модификацией углерода используются в ювелирном деле и ракетостроении. В целом промышленность современности не может обойтись без углерода, он необходим практически везде.
Рекомендованная литература и полезные ссылки
- Savvatimskiy, A (2005). “Measurements of the melting point of graphite and the properties of liquid carbon (a review for 1963–2003)”. Carbon. 43 (6): 1115–1142. doi:10.1016/j.carbon.2004.12.027
- Химическая энциклопедия / Редкол.: Кнунянц И.Л. и др.. — М.: Советская энциклопедия, 1988. — Т. 1. — 623 с.
- ChemNet. Углерод: история открытия элемента.
- Лейпунский О. И. Об искусственных алмазах (рус.) // Успехи химии. — Российская академия наук, 1939. — Вып. 8. — С. 1519—1534.
- Seal M. The effect of surface orientation on the graphitization of diamond. // Phis. Stat. Sol., 1963, v. 3, p. 658.
Углерод, видео
И в завершение образовательное видео по теме нашей статьи.

Автор: Павел Чайка, главный редактор журнала Познавайка
При написании статьи старался сделать ее максимально интересной, полезной и качественной. Буду благодарен за любую обратную связь и конструктивную критику в виде комментариев к статье. Также Ваше пожелание/вопрос/предложение можете написать на мою почту pavelchaika1983@gmail.com или в Фейсбук, с уважением автор.
Источник
Углерод С находится в периодической таблице Менделеева под номером 6. Еще первобытные люди обратили внимание, что после сжигания древесины образуется уголь, которым можно рисовать на стенах пещеры. В составе любых органических соединений есть углерод. Наиболее изучены две аллотропные модификации углерода: графит и алмаз.
Графит — мягкое черное вещество, которое легко оставляет следы на бумаге, имеет металлический блеск.
Помимо этого, графит является отличным проводником тепла и электрического тока. Графит используют в промышленности для изготовления графитных смазок, а также для производства карандашей.
Графитовый сланец
[Deposit Photos]
В отличие от графита, структура алмаза (другой аллотропной модификации) напоминает тетраэдр. Кроме углерода, в состав алмаза также входят хром, кремний, алюминий, марганец, титан, железо. Наибольшую долю в составе алмаза углерод делит с азотом. Благодаря своей структуре он не проводит электрический ток и обладает слабой теплопроводностью. Алмазы используют для изготовления драгоценных камней — бриллиантов. Искусственно созданные алмазы используют для изготовления режущих инструментов, абразивных материалов.
[Wikipedia]
Еще одной аллотропной модификацией углерода признан фуллерен. Он состоит из множества атомов углерода, соединенных ковалентными связями. Молекулы в сложной структуре фуллерена удерживаются электростатическими и вандерваальсовыми силами. Свойства фуллерена еще не до конца изучены. Но уже известно, что благодаря своей способности поглощать свободные радикалы эта аллотропная модификация углерода может применяться при изготовлении лекарств.
Молекула фуллерена
[Deposit Photos]
Химические свойства углерода
1. Углерод является неметаллом и способен взаимодействовать с металлами и образовывать карбиды:
Ca + 2C = CaC₂
2. В кислородной среде углерод сгорает в два этапа:
2С + O₂ = 2CO
2СO₂ + О₂ = 2СО₂
3. При взаимодействии углерода и водорода получается органическое вещество — метан:
С + 2H₂ = CH₄
4. При испарении воды под раскаленным углем образуются угарный газ и водород:
C + H₂O = CO + H₂
5. Углерод не реагирует с хлором, бромом и йодом, но взаимодействует со фтором:
С + 2F₂ = CF₄
6. Реагирует с серой:
С + 2S = CS₂
7. Углерод способен восстанавливать металлы из их оксидов:
2ZnO + C = 2Zn + CO₂
8. При повышении температуры реакции углерод взаимодействует с серной кислотой:
C + 2H₂SO₄ = CO₂ + 2SO₂ + 2H₂O
Чтобы лучше изучить свойства этого элемента, рекомендуем провести несколько наглядных экспериментов.
Углерод в органической химии
Углерод занимает особое место в периодической cистеме. Благодаря своему строению он образует длинные цепочки связей линейной или циклической структуры. Известно более 10 миллионов органических соединений. Несмотря на свое разнообразие, на воздухе и под действием температуры они всегда будут превращаться в углекислый газ и воду.
[Deposit Photos]
Роль углерода в нашей повседневной жизни огромна. Без углекислого газа не будет происходить фотосинтез — один из основных биологических процессов.
Применение углерода
Углерод широко применяется в медицине для создания различных лекарств органической природы. Изотопы углерода позволяют проводить радиоуглеродный анализ. Без углерода невозможна работа металлургической промышленности. Уголь, сгорающий в твердотопливных пиролизных котлах, служит источником энергии. В нефтеперерабатывающей промышленности из органических соединений углерода производят бензин и дизельное топливо. В значительной мере углерод необходим для производства сахара. Также он применяется в синтезе органических соединений, важных для всех сфер повседневной жизни.
Источник
В природе углерода не так уж и много, но он есть везде:  в воздухе (углекислый газ и угарный газ), растворен в океанах и реках, залегает в ископаемых породах в земле, содержится в каждой клетке растения, животного, человека. Существует круговорот углерода в природе:
в воздухе (углекислый газ и угарный газ), растворен в океанах и реках, залегает в ископаемых породах в земле, содержится в каждой клетке растения, животного, человека. Существует круговорот углерода в природе:
— углекислый газ выделяется в атмосферу с вулканическими газами, из горячих источников, из поверхностных слоев рек и океанов, при сгорании топлив, при дыхании растений и животных;
— в тоже время, углекислый газ поглощается растениями, переходит в организм животных и людей, а после их смерти возвращается в почву.
В чистом виде и в значимых количествах углерод встречается только в виде алмазов и графитов. Но он — составная часть ископаемого топлива (уголь, нефть, газ, сланцы), торфа, битумов, природных минералов (мел, известняк, доломиты, карбонаты).
Токсическое действие
 При разработках угольных месторождений, при сжигании топлив, в процессе деятельности человека в воздух поступает большое количество аэрозолей углерода, попадающих в органы дыхания человека и животных. Регулярное вдыхание аэрозолей с высокой концентрацией углерода приводят к таким заболеваниям, как пылевой бронхит, антракоз. На всех производствах, связанных с углеродными аэрозолями и пылью, обязательно нормируется ПДК содержания алмазов, кокса, угля, углеродной пыли, сажи и др. Работники обязательно должны использовать средства защиты органов дыхания при работе с ними.
При разработках угольных месторождений, при сжигании топлив, в процессе деятельности человека в воздух поступает большое количество аэрозолей углерода, попадающих в органы дыхания человека и животных. Регулярное вдыхание аэрозолей с высокой концентрацией углерода приводят к таким заболеваниям, как пылевой бронхит, антракоз. На всех производствах, связанных с углеродными аэрозолями и пылью, обязательно нормируется ПДК содержания алмазов, кокса, угля, углеродной пыли, сажи и др. Работники обязательно должны использовать средства защиты органов дыхания при работе с ними.
Угарный газ и углекислый газ обладают токсическим действием, превышение ПДК этих газов в воздухе может вызвать летальный исход. Поэтому в закрытых помещениях большое внимание должно уделяться поглощению и удалению из воздуха углекислоты, выделяемой при дыхании.
Токсическим действием обладает радиоактивный изотоп С-14. Встраиваясь в молекулы белков, особенно в ДНК и РНК, он может оказывать мутагенное воздействие, поэтому для него тоже установлены ПДК содержания в воздухе рабочего помещения.
Применение
Нет ни одной области промышленности, в которой в той или иной степени не использовался бы углерод. Расскажем об основных сферах его использования:
• Основные виды ископаемого топлива на земле: нефть, уголь и газ — это соединения углерода. Они нужны для получения тепла, энергии, огромного количества химических материалов. 
• В сельском хозяйстве, в медицине, энергетике, в ядерной отрасли.
• В промышленной индустрии очень востребованы карбонаты.
• Графит используется при изготовлении карандашей, электродов, высокотемпературных и низкотемпературных смазок, красителей; тиглей для металлических заготовок, углепластиков, углеродных волокон, стеклоуглерода и других углеграфитовых материалов, отличающихся особо высокой жаростойкостью.
• Стеклоуглерод идет на производство тиглей и электродов.
• Техуглерод применяется как наполнитель при производстве резин для шин и пластмасс. Придает им прочность, долговечность и некоторые особые свойства.
• Алмазы применяются в технике, сверлении, лазерных установках, в ювелирном деле. Технические алмазы используются для получения абразивных материалов. Только сложность обработки и высокая стоимость мешают алмазам стать лучшим материалом для подложек процессоров.
• В медицине используется активированный уголь для вывода токсинов, а графит — в мазях для лечения болезней кожи.
• Фильтры на основе угля применяются в противогазах, респираторах, лицевых масках и сменных патронах для них; системах очистки воды.
• В научных исследованиях радиоуглеродный анализ на основе изотопа С-14 — один из самых важных анализов в археологии, геологии, палеонтологии.
• Большие перспективы у применения новых неорганических материалов на основе углерода. Об этом — следующая статья.
Источник
Полный курс химии вы можете найти на моем сайте CHEMEGE.RU. Чтобы получать актуальные материалы и новости ЕГЭ по химии, вступайте в мою группу в ВКонтакте или на Facebook. Если вы хотите подготовиться к ЕГЭ по химии на высокие баллы, приглашаю на онлайн-курс “40 шагов к 100 баллам на ЕГЭ по химии“.
1. Положение углерода в периодической системе химических элементов
2. Электронное строение углерода
3. Физические свойства и нахождение в природе
4. Качественные реакции
5. Химические свойства
5.1. Взаимодействие с простыми веществами
5.1.1. Взаимодействие с галогенами
5.1.2. Взаимодействие с серой и кремнием
5.1.3. Взаимодействие с водородом и фосфором
5.1.4. Взаимодействие с азотом
5.1.5. Взаимодействие с активными металлами
5.1.6. Горение
5.2. Взаимодействие со сложными веществами
5.2.1. Взаимодействие с водой
5.2.2. Взаимодействие с оксидами металлов
5.2.3. Взаимодействие с серной кислотой
5.2.4. Взаимодействие с азотной кислотой
5.2.5. Взаимодействие с солями
Бинарные соединения углерода – карбиды
Оксид углерода (II)
1. Строение молекулы и физические свойства
2. Способы получения
3. Химические свойства
3.1. Взаимодействие с кислородом
3.2. Взаимодействие с хлором
3.3. Взаимодействие с водородом
3.4. Взаимодействие с щелочами
3.5. Взаимодействие с оксидами металлов
3.6. Взаимодействие с прочими окислителями
Оксид углерода (IV)
1. Строение молекулы и физические свойства
2. Способы получения
3. Химические свойства
3.1. Взаимодействие с основными оксидами и основаниями
2.3. Взаимодействие с карбонатами и гидрокарбонатами
2.4. Взаимодействие с восстановителями
Карбонаты и гидрокарбонаты
Углерод
Положение в периодической системе химических элементов
Углерод расположен в главной подгруппе IV группы (или в 14 группе в современной форме ПСХЭ) и во втором периоде периодической системы химических элементов Д.И. Менделеева.
Электронное строение углерода
Электронная конфигурация углерода в основном состоянии
Электронная конфигурация углерода в возбужденном состоянии
Атом углерода содержит на внешнем энергетическом уровне 2 неспаренных электрона и 1 неподеленную электронную пару в основном энергетическом состоянии и 4 неспаренных электрона в возбужденном энергетическом состоянии.
Степени окисления атома углерода – от -4 до +4.
Характерные степени окисления -4, 0, +2, +4.
Физические свойства
Углерод в природе существует в виде нескольких аллотропных модификаций: алмаз, графит, карбин, фуллерен.
Алмаз – это модификация углерода с атомной кристаллической решеткой. Алмаз – самое твердое минеральное кристаллическое вещество, прозрачное, плохо проводит электрический ток и тепло. Атомы углерода в алмазе находятся в состоянии sp³-гибридизации.
Алмаз
Кристаллы алмаза
Графит – это аллотропная модификация, в которой атомы углерода находятся в состоянии sp² -гибридизации. При этом атомы связаны в плоские слои, состоящие из шестиугольников, как пчелиные соты. Слои удерживаются между собой слабыми связями. Это наиболее устойчивая при нормальных условиях аллотропная модификация углерода.
Графит – мягкое вещество серо-стального цвета, с металлическим блеском. Хорошо проводит электрический ток. Жирный на ощупь.
Графит
Карбин – вещество, в составе которого атомы углерода находятся в sp-гибридизации. Состоит из цепочек и циклов, в которых атомы углерода соединены двойными и тройными связями. Карбин – мелкокристаллический порошок серого цвета.
[=C=C=C=C=C=C=]n или [–C≡C–C≡C–C≡C–]n
Карбин
Карбин
Фуллерен – это искусственно полученная модифицикация углерода. Молекулы фуллерена – выпуклые многогранники С₆₀, С₇₀ и др. Многогранники образованы пяти- и шестиугольниками, в вершинах которых расположены атомы углерода.
Фуллерены – черные вещества с металлическим блеском, обладающие свойствами полупроводников.
Фуллерен
В природе углерод встречается как в виде простых веществ (алмаз, графит), так и в виде сложных соединений (органические вещества – нефть, природные газ, каменный уголь, карбонаты).
Качественные реакции
Качественная реакция на карбонат-ионы CO₃²⁻ – взаимодействие солей-карбонатов с сильными кислотами. Более сильные кислоты вытесняют угольную кислоту из солей. При этом выделяется бесцветный газ, не поддерживающий горение – углекислый газ.
Например, карбонат кальция растворяется в соляной кислоте:
CaCO₃ + 2HCl → CaCl₂ + H₂O + CO₂
Видеоопыт взаимодействия карбоната кальция с соляной кислотой можно посмотреть здесь.
Качественная реакция на углекислый газ CO₂ – помутнение известковой воды при пропускании через нее углекислого газа:
CO₂ + Ca(OH)₂ → CaCO₃ + H₂O
При дальнейшем пропускании углекислого газа осадок растворяется, т.к. карбонат кальция под действием избытка углекислого газа переходит в растворимый гидрокарбонат кальция:
CaCO₃ + CO₂ + H₂O → Ca(HCO₃)₂
Карбонат кальция с углекислым газом
Видеоопыт взаимодействия гидроксида кальция с углекислым газом (качественная реакция на углекислый газ) можно посмотреть здесь.
Углекислый газ СО₂ не поддерживает горение. Угарный газ CO горит голубым пламенем.
Горение угарного газа
Соединения углерода
Основные степени окисления углерода – +4, +2, 0, -1 и -4.
Наиболее типичные соединения углерода:
Химические свойства
При нормальных условиях углерод существует, как правило, в виде атомных кристаллов (алмаз, графит), поэтому химическая активность углерода – невысокая.
- Углерод проявляет свойства окислителя (с элементами, которые расположены ниже и левее в Периодической системе) и свойства восстановителя (с элементами, расположенными выше и правее). Поэтому углерод реагирует и с металлами, и с неметаллами.
1.1. Из галогенов углерод при комнатной температуре реагирует с фтором с образованием фторида углерода:
C + 2F₂ → CF₄
1.2. При сильном нагревании углерод реагирует с серой и кремнием с образованием бинарного соединения сероуглерода и карбида кремния соответственно:
C + 2S → CS₂
C + Si → SiC
1.3. Углерод не взаимодействует с фосфором.
При взаимодействии углерода с водородом образуется метан. Реакция идет в присутствии катализатора (никель) и при нагревании:
С + 2Н₂ → СН₄
1.4. С азотом углерод реагирует при действии электрического разряда, образуя дициан:
2С + N₂ → N≡C–C≡N
1.5. В реакциях с активными металлами углерод проявляет свойства окислителя. При этом образуются карбиды:
4C + 3Al → Al₄C₃
2C + Ca → CaC₂
1.6. При нагревании с избытком воздуха графит горит, образуя оксид углерода (IV):
C + O₂ → CO₂
при недостатке кислорода образуется угарный газ СО:
2C + O₂ → 2CO
Алмаз горит при высоких температурах:
Горение алмаза в жидком кислороде
Графит также горит
Графитовые стержни под напряжением:
2. Углерод взаимодействует со сложными веществами:
2.1. Раскаленный уголь взаимодействует с водяным паром с образованием угарного газа и водорода:
CO + H₂ + O → C + 2O + H₂O
2.2. Углерод восстанавливает многие металлы из основных и амфотерных оксидов. При этом образуются металл и угарный газ. Получение металлов из оксидов с помощью углерода и его соединений называют пирометаллургией.
Например, углерод взаимодействует с оксидом цинка с образованием металлического цинка и угарного газа:
2ZnO + C → 2Zn + CO
Также углерод восстанавливает железо из железной окалины:
4С + Fe₃O₄ → 3Fe + 4CO
При взаимодействии с оксидами активных металлов углерод образует карбиды.
Например, углерод взаимодействует с оксидом кальция с образованием карбида кальция и угарного газа. Таким образом, углерод диспропорционирует в данной реакции:
3С + СаО → СаС₂ + СО
9С + 2Al₂O₃ → Al₄C₃ + 6CO
2.3. Концентрированная серная кислота окисляет углерод при нагревании. При этом образуются оксид серы (IV), оксид углерода (IV) и вода:
C + 2H₂SO₄(конц) → CO₂ + 2SO₂ + 2H₂O
2.4. Концентрированная азотная кислотой окисляет углерод также при нагревании. При этом образуются оксид азота (IV), оксид углерода (IV) и вода:
C + 4HNO₃ (конц) → CO₂ + 4NO₂ + 2H₂O
2.5. Углерод проявляет свойства восстановителя и при сплавлении с некоторыми солями, в которых содержатся неметаллы с высокой степенью окисления.
Например, углерод восстанавливает сульфат натрия до сульфида натрия:
4C + Na₂SO₄ → Na₂S + 4CO
Карбиды
Карбиды – это соединения элементов с углеродом. Карбиды разделяют на ковалентные и ионные в зависимости от типа химической связи между атомами.
Создать карусель Добавьте описание
Все карбиды проявляют свойства восстановителей и могут быть окислены сильными окислителями.
Например, карбид кремния окисляется концентрированной азотной кислотой при нагревании до углекислого газа, оксида кремния (IV) и оксида азота (II):
SiC + 8HNO₃ → 3SiO₂ + 3CO₂ + 8NO + 4H₂O
Оксид углерода (II)
Строение молекулы и физические свойства
Оксид углерода (II) (“угарный газ”) – это газ без цвета и запаха. Сильный яд. Небольшая концентрация угарного газа в воздухе может вызвать сонливость и головокружение. Большие концентрации угарного газа вызывают удушье.
Строение молекулы оксида углерода (II) – линейное. Между атомами углерода и кислорода образуется тройная связь, за счет дополнительной донорно-акцепторной связи:
Способы получения
В лаборатории угарный газ можно получить действием концентрированной серной кислоты на муравьиную или щавелевую кислоты:
НСООН → CO + H₂O
H₂C₂O₄ → CO + CO₂ + H₂O
В промышленности угарный газ получают в газогенераторах при пропускании воздуха через раскаленный уголь:
C + O₂ → CO₂
CO₂ + C → 2CO
Еще один важный промышленный способ получения угарного газа – паровая конверсия метана. При взаимодействии перегретого водяного пара с метаном образуется угарный газ и водород:
СН₄ + Н₂O → СО + 3Н₂
Также возможна паровая конверсия угля:
CO + H₂ + O → C + 2O + H₂O
Угарный газ в промышленности также можно получать неполным окислением метана:
2СН₄ + О₂ → 2СО + 4Н₂
Химические свойства
Оксид углерода (II) – несолеобразующий оксид. За счет углерода со степенью окисления +2 проявляет восстановительные свойства.
- Угарный газ горит в атмосфере кислорода. Пламя окрашено в синий цвет:
2СO + O₂ → 2CO₂
2. Оксид углерода (II) окисляется хлором в присутствии катализатора или под действием света с образованием фосгена. Фосген – ядовитый газ.
CO + Cl₂ → COCl₂
3. Угарный газ взаимодействует с водородом при повышенном давлении. Смесь угарного газа и водорода называется синтез-газ. В зависимости от условий из синтез-газа можно получить метанол, метан, или другие углеводороды.
Например, под давлением больше 20 атмосфер, при температуре 350°C и под действием катализатора угарный газ реагирует с водородом с образованием метанола:
СО + 2Н₂ → СН₃ОН
4. Под давлением оксид углерода (II) реагирует с щелочами. При этом образуется формиат – соль муравьиной кислоты.
Например, угарный газ реагирует с гидроксидом натрия с образованием формиата натрия:
CO + NaOH → HCOONa
5. Оксид углерода (II) восстанавливает металлы из оксидов.
Например, оксид углерода (II) реагирует с оксидом железа (III) с образованием железа и углекислого газа:
3CO + Fe₂O₃ → 2Fe + 3CO₂
Оксиды меди (II) и никеля (II) также восстанавливаются угарным газом:
СО + CuO → Cu + CO₂
СО + NiO → Ni + CO₂
6. Угарный газ окисляется и другими сильными окислителями до углекислого газа или карбонатов.
Например, пероксидом натрия:
CO + Na₂O₂ → Na₂CO₃
Оксид углерода (IV)
Строение молекулы и физические свойства
Оксид углерода (IV) (углекислый газ) – газ без цвета и запаха. Тяжелее воздуха. Замороженный углекислый газ называют также “сухой лед”. Сухой лед легко подвергается сублимации – переходит из твердого состояния в газообразное.
Смешивая сухой лед и различные вещества, можно получить интересные эффекты. Например, сухой лед в пиве:
Углекислый газ не горит, поэтому его применяют при пожаротушении.
Молекула углекислого газа линейная, атом углерода находится в состоянии sp-гибридизации, образует две двойных связи с атомами кислорода:
Обратите внимание! Молекула углекислого газа не полярна. Каждая химическая связь С=О по отдельности полярна, а вся молекула не будет полярна. Объяснить это очень легко. Обозначим направление смещения электронной плотности в полярных связях стрелочками (векторами):
Теперь давайте сложим эти векторы. Сделать это очень легко. Представьте, что атом углерода – это покупатель в магазине. А атомы кислорода – это консультанты, которые тянут его в разные стороны. В данном опыте консультанты одинаковые, и тянут покупателя в разные стороны с одинаковыми силами. Несложно увидеть, что покупатель двигаться не будет ни влево, ни вправо. Следовательно, сумма этих векторов равна нулю. Следовательно, полярность молекулы углекислого газа равна нулю.
Способы получения
В лаборатории углекислый газ можно получить разными способами:
- Углекислый газ образуется при действии сильных кислот на карбонаты и гидрокарбонаты металлов. При этом взаимодействуют с кислотами и нерастворимые карбонаты, и растворимые.
Например, карбонат кальция растворяется в соляной кислоте:
CaCO₃ + 2HCl → CaCl₂ + H₂O + CO₂
Видеоопыт взаимодействия карбоната кальция с соляной кислотой можно посмотреть здесь.
Еще один пример: гидрокарбонат натрия реагирует с бромоводородной кислотой:
NaHCO₃ + HBr → NaBr + H₂O + CO₂
2. Растворимые карбонаты реагируют с растворимыми солями алюминия, железа (III) и хрома (III). Карбонаты трехвалентных металлов необратимо гидролизуются в водном растворе.
Например: хлорид алюминия реагирует с карбонатом калия. При этом выпадает осадок гидроксида алюминия, выделяется углекислый газ и образуется хлорид калия:
2AlCl₃ + 3K₂CO₃ + 3H₂O → 2Al(OH)₃↓ + CO₂↑ + 6KCl
3. Углекислый газ также образуется при термическом разложении нерастворимых карбонатов и при разложении растворимых гидрокарбонатов.
Например, карбонат кальция разлагается при нагревании на оксид кальция и углекислый газ:
CaCO₃ → CaO + CO₂
Химические свойства
Углекислый газ – типичный кислотный оксид. За счет углерода со степенью окисления +4 проявляет слабые окислительные свойства.
- Как кислотный оксид, углекислый газ взаимодействует с водой. Реакция очень сильно обратима, поэтому мы считаем, что в реакциях угольная кислота распадается почти полностью при образовании.
CO₂ + H₂O ↔ H₂CO₃
2. Как кислотный оксид, углекислый газ взаимодействует с основными оксидами и основаниями. При этом углекислый газ реагирует только с сильными основаниями (щелочами) и их оксидами. При взаимодействии углекислого газа с щелочами возможно образование как кислых, так и средних солей.
Например, гидроксид калия взаимодействует с углекислым газом. В избытке углекислого газа образуется кислая соль, гидрокарбонат калия:
KOH + CO₂ → KHCO₃
При избытке щелочи образуется средняя соль, карбонат калия:
2KOH + CO₂ → K₂CO₃ + H₂O
Помутнение известковой воды – качественная реакция на углекислый газ:
Ca(OH)₂ + CO₂ → CaCO₃ + H₂O
Видеоопыт взаимодействия гидроксида кальция (известковая вода) с углекислым газом можно посмотреть здесь.
3. Углекислый газ взаимодействует с карбонатами. При пропускании СО₂ через раствор карбонатов образуются гидрокарбонаты.
Например, карбонат натрия взаимодействует с углекислым газом. В избытке углекислого газа образуется кислая соль, гидрокарбонат натрия:
Na₂CO₃ + CO + H₂O → 2NaHCO₃
4. Как слабый окислитель, углекислый газ взаимодействует с некоторыми восстановителями.
Например, углекислый газ взаимодействует с углеродом с образованием угарного газа:
CO₂ + C → 2CO
Магний горит в атмосфере углекислого газа:
2Мg + CO₂ → C + 2MgO
Видеоопыт взаимодействия магния с углекислым газом можно посмотреть здесь.
Поэтому углекислый газ нельзя применять для пожаротушения горящего магния.
Углекислый газ взаимодействует с пероксидом натрия. При этом пероксид натрия диспропорционирует:
2CO₂ + 2Na₂O₂ → 2Na₂CO₃ + O₂
Карбонаты и гидрокарбонаты
При нагревании карбонаты (все, кроме карбонатов щелочных металлов и аммония) разлагаются до оксида металла и оксида углерода (IV).
CaCO₃ → CaO + CO₂
Карбонат аммония при нагревании разлагается на аммиак, воду и углекислый газ:
(NH₄)₂CO₃ → 2NH₃ + 2H₂O + CO₂
Гидрокарбонаты при нагревании переходят в карбонаты:
2NaHCO₃ → Na₂CO₃ + CO₂ + H₂O
Качественной реакцией на ионы СО₃²⁻ и НСО³⁻ является их взаимодействие с более сильными кислотами, последние вытесняют угольную кислоту из солей, а та разлагается с выделением СО₂.
Например, карбонат натрия взаимодействует с соляной кислотой:
Na₂CO₃ + 2HCl → 2NaCl + CO₂↑ + H₂O
Гидрокарбонат натрия также взаимодействует с соляной кислотой:
NaHCO₃ + HCl → NaCl + CO₂↑ + H₂O
Гидролиз карбонатов и гидрокарбонатов
Растворимые карбонаты и гидрокарбонаты гидролизуются по аниону. Гидролиз протекает ступенчато и обратимо, т.е. чуть-чуть:
I ступень: CO₃²⁻ + H₂O = HCO₃⁻ + OH⁻
II ступень: HCO₃⁻ + H₂O = H₂CO₃ + OH⁻
Однако карбонаты и гидрокарбонаты алюминия, хрома (III) и железа (III) гидролизуются необратимо, полностью, т.е. в водном растворе не существуют, а разлагаются водой:
Al??
