На каких химических свойствах кислорода основано его применение
Кислород – химический элемент VI группы периодической системы Менделеева и самый распространенный элемент в земной коре (47% от ее массы). Кислород является жизненно важным элементом почти всех живых организмов. Более подробно о функциях и применении кислорода в этой статье.

Общие сведения
Кислород представляет собой бесцветный газ без вкуса и запаха, который плохо растворяется в воде. Он входит в состав воды, минералов, горных пород. Свободный кислород образуется благодаря процессам фотосинтеза. Кислород играет наиважнейшую роль в жизни человека. Прежде всего кислород необходим для дыхания живых организмов. Также он принимает участие в процессах разложения погибших животных и растений.
Воздух содержит около 20,95% по объему кислорода. В гидросфере содержится почти 86% по массе кислорода.
Кислород был получен одновременно двумя учеными, но сделали они это независимо друг от друга. Швед К. Шееле получил кислород при прокаливании селитры и других веществ, а англичанин Дж. Пристли – при нагревании оксида ртути.

Рис. 1. Получение кислорода из оксида ртути
Применение кислорода в промышленности
Области применения кислорода обширны.
В металлургии он необходим для производства стали, которую получают из металлолома и чугуна. Во многих металлургических агрегатах для лучшего сжигания топлива используют воздух, обогащенный кислородом.
В авиации кислород используется как окислитель топлива в ракетных двигателях. Также он необходим для полетов в космос и в условиях, где нет атмосферы.
В области машиностроения кислород очень важен для резки и сварки металлов. Чтобы расплавить металл нужна специальная горелка, состоящая из металлических труб. Эти две трубы вставляются друг в друга. Свободное пространство между ними заполняют ацетиленом и зажигают. Кислород же в это время пускают по внутренней трубке. И кислород и ацетилен подаются из баллона под давлением. Образуется пламя, температура в котором достигает 2000 градусов. При такой температуре плавится практически любой металл.

Рис. 2. Ацетиленовая горелка
Применение кислорода в целлюлозно-бумажной промышленности очень важно. Он используется для отбеливания бумаги, при спиртовании, при вымывании лишних компонентов из целлюлозы (делигнификация).
В химической промышленности кислород используется в качестве реагента.
Для создания взрывчатых веществ необходим жидкий кислород. Жидкий кислород производится путем сжижения воздуха и последующего отделения кислорода от азота.
Применение кислорода в природе и жизни человека
Кислород играет наиважнейшую роль в жизни человека и животных. Свободный кислород существует на нашей планете благодаря фотосинтезу. Фотосинтез – это процесс образования органического вещества на свету с помощью углекислого газа и воды. В результате этого процесса образуется кислород, который необходим для жизнедеятельности животных и человека. Животные и человек потребляют кислород постоянно, растения же расходуют кислород только ночью, а днем производят его.
Применение кислорода в медицине
Кислород находит применение и в медицине. Особенно актуально его использование при затрудненном дыхании во время некоторых заболеваний. Он применяется для обогащения дыхательных путей при туберкулезе легких, а также используется в наркозной аппаратуре. Кислород в медицине используется для лечения бронхиальной астмы, болезней желудочно-кишечного тракта. Для этих целей используют кислородные коктейли.
Также большое значение имеют кислородные подушки – прорезиненная емкость, заполненная кислородом. Она служит для индивидуального применения медицинского кислорода.
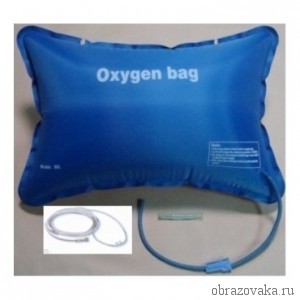
Рис. 3. Кислородная подушка
Что мы узнали?
В данном сообщении, которое охватывает тему «Кислород» по химии 9 класса кратко даны общие сведения о свойствах и применении этого газа. Кислород крайне важен для машиностроения, медицины, металлургической области и т.д.
Тест по теме
Доска почёта
Чтобы попасть сюда – пройдите тест.
-
Лидия Маслова
10/10
Тимофей Кот
10/10
Эльшан Асланов
9/10
Александр Джураев
9/10
Любовь Жовтенко
9/10
Андрей Бордюгов
9/10
Оценка доклада
Средняя оценка: 4.6. Всего получено оценок: 424.
Источник
Четыре элемента-«халькогена» (т.е. «рождающих медь») возглавляют главную подгруппу VI группы (по новой классификации – 16-ю группу) периодической системы. Кроме серы, теллура и селена к ним также относится кислород. Давайте подробно разберем свойства этого наиболее распространенного на Земле элемента, а также применение и получение кислорода.
Распространенность элемента
Содержание кислорода в земной коре составляет практически 50%. Он находится в различных минералах в виде оксидов и солей.
В связанном виде кислород входит в химический состав воды – его процентное соотношение составляет порядка 89%, а также в состав клеток всех живых существ – растений и животных.
В воздухе кислород находится в свободном состоянии в виде О2, занимая пятую часть его состава, и в виде озона – О3.
Физические свойства
Кислород О2 представляет собой газ, который не обладает цветом, вкусом и запахом. В воде растворяется слабо. Температура кипения – 183 градуса ниже нуля по Цельсию. В жидком виде кислород имеет голубой цвет, а в твердом виде образует синие кристаллы. Температура плавления кислородных кристаллов составляет 218,7 градуса ниже нуля по Цельсию.
Химические свойства
При нагревании этот элемент реагирует со многими простыми веществами, как металлами, так и неметаллами, образуя при этом так называемые оксиды – соединения элементов с кислородом. Химическая реакция, в которую элементы вступают с кислородом, называется окислением.
Например,
4Na + О2= 2Na2O
S + О2 = SO2
Некоторые из сложных веществ также вступают в реакцию с кислородом, тоже образуя при этом оксиды:
СН4 + 2О2= СО2 + 2Н2О
2СО + О2 = 2СО2
Если какое-либо вещество медленно реагирует с кислородом, то такое окисление называется медленным. Например, это процессы разложения пищевых продуктов, гниение.
Получение кислорода
Этот химический элемент можно получить как в лаборатории, так и на промышленном предприятии.
Получение кислорода в лаборатории проводится несколькими способами:
1. С помощью реакции разложения бертолетовой соли (хлората калия).
2. Через разложение перекиси водорода при нагревании ее в присутствии оксида марганца, выступающего в роли катализатора.
3. Через разложение перманганата калия.
Получение кислорода в промышленности проводится такими способами:
1. Для технических целей кислород получают из воздуха, в котором обычное его содержание составляет порядка 20%, т.е. пятую часть. Для этого воздух сначала сжигают, получая смесь с содержанием жидкого кислорода около 54%, жидкого азота – 44% и жидкого аргона – 2%. Затем эти газы разделяют с помощью процесса перегонки, используя сравнительно небольшой интервал между температурами кипения жидкого кислорода и жидкого азота – минус 183 и минус 198,5 градуса соответственно. Получается, что азот испаряется раньше, чем кислород.
Современная аппаратура обеспечивает получение кислорода любой степени чистоты. Азот, который получается при разделении жидкого воздуха, используется в качестве сырья при синтезе его производных.
2. Электролиз воды также дает кислород очень чистой степени. Этот способ получил распространение в странах с богатыми ресурсами и дешевой электроэнергией.
Применение кислорода
Кислород является основным по значению элементом в жизнедеятельности всей нашей планеты. Этот газ, который содержится в атмосфере, расходуется в процессе дыхания растениями, животными и людьми.
Получение кислорода очень важно для таких сфер деятельности человека, как медицина, сварка и резка металлов, взрывные работы, авиация (для дыхания людей и для работы двигателей), металлургия.
В процессе хозяйственной деятельности человека кислород расходуется в больших количествах – например, при сжигании различных видов топлива: природного газа, метана, угля, древесины. Во всех этих процессах образуется оксид углерода. При этом природа предусмотрела процесс естественного связывания данного соединения с помощью фотосинтеза, который проходит в зеленых растениях под действием солнечного света. В результате этого процесса образуется глюкоза, которую растение потом расходует для строительства своих тканей.
Источник
Химические свойства кислорода. Оксиды. Применение. Круговорот кислорода в природе
Данный урок посвящен изучению химических свойств простого вещества кислорода. Из материалов урока вы узнаете, на каких свойствах кислорода основано его применение в металлургии, медицине, пищевой промышленности и других областях.
I. Химические свойства кислорода
Кислород энергично реагирует со многими веществами: простыми – металлами и неметаллами и сложными.
Химические реакции взаимодействия веществ с кислородом называются реакциями окисления.
Химическая реакция, при которой происходит окисление веществ с выделением тепла и света называется реакцией горения.
Продуктами реакций взаимодействия веществ с кислородом, в большинстве случаев, являются оксиды.
Оксиды – это сложные вещества, которые состоят из двух элементов, одним из которых является кислород.
Общая формула оксидов: ЭхОу , где Э – это химический элемент в валентности = Nгруппы(для элементов главных подгрупп «А»), О – это кислород в валентности (II), Х и У – это индексы, полученные исходя из валентностей элемента.
1. С большинством металлов кислород реагирует уже при комнатной температуре, образуя оксиды.
- Железо сгорает в кислороде при температуре с треском и разбрасыванием искр, при этом образуется железная окалина Fe3O4 – это соединение двух оксидов железа: FeOв валентности (II) и Fe2O3в валентности (III):
3Fe + 2O2 = FeO· Fe2O3(железная окалина Fe3O4)
- А вот медь не горит в кислороде, а окисляется кислородом при нагревании. При этом образуется оксид меди (II): 2Cu + O2 = 2CuO
- Взаимодействия кислорода с магнием.
Видео – эксперимент: “Взаимодействие кислорода с магнием”
В атмосфере кислорода магний вспыхивает ослепительным белым пламенем.При горении магния выделяются ультрафиолетовые лучи. 2Mg + O2= 2MgO
2. С неметаллами (за исключением гелия, неона, аргона) кислород реагирует, как правило, при нагревании. Так, с фосфором он реагирует при температуре ~ 60 °С, образуя Р2О5, с серой – при температуре около 250 °С.
- Взаимодействие с серой: S + О2 = SO2
В чистом кислороде сера сгорает быстрее, чем на воздухе.
- С графитом кислород реагирует при 700 °С: С + О2 = СО2.
Если сжечь уголь в сосуде с кислородом, то в этом случае уголь сгорит быстрее, чем на воздухе. То есть, скорость горения угля в кислороде выше, чем на воздухе.
- Взаимодействие кислорода с азотом начинается лишь при 1200 ° С или в электрическом разряде: N2 + О2= 2NО
- Горение фосфора в кислороде: 4P + 5O2 = 2P2O5
3. Кислород реагирует и со многими сложными соединениями, например с оксидом азота (II) он реагирует уже при комнатной температуре: 2NО + О2 = 2NО2
Сероводород, реагируя с кислородом при нагревании, дает серу: 2Н2S + О2 = 2S+ 2Н2О
или оксид серы (IV): 2Н2S + ЗО2 = 2SО2 + 2Н2О в зависимости от соотношения между кислородом и сероводородом.
Алгоритм составления реакций взаимодействия веществ с кислородом
II. Применение кислорода
Применение любого вещества связано с его свойствами. Так и применение кислорода обусловлено, в основном, его способностями поддерживать дыхание и обеспечивать горение.
Рассмотрим основные области применения кислорода.
1. В металлургии, для резки и сварки металлов
Кислород используют в металлургии при производстве стали. Также, во многих металлургических агрегатах для более эффективного сжигания топлива вместо воздуха в горелках используют кислородо-воздушную смесь, т.е. обогащают воздух кислородом.
Рис. 1. Производство стали
Кислород в баллонах широко используется для газопламенной резки и сварки металлов. Горючий газ ацетилен, сгорая в токе кислорода, позволяет получить температуру выше 3000°С! Это приблизительно вдвое больше температуры плавления железа.
2. Окислитель топлива
Кислород, входящий в состав воздуха, применяют для сжигания топлива: например, в двигателях автомобилей, тепловозов и теплоходов.
В качестве окислителя для ракетного топлива применяется жидкий кислород. Смесь жидкого кислорода и жидкого озона — один из самых мощных окислителей ракетного топлива.
3. Применение в медицинских целях
В медицине кислород тоже нашел свое применение. Кислород используется для обогащения дыхательных газовых смесей при нарушении дыхания, для лечения астмы, профилактики гипоксии в виде кислородных коктейлей, кислородных подушек. Однако чистым кислородом при нормальном давлении долго дышать нельзя – это опасно для здоровья.
4. Применение в пищевой промышленности
В пищевой промышленности кислород зарегистрирован в качестве пищевой добавки E948, как пропеллент и упаковочный газ. Пропелленты — газы, выдавливающие пищевые продукты из ёмкости (контейнера, баллончика со спреем, танка или хранилища для сыпучих продуктов).
5. Биологическая роль
Кислород выполняет бесценную биологическую роль.
Кислород необходим практически всем живым существам для дыхания. Дыхание – это окислительно-восстановительный процесс, где кислород является окислителем. С помощью дыхания живые существа вырабатывают энергию, необходимую для поддержания жизни.
III. Круговорт кислорода в природе
В природе кислород образуется в процессе фотосинтеза, который происходит в зелёных растениях на свету. В целях сохранения кислорода в воздухе вокруг городов и крупных промышленных центров создаются зоны зелёных насаждений.
10 удивительных фактов о кислороде, которые должен знать каждый
Наша планета поддерживает жизнь благодаря наличию воды, атмосферы и ее защитных слоев. Земля могла бы быть каменной пустыней, если бы не кислород — элемент, питающий жизнь на нашей планете. Вот интересные факты о газе, который содержится в нашей атмосфере в количестве 21 % ее объема.
1. Кислород не горит
Как ни удивительно, это чистая правда. Кислород способствует горению других элементов, но не горит сам. И хорошо, ведь если бы это было не так, одной горящей, спички было бы достаточно, чтобы сжечь весь кислород в атмосфере нашей планеты.
2. Кислород хорошо растворяется
Он растворяется в воде почти в два раза лучше, чем азот. Если бы у этого элемента была такая же растворимость, как у азота, в морях, озерах и реках было бы намного меньше кислорода, что сделало бы жизнь намного труднее для огромного количества живых организмов.
3. Вес кислорода
Этот газ отвечает за почти две трети веса большинства живых организмов, главным образом потому, что живые существа состоят из большого количества воды, а 88,9 % веса воды составляет кислород.
4. Нестабильный газ
Кислород (O) нестабилен в атмосфере нашей планеты и регулярно исчезает, поэтому его запас должен постоянно пополняться фотосинтезом. Без растительности и водорослей наша атмосфера почти не содержала бы O.
Кстати, говоря о водорослях, зеленые морские водоросли обеспечивают приблизительно 70 % кислорода, произведенного на Земле посредством фотосинтеза, остальные 30 % произведены оставшимися зелеными растениями.
5. Инопланетная жизнь
Если мы обнаружим какие-либо другие планеты с атмосферами, богатыми кислородом, можно быть практически уверенными, что на этих планетах присутствует жизнь. Значительное количество O наблюдается только там, где оно может пополняться живыми организмами.
6. Земная кора
Всего пять химических элементов составляют более 90 % веса земной коры. Почти половина этого веса — кислород. Кремний, алюминий, железо и кальций — оставшиеся элементы.
7. Холод
Мировые океаны содержат немало растворенного в воде кислорода, который поддерживает жизнь. Полярные океаны, будучи самыми холодными, содержат больше растворенного кислорода и поэтому поддерживают огромное количество живых организмов.
8. Озон
Озон (O3) – аллотропная форма кислорода, которая реагирует лучше, чем обычный кислород. Озон выделяется в природе во время крупных электрических выбросов (штормы и грозы с молниями) или ультрафиолетовым излучением в верхних слоях атмосферы Земли. Озон действует как защитный слой, предохраняющий нас от вредного воздействия ультрафиолетовых лучей. Иногда озон вместо хлора используется в обработке питьевой воды.
9. Вода
Вода (H2O) является самой широко известной молекулой, содержащей кислород. Другие известные молекулы являются оксидами, например, оксид железа, или ржавчина (Fe2O3), углекислый газ (CO2), окись алюминия (Al2O3) и кварц (SiO2).
10. Яд или афродизиак?
Слишком большое количество кислорода может оказаться токсичным. Это опасно во время подводного плавания, когда в легкие попадает большее количество О, чем обычно.
Кроме того, кислород, по мнению многих, вызывает состояние эйфории, но его воображаемые эффекты на спортивных состязаниях не доказаны с медицинской точки зрения.
IV. Выполните тест
V. Лабиринт “Кислород”
VI. Кроссворд
ЦОРы
Видео: “Горение магния в кислороде”
Видео-презентация:“Круговорот кислорода в природе”
Видео: “Горение фосфора в кислороде”
Домашнее задание
- Параграф 23,24
- Стр. 80 упр. 5-7 (письменно)
- Выполните тест
- ИДЗ
Источник
Цель урока: изучить физические и химические
свойства кислорода, дать общее понятие об
оксидах, реакциях горения; рассмотреть
практическую значимость и применение; доказать,
что кислород – один из важнейших элементов на
Земле.
Задачи урока:
Образовательные:
- Расширить представления обучающихся о
кислороде. - Познакомить со свойствами и применением
кислорода. - Совершенствовать умения составлять уравнения
химических реакций.
Воспитательные:
- Формировать умения работать в парах у каждого
обучающегося, считаться с мнением соседа и
отстаивать свою точку зрения корректно, выполняя
упражнения. - Воспитывать бережное отношение к своему
здоровью, окружающей природе, учить понимать
прекрасное, ценить произведения искусства.
Развивающие:
- Способствовать продолжению развития
устойчивого интереса к химической науке и
практике. - Совершенствовать навыки самостоятельной
работы, развивать умения наблюдать,
формулировать высказывания. - Способствовать развитию исследовательских
навыков, соблюдая правила техники безопасности. - Совершенствовать умения обобщать и делать
выводы.
Планируемые результаты:
- личностные: готовность и способность
учащихся к саморазвитию, самоопределению;
ответственное отношение к учению; способность
ставить цели и строить жизненные планы;
формирование коммуникативной культуры, ценности
здорового и безопасного образа жизни; - метапредметные: уметь ставить цель и
планировать пути её достижения, выбирая более
рациональные способы решения данной проблемы;
учиться корректировать свои действия в связи с
изменением создавшейся ситуации; уметь
создавать, применять и преобразовывать знаки и
символы, модели и схемы для решения учебных и
познавательных задач; уметь осознанно
использовать речевые средства в соответствии с
задачей коммуникации для выражения своих мыслей
и потребностей; уметь организовывать совместную
работу со сверстниками в парах; уметь находить
информацию в различных источниках; владеть
навыками самоконтроля, самооценки; - предметные:
- знать: основные химические понятия
“катализаторы”, “оксиды”, “реакции горения”,
“реакции окисления”; физические и химические
свойства кислорода; области применения
кислорода. - уметь: отличить кислород от других газов;
составлять уравнения реакций горения веществ в
кислороде; записывать химические формулы
оксидов и давать им названия; объяснять, как
происходит круговорот кислорода в природе.
- знать: основные химические понятия
Тип урока: урок формирования умений и навыков.
Форма работы: фронтальная,
групповая,
работа в парах, игровая.
Методы обучения: словесный,
частично-поисковый,
наглядный, демонстрационный, интерактивный.
Приемы обучения: постановка проблемных
вопросов.
Оборудование: компьютер, проектор,
презентация “Свойства и применение кислорода.
Круговорот кислорода в природе”, колбы, пинцет,
ложки для сжигания веществ, спиртовка.
Реактивы: уголь, сера, красный фосфор,
железная пластина, вода, известковая вода.
ХОД УРОКА
І. Организационный момент. (1 мин.)
(Слайд № 1)Учитель: Добрый день! Прошу
всех садиться. Тема сегодняшнего урока
“Свойства и применение кислорода”.
(Слайд № 2) Мы с вами рассмотрим физические и
химические свойства кислорода, сформулируем
общие понятия об оксидах, реакциях горения,
окисления; ознакомимся с практической
значимостью и применением кислорода; а также
докажем, что кислород – один из важнейших
элементов на Земле.
ІІ. Актуализация знаний. (7 мин.).
Работа с карточками. От 2 до 4 обучающихся
получают задание на карточках и выполняют его у
доски.
(Слайд № 3) Фронтальный опрос “А ну-ка,
химики”.
Учитель: Но перед тем как приступить к
изучению новой темы, вам следует ответить на
следующие вопросы:
Химический знак кислорода? Ответ: О
Относительная атомная масса кислорода? Ответ:
16.
Химическая формула кислорода? Ответ: О2.
Относительная молекулярная масса кислорода? Ответ:
32.
В соединениях кислород обычно какой
валентности? Ответ: II.
Расскажите о нахождении кислорода в природе. Ответ:
Кислород — самый распространенный химический
элемент в земной коре. Кислород — самый
распространенный на Земле элемент, на его долю
приходится около 49% массы твердой земной коры.
Морские и пресные воды содержат огромное
количество связанного кислорода — 85,5% (по
массе), в атмосфере содержание свободного
кислорода составляет 21% по объёму и 23% по массе.
Более 1500 соединений земной коры в своем составе
содержат кислород. Кислород входит в состав
многих органических веществ и присутствует во
всех живых клетках. По числу атомов в живых
клетках он составляет 20,9%, по массовой доле —
около 65 %.
Перечислите способы получения кислорода в
лаборатории? Ответ: В лаборатории
кислород получают следующими способами:
1) Разложение перманганата калия. 2KMnO4 =
K2MnO4+MnO2+O2
2) Разложение перекиси водорода. 2H2O2
= 2H2O + O2
3) Разложение бертолетовой соли. 2KClO3 =
2KCl + 3O2
8. Перечислите способы получения кислорода в
промышленности. Ответ: В промышленности
кислород получают:
1) Электролиз воды. 2H2O = 2H2 + O2
2) Из воздуха. ВОЗДУХ давление, -183oC=O2
(голубая жидкость).
В настоящее время в промышленности кислород
получают из воздуха. В лабораториях небольшие
количества кислорода можно получать нагреванием
перманганата калия (марганцовка) KMnO4.
Кислород мало растворим в воде и тяжелее воздуха,
поэтому его можно получать двумя способами:
(Слайд № 4). 9. Установите соответствие
между способом получения кислорода и уравнением
химической реакцией. Работа в парах.
| Способы получения кислорода | Уравнения химических реакций |
| А. Разложение перманганата калия. Б. В. Разложение бертолетовой соли. Г. Электролиз воды. Д. Из воздуха. | 1) 2KClO3 = 2KCl + 3O2 2) 2H2O2 = 2H2O + O2 3) ВОЗДУХ = O2 4) 2KMnO4 = K2MnO4 + MnO2 + O2 5) 2H2O = 2H2 + O2 |
Ответ: А-4; Б-2; В-1; Г-5; Д-3.
10. Что называют катализаторами? Где эти
вещества применяются? Ответ: Вещества,
которые ускоряют химические реакции, но сами при
этом не расходуются, называют катализаторами.
Катализаторы широко применяют в химической
промышленности. С их помощью удается повысить
производительность химических процессов,
снизить себестоимость выпускаемой продукции и
более полно использовать сырье.
(Слайд № 5). На какой диаграмме распределение
массовых долей элементов отвечает
количественному составу (NH4)3PO4? Ответ:
4.
ІІІ. Изучение нового материала. (12 мин.)
(Слайд № 6) Учитель: Физические свойства. Кислород
– бесцветный газ, без вкуса и запаха, относительно
малорастворим в воде (в 100 объемах воды при
температуре 20?С растворяется 3,1 объема
кислорода). Кислород немного тяжелее воздуха: 1л
кислорода при нормальных условиях весит 1,43 г, а 1л
воздуха — 1,29г. (Нормальные условия – сокращенно:
н.у. – температура 0oС и давление 760 мм.рт.ст.,
или 1 атм. 0,1 МПа). При
давлении 760 мм.рт.ст. и температуре -183oС
кислород сжижается, а при снижении температуры
до -218,8oС затвердевает.
(Слайд № 7) Химические свойства. Техника
безопасности (провести инструктаж!)
Кислород при нагревании энергично реагирует
со многими веществами, при этом выделяются
теплота и свет. Такие реакции называют реакциями
горения. Если опустить в сосуд с кислородом O2
тлеющий уголек, то он раскаляется добела и
сгорает, образуя оксид углерода (IV) СO2.
Чтобы определить, какое образовалось вещество, в
сосуд наливают известковую воду — раствор
гидроксида кальция Са(ОН)2. Она мутнеет, так
как при этом образуется нерастворимый карбонат
кальция СаСO3:
CO2 + Ca(OH)2 = CaCO3 + H2O
Видеодемонстрация №1 “Горение угля в
кислороде”
https://files.school-collection.edu.ru/dlrstore/695aa82a-e84a-fa4d-7b04-16d28ded2fbb/index.htm
(Слайд № 8) Сера горит в O2 ярким синим
пламенем с образованием газа с резким запахом —
оксида серы (IV)
S + O2 = SO2
Видеодемонтсрация №2 “Горение серы в
кислороде”
https://files.school-collection.edu.ru/dlrstore/600cd365-f9f2-ae10-56e4-98ee0af7e4c6/index.htm
(Слайд № 9) Горение фосфора в кислороде
Видеодемонстрация №3 “Горение фосфора в
кислороде”
https://files.school-collection.edu.ru/dlrstore/f83beda5-449d-d3dc-442c-a474a89eeca6/index.htm
Опыт следует проводить под тягой. Следует
соблюдать правила обращения с нагревательными
приборами. Не допускать попадания горящего
фосфора на рабочую поверхность стола. Не вдыхать
выделяющийся дым фосфорного ангидрида.
Фосфор Р сгорает в O2 ярким пламенем с
образованием белого дыма, состоящего из твердых
частиц оксида фосфора (V).
4P + 5O2 = 2P2O5
(Слайд № 10) Горение железа в кислороде
Видеодемонстрация №4 “Горение железа в
кислороде”
https://files.school-collection.edu.ru/dlrstore/deb6e939-f8c8-fea7-fe24-7b2c80013fd7/index.htm
В кислороде горят и такие вещества, которые
обычно считают негорючими, например железо. Если
к тонкой стальной проволоке прикрепить спичку,
зажечь ее и опустить в сосуд с кислородом, то от
спички загорится и железо. Горение железа
происходит с треском и разбрасыванием ярких
раскаленных искр — расплавленных капель
железной окалины Fe3O4. В этом соединении два атома
железа трехвалентны и один двухвалентен. Поэтому
реакцию горения железа в кислороде можно
выразить следующим уравнением:
3Fe + 2O2 = FeO * Fe2O3 или Fe3O4
(Слайд № 11) Взаимодействие вещества с
кислородом относится к реакциям окисления.
(Слайд № 12) Горение — это химическая реакция,
при которой происходит окисление веществ с
выделением теплоты и света.
(Слайд № 13) В большинстве случаев при
взаимодействии веществ с кислородом образуются
оксиды.Оксиды — это сложные вещества,
которые состоят из двух элементов, одним из
которых является кислород.
(Слайд № 14) Известны химические элементы,
которые непосредственно с кислородом не
соединяются. К ним относятся золото Au и некоторые
другие. Оксиды этих элементов получают косвенным
путем.
(Слайд № 15) Применение кислорода. Основано
на его химических свойствах. В больших
количествах кислород используют для ускорения
химических реакций в разных отраслях химической
промышленности и в металлургии. Например, при
выплавке чугуна для повышения
производительности доменных печей в них подают
воздух, обогащенный кислородом.
(Слайд № 16) При сжигании смеси ацетилена или
водорода с кислородом в специальных горелках
температура пламени достигает 3000oС. Такое
пламя используется для сварки металлов. Если
берут кислород в избытке, то пламенем можно
резать металл.
(Слайд № 17) Жидкий кислород применяют в
ракетных двигателях.
(Слайд № 18) В медицине кислород служит для
облегчения затрудненного дыхания. В этом случае
кислородом заполняют специальные подушки.
Кислородные маски необходимы в высотных полетах,
в космосе и при работе под водой.
Кислород расходуется в громадных количествах
на многие химические реакции, например на
сжигание топлива.
(Слайд № 19) Из сказанного видно, что очень
много кислорода расходуется на разнообразную
деятельность человека, тратится на процессы
дыхания человека, животных, растений, а также на
процессы гниения. Человек при дыхании в течение 1
мин в среднем употребляет 0,5 дм3 кислорода,
в течении суток — 720 дм3, а в год — 262,8 м3
кислорода, что все жители земного шара (5
миллиардов) в течение года для дыхания
используют 1578 миллиардов кубических метров
кислорода. Если такой объем кислорода при
нормальном давлении поместить в железнодорожные
цистерны, то поезд был бы протяженностью более 300
млн км, что равняется расстоянию до Солнца и
обратно.
(Слайд № 20) Но все же общая масса кислорода в
воздухе заметно не изменяется. Это объясняется
процессом фотосинтеза, происходящим в зеленых
растениях на свету. В результате этого процесса
выделяется кислород. С фотосинтезом вы уже
знакомились в курсе ботаники. Упрощенно процесс
фотосинтеза изображают так:
6CO2 + 6H2O = C6H12O6
+ 6O2.
Так в природе происходит непрерывный
круговорот кислорода.
В целях сохранения кислорода в воздухе вокруг
городов и крупных промышленных центров
создаются зоны зеленых насаждений. Специальная
служба систематически контролирует содержание
кислорода в воздухе. При необходимости применяют
меры по устранению загрязнения воздуха.
Физкультминутка. (1 мин.)
IV. Закрепление знаний. (6 мин.)
(Слайд № 21) Задание №1. “Правда или ложь? Если
знаешь – разберешь”
Для кислорода верны следующие утверждения:
а) Кислород – бесцветный газ, без вкуса и
запаха.
б) Кислород немного легче воздуха.
в) В кислороде горят и такие вещества, которые
обычно считают негорючими, например железо.
г) Известны химические элементы, которые
непосредственно с кислородом соединяются. К ним
относятся золото Au и некоторые другие.
д) Применение кислорода основано на его
физических свойствах.
е) Непрерывный круговорот кислорода
непосредственно связан с таким процессом, как
фотосинтез.
Ответ: а; в; е.
(Слайд № 22) Задание №2. “Скорая помощь”
Вставьте пропущенные вещества в уравнениях
реакций:
а) …….. + Ca(OH)2 = CaCO3 + H2O
б) S + ……. = SO2
в) ….. + 2O2 = FeO * Fe2O3 или Fe3O4
Ответ: а)CO2 б)O2 в) 3Fe
(Слайд № 23) Задание №3. “Мозговой штурм”
Расставьте коэффициенты в уравнениях реакций.
а) CO2 + H2O = C6H12O6 + O2
б) P + O2 = P2O5
(Слайды № 24-25) Задание №4. “Ассоциации”
С каким применением кислорода ассоциируется
данное изображение?
1) в металлургии;
2) для резки металлов;
3) в авиации для дыхания;
4) в авиации для двигателей;
5) для сварки металлов;
6) на взрывных работах;
7) в медицине.
(Слайд № 26) V. Домашнее задание. (1 мин.)
Параграф 20, 21; №6-9 (с.60). Решите задачи 1-2 (с.60).
Творческое задание: подготовить сообщение
№10 с. 60 “Что делается в вашей местности для
поддержания определенного содержания кислорода
в воздухе? В чем может заключаться ваше участие в
этой деятельности?”
(Слайд № 27) VI. Рефлексия. (1 мин.)
Учитель:
- Сегодня я узнал…
- было трудно…
- я понял, что…
- я научился…
- я смог…
- было интересно узнать, что…
- меня удивило…
- мне захотелось…
VII. Подведение итогов урока. (1 мин.)
(Слайд № 28)
В чём горят дрова и газ,
Фосфор, водород, алмаз?
Дышит чем любой из нас
Каждый миг и каждый час?
Без чего мертва природа?
Правильно, без….
Обучающиеся: кислорода
(Слайд № 29) Учитель: Правильно. Спасибо за
урок! До свидания!
Литература
[1] Горковенко М. Ю. Поурочные разработки по
химии 8 класс к учебникам О. С. Габриеляна, Л. С.
Гузея, Г. Е. Рудзитиса. – М: “ВАКО”, 2004;
[2] Радецкий А. М., Горшкова В. П. Дидактический
материал: химия 8-9 классы — М: Просвещение, 1997.
[3] Химия: неорганическая химия: учебник для 8
класса общеобразовательных учреждений/ Г. Е.
Рудзитис, Ф.Г. Фельдман. – М: “Просвещение”, 2014 г.
Интернет-ресурсы
- https://files.school-collection.edu.ru/
- https://www.e-osnova.ru/
Источник
