Какой продукт образуется в результате гликолиза и поступает в митохондрию

Энергетический
обмен (катаболизм,
диссимиляция) — совокупность реакций расщепления органических веществ,
сопровождающихся выделением энергии. Энергия, освобождающаяся при распаде
органических веществ, не сразу используется клеткой, а запасается в форме АТФ и
других высокоэнергетических соединений. АТФ — универсальный источник
энергообеспечения клетки. Синтез АТФ происходит в клетках всех организмов в
процессе фосфорилирования — присоединения неорганического фосфата к АДФ.
У аэробных организмов (живущих в кислородной среде)
выделяют три этапа энергетического обмена: подготовительный, бескислородное
окисление и кислородное окисление; у анаэробных организмов (живущих в бескислородной
среде) и аэробных при недостатке кислорода — два этапа: подготовительный,
бескислородное окисление.
Подготовительный
этап
Заключается в ферментативном расщеплении сложных
органических веществ до простых: белковые молекулы — до аминокислот, жиры — до
глицерина и карбоновых кислот, углеводы — до глюкозы, нуклеиновые кислоты — до
нуклеотидов. Распад высокомолекулярных органических соединений осуществляется
или ферментами желудочно-кишечного тракта или ферментами лизосом. Вся
высвобождающаяся при этом энергия рассеивается в виде тепла. Образовавшиеся
небольшие органические молекулы могут быть использованы в качестве
«строительного материала» или могут подвергаться дальнейшему расщеплению.
Бескислородное окисление, или гликолиз
Этот этап заключается в дальнейшем расщеплении
органических веществ, образовавшихся во время подготовительного этапа,
происходит в цитоплазме клетки и в присутствии кислорода не нуждается. Главным
источником энергии в клетке является глюкоза. Процесс бескислородного неполного
расщепления глюкозы — гликолиз.
В реакциях гликолиза шестиуглеродная молекула глюкозы С6 расщепляется на две молекулы
пировиноградной кислоты С3. При этом от каждой молекулы глюкозы
отщепляется четыре атома водорода и образуются две молекулы АТФ. Атомы водорода
присоединяются к переносчику НАД (никотинамидаденинди-нуклеотид), который
переходит в свою восстановленную форму НАД – Н + Н+ (НАД очень сходен с НАДФ, т. е. с
переносчиком атомов водорода при фотосинтезе).

Полезный выход энергии этого этапа — две
молекулы АТФ, что составляет 40%; 60% рассеивается в виде тепла.
Кислородное окисление, или дыхание
Наиболее важным является кислородный этап аэробного
дыхания. Он протекает в митохондриях и требует присутствия кислорода.
Продукт гликолиза — пировиноградная кислота — заключает в
себе значительную часть энергии, и дальнейшее ее высвобождение осуществляется в
митохондриях. Здесь пировиноградная кислота подвергается ферментативному
расщеплению.

Углекислый газ выделяется из митохондрий в цитоплазму клетки, а затем в
окружающую среду.
Атомы водорода, акцептированные НАД и ФАД (кофермент
флавинадениндинуклеотид), вступают в цепь реакций, конечный результат которых —
синтез АТФ. Это происходит в следующей последовательности:

- Атомы водорода отщепляются от НАД и ФАД, захватываются переносчиками,
встроенными во внутреннюю мембрану митохондрий, где происходит их окисление;
- Н+ выносятся
переносчиками на наружную поверхность крист, накапливаются в межмембранном
пространстве, образуя протонный резервуар; - Электроны (е-) атомов водорода возвращаются по цепи
дыхательных ферментов в матрикс и присоединяются к атомам кислорода, который
постоянно поступает в митохондрию. Атомы кислорода при этом становятся
отрицательно заряженными.На мембране возникает разность потенциалов. Когда разность потенциалов
достигает 200 мВ, начинает действовать протонный канал в молекулах фермента
АТФ-синтетазы, которые встроены во внутреннюю мембрану;
- Через протонный канал Н- устремляются обратно в матрикс
митохондрий, создавая высокий уровень энергии, большая часть которой идет на
синтез АТФ из АДФ и фосфорной кислоты, а протоны соединяются с отрицательно
заряженными частицами кислорода, образуя воду — второй конечный продукт
клеточного дыхания.
Аэробное дыхание, включающее бескислородный и кислородный этапы, можно
выразить суммарным уравнением:

Таким образом, кислород, поступивший в митохондрии, необходим для
присоединения электронов, а затем и протонов. При отсутствии кислорода
процессы, связанные с транспортом протонов и электронов в митохондриях,
прекращаются, а следовательно, невозможно протекание и бескислородного этапа,
так как все переносчики атомов водорода оказываются загруженными.
При распаде молекулы глюкозы высвобождается 200 кДж/ моль. В АТФ
запасается 55% энергии, остальная рассеивается в виде тепла.
| Подготовительный этап | Бескислородный этап | Кислородный этап | |
| Место расщепления | Органы пищеварения, клетки под действием ферментов | Внутри клетки | Митохондрии |
| Активатор расщепления | Ферменты пищеварительных соков | Ферменты мембран клеток | Ферменты митохондрий |
| Результат расщепления соединений клетки | Белки до аминокислот Жиры до глицерина и жирных кислот Углеводы до глюкозы | Глюкоза до 2 молекул пировиноградной кислоты + энергия | Пировиноградная кислота до СО2 и Н2О |
| Выделившаяся энергия | Рассеивается в виде тепла | 40% запасается в виде АТФ 60% рассеивается в виде тепла | 55% запасается в виде АТФ |
| Количество энергии в виде АТФ | 2 молекулы | 36 молекул |
Анаэробное дыхание. При отсутствии или
недостатке кислорода, играющего роль конечного акцептора электронов в
кислородном дыхании, цепь передачи электронов через мембрану не осуществляется,
а значит, не создается протонный резервуар, обеспечивающий энергией синтез АТФ.
В этих условиях клетки способны синтезировать АТФ, расщепляя питательные
вещества в процессе анаэробного
дыхания. Анаэробное дыхание
осуществляют многие виды бактерий, микроскопические грибы и простейшие.
Некоторые клетки, временами испытывающие недостаток кислорода (например,
мышечные клетки или клетки растений), тоже обладают способностью к анаэробному
дыханию.
Анаэробное дыхание — эволюционно более ранняя и энергетически
менее рациональная форма получения энергии из питательных веществ по сравнению
с кислородным дыханием.
В основе анаэробного дыхания лежит процесс, в ходе которого глюкоза
расщепляется до пировиноградной кислоты и высвобождаются атомы водорода.
Акцептором атомов водорода, отщепляемых в результате дыхания, является
пировиноградная кислота, которая превращается в молочную.

Описанный процесс получил название молочнокислого брожения.

Молочнокислое брожение осуществляют молочнокислые бактерии
(например, кокки из рода стрептококк). Образование молочной кислоты по такому
типу происходит также в животных клетках в условиях дефицита кислорода.
В природе широко распространено спиртовое брожение, которое осуществляют дрожжи. В
отсутствие кислорода дрожжевые клетки образуют из глюкозы этиловый спирт и СО;.
Вначале спиртовое брожение идет аналогично молочнокислому, но последние реакции
приводят к образованию этилового спирта. От каждой молекулы пировиноградной
кислоты отщепляется молекула С02, и образуется молекула двууглеродного
соединения —уксусного альдегида, который
затем восстанавливается до этилового спирта атомами водорода.

Суммарное уравнение:

Спиртовое брожение, кроме дрожжей, осуществляют некоторые
анаэробные бактерии. Этот тип брожения наблюдается в растительных клетках в
отсутствие кислорода.
Наиболее распространенным питательным веществом, которое
используется для анаэробного высвобождения энергии, является глюкоза. Однако
следует помнить, что любое органическое вещество при соответствующих условиях
может выступать источником энергии для синтеза АТФ.
При недостатке в клетке глюкозы в дыхание могут вовлекаться жиры
и белки. Продуктами брожения являются различные органические кислоты (молочная,
масляная, муравьиная, уксусная), спирты (этиловый, бутиловый, амиловый),
ацетон, а также углекислый газ и вода.
Источник
Кислород транспортируется по дыхательным путям к месту окисления в активных тканях. При интенсивных нагрузках активные клетки скелетной мышцы устанавливают потребность в кислороде, поскольку более 90% энергии тратится на мышцы. Кислород связывается с гемоглобином в эритроцитах, в то время как субстраты перемещаются в плазму. Поставка кислорода должна быть непрерывной, поскольку в организме большинства млекопитающих имеется лишь минимальный запас кислорода, а субстраты хранятся как в мышечных клетках, так и в тканях в большом количестве.
ООкислительное фосфорилирование в митохондриях
Аэробный энергетический обмен происходит в митохондриях и приводит к наибольшему выходу энергии. Как следует из названия, для этого процесса требуется кислород. Аэробный гликолиз – наиболее эффективный способ образования энергии. В анаэробных условиях только 2 моль АТФ синтезируется из 1 моль гликогена, в то время как в присутствие кислорода 38 моль АТФ может синтезироваться из того же количества гликогена (рис. 3). Чистый выход АТФ 36 моль, за вычетом потраченных 2 моль АТФ (38 молекул в сердечной мышце, столько же в почках и печени). В митохондриях мышечных клеток атомы водорода выделяются из восстановленных веществ, которые образуются в ходе цикла трикарбоновых кислот, в процессе, называемом окислительным фосфорилированием. Специальные белковые комплексы, переносящие электроны, передают электроны от атома водорода молекуле кислорода. Энергия, высвобождаемая во время транспорта электронов, сохраняется в виде АТФ. Электроны по дыхательной цепи переносятся в порядке повышения окислительно-восстановительного потенциала -от более электроотрицательного вещества к более электроположительному кислороду.
В клетках при высоком парциальном давлении кислорода потребность в энергии определяет уровень митохондриального дыхания, а снабжение субстратами определяет энергетический уровень клетки, при котором достигается этот уровень митохондриального дыхания. Запас АТФ и КФ мало сравним с количеством энергии, которая требуется для активной мышечной работы. Из-за малого запаса макроэргических фосфатов АТФ может тратиться больше или меньше, чем синтезироваться, лишь в небольшие промежутки времени. Таким образом, синтез АТФ должен происходить, когда обычно клеточные процессы гидролизуют АТФ. Поэтому митохондриальное окислительное фосфорилирование тесно связано с несколькими обменными путями и быстро отвечает на изменения в клеточных потребностях в АТФ. Однако связь дыхательной цепи с другими обменными процессами не столь высокая. Было подсчитано, что около 1~3% кислорода, поступившего в дыхательную цепь в состоянии покоя, выходит из нее в виде пероксида. Образование высокореакционноспособных частиц кислорода может иметь некоторое влияние, как в состоянии покоя, так и при физических нагрузках.
ЦЦикл трикарбоновых кислот
Митохондрии в скелетных мышцах потребляют наибольшее количество кислорода и служат основным источником энергии в обменном процессе для поддержания нормальной работы. Цикл лимонной кислоты (также называемый циклом Кребса или циклом трикарбоновых кислот) – это ряд реакций в митохондриях, которые приводят к распаду ацетил-КоА, высвобождая восстановительные эквиваленты, которые используются в окислительном фосфорилировании для образования АТФ из АДФ. Цикл трикарбоновых кислот играет основную роль в аэробных обменных процессах. Он является заключительным путем метаболизма глюкозы (гликолиз), жиров (бета-окисление жирных кислот) и белков. Как в состоянии покоя, так и при физических нагрузках бета-окисление жирных кислот и гликолиз предоставляют более 95% ацетил-КоА, вступающего в цикл трикарбоновых кислот.
В цикле лимонной кислоты ацетил-КоА соединяется с оксалоацетатом, формируя соль лимонной кислоты. В последующих реакциях оксалоацетат снова регенерируется. В результате выделяется 3 НАД Н, 1 ФАД Н2, 1 ГТФ и 2 С02. Далее восстановительными эквивалентами подвергаются окислительному фос-форилированию. 3 НАД Н и 1 ФАД Н2 дают в результате 12 АТФ.
Источник
Гликолиз – процесс окисления глюкозы, при котором из одной молекулы глюкозы образуются две молекулы пировиноградной кислоты, не является мембранозависимым процессом. Он происходит в цитоплазме. Однако ферменты гликолиза связаны со структурами цитоскелета. Суть гликолиза состоит в том, что молекула глюкозы (C6H12O6) без участия кислорода распадается на две молекулы пировиноградной кислоты (СН3СОСООН). При этом окисление идет за счет отщепления от молекулы глюкозы четырех атомов водорода, связывающихся со сложным органическим веществом НАД с получением двух молекул НАД•Н. Выделяющаяся при этом энергия запасается (40% от общего количества) в виде макроэргических связей двух молекул АТФ. 60% энергии выделяется в виде тепла. При последующем окислении НАД•Н получается еще 6 молекул АТФ. Таким образом, полный энергетический выход гликолиза в анаэробных условиях составляет 8 молекул АТФ.
На схеме в рамках обозначены исходные субстраты и конечные продукты гликолиза, цифрами в скобках – число молекул.
Для распада и частичного окисления молекулы глюкозы требуется протекание 11 сложных последовательных реакций.
Реакции гликолиза
Ход реакций
Ферменты, Активаторы, ингибиторы
Подготовительная стадия гликолиза
Стадия активации глюкозы проходит в 5 реакций, в ходе которых 1 молекула гексозы (глюкозы) расщепляется на 2 молекулы триоз-глицеральдегидфосфата
1. Необратимая реакция фосфорилирования глюкозы
Процесс гликолиза начинается с фосфорилирования глюкозы за счет АТФ – первая реакция. Это первая пусковая реакция гликолиза. Ее результатом является глюкозо-6-фосфат, имеющий отрицательный заряд. В гликолизе может участвовать не только глюкоза, но и другие гексозы (фруктоза), но в результате фосфорилирования и активации все равно образуется глюкозо-6-фосфат.

фермент: гексокиназа
Активаторы: АДФ, Н3РO4.
Ингибиторы: глюкозо-6-Ф, фосфоенолпируват.
2. Обратимая реакция изомеризации глюкозо-6-фосфата
Во второй реакции происходит изомеризация (внутримолекулярные перестройки) глюкозо-6-фосфата во фруктозо-6-фосфат.

фермент: глюкозо-6-фосфатизомераза
3. Необратимая реакция фосфорилирования фруктозо-6-фосфата (ключевая стадия гликолиза)
В третьей реакции происходит фосфорилирование (присоединение остатка ортофосфорной кислоты) фруктозо-6-фосфата с образованием фруктозо-1,6-дифосфата. При этом затрачивается еще одна молекула АТФ (уже вторая) – это вторая пусковая реакция гликолиза. Она идет в присутствии Mg2+ и является необратимой, так как сопровождается масштабным уменьшением свободной энергии.

фермент: фосфофруктокиназа
Активаторы: АДФ, АМФ, Н3РO4, К+.
Ингибиторы: АТФ, цитрат, НАДН.
4. Обратимая реакция дихотомического расщепления фруктозо-1,6-дифосфата
В четвертой реакции гликолиза происходит расщепление фруктозо-1,6-дифосфата на две молекулы глицеральдегид-3-фосфата.

фермент: алъдолаза
5. Обратимая реакция изомеризации дигидроксиацетона-3-фосфат в глицеральдегид-3-фосфат
В пятой реакции происходит изомеризация полученных триозофосфатов. На этом заканчивается первая стадия гликолиза.

фермент: триозофосфатизомераза
Стадия генерации АТФ
Проходит в 6 реакций (или 5), в ходе которых энергия окислительных реакций трансформируется в химическую энергию АТФ (субстратное фосфорилирование).
6. Окисление глицеральдегид-3-фосфата до 1,3-дифосфоглицерата (реакция гликолитической оксиредукции)
В шестой реакции происходит окисление альдегидной группы до карбоксильной. Выделившийся Н+ акцептируется NAD, который восстанавливается до NADH. Освобождающаяся энергия затрачивается для образования высокоэнергетической связи 1,3-бифосфоглицерата (1,3-бифосфоглицериновая кислота).

фермент: глицералъдегид-3-фосфат-дегидрогеназа
7. Субстратное фосфорилирование АДФ (7)
В седьмой реакции фосфорильная группа 1,3-бифосфоглицерата переносится на ADP, в результате чего образуется АТР (напоминаем, что следует иметь в виду две параллельные цепи реакций, с участием двух молекул триоз, образовавшихся из одной молекулы гексозы, следовательно, синтезируется не одна, а две молекулы АТР).

фермент: фосфоглицераткиназа
8. Реакция изомеризации 3-фосфоглицерата в 2-фосфоглицерат
В восьмой реакции гликолиза происходит перенос фосфатной группы с третьего атома углерода на второй. В результате образуется 2-фосфоглицерат (2-фосфоглицериновая кислота).

9. Реакция енолизации
Девятая реакция сопровождается внутримолекулярными окислительно-восстановительными процессами, в результате которых образуется фосфоенолпируват (фосфоенолпировиноградная кислота) с высокоэнергетической связью во втором атоме углерода и отщепляется молекула воды

фермент: енолаза
10. Реакция субстратного фосфорилирования
В ходе десятой реакции фосфорильная группа переносится на ADP. При этом синтезируется АТР и пируват (пировиноградная кислота). Эта реакция также необратима, поскольку высокоэкзергонична.

фермент: пируваткиназа
11. Реакция обратимого восстановления пировиноградной кислоты до молочной кислоты (в анаэробных условиях)
Если после гликолиза следует аэробное расщепление, пируват мигрирует в матрикс митохондрий, где, взаимодействуя с коэнзимом-А, участвует в образовании ацетил-СоА. В анаэробных условиях пируват при участии NADH восстанавливается до лактата (молочной кислоты), который при этом является конечным продуктом гликолиза. Затем в аэробных условиях лактат может обратно превратиться в пируват и окислиться в митохондриях.

фермент: лактатдегидрогеназа
1. Биология для поступающих в вузы / Г.Л. Билич, В.А. Крыжановский. — 2008.
2. Биология в таблицах и схемах / Спб. — 2004.
3. Биохимия в схемах и таблицах / И. В. Семак – Минск — 2011.
Источник
Гликолиз (от
греч. glycys – сладкий и lysis –
растворение, распад) – это последовательность ферментативных реакций,
приводящих к превращению глюкозы в пируват с одновременным образованием АТФ.
При аэробных
условиях пируват проникает в митохондрии, где полностью окисляется до СО2
и Н2О. Если содержание кислорода недостаточно, как это может иметь
место в активно сокращающейся мышце, пируват превращается в лактат.
Итак,
гликолиз – не только главный путь утилизации глюкозы в клетках, но и уникальный
путь, поскольку он может использовать кислород, если
последний
доступен (аэробные условия), но может протекать и в отсутствие кислорода
(анаэробные условия).
Анаэробный гликолиз – сложный ферментативный процесс распада глюкозы,
протекающий в тканях человека и животных без потребления кислорода. Конечным
продуктом гликолиза является молочная кислота. В процессе гликолиза образуется
АТФ. Суммарное уравнение гликолиза можно представить следующим образом:

В анаэробных
условиях гликолиз – единственный процесс в животном организме, поставляющий
энергию. Именно благодаря гликолизу организм человека и животных определенный
период может осуществлять ряд физиологических функций в условиях
недостаточности кислорода. В тех случаях, когда гликолиз протекает в
присутствии кислорода, говорят об аэробном гликолизе .
Последовательность
реакций анаэробного гликолиза, так же как и их промежуточные продукты, хорошо
изучена. Процесс гликолиза катализируется одиннадцатью ферментами, большинство
из которых выделено в гомогенном, клисталлическом или высокоочищенном виде и
свойства которых достаточно известны. Заметим, что гликолиз протекает в
гиало-плазме (цитозоле) клетки.
Первой
ферментативной реакцией гликолиза является фосфорилирование, т.е. перенос
остатка ортофосфата на глюкозу за счет АТФ. Реакция катализируется ферментом
гексокиназой:
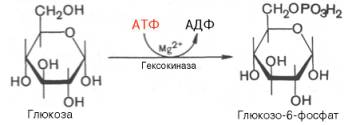
Образование
глюкозо-6-фосфата в гексокиназной реакции сопровождается освобождением
значительного количества свободной энергии системы и может считаться
практически необратимым процессом.
Наиболее
важным свойством гексокиназы является ее ингибирование глюкозо-6-фосфатом, т.е.
последний служит одновременно и продуктом реакции, и аллостерическим
ингибитором.
Фермент
гексокиназа способен катализировать фосфорилирование не только D-глюкозы, но и
других гексоз, в частности D-фруктозы, D-маннозы и т.д. В печени, кроме
гексокиназы, существует фермент глюкокиназа, который катализирует фосфорилирование
только D-глюкозы. В мышечной ткани этот фермент отсутствует (подробнее см.
главу 16).
Второй
реакцией гликолиза является превращение глюкозо-6-фос-фата под действием
фермента глюкозо-6-фосфатизомеразы во фруктозо-6-фосфат:
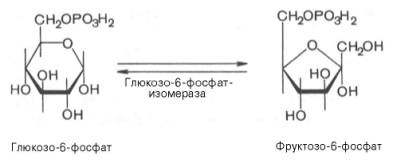
Эта реакция
протекает легко в обоих направлениях, и для нее не требуется каких-либо
кофакторов.
Третья
реакция катализируется ферментом фосфофруктокиназой; образовавшийся
фруктозо-6-фосфат вновь фосфорилируется за счет второй молекулы АТФ:
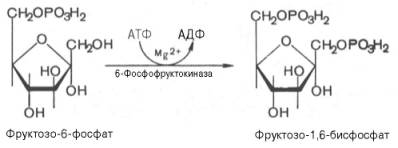
Данная
реакция аналогично гексокиназной практически необратима, протекает в
присутствии ионов магния и является наиболее медленно текущей реакцией
гликолиза. Фактически эта реакция определяет скорость гликолиза в целом.
Фосфофруктокиназа
относится к числу аллостерических ферментов. Она ингибируется АТФ и
стимулируется АМФ . При значительных величинах отношения АТФ/АМФ активность
фосфофруктокиназы угнетается и гликолиз замедляется. Напротив, при снижении
этого коэффициента интенсивность гликолиза повышается. Так, в неработающей
мышце активность фосфофруктокиназы низкая, а концентрация АТФ относительно
высокая. Во время работы мышцы происходит интенсивное потребление АТФ и
активность фосфофруктокиназы повышается, что приводит к усилению процесса
гликолиза.
Четвертую
реакцию гликолиза катализирует фермент альдолаза. Под влиянием этого фермента
фруктозо-1,6-бисфосфат расщепляется на две фосфотриозы:
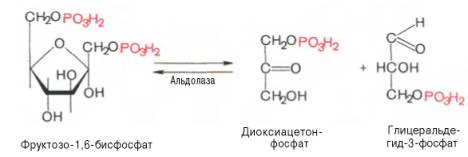
Эта реакция
обратима. В зависимости от температуры равновесие устанавливается на различном
уровне. При повышении температуры реакция сдвигается в сторону большего
образования триозофосфатов (дигидро-ксиацетонфосфата и
глицеральдегид-3-фосфата).
Пятая реакция – это реакция изомеризации триозофосфатов. Катализируется ферментом
триозофосфатизомеразой:

Равновесие
данной изомеразной реакции сдвинуто в сторону дигид-роксиацетонфосфата: 95%
дигидроксиацетонфосфата и около 5% глице-ральдегид-3-фосфата. В последующие
реакции гликолиза может непосредственно включаться только один из двух
образующихся триозофосфатов, а именно глицеральдегид-3-фосфат. Вследствие этого
по мере потребления в ходе дальнейших превращений альдегидной формы фосфотриозы
ди-гидроксиацетонфосфат превращается в глицеральдегид-3-фосфат.
Образованием
глицеральдегид-3-фосфата как бы завершается первая стадия гликолиза. Вторая
стадия – наиболее сложная и важная. Она включает окислительно-восстановительную
реакцию (реакция гликолитической оксидоредукции), сопряженную с субстратным
фосфорилированием, в процессе которого образуется АТФ.
В результате
шестой реакции глицеральдегид-3-фосфат в присутствии фермента
глицеральдегидфосфатдегидрогеназы, кофермента НАД и неорганического фосфата
подвергается своеобразному окислению с образованием 1,3-бисфосфоглицериновой
кислоты и восстановленной формы НАД (НАДН). Эта реакция блокируется йод- или
бромацетатом, протекает в несколько этапов:
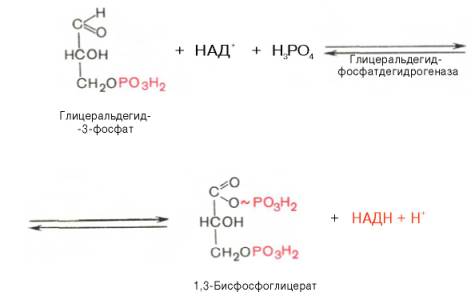
1,3-Бисфосфоглицерат
представляет собой высокоэнергетическое соединение (макроэргическая связь
условно обозначена знаком «тильда» ~). Механизм действия
глицеральдегидфосфатдегидрогеназы сводится к следующему: в присутствии
неорганического фосфата НАД+ выступает как акцептор водорода,
отщепляющегося от глицеральдегид-3-фосфата. В процессе образования НАДН
глицеральдегид-3-фосфат связывается с молекулой фермента за счет SH-групп
последнего. Образовавшаяся связь богата энергией, но она непрочная и
расщепляется под влиянием неорганического фосфата, при этом образуется
1,3-бисфосфоглицериновая кислота.
Седьмая реакция катализируется фосфоглицераткиназой, при этом происходит передача
богатого энергией фосфатного остатка (фосфатной группы в положении 1) на АДФ с
образованием АТФ и 3-фосфогли-цериновой кислоты (3-фосфоглицерат):
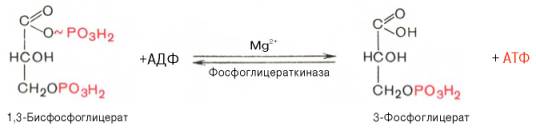
Таким
образом, благодаря действию двух ферментов (глицеральде-гидфосфатдегидрогеназы
и фосфоглицераткиназы) энергия, высвобождающаяся при окислении альдегидной
группы глицеральдегид-3-фосфата до карбоксильной группы, запасается в форме
энергии АТФ. В отличие от окислительного фосфорилирования образование АТФ из
высокоэнергетических соединений называется субстратным фосфорилированием.
Восьмая реакция
сопровождается внутримолекулярным переносом оставшейся фосфатной группы, и
3-фосфоглицериновая кислота превращается в 2-фосфоглицериновую кислоту
(2-фосфоглицерат).
Реакция
легкообратима, протекает в присутствии ионов Mg2+. Кофактором
фермента является также 2,3-бисфосфоглицериновая кислота аналогично тому, как в
фосфоглюкомутазной реакции роль кофактора выполняет глюкозо-1,6-бисфосфат:

Девятая
реакция катализируется ферментом енолазой, при этом 2-фосфоглицериновая кислота
в результате отщепления молекулы воды переходит в фосфоенолпировиноградную
кислоту (фосфоенолпируват), а фосфатная связь в положении 2 становится
высокоэргической:
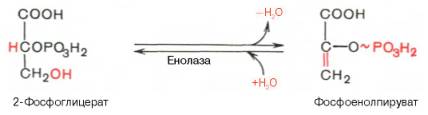
Енолаза
активируется двухвалентными катионами Mg2+или
Мn2+ и ингибируется фторидом.
Десятая
реакция характеризуется разрывом высокоэргической связи и переносом фосфатного
остатка от фосфоенолпирувата на АДФ (субстратное фосфорилирование).
Катализируется ферментом пируваткиназой:
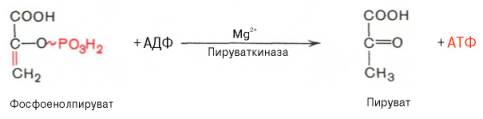
Для действия
пируваткиназы необходимы ионы Mg2+, а также
одновалентные катионы щелочных металлов (К+ или др.). Внутри клетки
реакция является практически необратимой.
В результате
одиннадцатой реакции происходит восстановление пировиноградной кислоты и
образуется молочная кислота. Реакция протекает при участии фермента
лактатдегидрогеназы и кофермента НАДН, образовавшегося в шестой реакции:

Последовательность
протекающих при гликолизе реакций представлена на рис. 10.3.
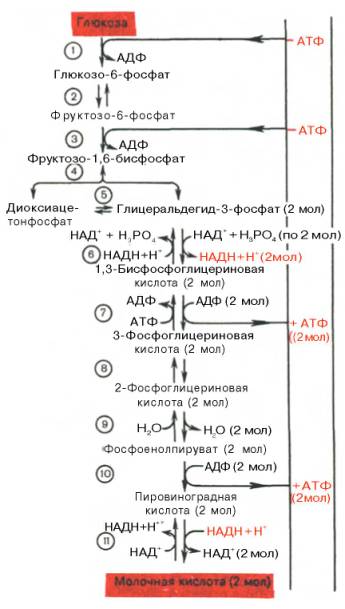
Рис. 10.3. Последовательность реакций гликолиза.
1 –
гексокиназа; 2 – фосфоглюкоизоме-раза; 3 – фосфофруктокиназа; 4 – альдо-лаза; 5
– триозофосфатизомераза; 6 – гли-церальдегидфосфатдегидрогеназа; 7
-фосфоглицераткиназа; 8 – фосфоглицеромутаза; 9 – енолаза; 10 –
пируватки-наза; 11 –
лактатдегидрогеназа.
Реакция
восстановления пирувата завершает внутренний окислительно-восстановительный
цикл гликолиза. НАД+ при этом играет роль промежуточного переносчика
водорода от глицеральдегид-3-фосфата (6-я реакция) на пировиноградную кислоту
(11-я реакция), при этом сам он регенерируется и вновь может участвовать в
циклическом процессе, получившем название гликолитический оксидоредукции.
Биологическое
значение процесса гликолиза заключается прежде всего в образовании богатых
энергией фосфорных соединений. На первых стадиях гликолиза затрачиваются 2
молекулы АТФ (гексокиназная и фосфофрук-токиназная реакции). На последующих
образуются 4 молекулы АТФ (фосфоглицераткиназная и пируваткиназная реакции).
Таким образом, энергетическая эффективность гликолиза в анаэробных условиях
составляет 2 молекулы АТФ на одну молекулу глюкозы.
Как
отмечалось, основной реакцией, лимитирующей скорость гликолиза, является
фосфофруктокиназная. Вторая реакция, лимитирующая скорость и регулирующая
гликолиз – гексокиназная реакция. Кроме того, контроль гликолиза
осуществляется также ЛДГ
и ее изоферментами.
В тканях с
аэробным метаболизмом (ткани сердца, почек и др.) преобладают изоферменты ЛДГ1
и ЛДГ2 (см. главу 4). Эти изоферменты инги-бируются даже небольшими
концентрациями пирувата, что препятствует образованию молочной кислоты и
способствует более полному окислению пирувата (точнее, ацетил-КоА) в цикле
трикарбоновых кислот.
В тканях
человека, в значительной степени использующих энергию гликолиза (например,
скелетные мышцы), главными изоферментами являются ЛДГ5 и ЛДГ4.
Активность ЛДГ5 максимальна при тех концентрациях пирувата, которые
ингибируют ЛДГ1. Преобладание изоферментов ЛДГ4 и ЛДГ5
обусловливает интенсивный анаэробный гликолиз с быстрым превращением пирувата в
молочную кислоту.
Как
отмечалось, процесс анаэробного распада гликогена получил название
гликогенолиза. Вовлечение D-глюкозных единиц гликогена в процесс гликолиза
происходит при участии 2 ферментов – фосфорилазы а и фосфо-глюкомутазы. Образовавшийся в результате
фосфоглюкомутазной реакции глюкозо-6-фосфат может включаться в процесс
гликолиза. После образования глюкозо-6-фосфата дальнейшие пути гликолиза и
гликогенолиза полностью совпадают:
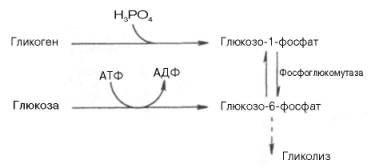
В процессе
гликогенолиза в виде макроэргических соединений накапливаются не две, а три
молекулы АТФ (АТФ не тратится на образование глюкозо-6-фосфата). Кажется, что
энергетическая эффективность глико-генолиза выглядит несколько более высокой по
сравнению с процессом гликолиза, но эта эффективность реализуется только при
наличии активной фосфорилазы а.
Следует иметь в виду, что в процессе активации фосфо-рилазы b расходуется АТФ (см. рис. 10.2).
Еще по теме:
- ГЛИКОЛИЗ – химическая энциклопедия
- Гликолиз – биохимический справочник
- Гликолиз – Наглядная биохимия
Источник
