Какой объем раствора может содержаться в карпуле
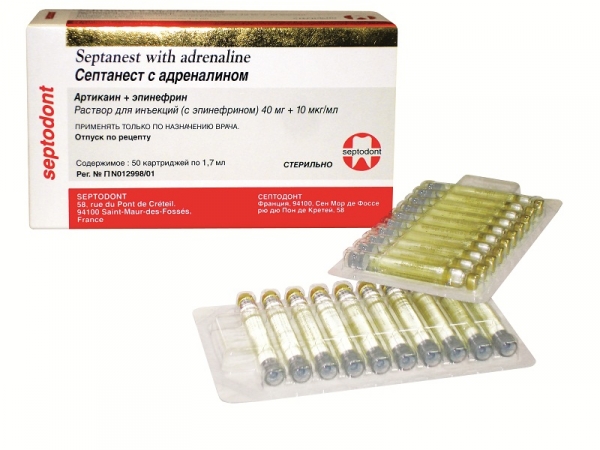
Безболезненность всех диагностических и лечебных манипуляций является важнейшим условием эффективного лечения стоматологических заболеваний. Однако, к сожалению, до сих пор у многих пациентов визит к стоматологу ассоциируется в первую очередь с болью. Распространенность страха, связанного с возможной болезненностью стоматологического лечения, по данным различных авторов, составляет 61–92%. А совсем не обращаются к стоматологу из-за страха 5-14% населения! Кроме того, сама атмосфера стоматологического кабинета, даже в условиях эмоционально-нейтральной ситуации, способствует появлению у пациентов заметных негативных вегетативных реакций. Типичным их проявлением является резкое повышение уровня артериального давления (АД) и частоты сердечных сокращений (ЧСС). По-прежнему высокой (около 10% случаев) остается частота осложнений и системных побочных реакций при проведении инъекционной анестезии на амбулаторном стоматологическом приеме.
Попытки решить проблему повышения эффективности местного обезболивания в стоматологии с одновременным снижением влияния на пациента психотравмирующих факторов и риска развития осложнений не прекращаются и по сегодняшний день.
В значительной степени эту задачу позволяет решить «карпульная» анестезия (рис. 1). Однако следует признать, что достаточно часто карпулированные анестетики применяются практическими врачами-стоматологами не оптимально, без учета особенностей их состава, фармакологических характеристик и возможных нежелательных побочных эффектов. Зачастую стоматолог даже не знает, какой анестетик находится в карпуле, какие в нем содержатся лекарственные добавки, какие возможны побочные эффекты и осложнения…
Рис. 1. Комплект инструментов и медикаментов для «карпульной анестезии»:
а – карпулы с анестетиком
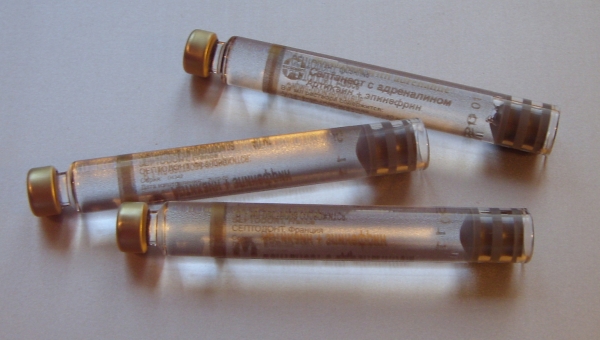
б – иглы

в – карпульный шприц
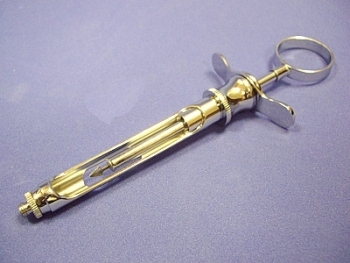
Инъекционная анестезия нашла широкое применение в терапевтической стоматологии. Под местным обезболиванием в настоящее время проводится лечение кариеса и других поражений твердых тканей зубов, эндодонтические манипуляции, профессиональная чистка зубов и пародонтологические вмешательства, иногда – даже отбеливание зубов.
Кроме «классических» требований, предъявляемым ко всем местным анестетикам (минимальные токсичность и аллергенность, отсутствие повреждающего действия на ткани организма и структуры нерва, низкая вероятность развития осложнений и побочных эффектов, быстрая биотрансформация в организме и т.п.), к препаратам, применяемым для местного обезболивания в терапевтической стоматологии, предъявляются требования, отражающие специфику лечебно-профилактическим манипуляций, проводимых стоматологами-терапевтами.
Наиболее значимые дополнительные требования к анестетикам, применяемым в клинике терапевтической стоматологии, по нашему мнению, можно сформулировать следующим образом:
− обеспечивать глубокую, полную анестезию твердых тканей и пульпы зубов, периапикальных тканей и слизистой оболочки рта в области проведения вмешательства, в том числе быть эффективными при инфильтрационной анестезии моляров и премоляров нижней челюсти;
− иметь максимально быстрое время наступления анестезии (1-5 мин);
− продолжительность эффективной анестезии должна обеспечивать безболезненность проведения всех лечебно-профилактических мероприятий, в т.ч. и на заключительных этапах лечения (удаление матрицы и межзубных клиньев, шлифование и полирование реставраций в поддесневой области, пломбирование корневых каналов горячей гуттаперчей, наложение швов после пародонтологических вмешательств и т.д.). Таким образом, учитывая продолжительность наиболее распространенных терапевтических стоматологических процедур, длительность эффективного действия местного анестетика должна составлять 60-75 мин.
− обеспечивать быстрое и полное прекращение анестезии зубов и окружающих мягких тканей после окончания стоматологических манипуляций (оптимально – через 2,5-2 часа после проведения анестезии);
− сохранять химическую стабильность и фармакологические свойства на протяжении всего рекомендованного периода хранения (до 2-3 лет) при комнатной температуре, в том числе при возможных ее колебаниях.
Самый широкий ассортимент карпулированных анестетиков на российском стоматологическом рынке представляет компания «Septodont» (Франция):
− Septanest 4% 1:100.000;
− Septanest 4% 1:200.000;
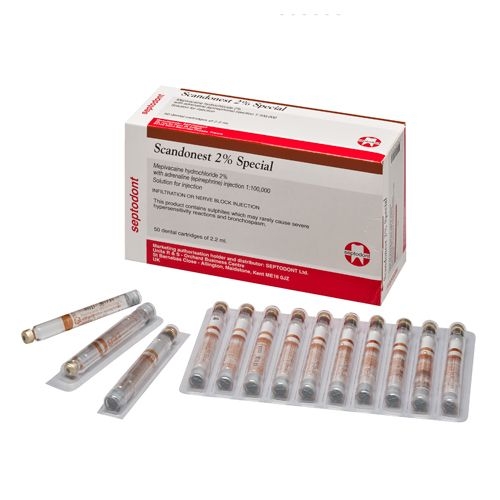
− Scandonest 2% Special;
− Scandonest 3%.
Septanest 4% 1:100.000 [Septanest with adrenaline Раствор для инъекций (с эпинефрином) 40 мг+10 мкг/мл] (рис. 2), по нашему мнению, следует рассматривать как основной анестетик для использования в терапевтической стоматологии. Этот препарат обладает глубоким обезболивающим эффектом. Быстрое наступление анестезии – 1-3 мин – позволяет экономить рабочее время врача. Длительность анестезии – 60-75 мин.
Рис. 2. Septanest 4% 1:100.000 (Septodont).

Septanest 4% 1:100.000 хорошо проникает в костную ткань, позволяя проводить большинство манипуляций под инфильтрационной анестезией, в том числе лечение моляров и премоляров нижней челюсти. При использовании этого препарата к проводниковой анестезии на нижней челюсти (торусальная, мандибулярная) мы прибегаем лишь при необходимости обезболивания большого участка зубочелюстной системы (например, при одномоментном депульпировании 3-4 жевательных зубов, хирургическом вмешательстве на пародонте 1–2 сегментов зубного ряда и т.д.).
Как показывает наш клинический опыт, применение Septanest 4% 1:100.000 эффективно для проводниковой и инфильтрационной анестезии при любых терапевтических стоматологических манипуляциях: лечении кариеса и других поражений твердых тканей зубов, длительных эстетических реставрациях зубов композитными материалами, эндодонтических манипуляциях, профессиональной чистке зубов, пародонтологических вмешательствах и т.д.
Septanest 4% 1:100.000 представляет собой 4% раствор артикаина с повышенным содержанием адреналина. Благодаря высокой концентрации вазоконстриктора увеличивается продолжительность и глубина анестезии за счет местной ишемии тканей и замедления вымывания анестетика из зоны инъекции [Петрикас А.Ж., 2009]. Замедление общего всасывания анестетика за счет локального сужения кровеносных сосудов уменьшает также выраженность возможных «общих» побочных эффектов от анестетика. Кроме того, местная ишемия тканей в зоне анестезии снижает кровоточивость, облегчая проведение лечебных манипуляций.
Важной особенностью Septanest 4% 1:100.000 по сравнению с аналогами является наличие в его составе натриевой соли ЭДТА. Данное вещество в сочетании с бисульфитом натрия значительно повышает стабильность адреналина. Именно благодаря наличию двух этих добавок концентрация адреналина в карпуле остается постоянной на протяжении всего рекомендованного срока хранения (2 года). Опасения, высказываемые в некоторых публикациях, о том, что наличие в анестетике ЭДТА может вызывать у пациента головную боль и тошноту, носят скорее теоретический характер. Мы не сталкивались с данными явлениями на протяжении всего периода использования данного анестетика в своей клинической практике.
За счет такого состава Septanest 4% 1:100.000 является единственным «не американским» анестетиком на основе артикаина, разрешенным к применению в США (на американский рынок он поставляется под торговой маркой «Septocaine»). Только «Septodont» экспортирует карпулированные анестетики на основе артикаина практически во все страны мира, включая наиболее сложные для регистрации лекарственных препаратов: США, Японию, Австралию, Англию, Скандинавские страны.
Septanest 4% 1:200.000 [Septanest with adrenaline Раствор для инъекций (с эпинефрином) 40 мг+5 мкг/мл] (рис. 3) имеет «нормальное» содержание адреналина. За счет этого сила обезболивающего действия у него несколько ниже, чем у Septanest 4% 1:100.000 [Петрикас А.Ж., 2009], а продолжительность эффективной анестезии составляет 30-45 мин. Тем не менее, этот препарат обладает обезболивающим эффектом, вполне достаточным для проведения большинства лечебных стоматологических вмешательств. Мы применяем Septanest 4% 1:200.000 для проводниковой и инфильтрационной анестезии при непродолжительных манипуляциях, связанных с препарированием и реставрацией зубов композитами, при профессиональной чистке зубов, нетравматичных и непродолжительных хирургических вмешательствах. Кроме того, использование Septanest 4% 1:200.000 показано при проведении анестезии детям, беременным женщинам и пациентам «групп риска». Мы рассматриваем Septanest 4% 1:200.000 как анестетик выбора для терапевтической стоматологии и основной анестетик для использования в хирургической стоматологии.
Рис. 3. Septanest 4% 1:200.000 (Septodont).
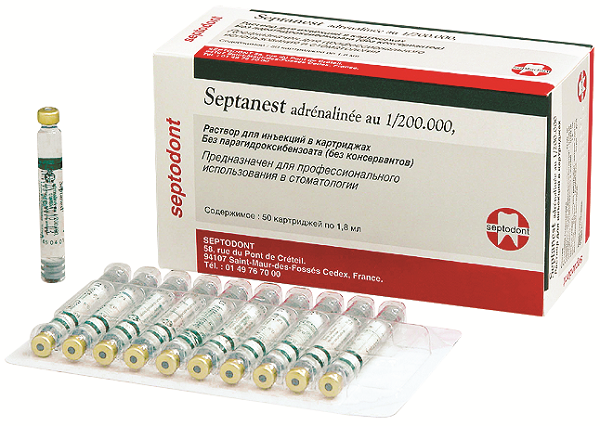
Scandonest 2% Special (рис. 4) – карпулированный анестетик на основе 2% мепивакаина с высоким содержанием адреналина (1:100000). На российском стоматологическом рынке аналогов не имеет. Особенностью этого препарата является выраженный и длительный сосудосуживающий эффект. Это обеспечивает увеличенную продолжительность и глубину анестезии, снижение кровоточивости операционного поля за счет местной ишемии тканей и замедления вымывания анестетика из зоны инъекции.
Рис. 4. Scandonest 2% Special (Septodont).
Время наступления анестезии 2-3 мин. Длительность анестезии на верхней челюсти – 60-120 мин, на нижней челюсти – 120-240 мин. Как уже отмечалось выше, Scandonest 2% Special обеспечивает длительный и глубокий обезболивающий эффект, достаточный для проведения большинства лечебных стоматологических манипуляций. Мы рекомендуем использовать этот препарат для проводниковой и инфильтрационной анестезии при любых стоматологических вмешательствах, в т.ч. продолжительных и сложных. Он может также применяться врачами-стоматологами в качестве «основного» анестетика.
Адреналинсодержащие анестетики, несомненно, являются основой местной анестезии в современной стоматологии, однако, следует помнить, что в следующих клинических ситуациях их применение противопоказано:
− наличие у пациента сердечно-сосудистых заболеваний (артериальная гипертензия, пароксизмальная тахикардия и другие виды тахисистолии, нарушения коронарного и мозгового кровообращения, порок сердца и т.д.);
− недавно перенесенный инфаркт миокарда (в течение последних 6 месяцев);
− закрытоугольная глаукома;
− лечение трициклическими антидепрессантами (амитриптилин, мелипрамин и т.д.), ингибиторами моноаминоксидазы (МАО), неселективными бета-адреноблокаторами, нейролептиками, сердечными гликозидами;
− тяжелые формы сахарного диабета, особенно в стадии декомпенсации;
− выраженный тиреотоксикоз, прием гормонов щитовидной железы (тиреотом);
− резко повышенный уровень тревожности;
− предстоящее прохождение пациентом допинг-контроля.
В перечисленных выше клинических ситуациях показано использование анестетиков, не содержащих адреналина и его стабилизаторов (бисульфита натрия и ЭДТА), например, Scandonest 3% (Septodont) (рис. 5).
Рис. 5. Scandonest 3% (Septodont).
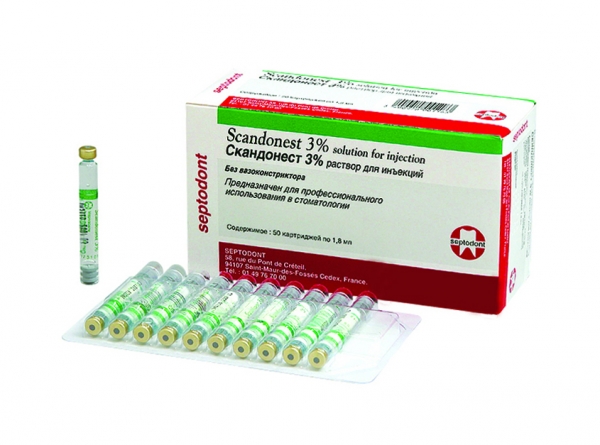
Scandonest 3% – карпулированный анестетик на основе 3% раствора мепивакаина добавления без адреналина и других вазоконстрикторов. Время наступления анестезии – 1-3 мин. Длительность анестезии – 10–20 мин. Данный препарат обеспечивает мягкий, неглубокий обезболивающий эффект, достаточный для проведения лишь кратковременных и нетравматичных лечебных манипуляций.
Мы рассматриваем Scandonest 3% как «запасной» анестетик, предназначенный для пациентов «групп риска» и рекомендуем применять его в следующих ситуациях:
− проводниковая и инфильтрационная анестезия при кратковременных и нетравматичных лечебно-диагностических манипуляциях;
− проведение анестезии пациентам, которым противопоказано применение анестетиков с вазоконстрикторами (гипертония, сахарный диабет, коронарная недостаточность и т.д.);
− проведение анестезии пациентам с отягощенным аллергологическим анамнезом: при бронхиальной астме, аллергических дерматозах, опасности аллергической реакции на сульфиты и ЭДТА.
Говоря о клиническом применении карпулированных анестетиков, следует особо остановиться на нескольких моментах.
1. Проблема уменьшения болезненности инъекции.
Проведение инъекционной анестезии в стоматологии обычно сопровождается болезненностью при вколе иглы, продвижении ее в тканях и введении анестезирующего препарата. Это вызывает у пациента неприятные ощущения и страх не только перед стоматологическими манипуляциями, но и перед самой анестезией, например, при последующих инъекциях у детей. Чтобы избежать этого и свести к минимуму перечисленные негативные явления, мы рекомендуем применять трехэтапную анестезию:
Первый этап – аппликация на место будущего вкола иглы на 1-1,5 мин местноанестезирующего средства (рис. 6, 7, 8), например, «Yilonor gel» (Septodont) (рис. 9). Он представляет собой анестезирующий гель на основе 5% лидокаина и антисептика цетримида, что позволяет одномоментно проводить и обезболивание, и антисептическую обработку слизистой оболочки в области места вкола иглы перед инъекционной анестезией. Перед инъекцией гель с поверхности слизистой оболочки должен быть удален (рис. 10).
Рис. 6. Трехэтапная анестезия: местноанестезирующий препарат наносится на бумажный блок.

Рис. 7. Трехэтапная анестезия: местноанестезирующий препарат наносится на ватный тампон.

Рис. 8. Трехэтапная анестезия: нанесение местноанестезирующего препарата на место будущего вкола иглы (экспозиция – 1-1,5 мин).
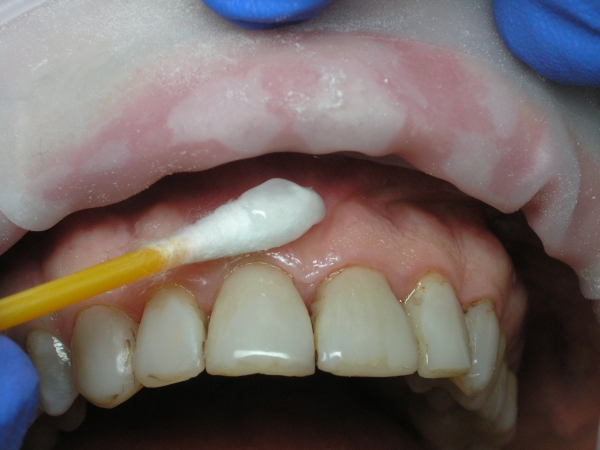
Рис. 9. «Xilonor gel» (Septodont).
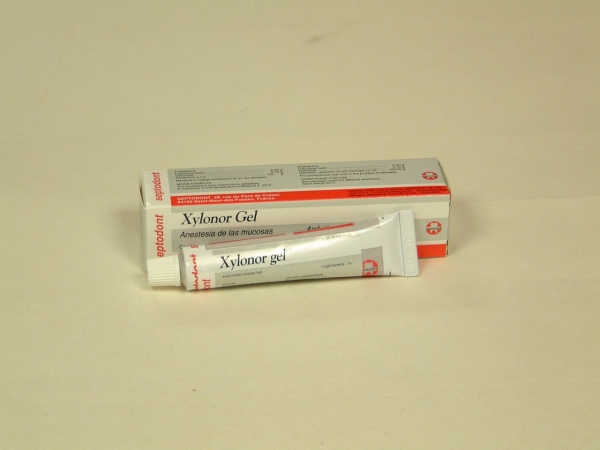
Рис. 10. Трехэтапная анестезия: удаление местноанестезирующего геля с поверхности слизистой оболочки сухим ватным тампоном.
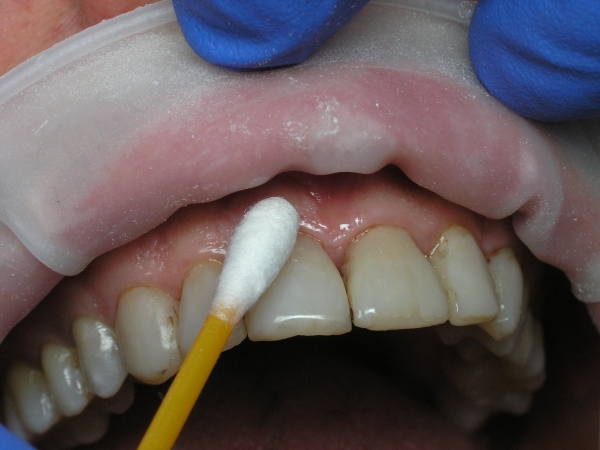
Второй этап – субмукозное (подслизистое) введение 0,2–0,3 мл раствора анестетика (рис. 11).
Рис. 11. Трехэтапная анестезия: субмукозное введение анестетика.
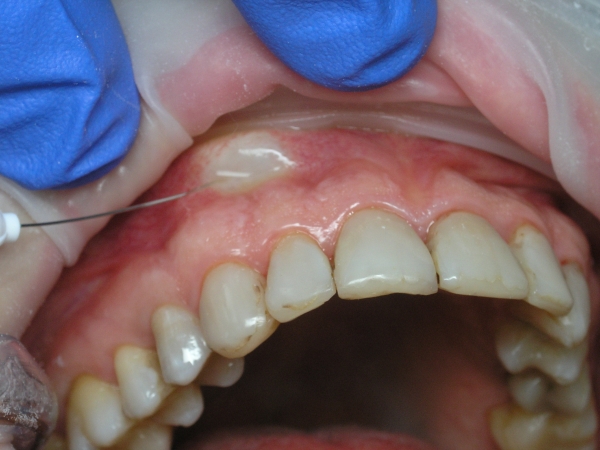
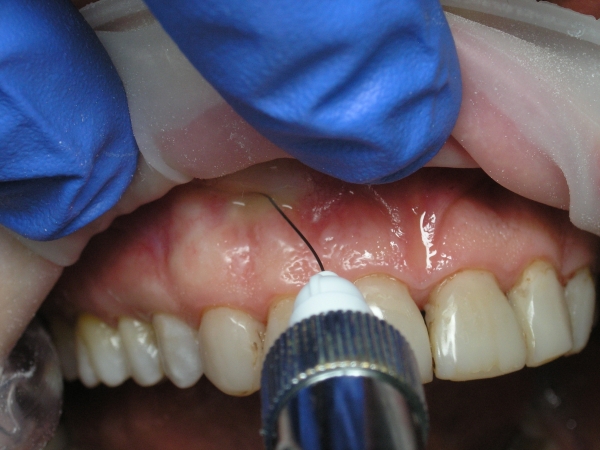
Третий этап – через 1-2 мин – поднадкостничное или интралигаментарное введение раствора 1,0-1,5 мл анестетика (рис. 12). Оптимальная скорость введения – 1 мл/мин.
Рис. 12. Трехэтапная анестезия: поднадкостничное введение анестетика.
Данная методика, хотя и занимает несколько больше времени, чем традиционная, по нашему мнению, более предпочтительна, так как позволяет свести болевые ощущения к минимуму.
2. Количество и скорость введения анестетика.
В связи с высокой эффективностью карпулированных анестетиков для достижения эффективной анестезии достаточно их небольшого количества (табл. 1).
Таблица 1. Рекомендованные объемы местноанестезирующих препаратов для проведения инъекционной анестезии при стоматологических вмешательствах у взрослых
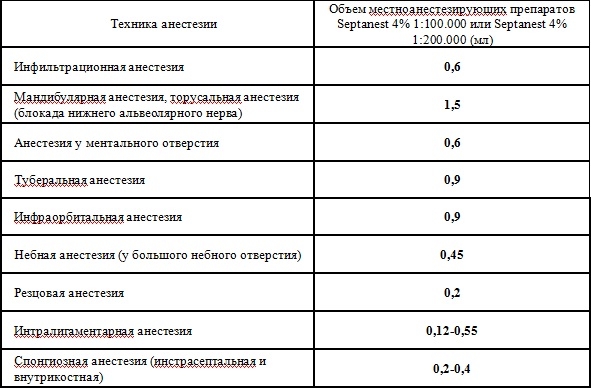
В некоторых случаях одной инъекции бывает недостаточно и врачу приходится «добавлять» анестезию. При этом не следует превышать максимально допустимой дозы анестетика. Наиболее безопасным считается разовое введение анестетика в количестве, не превышающем половины максимальной дозы (табл. 2).
Таблица 2. Максимальные и безопасные разовые дозы карпулированных анестетиков

Примечание: 1 карпула = 1,7 мл.
Введение местноанестезирующего препарата в просвет кровеносного сосуда может привести к осложнениям, связанным с общетоксическим действием анестетика и вазоконстриктора (токсическая реакция). Поэтому при проведении инъекционной анестезии, чтобы избежать этого явления обязательно нужно проводить аспирационную пробу.
Рекомендуется также соблюдать безопасную скорость введения анестетика. Чтобы артикаин при случайном прямом введении его в кровеносное русло не оказал общетоксического действия, содержимое карпулы (1,7 мл) должно вводиться в ткани не быстрее, чем в течение 20-25 с (соответствует скорости инактивации артикаина ферментативными системами крови). Оптимальной скоростью введения считается 0,5 мл за 15 с, что соответствует 1 мин для карпулы.
Препараты на основе мепивакаина, который метаболизируется в печени, должны вводиться еще медленнее. Скорость их введения не должна превышать 1 мл в минуту.
3. Проблема повторного использования карпул.
Зачастую в карпуле после анестезии остается достаточно большое количество анестезирующего препарата (рис. 13). Некоторые стоматологи оставляют такие карпулы, чтобы использовать их еще раз.
Это абсолютно недопустимо! Повторно использовать карпулу с остатками обезболивающего раствора другому пациенту, даже меняя иглы, запрещается!
Рис. 13. Такие карпулы повторно использовать нельзя!
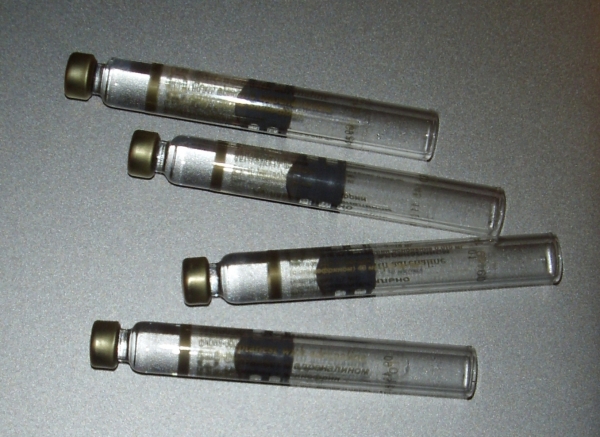
Даже если в карпуле не видно крови, опасность перекрестной передачи инфекции (СПИД, вирусный гепатит и т.д.) в случае повторного использования карпулы равна практически 100%. Это связано с тем, что из-за эластичности резиновой пробки-поршня после первичного введения анестетика и прекращения давления происходит аспирация в карпулу микроскопических частичек крови и тканей, невидимых для глаза. Тем не менее, этого количества вполне достаточно для передачи инфекции, в первую очередь, – вирусного гепатита, от одного пациента другому.
Таким образом, лишь комплексный подход к «карпульной» анестезии, предусматривающий учет свойств и состава местных анестетиков, общего и местного стоматологического статуса пациента, соблюдение технологии проведения анестезии и, самое главное, отношение к ней, как к эффективной, но потенциально опасной медицинской манипуляции, позволяет практическому врачу-стоматологу обеспечить эффективное обезболивание в сочетании с минимальным риском развития осложнений и нежелательных побочных эффектов.
Авторы: Николаев А.И., Николаев Д.А.
Смоленская государственная медицинская академия, кафедра терапевтической стоматологии
Источник
Введение
Еще не так давно технология местной анестезии включала приготовление местноанестезирующих средств путем разведения концентрированных растворов местных анестетиков и добавления при необходимости вазоконстрикторов непосредственно в лечебном учреждении. В связи с этим ответственность за соблюдение правильности выполнения всех этапов приготовления растворов целиком ложилась на сотрудников учреждения.
В значительном числе случаев приготовление растворов – в силу отсутствия специального оборудования, производилось с ошибками и неточностями, что приводило к осложнениям при инъекциях таких растворов пациентам.
Разработка карпульной технологии – революционное достижение в нашей специальности.
Перенос процесса производства местноанестезирующих средств в заводские условия обеспечил стерильность и высокую надежность технологии их изготовления. Современный процесс производства анестетиков полностью автоматизирован и контролируется на всех этапах, начиная с очистки воды и заканчивая разведением вазоконстрикторов. Благодаря этому врач-стоматолог может быть полностью уверен в качестве применяемых местноанестезирующих средств.[11]
Карпульная технология
Карпульная технология состоит из следующих основных компонентов:
- стандартизации лекарственных форм местноанестезирующих препаратов;
- производства в заводских условиях готовых к использованию препаратов в виде стандартизованного раствора в стандартизованной упаковке;
- техники инъекции препаратов с применением специальных инструментов (шприцев, игл) и способов их использования.
При самостоятельном изготовлении препаратов как состав, так и концентрация входящих в раствор веществ могли варьировать в значительных пределах. Внедрение карпульной технологии позволило перенести ответственность за качество вводимых препаратов на фирмы-производители.[10] При этом врачу необходимо лишь соблюсти ряд обязательных условий:
- местноанестезирующий препарат должен быть разрешен к применению Фармакологическим комитетом Минздрава РФ;
- в комплекте поставки должен быть сертификат соответствия данной партии препарата, подтверждающий (на основе экспертизы) его качество. Номер партии указывается на каждой упаковке и карпуле. Особое внимание обращается на срок хранения – применение просроченных препаратов не допускается.
Стерильности растворов удалось добиться благодаря созданию удобной герметичной конструкции – карпулы (или картриджа). Карпула обеспечивает длительное хранение и дозированную инъекцию находящегося в ней раствора. Кроме того, с ее помощью можно создать высокое давление, необходимое при интралигаментарной или интрасептальной анестезии, или разрежение – в случае проведения аспирационной пробы.[2]
Каждая карпула состоит из стеклянного или пластмассового цилиндра с силиконовым поршнем с одной стороны и резиновой пробкой и металлическим колпачком – с другой. Внутренний объем карпулы обычно составляет 2 мл, но за счет наличия пробки он сокращается до 1,7-1,8 мл.
Вследствие неправильной транспортировки и хранения могут возникать изменения внешнего вида карпул или упаковки, в которой они содержатся.
Наиболее опасными являются следующие:
- изменение цвета и консистенции раствора – пожелтение, помутнение или появление осадка;
- положение поршня, когда он выходит за край карпулы; при этом внутри могут находиться пузырьки размером более 2 мм;
- наличие ржавчины на карпуле;
- наличие вмятин или других повреждений на упаковке.
Рис.1. Карпульные анестетики в пластиковых упаковках (блистерах) по 10 шт.
Изменение цвета и консистенции раствора свидетельствует о нарушении его химического состава, которое чаще всего происходит в результате распада вазоконстриктора под влиянием тепла, света или продолжительного срока хранения.
Если в процессе хранения произошло замораживание содержимого карпулы и последующее его размораживание, что, как правило, сопровождается всасыванием воздуха, то в карпуле образуется пузырек большого размера, и поршень также выталкивается.
Пузырьки небольшого размера – при правильном положении пробки и поршня – могут быть следствием скопления газообразного азота, применяемого в производстве для предотвращения попадания в карпулу кислорода. Такие карпулы можно использовать.
Наличие ржавчины свидетельствуете нарушении целостности данной или хранившейся рядом карпулы и вытекании раствора наружу. В таком случае необходимо тщательно просмотреть карпулы и выявить поврежденную, чтобы она случайно не была использована.
Карпульныеинъекторы
Изобретением шприца мир обязан великому французскому ученому Блезу Паскалю, который в 1647 году сделал сразу два важнейших изобретения – гидравлический пресс и шприц, однако последний широкого применения не нашел. Шприц в том виде, в котором мы знаем его сейчас, был изобретён лишь в 1853 году Чарльзом Габриэлем Правазом (CharlesGabrielPravaz) и Александром Вудом (AlexanderWood) независимо друг от друга.
Первые шприцы изготавливались из каучукового цилиндра, внутрь которого помещался хорошо подогнанный поршень из кожи и асбеста с торчащим наружу металлическим штырем. На другом конце цилиндра укреплялась полая игла. Так как цилиндр был непрозрачным, насечки для дозировки лекарства делались не на нем, а на металлическом штыре поршня.
Близкий к современному универсальный шприц Праваца применялся в медицинской практике почти до середины XX века и представлял собой шприц с цилиндром из стекла и остальными частями из хромированного металла.
Важнейшим достижением начального периода применения местной анестезии явилась разработка функционального дентального шприца Блейхштайнером и Фишером. Главными их признаками были навинчивающаяся канюля и упоры для пальцев и ладони (рис.2).
Рис.2. Зубоврачебные шприцы для местной анестезии: а) шприцБлейхштайнера; б) шприц Фишера.
Наибольшее распространение в общей медицине имели шприцы типа «Рекорд» – цилиндр из термостойкого стекла, а остальные детали металлические (рис. 3, а, б). Иглы на шприц не навинчиваются, а удерживаются за счет фрикционности и конусности соединения, что увеличивает риск соскальзывания их во время введения раствора или промывания.
В конце 50-х годов XIX века Люэр (Luer) в Париже описал винтовое соединение иглы со шприцем, а затем заменил его конусообразной канюлей на конце шприца. Именно это соединение между шприцем и иглой используется в наши дни. Он также ликвидировал винтовой ход поршня и добавил градуировку на корпусе. Шприц Люэра состоит целиком из стекла (рис. 3, в).
Рис.3. Медицинские шприцы: а – «Рекорд»; б – «Рекорд»; в – «Люэр»
Главным недостатком шприцев из стекла является то, что они быстро бьются. Поэтому стали выпускать шприцы из небьющейся термостойкой пластмассы. Первые попытки выпускать пластмассовые шприцы одноразового использования, стерилизованные фабричным путем, были сделаны в США в 40-е годы. В 1949—1950 Артур Смит получил патенты США на одноразовые шприцы.
Первые одноразовые шприцы массово стали производиться компанией «Becton, DickinsonandCompany» в 1954 году. Эти шприцы изготавливались из стекла.[1]
В 1956 Колин Мурдок (ColinMurdoch), фармацевт из Новой Зеландии изобрёл и запатентовал пластиковый одноразовый шприц.
В настоящее время многие изобретатели работают над реализацией идеи действительно одноразовых шприцов — то есть таких, которые было бы просто физически невозможно использовать дважды. Эта задача обусловлена борьбой с распространением ВИЧ и других инфекций. Некоторые изобретатели уже достигли определенных успехов и даже получили на них патенты, однако действительно надежное и экономичное решение этой задачи отсутствует.
Применение одноразовых общемедицинских шприцов в стоматологии затруднительно в силу ряда причин:
1. Аспирационная проба
Аспирация – всасывание среды, в которой располагается кончик иглы. Используется для того, чтобы по отсутствию появления крови в растворе удостовериться, что кончик иглы не находится внутри кровеносного сосуда. Это необходимо для того, чтобы предотвратить введение в кровеносное русло высококонцентрированных веществ, используемых в современной технологии местного обезболивания. Системные осложнения, вызванные внутрисосудистым введением анестетика, могут представлять опасность для жизни пациента. Поэтому аспирационную пробу следует проводить всегда для избежание нежелательных осложнений.
Наиболее простым способом осуществления аспирации является обратное движение поршня, которое и создает отрицательное давление в растворе. Обычные шприцы не имеют конструктивных приспособлений для аспирации, поэтому при их использовании приходится одной рукой держать шприц, а другой – оттягивать назад поршень. Помимо неудобства в работе такая техника создает дополнительную опасность возникновения осложнений. Неизбежные микродвижения рук относительно друг друга приведут к дрожанию острого кончика иглы и разрыву им тканей.
2. Чрезмерное введение вазоконстрикторов или ошибочных растворов
Несмотря на низкую системную токсичность местных анестетиков, полностью избежать побочных эффектов не удаётся. Системные побочные эффекты, как правило, связаны с одним из компонентов в составе местного анестетика. В качестве проявлений реакции можно назвать интоксикацию, как результат относительной или абсолютной передозировки, реакцию повышенной чувствительности, или же взаимодействие с другими препаратами.[13]
Местноанестезирующие препараты, применяемые в стоматологии, обладают относительно высоким терапевтическим индексом, т. е. концентрация анестетика в сыворотке крови после введения терапевтической дозы значительно ниже порога токсичности. Введение чрезмерной дозы анестетика приводит к повышению концентрации анестетика и вазоконстриктора в крови. В этой связи могут развиваться психогенные реакции, которые, в отдельных случаях очень тяжело отличить от истинной интоксикации, спровоцированной местным анестетиком. Системные побочные эффекты при применении местных анестетиков проявляются со стороны ЦНС и ССС.
3. Диаметр инъекционной иглы
В общемедицинских шприцах диаметр инъекционной иглы 0.6-0.8 мм., что недопустимо в стоматологии, так как вызывает ряд осложнений после проведения процедуры инъекции. Например, травма слизистой оболочки полости рта; травма нервных стволов; чрезмерный болевой эффект; гематомы; воспаления.
Для сравнения, диаметр иглы, применяемой в современной стоматологии 0.3-0.4 мм.
4. Нарушение стерильности на этапе набора лекарственного препарата из ампулы
Набор лекарственного препарата из ампулы имеет определенную последовательность:
1. обработка ампулы;
2. предварительный набор вазоконстриктора в одноразовый шприц;
3. вскрытие ампулы;
4. набор лекарственного препарата;
5. смена иглы после набора.
Каждый из этапов может нести нарушение стерильности и, как следствие, различные осложнения.
Ключевым вопросом эффективного и безопасного применения местного обезболивания в стоматологии является использование карпульной технологии, современных местных анестезирующих препаратов (содержащих необходимое количество вазоконстрикторов), соответствующих инъекторов и одноразовых игл.
Разработка карпульной технологии – это революционной достижение современной стоматологии.
Карпульная технология состоит из следующих основных компонентов:
• стандартизации лекарственных форм местноанестезирующих препаратов;
• производства в заводских условиях препаратов в виде, готовом к использованию, который включает как стандартизованный раствор, так и стандартизованную упаковку;
• техники инъекции препаратов с применением специальных инструментов (шприцев, игл) и порядка их использования.
Впервые карпулы (картриджи) были созданы еще в 1917 г. во время I мировой войны американским военным хирургом Харвеем Куком (Harvey S.Cook), который изобрел цилиндрические ампулы – прообраз современных карпул.Карпула представляла собой стеклянную цилиндрическую трубку, закрывающуюся с одной стороны резиновым поршнем (пробкой), а с другой – резиновой мембраной, прокалываемой иглой во время инъекции (рис. 4).
Рисунок 4. Составные элементы карпулы: 1 – алюминиевый колпачок, 2 – эластичная мембрана, 3 – стеклянная ампула, 4 – эластичный поршень-пробка.
Другим достижением явилась разработка H.S. Cook в 1921 году карпульного шприца (рис. 5) для обезболивания зубов, который заряжается цилиндрической ампулой (карпулой) с раствором местного анестетика, с двумя резиновыми пробками на концах (диафрагма и поршень). Эта герметичная и экономичная система обеспечивает высокий уровень асептики, предупреждает возможность подмены растворов лекарственных средств.
Конструкция этого шприца была усовершенствована в 1957 году добавлением аспирационного плунжера для определения попадания иглы в кровеносные сосуды, чтобы предотвратить внутрисосудистую инъекцию. В то время наладить серийное производство карпульного шприца и карпулы не удалось из-за сложности конструкции.
Рис.5. Карпульный шприц
Объем карпулы в 1,8 мл в 1947 г. произвольно выбрала фирма “Вауеr”, и он стал стандартом. В Великобритании, Австралии и некоторых странах Азии производятся карпулы объемом 2,2 мл. Главным достоинством стоматологической картриджной системы является быстрая (менее минуты) подготовка к инъекции и гарантированная производителем стерилизация тех элементов (иглы и картриджи), которые контактируют с субэпителиальными тканями.
Одним из недостатков классической картриджной системы была невозможность аспирации – обратного оттягивания поршня, чтобы исключить случайное попадание иглы в просвет сосуда. Для совмещения поршня-пробки картриджа со штоком (толкателем) шприца были Предложены винтовое соединение и гарпунное, требовавшие конструктивных изменений как самого картриджа, так и шприца. Последняя фирма в 1959 г. разработала к этому шприцу разовые стерильные иглы.
Изобретение безыгольныхинъекторов М. Локхардом в 1940 году дало возможность обеспечивать в сжатые сроки проведение большого количества инъекций в условиях стерильности, что требуется в эпидемиологической и военно-медицинской практике. Первое их использование для инъекций в полости рта относится к 1958году. “БИ-8” – отечественный безыгольный стоматологический инъектор (рис.6), который разрабатывал коллектив воронежских конструкторов совместно со специалистами-медиками в 1968 году.
Рис.6. Безыгольный стоматологический инъектор
В практику отечественной стоматологии безыгольныеинъекторы для местной анестезии были введены в 1973 году, но в амбулаторной стоматологии они себя не оправдали из-за сложных конструктивных параметров: крупные размеры, сложные устройства, требующие четких знаний правил эксплуатации, большое давление (до 300 атм.) и высокая скорость тончайшей струи вещества (до 800 км/ч), что обеспечивает проникновение ее в ткани, производя при этом микроразрывы структур. Все это делает инъектор источником повышенной опасности как для пациента, так и для медицинского персонала.[12]
Несмотря на внедрение в клиническую практику и экономическую эффективность, безыгольныеинъекторы разработанных конструкций не решали проблемы “шприцевого” гепатита и не соответствовали современным эпидемиологическим требованиям. В 1989 г. применение безыгольныхинъекторов в нашей стране было повсеместно прекращено “в целях обеспечения безопасности от кровяных инфекций” на основании Письма Минздрава СССР № 06-14/28-14 от 24 июля 1989 г. “О применении инактивированных гриппозных вакцин”. Произошел возврат к шприцевой вакцинации и анестезии.
За рубежом в общемедицинской практике получили широкое распространение шприцы одноразового использования из полимерных материалов. В основном использовались две группы конструкций. К первой относились шприцы с эластичным уплотнением, выполненным из силиконовой резины (фирмы “Sherwood”, США; “BectonDickinson”, Франция и др.).[7]
Технология производства включала дополнительные операции изготовления силиконовых резиновых уплотнений, что повышало надежность конструкции в работе. Ко второй группе относились шприцы с эластичными цилиндрами и жесткими штоками (фирма “Вrаun”, ФРГ). Эти шприцы были менее надежны в работе из-за частичного перетекания жидкости между поршнем и цилиндром.
В нашей стране в 60-е годы предпринимались попытки разработать шприцы из полимерных материалов, но по разным причинам они были неудачными. Несмотря на это, работы над шприцами одноразового использования из полимерного материала продолжались, потому что преимущества этих шприцев были очевидны и заключались не только в технологии их изготовления, но и в значительном снижении проблемы “шприцевого” пути передачи вирусного гепатита В и других инфекций.
В 2010 году российская компания «АЭРС-МЕД» разработала и запатентовала «Комплект для инъекций однократного применения АЭРС». Ведущая научная кафедра России в области стоматологии общей практ?
