Какой галоген не проявляет восстановительных свойств

| Группа → | 17 (VIIA) | ||||||
|---|---|---|---|---|---|---|---|
| ↓ Период | |||||||
| 2 |
| ||||||
| 3 |
| ||||||
| 4 |
| ||||||
| 5 |
| ||||||
| 6 |
| ||||||
| 7 |
| ||||||
Галоге́ны (от греч. ἁλός — «соль» и γένος — «рождение, происхождение»; иногда употребляется устаревшее название гало́иды) — химические элементы 17-й группы периодической таблицы химических элементов Д. И. Менделеева (по устаревшей классификации — элементы главной подгруппы VII группы)[1].
Реагируют почти со всеми простыми веществами, кроме некоторых неметаллов. Все галогены — энергичные окислители, поэтому встречаются в природе только в виде соединений. С увеличением порядкового номера химическая активность галогенов уменьшается, химическая активность галогенид-ионов F−, Cl−, Br−, I−, At− уменьшается.
К галогенам относятся фтор F, хлор Cl, бром Br, иод I, астат At, а также (формально) искусственный элемент теннессин Ts.
Все галогены — неметаллы, являются сильными окислителями. На внешнем энергетическом уровне 7 электронов. При взаимодействии с металлами возникает ионная связь, и образуются соли. Галогены (кроме фтора) при взаимодействии с более электроотрицательными элементами могут проявлять и восстановительные свойства вплоть до высшей степени окисления +7.
Этимология[править | править код]
Термин «галогены» в отношении всей группы элементов (на тот момент были известны фтор, хлор, бром и иод) был предложен в 1841 году шведским химиком Й. Берцелиусом. Первоначально слово «галоген» (в буквальном переводе с греческого — «солерод») было предложено в 1811 году немецким учёным И. Швейггером в качестве названия для недавно открытого хлора, однако в химии закрепилось название, которое предложил Г. Дэви[2].
Строение атомов и степени окисления[править | править код]
Электронная конфигурация внешней электронной оболочки атомов галогенов ns2np5: фтор — 2s22p5, хлор — 3s23p5, бром — 4s24p5, иод — 5s25p5, астат — 6s26p5.
Имея на внешней электронной оболочке 7 электронов, атомы всех галогенов легко присоединяют недостающий до завершения оболочки 1 электрон и в своих соединениях проявляют степень окисления −1. Хлор, бром, иод и астат в соединениях с более электроотрицательными элементами проявляют положительные степени окисления: +1, +3, +5, +7. Для фтора характерна постоянная степень окисления −1.
Распространённость элементов и получение простых веществ[править | править код]
Как уже было сказано выше, галогены имеют высокую реакционную способность, поэтому встречаются в природе обычно в виде соединений.
Их распространённость в земной коре уменьшается при увеличении атомного радиуса от фтора к иоду. Количество астата в земной коре измеряется граммами, а теннессин в природе отсутствует. Фтор, хлор, бром и иод производятся в промышленных масштабах, причём объёмы производства хлора значительно выше, чем трёх других стабильных галогенов.
В природе эти элементы встречаются в основном в виде галогенидов (за исключением иода, который также встречается в виде иодата натрия или калия в месторождениях нитратов щелочных металлов). Поскольку многие хлориды, бромиды и иодиды растворимы в воде, то эти анионы присутствуют в океане и природных рассолах. Основным источником фтора является фторид кальция, который очень малорастворим и находится в осадочных породах (как флюорит CaF2).
Основным способом получения простых веществ является окисление галогенидов. Высокие положительные стандартные электродные потенциалы Eo(F2/F−) = +2,87 В и Eo(Cl2/Cl−) = +1,36 В показывают, что окислить ионы F− и Cl− можно только сильными окислителями. В промышленности применяется только электролитическое окисление. При получении фтора нельзя использовать водный раствор, поскольку вода окисляется при значительно более низком потенциале (+1,32 В) и образующийся фтор стал бы быстро реагировать с водой. Впервые фтор был получен в 1886 г. французским химиком Анри Муассаном при электролизе раствора гидрофторида калия KHF2 в безводной плавиковой кислоте.
В промышленности хлор в основном получают электролизом водного раствора хлорида натрия в специальных электролизёрах. При этом протекают следующие реакции:
полуреакция на аноде:
полуреакция на катоде:
Окисление воды на аноде подавляется использованием такого материала электрода, который имеет более высокое перенапряжение по отношению к O2, чем к Cl2 (таким материалом является, в частности, RuO2).
В современных электролизёрах катодное и анодное пространства разделены полимерной ионообменной мембраной. Мембрана позволяет катионам Na+ переходить из анодного пространства в катодное. Переход катионов поддерживает электронейтральность в обеих частях электролизёра, так как в течение электролиза отрицательные ионы удаляются от анода (превращение 2Cl− в Cl2) и накапливаются у катода (образование OH−). Перемещение OH− в противоположную сторону могло бы тоже поддерживать электронейтральность, но ион OH− реагировал бы с Cl2 и сводил на нет весь результат.
Бром получают химическим окислением бромид-иона, находящегося в морской воде. Подобный процесс используется и для получения иода из природных рассолов, богатых I−. В качестве окислителя в обоих случаях используют хлор, обладающий более сильными окислительными свойствами, а образующиеся Br2 и I2 удаляются из раствора потоком воздуха.
Физические свойства галогенов[править | править код]
| Вещество | Агрегатное состояние при обычных условиях | Цвет | Запах |
|---|---|---|---|
| Фтор F2 | Газ, не сжижается при обычной температуре | Светло-желтый | Резкий, раздражающий |
| Хлор CI2 | Газ, сжижающийся при обычной температуре под давлением | Жёлто-зелёный | Резкий, удушливый |
| Бром Br2 | Тяжёлая летучая жидкость | Буровато-коричневый | Резкий, зловонный |
| Иод I2 | Твёрдое вещество | Тёмно-серый с металлическим блеском | Резкий |
| Астат At2 | Твёрдое вещество | Сине-чёрный с металлическим блеском | Вероятно, резкий |
| Простое вещество | Температура плавления, °C | Температура кипения, °C |
| F2 | −220 | −188 |
| Cl2 | −101 | −34 |
| Br2 | −7 | 58 |
| I2 | 113,5 | 184,885 |
| At2 | 244 | 309[3] |
Химические свойства галогенов[править | править код]
Все галогены проявляют высокую окислительную активность, которая уменьшается при переходе от фтора к теннессину. Фтор — самый активный из галогенов, реагирует со всеми металлами без исключения, многие из них в атмосфере фтора самовоспламеняются, выделяя большое количество теплоты, например:
Без нагревания фтор реагирует и со многими неметаллами (H2, S, С, Si, Р); все реакции при этом сильно экзотермические и могут протекать со взрывом, например:
При нагревании фтор окисляет все другие галогены по схеме
Hal2 + F2 = 2НalF
причём в соединениях HalF степени окисления хлора, брома, иода и астата равны +1.
Наконец, при облучении фтор реагирует даже с тяжёлыми инертными (благородными) газами:
Взаимодействие фтора со сложными веществами также протекает очень энергично. Так, он окисляет воду, при этом реакция носит взрывной характер:
Свободный хлор также очень реакционноспособен, хотя его активность и меньше, чем у фтора. Он непосредственно реагирует со всеми простыми веществами, за исключением кислорода, азота и благородных газов:
Особый интерес представляет реакция с водородом. Так, при комнатной температуре, без освещения хлор практически не реагирует с водородом, тогда как при нагревании или при освещении (например, на прямом солнечном свету) эта реакция протекает со взрывом по приведенному ниже цепному механизму:
Возбуждение этой реакции происходит под действием фотонов , которые вызывают диссоциацию молекул Cl2 на атомы — при этом возникает цепь последовательных реакций, в каждой из которых появляется частица, инициирующая начало последующей стадии.
Реакция между Н2 и Cl2 послужила одним из первых объектов исследования цепных фотохимических реакций. Наибольший вклад в развитие представлений о цепных реакциях внёс русский учёный, лауреат Нобелевской премии (1956 год) Н. Н. Семёнов.
Хлор вступает в реакцию со многими сложными веществами, например замещения и присоединения с углеводородами:
Хлор способен при нагревании вытеснять бром или иод из их соединений с водородом или металлами:
а также обратимо реагирует с водой, образуя равновесную смесь веществ, называемую хлорной водой:
Хлор может таким же образом реагировать (диспропорционировать) со щелочами:
- на холоде
- при нагревании:
Химическая активность брома меньше, чем у фтора и хлора, но все же достаточно велика в связи с тем, что бром обычно используют в жидком состоянии, и поэтому его исходные концентрации при прочих равных условиях больше, чем у хлора. Он вступает в те же реакции, что и хлор. Являясь более мягким реагентом, бром находит широкое применение в органической химии. Бром, так же как и хлор растворяется в воде и, частично реагируя с ней, образует так называемую «бромную воду».
Растворимость в воде иода — 0,3395 грамма на литр при 25 градусах Цельсия[4], это меньше, чем у брома. Водный раствор иода называется «иодной водой»[5]. Иод способен растворяться в растворах иодидов с образованием комплексных анионов:
Образующийся раствор называется раствором Люголя.
Иод существенно отличается по химической активности от остальных галогенов. Он не реагирует с большинством неметаллов, а с металлами медленно реагирует только при нагревании. Взаимодействие же иода с водородом происходит только при сильном нагревании, реакция является эндотермической и обратимой:
Таким образом, химическая активность галогенов последовательно уменьшается от фтора к астату. Каждый галоген в ряду F — At может вытеснять последующий из его соединений с водородом или металлами, то есть каждый галоген в виде простого вещества способен окислять галогенид-ион любого из последующих галогенов[6].
Астат ещё менее реакционноспособен, чем иод. Но и он реагирует с металлами (например с литием):
При диссоциации образуются не только анионы, но и катионы At+: HAt диссоциирует на:
Применение галогенов и их соединений[править | править код]
Природное соединение фтора — криолит Na3AlF6 — применяется при получении алюминия. Соединения фтора используются в качестве добавок в зубные пасты для предотвращения заболеваний кариесом.
Хлор широко используется для получения соляной кислоты, в органическом синтезе при производстве пластмасс и синтетических волокон, каучуков, красителей, растворителей и др. Многие хлорсодержащие соединения используют для борьбы с вредителями в сельском хозяйстве. Хлор и его соединения применяются для отбеливания льняных и хлопчатобумажных тканей, бумаги, обеззараживания питьевой воды. Правда, применение хлора для обеззараживания воды далеко не безопасно, для этих целей лучше использовать озон.
Простые вещества и соединения брома и иода используются в фармацевтической и химической промышленности.
Токсичность галогенов[править | править код]
Вследствие высокой реакционной способности (особенно это ярко проявляется у фтора) все галогены являются ядовитыми веществами с сильно выраженным удушающим и поражающим ткани воздействиями.
Большую опасность представляют пары и аэрозоль фтора, так как в отличие от других галогенов имеют довольно слабый запах и ощущаются только в больших концентрациях.
Примечания[править | править код]
- ↑ Periodic Table of the Elements (англ.) (недоступная ссылка). IUPAC. — PDF. Дата обращения 25 октября 2013. Архивировано 22 августа 2015 года.
- ↑ Snelders, H. A. M. J. S. C. Schweigger: His Romanticism and His Crystal Electrical Theory of Matter (англ.) // Isis (англ.)русск. : journal. — 1971. — Vol. 62, no. 3. — P. 328. — doi:10.1086/350763.
- ↑ Бердоносов С.С. Астат // Химическая энциклопедия : в 5 т. / Гл. ред. И. Л. Кнунянц. — М.: Советская энциклопедия, 1988. — Т. 1: А—Дарзана. — 623 с. — 100 000 экз. — ISBN 5-85270-008-8.
- ↑ Стасиневич Д.С. Иод // Краткая химическая энциклопедия / Отв. ред. И. Л. Кнунянц. — М.: Советская Энциклопедия, 1963. — Т. 2. Ж—Малоновый эфир.
- ↑ Ходаков Ю.В., Эпштейн Д.А., Глориозов П.А. § 84. Фтор, бром, иод // Неорганическая химия: Учебник для 7—8 классов средней школы. — 18-е изд. — М.: Просвещение, 1987. — С. 197—199. — 240 с. — 1 630 000 экз.
- ↑ Н. Е. Кузьменко, В. В. Еремин, В. А. Попков. Начала химии. Современный курс для поступающих в вузы: учебник / Кузьменко, Н. Е.. — 16. — 107045, Москва, Луков пер., д. 8.: “Экзамен”, 2013. — С. 343—347. — 831 с. — ISBN 978-5-377-06154-0.
Литература[править | править код]
- Greenwood, Norman N. (англ.)русск.; Earnshaw, Alan. Chemistry of the Elements (неопр.). — 2nd. — Butterworth–Heinemann (англ.)русск., 1997. — ISBN 0080379419.
Источник
Галогены (греч. hals – соль + genes – рождающий) – химические элементы VIIa группы: F, Cl, Br, I, At. Реагируют с большинством
других элементов и органических соединений.
Галогены широко распространены в природе. Их химическая активность падает от фтора к астату.

Общая характеристика элементов VIIa группы
От F к At (сверху вниз в периодической таблице) происходит увеличение: атомного радиуса, металлических, основных, восстановительных свойств.
Уменьшается электроотрицательность, энергия ионизация, сродство к электрону.
Все галогены относятся к неметаллам, являются сильными окислителями.
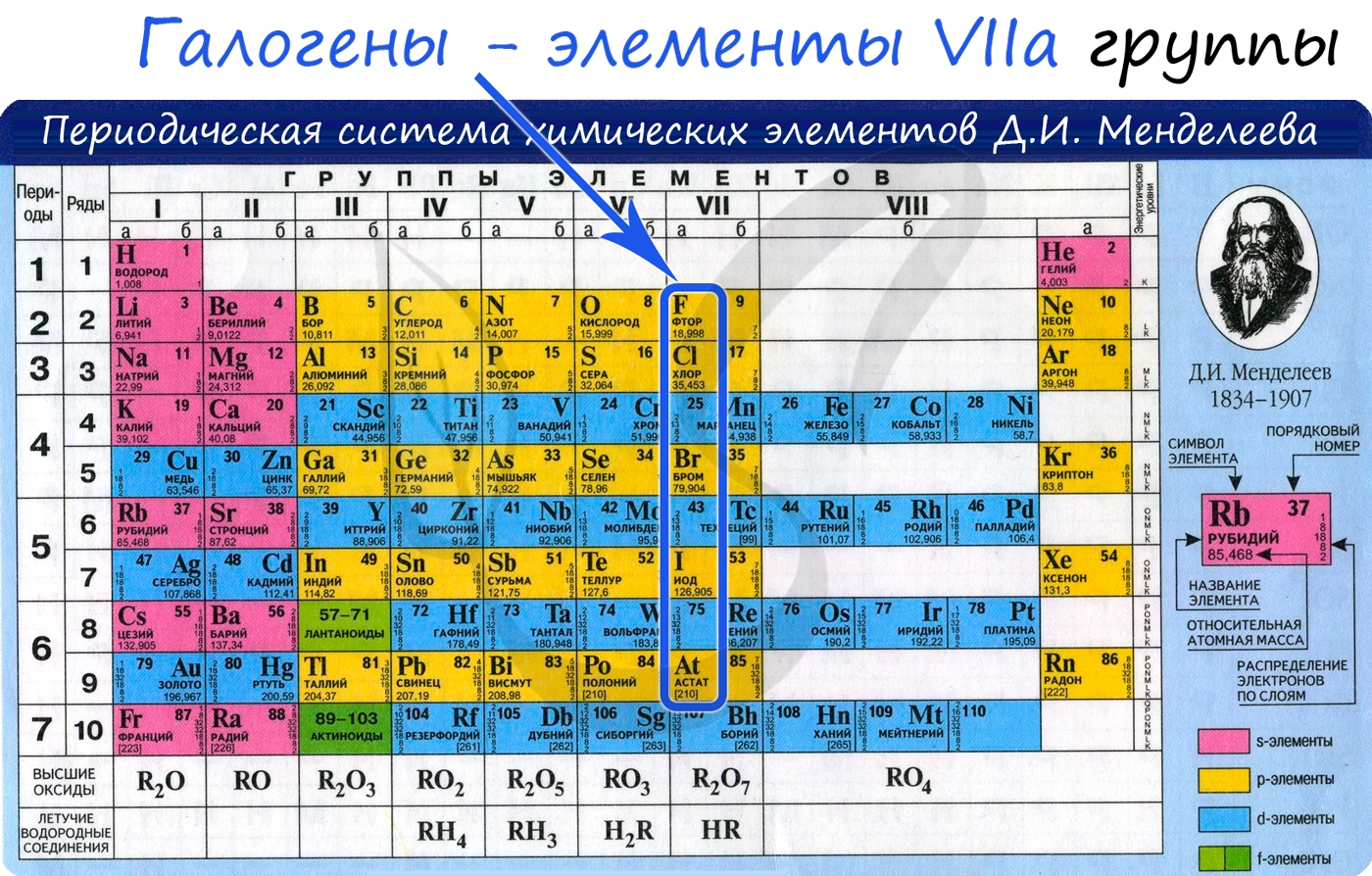
Электронные конфигурации у данных элементов схожи, так как они находятся в одной группе (главной подгруппе!), общая формула ns2np5:
- F – 2s22p5
- Cl – 3s23p5
- Br – 4s24p5
- I – 5s25p5
- At – 6s26p5
Для галогенов характерны нечетные степени окисления: -1, +1, +3, +5, +7. Это связано с электронной конфигурацией атомов
в возбужденном состоянии.

Природные соединения
- NaCl – галит (каменная соль)
- CaF2 – флюорит, плавиковый шпат
- NaCl*KCl – сильвинит
- 3Ca3(PO4)2*CaF2 – фторапатит
- MgCl2*6H2O – бишофит
- KCl*MgCl2*6H2O – карналлит

Простые вещества – F2, Cl2, Br2, I2
Галогены в чистом виде можно получить путем электролиза водных растворов и расплавов их солей. Например, хлор в промышленности получают
электролизом водного раствора хлорида натрия.
NaCl + H2O → (электролиз) NaOH + H2↑ + Cl2↑
Электролизом расплава гидрофторида калия KHF2 в безводной плавиковой кислоте – HF – был впервые получен фтор.
HF → F2 + H2
Более активные галогены способны вытеснять менее активные. Активность галогенов убывает: F → Cl → Br → I.
Cl2 + KBr → Br2 + KCl
Cl2 + KI → I2 + KCl

В лабораторных условиях галогены могут быть получены следующими реакциями.
HCl + MnO2 → MnCl2 + Cl2 + H2O
HCl + KMnO4 → MnCl2 + Cl2 + KCl + H2O
Химические свойства
- Реакции с металлами
- Реакции с неметаллами
- Реакции с водой
- Реакции с щелочами
- Окислительные способности
Для галогенов характерна высокая реакционная способность. Фтор реагирует со всеми металлами без исключения, некоторые из них в атмосфере
фтора самовоспламеняются.
Al + F2 → AlF3
Cu + Cl2 → CuCl2
Na + Br2 → NaBr
Хлор, как и фтор, химически весьма активен. Не реагирует только с кислородом, азотом и благородными газами.
Cl2 + Si → SiCl4
Cl2 + H2 → HCl (на свету)

F2 + H2 → HF (в темноте со взрывом)
Галогены вступают в реакцию друг с другом. Чтобы определить степени окисления в получающихся соединениях, вспомните электроотрицательность 😉
Br2 + F2 → BrF (фтор более электроотрицателен, чем бром – F-)
Br2 + I2 → IBr3 (бром более электроотрицателен, чем йод – Br-)
Реакция фтора с водой протекает очень энергично, носит взрывной характер.
H2O + F2 → HF + O2
Хлор реагирует с водой обратимо, образуя хлорную воду – смесь хлорноватистой и соляной кислоты. Бром вступает в те же реакции, что и хлор.
Cl2 + H2O → HCl + HClO
H2O + Br2 → HBr + HBrO

Замечу, что активность йода существенно ниже, чем у остальных галогенов. С неметаллами йод почти не реагирует, а с металлами – только при
нагревании.
Cl2 + NaOH → NaCl + NaClO + H2O
Cl2 + NaOH → (t) NaCl + NaClO3 + H2O
Галогены способны вытеснять друг друга из солей. Более активные вытесняют менее активные.
KCl + F2 → KF + Cl2
KBr + Cl2 → KCl + Br2
KBr + I2 ⇸ (реакция не идет, так как йод менее активен, чем бром)
Галогеноводороды
Соединения, образованные из галогенов и водорода. К галогеноводородам относятся следующие вещества:
- HF – фтороводород (газ), фтороводородная (плавиковая) кислота (жидкость)
- HCl – хлороводород (газ), соляная кислота (жидкость)
- HBr – бромоводород, бромоводородная кислота
- HI – йодоводород, йодоводородная кислота
- HAt – астатоводород, астатоводородная кислота
При н.у. HCl, HBr, HI – газы, хорошо растворимые в воде.
Получение
В промышленности применяют получение прямым методом: реакцией водорода с галогенами.
H2 + Cl2 → HCl
В лабораторных условиях галогеноводороды можно получить в реакциях обмена между галогенсодержащими солями и сильными кислотами.
NaCl + H2SO4 → NaHSO4 + HCl↑
CaF2 + H2SO4 → CaSO4 + HF
PBr3 + H2O → HBr↑ + H3PO3
H2S + I2 → S + HI
Химические свойства
- Кислотные свойства
- С солями
- Восстановительные свойства
- Реакция с оксидом кремния
HF – является слабой кислотой, HCl, HBr, HI – сильные кислоты. Металлы, стоящие в ряду напряжений до водорода, способны вытеснить
водород из кислоты.
Mg + HBr → MgBr2 + H2↑
Zn + HCl → ZnCl2 + H2↑

Галогеноводороды реагируют с основными, амфотерными оксидами и основаниями с образованием соответствующих солей.
Na2O + HCl → NaCl + H2O
ZnO + HI → ZnI2 + H2O
KOH + HCl → KCl + H2O (реакция нейтрализации)

Cr(OH)3 + HCl → CrCl3 + H2O
Реакции протекают в тех случаях, если в результате выпадает осадок, выделяется газ или образуется слабый электролит (вода).
AgNO3 + HCl → AgCl + HNO3
Li2CO3 + HBr → LiBr + H2CO3
В некоторых реакциях проявляют себя как сильные восстановители, особенно HI.
HI + MnO2 → I2 + MnI2 + H2O
HI + H2SO4 → I2 + H2S + H2O
HI + O2 → H2O + I2
HI + Br2 → HBr + I2
HCl + H2SO4 → Cl2 + SO2 + H2O

В целом взаимодействие галогеноводородов с оксидами неметаллов нехарактерно. В этой связи важно выделить реакцию SiO2 с
плавиковой кислотой.
SiO2 + HF → SiF4 + H2O
© Беллевич Юрий Сергеевич 2018-2020
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение
(в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов
без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования,
обратитесь, пожалуйста, к Беллевичу Юрию.
Источник
