Какое свойство у гелия

Гелий – инертный газ 18-й группы периодической таблицы. Это второй самый легкий элемент после водорода. Гелий – газ без цвета, запаха и вкуса, который становится жидким при температуре -268.9 °C. Точки кипения и замерзания его ниже, чем у любого другого известного вещества. Это единственный элемент, который не затвердевает при охлаждении при нормальном атмосферном давлении. Чтобы гелий перешел в твердое состояние, необходимо 25 атмосфер при температуре 1 К.
История открытия
Гелий был найден в газовой атмосфере, окружающей Солнце, французским астрономом Пьером Жансеном, который в 1868 году во время затмения обнаружил яркую желтую линию в спектре солнечной хромосферы. Первоначально предполагалось, что эта линия представляла элемент натрий. В том же году английский астроном Джозеф Норман Локьер наблюдал желтую линию в солнечном спектре, которая не соответствовала известным линиям натрия D1 и D2, и поэтому он назвал ее линией D3. Локьер пришел к выводу, что она была вызвана веществом на Солнце, неизвестном на Земле. Он и химик Эдуард Франкленд в названии элемента использовали греческое название Солнца «гелиос».
В 1895 году британский химик сэр Уильям Рамзай доказал существование гелия на Земле. Он получил образец ураноносного минерала клевеита, и после исследования газов, образовавшихся при его нагреве, он обнаружил, что ярко-желтая линия в спектре совпадает с линией D3, наблюдаемой в спектре Солнца. Таким образом, новый элемент был окончательно установлен. В 1903 году Рамзи и Фредерик Содду определили, что гелий является продуктом спонтанного распада радиоактивных веществ.

Распространение в природе
Масса гелия составляет около 23% всей массы Вселенной, и элемент является вторым по распространенности в космосе. Он сосредоточен в звездах, где образуется из водорода в результате термоядерного синтеза. Хотя в земной атмосфере гелий находится в концентрации 1 часть на 200 тыс. (5 промилле) и в небольших количествах содержится в радиоактивных минералах, метеоритном железе, а также в минеральных источниках, большие объемы элемента встречаются в Соединенных Штатах (особенно в Техасе, Нью-Мексико, Канзасе, Оклахоме, Аризоне и Юте) в качестве компонента (до 7,6%) природного газа. Небольшие его запасы были обнаружены в Австралии, Алжире, Польше, Катаре и России. В земной коре концентрация гелия равна лишь около 8 частей на миллиард.
Изотопы
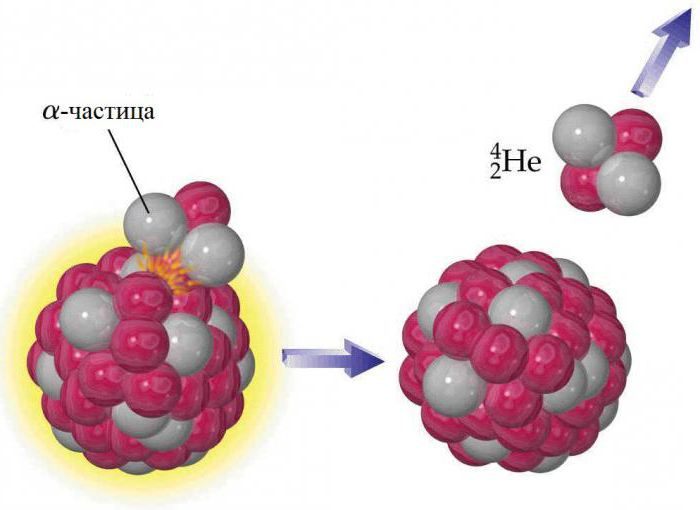
Ядро каждого атома гелия содержит два протона, но, как и у других элементов, у него есть изотопы. Они содержат от одного до шести нейтронов, поэтому их массовые числа находятся в диапазоне от трех до восьми. Стабильными из них являются элементы, у которых масса гелия определяется атомными числами 3 (3He) и 4 (4He). Все остальные радиоактивны и очень быстро распадаются на другие вещества. Земной гелий не является изначальной составляющей планеты, он образовался в результате радиоактивного распада. Альфа-частицы, испускаемые ядрами тяжелых радиоактивных веществ, представляют собой ядра изотопа 4He. Гелий не накапливается в больших количествах в атмосфере, потому что гравитации Земли недостаточно, чтобы предотвратить его постепенную утечку в космос. Следы 3He на Земле объясняются отрицательным бета-распадом редкого элемента водорода-3 (трития). 4He является наиболее распространенным из стабильных изотопов: соотношение числа атомов 4He к 3He составляет около 700 тыс. к 1 в атмосфере и около 7 млн к 1 в некоторых гелийсодержащих минералах.
Физические свойства гелия
Температура кипения и плавления у этого элемента самые низкие. По этой причине гелий существует в виде газа, за исключением экстремальных условий. Газообразный He в воде растворяется меньше, чем какой-либо другой газ, а скорость диффузии через твердые тела в три раза больше, чем у воздуха. Его показатель преломления ближе всего приближается к 1.
Теплопроводность гелия уступает лишь теплопроводности водорода, а его удельная теплоемкость необычайно высокая. При обычных температурах при расширении он нагревается, а ниже 40 K – охлаждается. Поэтому при Т<40 K гелий можно превратить в жидкость путем расширения.
Элемент является диэлектриком, если не находится в ионизированном состоянии. Как и у других благородных газов, у гелия есть метастабильные энергетические уровни, которые позволяют ему оставаться ионизированным в электрическом разряде, когда напряжение остается ниже потенциала ионизации.
Гелий-4 уникален тем, что обладает двумя жидкими формами. Обычная называется гелий I и существует при температурах от точки кипения 4,21 К (-268,9 °C) до около 2,18 К (-271 °C). Ниже 2,18 K теплопроводность 4He становится в 1000 раз больше, чем у меди. Эта форма называется гелий II, чтобы отличить ее от обычной. Она обладает сверхтекучестью: вязкость настолько низкая, что не может быть измерена. Гелий II растекается в тонкую пленку на поверхности любого вещества, которого касается, и эта пленка течет без трения даже против силы тяжести.
Менее обильный гелий-3 образует три различные жидкие фазы, две из которых сверхтекучи. Сверхтекучесть в 4He была обнаружена советским физиком Петром Леонидовичем Капицей в середине 1930-х годов, и такое же явление в 3He было впервые замечено Дугласом Д. Ошеровым, Дэвидом М. Ли, и Робертом С. Ричардсоном из США в 1972 году.
Жидкая смесь двух изотопов гелия-3 и -4 при температурах ниже 0,8 К (-272.4 °C) разделяется на два слоя – практически чистого 3He и смеси 4He с 6% гелия-3. Растворение 3He в 4He сопровождается охлаждающим эффектом, который используется в конструкции криостатов, в которых температура гелия опускается ниже 0,01 К (-273,14 °C) и поддерживается такой в течение нескольких дней.

Соединения
В нормальных условиях гелий химически инертен. В экстремальных можно создать соединения элемента, которые при нормальных показателях температуры и давления не являются стабильными. Например, гелий может образовывать соединения с йодом, вольфрамом, фтором, фосфором и серой, когда он подвергается действию электрического тлеющего разряда при бомбардировке электронами или в состоянии плазмы. Таким образом, были созданы HeNe, HgHe10, WHe2 и молекулярные ионы Не2+, Не2++, HeH+ и HeD+. Эта техника также позволила получить нейтральные молекулы Не2 и HgHe.
Плазма
Во Вселенной преимущественно распространен ионизированный гелий, свойства которого существенно отличаются от молекулярного. Электроны и протоны его не связаны, и он обладает очень высокой электропроводностью даже в частично ионизированном состоянии. На заряженные частицы сильное воздействие оказывают магнитные и электрические поля. Например, в солнечном ветре ионы гелия вместе с ионизированным водородом взаимодействуют с магнитосферой Земли, вызывая северные сияния.

Открытие месторождений в США
После бурения скважины в 1903 году в Декстере, штат Канзас, был получен негорючий газ. Первоначально не было известно, что в нем содержится гелий. Какой газ был найден, определил геолог штата Эразмус Хаворт, который собрал его образцы и в университете Канзаса с помощью химиков Кэди Гамильтона и Дэвида Макфарланда обнаружил, что тот содержит 72% азота, 15% метана, 1% водорода и 12% не было идентифицировано. Проведя последующие анализы, ученые обнаружили, что 1,84% пробы составляет гелий. Так узнали о том, что данный химический элемент присутствует в огромных количествах в недрах Великих равнин, откуда его можно извлечь из природного газа.
Промышленное производство
Это сделало Соединенные Штаты лидером мирового производства гелия. По предложению сэра Ричарда Трельфалла, ВМС США профинансировали три небольших экспериментальных завода для получения этого вещества во время Первой мировой войны с целью обеспечить заградительные аэростаты легким негорючим подъемным газом. По данной программе были произведены в общей сложности 5700 м3 92-процентного He, хотя до этого были получены лишь менее 100 л газа. Часть этого объема была использована в первом в мире гелиевом дирижабле ВМФ США С-7, который совершил свой первый рейс из Хэмптон-Роудс (штат Вирджиния) в Боллинг-Филд (Вашингтон, округ Колумбия) 7 декабря 1921 года.
Хотя процесс низкотемпературного сжижения газа в то время не был достаточно разработан, чтобы оказаться существенным во время Первой мировой войны, производство продолжалось. Гелий в основном использовался в качестве подъемного газа в летательных аппаратах. Спрос на него вырос во время Второй мировой войны, когда его стали применять при экранированной дуговой сварке. Элемент также имел важное значение в проекте создания атомной бомбы «Манхэттен».

Национальный запас США
В 1925 году правительство Соединенных Штатов создало Национальный запас гелия в Амарилло, штат Техас, с целью обеспечения военных дирижаблей во время войны и коммерческих воздушных кораблей в мирное время. Использование газа после Второй мировой сократилось, но запас был увеличен в 1950-х годах для обеспечения, среди прочего, его поставок в качестве теплоносителя, применяемого в производстве кислородно-водородного ракетного топлива в период космической гонки и холодной войны. Использование гелия в США в 1965 году в восемь раз превысило пиковое потребление военного времени.
После принятия закона о гелии 1960 года Горное бюро подрядило 5 частных предприятий для извлечения элемента из природного газа. Для этой программы был построен 425-км газопровод, соединивший эти заводы с правительственным частично истощенным газовым месторождением неподалеку от Амарилло в Техасе. Гелий-азотная смесь закачивалась в подземное хранилище и оставалась там, пока в ней не возникала необходимость.
К 1995 году был собран запас объемом миллиард кубометров, а задолженность Национального резерва составила 1,4 млрд долларов, что побудило Конгресс США в 1996 г. поэтапно отказаться от него. После принятия в 1996 г. закона о приватизации гелия Министерство природных ресурсов приступило к ликвидации хранилища в 2005 году.

Чистота и объемы производства
Гелий, произведенный до 1945 года, имел чистоту около 98%, остальные 2% приходились на азот, что было достаточным для дирижаблей. В 1945 г. было произведено небольшое количество 99,9-процентного газа для использования в дуговой сварке. К 1949 г. чистота получаемого элемента достигла 99,995%.
На протяжении многих лет Соединенные Штаты производили более 90% мирового объема коммерческого гелия. Начиная с 2004 года, ежегодно его вырабатывалось 140 млн м3, 85% из которых приходится на США, 10% производилось в Алжире, а остальное – в России и Польше. Основными источниками гелия в мире являются газовые месторождения Техаса, Оклахомы и Канзаса.
Процесс получения
Гелий (чистотой 98,2%) выделяют из природного газа путем сжижения других компонентов при низких температурах и при высоких давлениях. Адсорбция других газов охлажденным активированным углем позволяет добиться чистоты 99,995%. Небольшой объем гелия производится при сжижении воздуха в больших масштабах. Из 900 т воздуха можно получить около 3,17 куб. м газа.

Сферы применения
Благородный газ нашел применение в разных областях.
- Гелий, свойства которого позволяют получать сверхнизкие температуры, используется как охлаждающий агент в Большом адронном коллайдере, сверхпроводящих магнитах аппаратов МРТ и спектрометров ядерного магнитного резонанса, спутниковой аппаратуры, а также для сжижения кислорода и водорода в ракетах «Аполлон».
- В качестве инертного газа для сварки алюминия и др. металлов, при производстве оптоволокна и полупроводников.
- Для создания давления в топливных баках ракетных двигателей, особенно тех, которые работают на жидком водороде, т. к. только гелий газообразный сохраняет свое агрегатное состояние, когда водород остается жидким);
- He-Ne газовые лазеры используются для сканирования штрих-кодов на кассах в супермаркетах.
- Гелий-ионный микроскоп позволяет получить лучшие изображения, чем электронный.
- Благодаря высокой проницаемости благородный газ используется для проверки утечек, например, в системах кондиционирования воздуха автомобилей, а также для быстрого наполнения подушек безопасности при столкновении.
- Низкая плотность позволяет наполнять декоративные шары с гелием. Инертный газ заменил взрывоопасный водород в дирижаблях и воздушных шарах. Например, в метеорологии, шары с гелием используются для подъема измерительных приборов.
- В криогенной технике служит теплоносителем, поскольку температура этого химического элемента в жидком состоянии минимально возможная.
- Гелий, свойства которого обеспечивают ему низкую реактивность и растворимость в воде (и крови), в смеси с кислородом нашел применение в дыхательных составах для подводного плавания с аквалангом и проведения кессонных работ.
- Метеориты и горные породы анализируются на содержание данного элемента для определения их возраста.
Гелий: свойства элемента
Основные физические свойства He следующие:
- Атомный номер: 2.
- Относительная масса атома гелия: 4,0026.
- Точка плавления: нет.
- Точка кипения: -268,9 °C.
- Плотность (1 атм, 0 °C): 0,1785 г/п.
- Состояния окисления: 0.
Источник
химический элемент, атомный номер 2, атомная масса 4,0026, относится к инертным газам, без цвета и запаха. Объемное содержание гелия в воздухе 0,00052%. Гелий значительно легче воздуха, плотность 0,1785 кг/м3 при нулевой температуре и нормальном давлении. Температура кипения -268,9°С. Потенциал ионизации 25,4 В. Бесцветный, неядовитый, негорючий и невзрывоопасный газ, хорошо диффундирует через твердые тела. Химическая формула – He.

История открытия гелия
Впервые гелий был обнаружен во время солнечного затмения 1868 г. астрономы впервые применили спектроскопию для исследования атмосферы Солнца.
24 октября 1868 г. Французская академия наук получила два сообщения – от Пьера Жюль Сезара Жансена (Pierre Jules Cesar Janssen) из Индии и от Джозефа Нормана Локьера (Joseph Norman Lockyer) из Лондона – об открытии ими в спектре солнечной короны новой ярко-желтой линии, которой впоследствии был присвоен символ D3. Совпадение двух независимых сообщений из разных концов мира свидетельствовало о возможности методами спектроскопии проникнуть в тайны солнечной атмосферы и других далеких звезд.
Вопрос о том, какому веществу отвечает линия D3, долго еще оставался открытым. Было лишь установлено, что в спектрах элементов, известных на нашей планете, пока не обнаружено спектральной линии, подобной ярко-желтой линии D3. Локьер ошибочно считал, что раскаленный газ, излучение которого дает таинственную линию D3, является модификацией водорода, не встречающейся на Земле.
В августе 1871 г. Кельвин заявил, что линия D3 до сих пор не идентифицирована с каким-либо земным элементом. Возможно, что она принадлежит новому веществу, которому Локьер и Жансен предложили дать название гелий (от греческого слова гелиос – солнце).
В 1895 г. Сэр Уильям Рамзай (Sir William Ramsay) изучал газ, выделенный им из минерала клевеита, и в гейслеровой трубке неожиданно обнаружил яркую желтую линию. Выдающийся спектроскопист того времени Уильям Крукс (William Crookes) определил длину волны новой линии (5874,9 А) и установил, что это линия D3, на этом основании Рамзай сообщил (23 марта 1895 г.) об открытии им гелия на Земле.
Такова история открытия важнейшего представителя группы инертных газов, который сначала был обнаружен в солнечной атмосфере, а затем (через 27 лет) – на Земле.
Вскоре гелий был обнаружен в других минералах и горных породах, содержащих уран. Наличие гелия в земной коре позволило сделать вывод о его содержании в атмосфере, хотя многие ученые утверждали, что этот легкий газ, выделяющийся из земной коры, полностью уносится из атмосферы в космическое пространство. Вскоре Генрих Кайзер, а затем Зигберт Фридлендер (1896 г.), а также Эдвард Бэли в результате анализа первой выпаренной фракции жидкого воздуха доказали его присутствие в атмосфере.
Способы получения гелия
Гелий получают из гелийсодержащих природных газов, минералов и воздуха. Об этом мы писали в статье о производстве гелия, поэтому здесь не будем повторять написанное.
Применение гелия
В промышленности гелий применяют в меньших масштабах, чем газ аргон. Чаще всего его используют:
- хладагент – охлаждение сверхпроводящих магнитов в медицинских сканерах МРТ;
- металлургия – выплавка чистых металлов;
- подводно-спасательное дело – в составе дыхательных смесей;
- сварочное производство – защитный газ;
- в индустрии развлечений – заполнение шариков.
Применение гелия в сварке
В связи с тем, что He примерно в 10 раз легче Ar, что понижает эффективность защиту сварочной ванны при сварке в нижнем положении, но способствует лучшей защите при сварке в потолочном положении, поэтому расход гелия при сварке увеличивается в 1,5-3 раза.
Применяют его в основном при сварке неплавящимся электродом химически чистых и активных материалов и сплавов, а также сплавов на основе алюминия и магния.

Гелий становится предпочтительнее аргона при необходимости дополнительной защиты швов при сварке в потолочном положении. Особенно при сварке титановых сплавов и других химически активных металлов, поглощающих азот и кислород не только в расплавленном состоянии, но и в твердом при нагреве выше определенной температуры.
Однако не только защитные свойства Ar и He различны. Различными являются и характеристики дуги в этих газах. Так, при одинаковой силе тока напряжение дуги в гелии значительно выше, чем дуги в аргоне. Такая дуга имеет большую проплавляющую способность и менее концентрирована (создает иную форму проплавления, более равномерную, в то время как дуга в аргоне при сварке, например, титановых сплавов вольфрамовым электродом дает большое проплавление в центре и значительно меньшее по краям ванны). Перепад напряжения в столбе дуги в гелии больше, чем в аргоне, поэтому изменение длины дуги заметнее сказывается на напряжении и общей ее теплоэффективности. Для более развернутой информации обязательно прочитайте статью о сварочной дуге в инертных газах.

Форма шва и проплавление для различных защитных газов
В зависимости от применения того или иного газа меняется и поверхностное натяжение на границе металл-газовая фаза. Так, для хромоникелевых сталей аустенитного класса поверхностное натяжение жидкого металла при сварке в He заметно меньше, чем в Ar. Это сказывается и на формировании поверхности швов. Более плавные переходы от шва к основному металлу, при сварке в гелии, имеют место и для других металлов, в частности титановых сплавов и в ряде случаев оказывают влияние на некоторые характеристики работоспособности сварных соединений.
Чаще всего He используют для образования инертных газовых смесей c Ar. Обладая большей плотностью, чем гелий, такие смеси лучше защищают металл сварочной ванны от воздуха и увеличивают производительность сварки в целом. В смеси в полной мере реализуются преимущества обоих газов:
- аргон – обеспечивает стабильность горения дуги;
- гелий – обеспечивает высокую степень проплавления.
Опасность и вред гелия
Гелий не относится к ядовитым и токсичным газам, поэтому в малых количествах он не является опасным. Он может оказать действие как удушающий газ (асфиксант) только в том случае, если в результате утечки уровень кислорода окажется ниже допустимой концентрации. Но утечку гелия очень легко выявить т.к. за счет сжимания голосовых связок у человека меняется голос. Мы все знаем данный комический и мультяшный эффект, когда при вдыхании гелия из шарика голос становится более высоким.
Гелий является опасным, только в случае снижения уровня кислорода в окружающей среде ниже допустимой концентрации.
Хранение и траспортировка гелия
Транспортируют и хранят гелий в газообразном состоянии в стальных баллонах при давлении 15 МПа или в сжиженном состоянии при давлении менее 0,2 МПа.
Баллоны с гелием окрашены в коричневый цвет с надписью белыми буквами «ГЕЛИЙ». Баллоны должны соответствовать требованиям ГОСТ 949.

Методы определения доли примесей и условий поставки регламентируются ГОСТ 20461.
Характеристики гелия
Характеристики He указаны в таблицах ниже:
Коэффициенты перевода объема и массы He при Т=15°С и Р=0,1 МПа
Масса, кг | Объем | |
|---|---|---|
Газ, м3 | Жидкость, л | |
0,167 | 1 | 1,336 |
0,125 | 0,749 | 1 |
1 | 5,988 | 8,000 |
Коэффициенты перевода объема и массы He при Т=0°С и Р=0,1 МПа
Масса, кг | Объем | |
|---|---|---|
Газ, м3 | Жидкость, л | |
0,178 | 1 | 1,425 |
0,125 | 0,702 | 1 |
1 | 5,618 | 8,000 |
Гелий в баллоне
Наименование | Объем баллона, л | Масса газа в баллоне, кг | Объем газа (м3) при Т=15°С, Р=0,1 МПа |
|---|---|---|---|
He | 40 | 1,002 | 6,0 |
- Сколько литров гелия в баллоне?
Ответ: 40 литров - Сколько гелия в баллоне 40л?
Ответ: 6,5 м3 или 10,85 кг - Сколько весит баллон с гелием 40 литров
Ответ:
58,5 кг – масса пустого баллона из углеродистой стали согласно ГОСТ 949;
1,002 – кг масса гелия в баллоне;
Итого: 58,5 + 1,002 = 59,502 кг вес баллона с аргоном.
Давление гелия в баллоне при различной температуре окружающей среды
Температура окружающей среды | Давление в баллоне, МПа |
|---|---|
-40 | 12,2 |
-30 | 12,7 |
-20 | 13,2 |
-10 | 13,7 |
14,3 | |
+10 | 14,7 |
+20 | 15,3 |
+30 | 15,8 |
Источник
