Какое свойство отличает принципиально кристалл от аморфных тел

В зависимости от внутреннего строения твердые тела бывают либо кристаллическими, либо аморфными. Молекулы и атомы кристаллов расположены в определенной, повторяющейся последовательности на больших расстояниях, сохраняя так называемый дальний порядок. Атомы и молекулы в аморфных телах размещены неупорядоченно, для них характерен ближний порядок со строением аналогичным жидкому состоянию вещества. Рассмотрим основные отличия кристаллических тел от аморфных, которые проявляются в их физических свойствах.

Твердые тела
Все твердые тела обладают следующими общими свойствами:
- Способностью долгое время сохранять форму и объем (геометрические размеры);
- Наличием упругих сил, которые возникают при небольших изменениях объема от внешнего воздействия (сжатия, растяжения или сдвига).
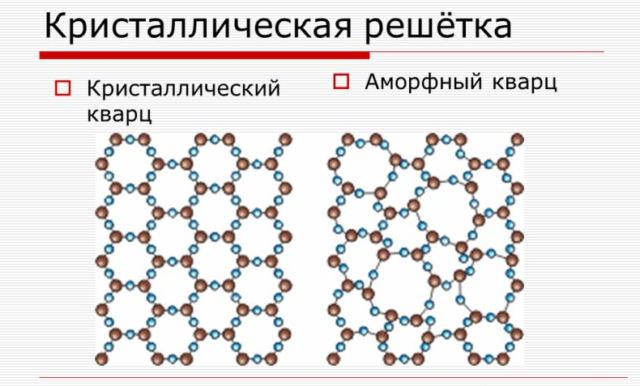
Рис. 1. Примеры решеток кристаллических и аморфных тел – кварц аморфный и кристаллический.
Современные ученые исследуют пространственное расположение атомов и молекул в твердых телах с помощью электронных микроскопов, которые позволяют получить изображение объекта с сильным увеличением (до 106 раз). Первый электронный микроскоп был изобретен в 30-х годах прошлого века. В 2018 г. с помощью последних версий этого прибора было получено разрешение 0,39 ангстрем. Напомним, что 1 ангстрем равен 10-8 см. В большинстве кристаллов это соответствует шагу атомной решетки.
Аморфные тела
Смола, воск, графит, изделия из стекла и янтаря, пластмассы — все это примеры аморфных тел (от греч.слова Amorphous — бесформенный, некристаллический).
Отсутствие дальнего порядка в расположении частиц вещества у аморфных тел приводит к тому, что их физические свойства одинаковы во всех направлениях. Такие тела называют изотропными (слово “изотропный” составлено из двух греческих слов: isos — ровный, tropos — направление). Изотропность физических свойств аморфных тел является следствием хаотичного расположения составляющих их молекул и атомов.
Характерной особенностью аморфных тел является отсутствие определенной температуры плавления, то есть отсутствует четкий переход от твердого состояния к жидкому: при нагревании аморфное тело становится только более текучим.
Кристаллические тела
Твердые тела, в которых молекулы и атомы расположены упорядоченно и образуют периодически повторяющуюся структуру, называются кристаллами. Физические свойства кристаллов (упругие, механические, тепловые, электрические, магнитные, оптические) в разных направлениях неодинаковы. Такое свойство называется анизотропностью. Анизотропия кристаллов объясняется тем, что при упорядоченном расположении частиц расстояния между ними и силы взаимодействия (притяжения и отталкивания) оказываются неодинаковыми в разных направлениях.
Различают кристаллические тела двух видов: монокристаллы и поликристаллы. Главным признаком монокристаллов является повторяющееся внутреннее строение (структура) во всем объеме тела.
Поликристалл — это совокупность (набор) сросшихся друг с другом, хаотически ориентированных, небольших кристаллов. Каждый маленький кристалл обладает свойствами анизотропии, но их совокупность — поликристалл — изотропен.

Рис. 2. Монокристаллы и поликристаллы.
Часто встречаются кристаллические тела одинаковые по своему химическому составу, но обладающие очень разные физические свойства. Самый известный пример — это углерод, имеющий две модификации: графит и алмаз. Разное строение кристаллических решеток является причиной того, что алмаз имеет рекордные показатели твердости, а графит из-за его мягкости используется в качестве грифелей для карандашей.

Рис. 3. Графит и алмаз.
Что мы узнали?
Итак, мы узнали, что кристаллические и аморфные тела кроме общих признаков, которые относят их к твердым телам, имеют совершенно разные физические свойства. Аморфные тела обладают изотропными свойствами, а для кристаллов характерна анизотропия физических параметров. Кристаллические тела делятся на монокристаллы и поликристаллы.
Тест по теме
Оценка доклада
Средняя оценка: 4. Всего получено оценок: 265.
Источник
Существует несколько агрегатных состояний, в которых находятся все тела и вещества. Это:
- газ;
- жидкость;
- плазма;
- твердое.
Если рассматривать общую совокупность планеты и космоса, то большая часть веществ и тел все же находится в состоянии газа и плазмы. Однако на самой Земле существенно и содержание твердых частиц. Вот о них мы и поговорим, выяснив, чем являются кристаллические и аморфные твердые тела.
Кристаллические и аморфные тела: общее понятие
Все твердые вещества, тела, предметы условно подразделяются на:
- кристаллические;
- аморфные.
Разница между ними огромная, ведь в основе подразделения лежат признаки строения и проявляемых свойств. Если говорить кратко, то твердыми кристаллическими именуются те вещества и тела, которые имеют определенный тип пространственной кристаллической решетки, то есть обладают способностью изменяться в определенном направлении, но не во всех (анизотропия).
Если же характеризовать аморфные соединения, то первый их признак – способность менять физические характеристики по всем направлениям одновременно. Это называется изотропией.
Строение, свойства кристаллических и аморфных тел совершенно различны. Если первые имеют четко ограниченную структуру, состоящую из упорядоченно расположенных частиц в пространстве, то у вторых всякий порядок отсутствует.

Свойства твердых тел
Кристаллические и аморфные тела тем не менее относятся к единой группе твердых, а значит, обладают всеми характеристиками данного агрегатного состояния. То есть общими свойствами для них будут следующие:
- Механические – упругость, твердость, способность к деформации.
- Тепловые – температуры кипения и плавления, коэффициент теплового расширения.
- Электрические и магнитные – проводимость тепловая и электрическая.
Таким образом, рассматриваемые нами состояния обладают всеми данными характеристиками. Только проявляться у аморфных тел они будут несколько иначе, нежели у кристаллических.
Важными свойствами для промышленных целей являются механические и электрические. Способность восстанавливаться после деформации или, напротив, крошиться и измельчаться – важная особенность. Также большую роль играет тот факт, может вещество проводить электрический ток либо не способно к этому.

Строение кристаллов
Если описывать строение кристаллических и аморфных тел, то в первую очередь следует указать тип частиц, которые их слагают. В случае кристаллов это могут быть ионы, атомы, атом-ионы (в металлах), молекулы (редко).
Вообще данные структуры характеризуются наличием строго упорядоченной пространственной решетки, которая формируется в результате расположения образующих вещество частиц. Если представить строение кристалла образно, то получится примерно такая картина: атомы (или другие частицы) располагаются друг от друга на определенных расстояниях так, чтобы в результате получилась идеальная элементарная ячейка будущей кристаллической решетки. Затем данная ячейка многократно повторяется, и так складывается общая структура.
Главной особенностью является то, что физические свойства в подобных структурах изменяются в параллелях, но не во всех направлениях. Называется подобное явление анизотропией. То есть если воздействовать на одну часть кристалла, то вторая сторона может не реагировать на это. Так, можно измельчить половину кусочка поваренной соли, однако вторая останется целой.
Типы кристаллов
Принято обозначать два варианта кристаллов. Первый – это монокристаллические структуры, то есть когда сама решетка 1. Кристаллические и аморфные тела в этом случае совсем различны по свойствам. Ведь для монокристалла характерна анизотропия в чистом виде. Он представляет собой самую маленькую структуру, элементарную.
Если же монокристаллы повторяются многократно и соединяются в одно целое, тогда речь идет о поликристалле. Тогда речь об анизотропии не идет, так как ориентация элементарных ячеек нарушает общую упорядоченную структуру. В этом отношении поликристаллы и аморфные тела близки друг другу по проявляемым физическим свойствам.

Металлы и их сплавы
Кристаллические и аморфные тела очень близки друг другу. В этом легко убедиться, взяв в качестве примера металлы и их сплавы. Сами по себе они при обычных условиях твердые вещества. Однако при определенной температуре начинают плавиться и, пока не произойдет полная кристаллизация, будут оставаться в состоянии тянущейся, густой, вязкой массы. А это уже и есть аморфное состояние тела.
Поэтому, строго говоря, практически каждое кристаллическое вещество может при определенных условиях стать аморфным. Так же, как и последнее при кристаллизации становится твердым веществом с упорядоченной пространственной структурой.
Металлы могут иметь разные типы пространственных структур, самыми известными и изученными из которых являются следующие:
- Простая кубическая.
- Гранецентрированная.
- Объемоцентрированная.
В основе структуры кристалла может лежать призма или пирамида, а ее главная часть представлена:
- треугольником;
- параллелограммом;
- квадратом;
- шестиугольником.
Идеальными свойствами изотропии обладает вещество, имеющее простую правильную кубическую решетку.

Понятие об аморфности
Кристаллические и аморфные тела внешне различить достаточно просто. Ведь последние часто можно перепутать с вязкими жидкостями. В основе структуры аморфного вещества также лежат ионы, атомы, молекулы. Однако они не образуют упорядоченной строгой структуры, а потому и свойства их изменяются во всех направлениях. То есть они изотропны.
Частицы располагаются хаотично, беспорядочно. Лишь иногда они могут образовывать небольшие локусы, что все равно не влияет на общие проявляемые свойства.
Свойства подобных тел
Они идентичны таковым у кристаллов. Различия лишь в показателях для каждого конкретного тела. Так, например, можно выделить такие характеристические параметры аморфных тел:
- упругость;
- плотность;
- вязкость;
- тягучесть;
- проводимость и полупроводимость.
Часто можно встретить граничные состояния соединений. Кристаллические и аморфные тела могут переходить в состояние полуаморфности.
Также интересна та черта рассматриваемого состояния, которая проявляется при резком внешнем воздействии. Так, если аморфное тело подвергнуть резкому удару или деформации, то оно способно повести себя как поликристалл и расколоться на мелкие кусочки. Однако если дать этим частям время, то вскоре они снова соединятся вместе и перейдут в вязкое текучее состояние.

У данного состояния соединений нет определенной температуры, при которой происходит фазовый переход. Этот процесс сильно растянут, иногда даже на десятки лет (например, разложение полиэтилена низкого давления).
Примеры аморфных веществ
Можно привести много примеров подобных веществ. Обозначим несколько самых наглядных и часто встречаемых.
- Шоколад – типичное аморфное вещество.
- Смолы, в том числе фенолформальдегидные, все пластики.
- Янтарь.
- Стекло любого состава.
- Битум.
- Гудрон.
- Воск и другие.
Аморфное тело образуется в результате очень медленной кристаллизации, то есть повышения вязкости раствора при понижении значения температуры. Часто сложно назвать подобные вещества твердыми, их относят скорее к вязким густым жидкостям.
Особое состояние имеют те соединения, которые при затвердевании вообще не кристаллизуются. Их называют стеклами, а состояние – стеклообразным.
Стеклообразные вещества
Свойства кристаллических и аморфных тел схожи, как мы выяснили, вследствие общего происхождения и единой внутренней природы. Но иногда от них отдельно рассматривают особое состояние веществ, именуемое стеклообразным. Это гомогенный минеральный раствор, который кристаллизуется и затвердевает без формирования пространственных решеток. То есть остается изотропным по изменению свойств всегда.
Так, например, обычное оконное стекло не имеет точного значения температуры плавления. Оно просто при повышении данного показателя медленно плавится, размягчается и переходит в жидкое состояние. Если же воздействие прекратить, то пойдет обратный процесс и начнется затвердевание, но без кристаллизации.
Такие вещества очень ценятся, стекло сегодня – один из самых распространенных и востребованных строительных материалов во всем мире.
Источник
КРИСТАЛЛОГРАФИЯ
СИММЕТРИЯ
Лекция 1
Лекция 1
ОБЩИЕ СВЕДЕНИЯ О СТРОЕНИИ И СВОЙСТВАХ КРИСТАЛЛИЧЕСКИХ ТЕЛ
Содержание
1.1. Кристаллография как наука.
1.2. Виды твёрдых тел.
1.3. Отличительные особенности кристаллических и аморфных тел.
1.4. Особые свойства кристаллов.
1.5. Виды связей в кристаллах.
1.6. Силы взаимодействия частиц.
1.7. Кристаллическая решётка. Элементарная ячейка.
1.8. Индексы Миллера.
1.9. Рентгеноструктурный анализ.
КРИСТАЛЛОГРАФИЯ КАК НАУКА
Кристаллография– наука об атомно-молекулярном строении, симметрии, физических свойствах, образовании и росте кристаллов. Как самостоятельная наука существует с середины XVIII века. Сначала она развивалась как геометрическая кристаллография в тесной связи с минералогией, которая устанавливала закономерности огранки природных кристалликов, имеющих естественную форму правильных многогранников (Р. Гаюи). Затем появилась теория симметрии внешней формы кристаллов (А.В. Гадолини).
Геометрическая кристаллографияопределяет совокупность методов описания кристаллов и закономерности их огранки. В этой теории возникла гипотеза об упорядоченном трёхмерно-периодическом расположении частиц в кристалле с образованием кристаллической решётки (О. Браве, Е.С. Фёдоров, А. Шёнфлис).
Экспериментальными исследованиями дифракции рентгеновских лучей на кристаллах было подтверждено решёточное строение кристаллов и положено начало структурной кристаллографии(М. Лауэ). В качестве основных структурная кристаллографияиспользует метод рентгеноструктурного анализа, электроно- и нейтронографии, а также методы оптической и электронной спектроскопии. В результате всех исследований к настоящему времени определена структура более 105химических веществ.
Предметом кристаллохимии является изучение законов взаимного расположения атомов и молекул в кристаллах, их химических связей и плотнейших упаковок, а также явлений изо- и полиморфизма.
Кристаллооптика занимается вопросами прохождения света через прозрачные анизотропные кристаллы, сформулировала многие закономерности взаимного влияния симметрии и анизотропии физических свойств.
Кристаллофизикарассматривает в едином русле форму, симметрию и физические свойства кристаллов; занимается вопросами исследования механических, оптических, электрических, магнитных и других свойств кристаллов. В этой части кристаллография смыкается с физикой твёрдого тела.
В кристаллографии изучаются разнообразные дефекты построения идеальной кристаллической решётки: точечные, линейные (дислокации), поверхностные и объёмные. Многие из них появляются в результате роста кристалла или при внешнем воздействии на кристалл напряжением, облучением и т. д.
Для современной кристаллографиихарактерно дальнейшее изучение атомной и дефектной структур кристаллов, процессов их роста, поиск новых свойств и материалов. Основная задача кристаллографии как науки на сегодняшний день – получение новых материалов с важными физическими свойствами. К решению этой задачи необходимо подходить комплексно, рассматривая атомную структуру, анизотропию свойств, взаимодействие кристаллов с окружающей средой в их взаимодействии.
В современной кристаллографии исследуются строение и свойства различных агрегатов из микрокристалликов (поликристаллов, текстур, керамик), а также вещества с атомной упорядоченностью, близкой к кристаллической (жидкокристаллические вещества, полимерные и композиционные материалы).
Симметричные и структурные закономерности, изучаемые в кристаллографии, используются при рассмотрении общих закономерностей строения и свойств аморфных тел и жидкостей, полимеров, квазикристаллов, макромолекул, надмолекулярных аморфно-кристаллических, а также биологических структур. Поэтому современная кристаллография представляет собой обобщённую кристаллографию,математический аппарат которой основан на дискретной геометрии, теории групп, тензорном исчислении и теории преобразований Фурье.
ВИДЫ ТВЕРДЫХ ТЕЛ
Твёрдое телосостоит из большого числа частиц. Этими частицами могут быть атомы, атомные остатки, ионы, молекулы, макромолекулы. Концентрация частиц в твёрдых телах высока: (1026 – 1029) м-3 . Расстояния между частицами составляют несколько нанометров.
Структуру твёрдых телисследуют дифракционными методами, основанными на дифракции рентгеновских лучей, электронов, нейтронов, используя при этом стандартные установки: рентгеновский дифрактометр, электронный микроскоп, ионный проектор и др. Физика твёрдого тела и кристаллография имеют прямое отношение к нанотехнологиям (рис. 1.1). Нанотехнологии разрабатываются на эффектах, возникающих на уровне атомных размеров.
Свойства твёрдых телобъясняются многими факторами и зависят от химического состава вещества, типа частиц, их внутреннего расположения, типа химической связи между частицами.
Свойства кристаллов широко применяются в оптике, акустике, радиоэлектронике, металловедении, металлургии, химии, медицине. Твёрдые тела встречаются в природе в виде кристаллических и аморфных тел, а также полимеров. В физике к твёрдым телам относят только кристаллические тела.
Рис. 1.1. Электронная микрофотография структуры алмаза вдоль направления [110]
Кристаллы– твёрдые тела, обладающие трёхмерной периодической атомной структурой и имеющие при равновесных условиях образования естественную форму правильных симметричных многогранников. Атомная структура кристалла описывается как совокупность повторяющихся в пространстве одинаковых элементарных ячеек, имеющих форму параллелепипеда. Кристаллы, выросшие в равновесных условиях, имеют форму правильных многогранников той или иной симметрии. Грани кристалла плоские, а рёбра между гранями – прямолинейные. Выросшие в неравновесных условиях кристаллы не имеют правильной огранки, но сохраняют кристаллическую структуру и все присущие данной структуре свойства. Неравновесные условия кристаллизации приводят к отклонениям только формы от правильного многогранника – к округлости граней и рёбер. Примерами кристаллических тел являются горный хрусталь, поваренная соль, драгоценные камни.
В кристаллахчастицы расположены правильными, симметричными, периодически повторяющимися рядами, сетками, решётками. Кристаллы вырастают в форме многогранников (рис. 1.2). Способность кристалла приобретать конкретную форму – это проявление его физических свойств, определяющихся его структурой, симметрией и химическими связями между его частицами.
Рис. 1.2. Внешний вид кристаллических тел
Кристаллические тела встречаются в природе в виде моно- и поликристаллов. Монокристаллы(большие одиночные кристаллы) получают при создании специальных условий кристаллизации (рис. 1.3).
Рис. 1.3.Монокристаллы кремния
Монокристалл состоит из блоков мозаики,размер которых в монокристалле составляет (10–6–10–8) м. Так как кристаллическая решетка в соприкасающихся блоках имеет различную ориентацию, то возникает переходный слой, в котором решетка постепенно переходит от одной ориентации, свойственной одному блоку, к другой ориентации, свойственной другому блоку. Поэтому решетка в этом слое искажена по сравнению с решеткой идеального кристалла. Поликристаллсостоит из беспорядочно ориентированных кристалликов (кристаллитов) малых размеров (рис. 1.2, справа). Размер кристаллитов порядка 10–4 м.
Аморфные тела– вещества, в атомном строении которых нет порядка: частицы расположены беспорядочно, независимо друг от друга (воск, пластилин). Отличительной особенностью аморфных тел является изотропностьвсех физических и механических свойств.
Полимерысостоят из многочисленных звеньев одинакового химического состава – макромолекул. Например, полимерным материалом является политетрафторэтилен, химическая формула которого (СF2)n, где n = 13.
К особым видам твёрдых тел относятся жидкокристаллические тела,нашедшие широкое применение в телевидении и сотовой связи, и закристаллизованные жидкости,которые обладают особыми свойствами.
ОТЛИЧИТЕЛЬНЫЕ ОСОБЕННОСТИ КРИСТАЛЛИЧЕСКИХ И АМОРФНЫХ ТЕЛ
Рассмотрим некоторые свойства твёрдых тел, которые характеризуют их как кристаллические или аморфные тела.
1. Кристаллыимеютупорядоченное расположение частиц на сколь угоднобольших расстояниях. Частицы расположены в узлах кристаллической решётки.Аморфные тела имеют упорядоченноерасположение частиц на небольших расстояниях (в так называемых группах) (рис.1. 4). Расположение частиц в веществе характеризуется наличием дальнего и ближнего порядков.
Рис. 1.4. Вещество H2O в двух агрегатных состояниях: воды (1) и льда (2)
2. Дальний порядок– упорядоченное расположение частиц на сколь угодно больших расстояниях от рассматриваемой частицы.
– характеризуется коэффициентом α.
Ближний порядок– упорядоченное расположение частиц на малых расстояниях от рассматриваемой частицы.
– характеризуется коэффициентом β.
| Агрегатное состояние вещества | коэффициент дальнего порядка α | коэффициент ближнего порядка β |
| кристаллические тела | 1 | 1 |
| аморфные тела | < 1 | > 0 |
| жидкости | 0 | 1 |
| газы | 0 | 0 |
3. Кристаллические и аморфные тела различаются ходом температурной зависимости температуры плавления.
4. Для кристаллов характерно наличие анизотропии. Анизотропия– зависимость свойств вещества от направления в кристалле. Например, слюда по-разному разламывается в различных направлениях. Анизотропией диэлектрической проницаемости объясняется существование в кристаллах турмалина двойного лучепреломления (рис. 1.5).
Рис. 1.5. Двойное лучепреломление в кристалле турмалина
Обладают анизотропией очень многие физические и механические свойства кристаллических тел, например: теплопроводность, электропроводность, скорость света, двойное лучепреломление. Аморфные тела изотропны,у них свойства одинаковы по всем направлениям в веществе. Примером является пластилин, который легко сжимается в любых направлениях.
Источник
