Какое свойство отличает от аморфного тела
Рассмотрим твердые тела подробнее. По упорядоченности мельчайших частиц, из которых состоят твердые тела, их можно разделить на аморфные и кристаллические.
Чем отличаются кристаллические и аморфные тела
У кристаллических тел есть строго упорядоченное положение мельчайших частиц. Эти частички образуют правильную кристаллическую решетку (рис. 1).
Примечание: Атомы кристаллических тел располагаются в узлах кристаллической решетки. Связи между атомами обозначены линиями. Эти линии у различных кристаллических тел образуют разные пространственные фигуры.
Рис.1. Кристаллические тела имеют более упорядоченную структуру в твердом состоянии, чем аморфные тела
Аморфные тела не обладают строгой упорядоченностью мельчайших частиц — молекул, из которых они состоят. У аморфных тел порядок есть, но он не так выражен, как у кристаллических тел. Аморфное тело по своему строению больше похоже на очень вязкую жидкость, чем на твердое тело. Поэтому, аморфные тела обладают текучестью.
Основные отличия кристаллических и аморфных тел приведены на рисунке 2.
Рис. 2. Сравниваем свойства кристаллических и аморфных тел
Примечания:
- Благодаря текучести, спустя много лет после изготовления, верхняя часть установленного в раму оконного стекла, становится немного тоньше, чем его нижняя часть.
- Канифоль со временем может принимать форму сосуда, в который ее поместили.
Переход:
- из жидкого в твердое состояние – кристаллизация;
- из твердого в жидкое состояние – плавление;
Плавление аморфных тел
Аморфные тела конкретной температуры плавления не имеют. Строение аморфных тел больше похоже на очень вязкую жидкость, чем на твердое кристаллическое тело. Во время нагревания они будут становиться более текучими, все больше проявляя свойство жидкости. При этом, хрупкость, присущая твердому состоянию, будет исчезать. Одновременно с плавлением, температура аморфных тел будет повышаться.
Важно! Одновременно с плавлением, температура аморфных тел будет непрерывно повышаться. Потому, что такие тела не имеют конкретной температуры плавления.
Примеры аморфных тел
- канифоль (смола хвойных деревьев);
- стекло;
- эбонит;
- сургуч;
- различные пластмассы;
Примечание: Эбонит («Эбенос» др.-греч. — чёрное дерево) – это вулканизированный каучук с добавлением большого количество серы, до 50 % от массы каучука. Цвет эбонита обычно тёмно-бурый или чёрный. Этот материал не проводит электрических ток – то есть, является хорошим изолятором.
Плавление кристаллических тел
Чтобы кристаллическое тело начало плавиться, его нужно нагреть до определенной температуры. Одни кристаллические тела будут плавиться при низкой температуре, а другие – при высокой. То есть, у каждого вещества своя температура плавления. Ее можно найти в справочнике физики. При этом, пока вещество не расплавится, его температура изменяться не будет.
Важно! Кристаллические тела имеют конкретную температуру плавления. Пока кристаллическое вещество полностью не расплавится, его температура не изменится!
Примечания:
- Кристаллические вещества плавятся при той же температуре, при которой они будут превращаться в твердое тело (кристаллизоваться).
- Чтобы жидкое вещество начало кристаллизоваться, оно сначала должно остыть до определенной температуры.
- Температура плавления и температура кристаллизации – это одна и та же температура.
Примеры кристаллических тел
- лед;
- свинец;
- алюминий;
- ртуть;
- железо;
- золото;
- серебро;
Как на графике выглядит процесс плавления кристаллического тела
Рассмотрим переход из твердого состояния в жидкое — плавление и, обратно — кристаллизацию, на примере льда.
Возьмем лед при начальной температуре «-40» градусов по Цельсию (рис. 3) и поместим его в кастрюльку. Поставим эту кастрюльку на газовую плиту и начнем нагревать лед.
Процесс нагревания льда изображается наклонной линией синего цвета. Потому, что время идет, а температура льда повышается.
Во время нагревания льда от отрицательной температуры до нуля градусов, в емкости будет содержаться только твердый лед.
Рис.3. Процесс плавления – это горизонтальная линия на температурном графике
Как только будет достигнута температура плавления льда – «0» градусов по Цельсию, лед начнет превращаться в жидкость. В кастрюльке начнет понемногу появляться вода. То есть, будет присутствовать и лед, и вода одновременно. Постепенно воды становится все больше, а льда – все меньше.
Мы продолжаем подавать тепловую энергию. Но температура льда во время плавления не меняется до тех пор, пока весь лед не расплавится и не превратится в жидкость.
Поэтому на графике температуры плавление кристаллических тел изображается горизонтальной линией. На рисунке 3 эта линия выделена красным цветом.
Примечания:
- Чтобы тело расплавить, ему нужно передать тепловую энергию. Значит, при плавлении, тепловая энергия поглощается телом.
- При плавлении кристаллических тел, вся полученная тепловая энергия тратится на разрушение кристаллической решетки. Поэтому кристаллические тела имеют конкретную температуру плавления. Она не будет повышаться до тех пор, пока все кристаллическое тело полностью не расплавится.
Когда лед полностью расплавится, в кастрюльке будет присутствовать только жидкая вода. На рисунке 5 это — крайняя правая точка на горизонтальной красной линии.
Если продолжать подводить тепловую энергию, температура воды начнет повышаться. Идет процесс нагревания воды. На графике процесс нагревания – это еще одна наклонная прямая линия, она располагается справа от красной линии плавления.
Как на графике выглядит процесс кристаллизации для кристаллического тела
Давайте теперь прекратим нагревание воды, вынесем кастрюльку на мороз и, оставим ее там на какое-то время. Вода начнет охлаждаться, ее температура будет понижаться. На рисунке 4 это отражено убывающей до нуля прямой наклонной синей линией.
Рис. 4. Процесс кристаллизации – это горизонтальная линия на температурном графике
Когда вода охладится до нуля градусов, начнется процесс превращения жидкости в твердое тело – лед. Потому, что ноль градусов Цельсия – это температура не только плавления, но и кристаллизации льда. Вначале начнут появляться маленькие льдинки. Этому соответствует левая часть красной горизонтальной линии на графике 4.
Примечание: Если в воде присутствуют пылинки, или другие мелкие примеси, то кристаллизация проходит быстрее. Такие мелкие примеси называют центрами кристаллизации.
Постепенно, количество льда увеличивается, а воды становится все меньше. При этом, температура воды и льда в кастрюльке продолжает оставаться равной нулю градусов по Цельсию.
Когда вся вода в кастрюльке превращается в лед – этому соответствует крайняя правая точка на красной линии на графике.
Только после этого температура льда начинает понижаться от нуля в отрицательную область температур. На рисунке это описано наклонной синей линией, примыкающей справа к горизонтальной красной линии.
Примечание: Чтобы тело перешло из жидкого состояния в твердое (кристаллизовалось), оно должно избавиться от избытка тепловой энергии. Значит, при кристаллизации, тело отдает энергию окружающим телам. Физики скажут так: «Тело выделяет тепловую энергию во внешнюю среду».
Выводы
- Все тела в твердом состоянии по их строению можно разделить на аморфные и кристаллические.
- Переход из твердого в жидкое состояние – это плавление, а из жидкого в твердое состояние – кристаллизация;
- Аморфные тела конкретной температуры плавления не имеют. Их строение больше похоже на очень вязкую жидкость, чем на твердое кристаллическое тело. Одновременно с плавлением, температура аморфных тел будет повышаться.
- Кристаллическое тело плавится и кристаллизуются при одной и той же температуре. Эту температуру называют температурой плавления (кристаллизации). Т. е. пока происходят процессы плавления и кристаллизации, температура не меняется.
- Во время плавления тело получает тепловую энергию (количество теплоты), а во время кристаллизации тело отдает тепловую энергию в окружающее пространство.
- Сколько теплоты тело получило во время плавления, столько же оно отдаст в окружающую среду во время кристаллизации. Потому, что выполняется закон сохранения энергии (тепловой).
- Чтобы твердое тело превратить в жидкость, ему нужно сообщить (передать) тепловую энергию.
- Чтобы жидкое тело превратить в твердое, нужно избавить его от излишка тепловой энергии.
- Перед тем, как расплавить твердое кристаллическое вещество, нужно нагреть его до температуры плавления. Температуру плавления различных веществ можно найти в справочнике физики.
Источник
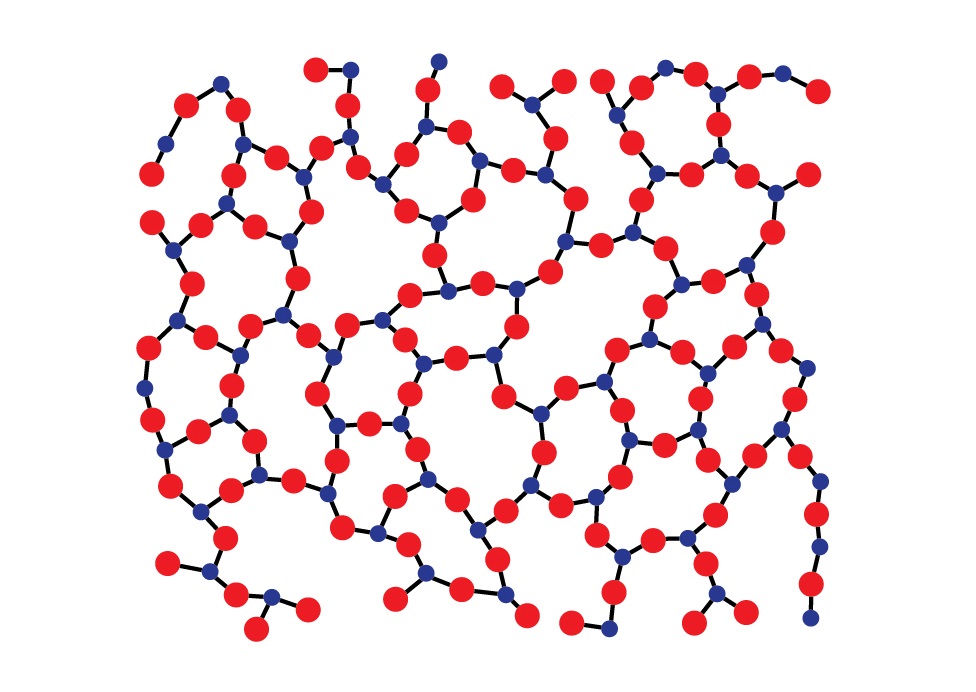
Аморфные тела (структура диоксида кремния)
Твердые тела разделяют на аморфные и кристаллические, в зависимости от их молекулярной структуры и физических свойств.
В отличие от кристаллов молекулы и атомы аморфных твердых тел не формируют решетку, а расстояние между ними колеблется в пределах некоторого интервала возможных расстояний. Иначе говоря, у кристаллов атомы или молекулы взаимно расположены таким образом, что формируемая структура может повторяться во всем объеме тела, что называется дальним порядком. В случае же с аморфными телами – сохраняется структура молекул лишь относительно каждой одной такой молекулы, наблюдается закономерность в распределении только соседних молекул – ближний порядок. Наглядный пример представлен ниже.
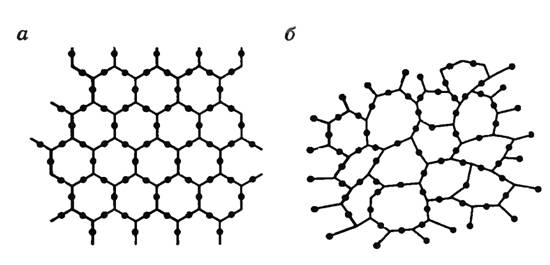
На рисунке слева (а) изображена решетка молекул кварца, а справа (б) расположение молекул кварцевого стекла, которое является аморфным телом.
К аморфным телам относится стекло и другие вещества в стеклообразном состоянии, канифоль, смолы, янтарь, сургуч, битум, воск, а также органические вещества: каучук, кожа, целлюлоза, полиэтилен и др.
Свойства аморфных тел
Особенность строения аморфных твердых тел придает им индивидуальные свойства:
- Слабо выраженная текучесть – одно из наиболее известных свойств таких тел. Примером будут потеки стекла, которое долгое время стоит в оконной раме.
- Аморфные твердые тела не обладают определенной температурой плавления, так как переход в состояние жидкости во время нагрева происходит постепенно, посредством размягчения тела. По этой причине к таким телам применяют так называемый температурный интервал размягчения.
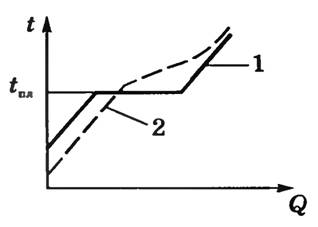
График перехода аморфного тела в жидкое состояние изображен пунктирной линией (2), а график перехода обычного твердого тела в жидкое состояние – сплошной (1).
- В силу своей структуры такие тела являются изотропными, то есть их физические свойства не зависят от выбора направления.
- Вещество в аморфном состоянии обладает большей внутренней энергией, нежели в кристаллическом. По этой причине аморфные тела способны самостоятельно переходить в кристаллическое состояние. Данное явление можно наблюдать как результат помутнения стекол с течением времени.
Стеклообразное состояние
В природе существуют жидкости, которые практически невозможно перевести в кристаллическое состояние посредством охлаждения, так как сложность молекул этих веществ не позволяет им образовать регулярную кристаллическую решетку. К таким жидкостям относятся молекулы некоторых органических полимеров.
Материалы по теме
Однако, при помощи глубокого и быстрого охлаждения, практически любое вещество способно перейти в стеклообразное состояние. Это такое аморфное состояние, которое не имеет явной кристаллической решетки, но может частично кристаллизироваться, в масштабах малых кластеров. Данное состояние вещества является метастабильным, то есть сохраняется при некоторых требуемых термодинамических условиях.
При помощи технологии охлаждения с определенной скоростью вещество не будет успевать кристаллизоваться, и преобразуется в стекло. То есть чем выше скорость охлаждения материала, тем меньше вероятность его кристаллизации. Так, например, для изготовления металлических стекол потребуется скорость охлаждения, равная 100 000 – 1 000 000 Кельвин в секунду.
В природе вещество существует в стеклообразном состоянии возникает из жидкой вулканической магмы, которая, взаимодействуя с холодной водой или воздухом, быстро охлаждается. В данном случае вещество зовется вулканическим стеклом. Также можно наблюдать стекло, образованная в результате плавления падающего метеорита, взаимодействующего с атмосферой – метеоритное стекло или молдавит.

Молдавит, естественное стекло, образованное ударом метеорита, из Беседин, Богемия, Чехия.
Источник
Схема атомно-молекулярного строения кристаллов и аморфных тел
Амо́рфные вещества́ (тела́) (от др.-греч. ἀ «не-» + μορφή «вид, форма») — конденсированное состояние веществ, атомная структура которых имеет ближний порядок и не имеет дальнего порядка, характерного для кристаллических структур. В отличие от кристаллов, стабильно-аморфные вещества не затвердевают с образованием кристаллических граней, и, (если не были под сильным анизотропным воздействием — деформацией или электрическим полем, например) обладают изотропией свойств, то есть не обнаруживают различия свойств в разных направлениях.
Аморфные вещества не имеют определённой точки плавления: при повышении температуры стабильно-аморфные вещества постепенно размягчаются и выше температуры стеклования () переходят в жидкое состояние. Вещества, обычно имеющие (поли-)кристаллическую структуру, но сильно переохлаждённые при затвердевании, могут затвердевать в аморфном состоянии, которое при последующем нагреве или с течением времени переходит в кристаллическое (в твёрдом состоянии с небольшим выделением тепла).
Аморфное состояние многих веществ получается при высокой скорости затвердевания (остывания) жидкого расплава, или при конденсации паров на охлаждённую заметно ниже температуры плавления поверхность-подложку. Соотношение реальной скорости охлаждения () и характеристической скорости кристаллизации определяет долю поликристаллов в аморфном объёме. Скорость кристаллизации — параметр вещества, слабо зависящий от давления и от температуры около точки плавления и сильно зависящий от сложности состава.
У металлов и сплавов аморфное состояние формируется, как правило, если расплав охлаждается за время порядка сотни и тысячи лет[источник не указан 135 дней]; для стёкол достаточно намного меньшей скорости охлаждения — долей-десятков миллисекунд[источник не указан 135 дней].
Кварц () также имеет низкую скорость кристаллизации, поэтому отлитые из квацевого расплава изделия имеют аморфное строение. Природный кварц, имевший сотни и тысячи лет для кристаллизации при остывании земной коры или глубинных слоёв вблизи вулканов, имеет крупнокристаллическое строение, в отличие от вулканического стекла, застывшего на поверхности и поэтому аморфного.
Из обычных полимеров (пластмасс) только полиэтилен имеет заметную скорость кристаллизации при комнатной температуре — порядка двух лет для мягкого (ПВД) и нескольких лет (даже с добавками-замедлителями кристаллизации) для твёрдого (ПНД) — уже примерно наполовину кристаллизованного вида. Это одна из причин охрупчивания со временем изделий из полиэтилена, особенно при повышенной температуре.
К стабильно-аморфным веществам принадлежат стёкла (искусственные и вулканические), естественные и синтетические смолы, клеи, парафин, воск и др. Аморфные вещества могут находиться либо в стеклообразном состоянии (при низких температурах), либо в состоянии расплава (при высоких температурах). Аморфные вещества переходят в стеклообразное состояние при температурах заметно ниже температуры стеклования . При температурах намного выше аморфные вещества ведут себя как расплавы, то есть находятся в расплавленном состоянии. Вязкость аморфных материалов — непрерывная функция температуры: чем выше температура, тем ниже вязкость аморфного вещества.
Структура[править | править код]
Исследования показали, что структуры жидкостей и аморфных тел имеют много общего.
В аморфных и жидких телах наблюдается ближний порядок в упаковке частиц (атомов или молекул).
Также бывают промежуточные полуаморфные (полукристаллические) состояния.
Свойства[править | править код]
Все физические свойства аморфного и поликристаллического состояний одного и того же вещества, кроме плотности, заметно, иногда сильно отличаются.
Электрические и механические свойства аморфных веществ ближе к таковым для монокристаллов, чем для поликристаллов, из-за отсутствия резких и сильно загрязнённых примесями межкристаллических границ с зачастую абсолютно другим химическим составом. Немеханические свойства полуаморфных состояний обычно являются промежуточными между аморфными и кристаллическими и изотропны.
При внешних воздействиях аморфные вещества обнаруживают одновременно упругие свойства, подобно кристаллическим твёрдым веществам, и текучесть, подобно жидкости, поэтому моделируются в механике сплошных сред как вязкоупругие среды. Так, при кратковременных воздействиях (ударах) они ведут себя как твёрдые вещества и при сильном ударе раскалываются на куски. Но при очень продолжительном воздействии (например, растяжении) аморфные вещества текут. Такими аморфным веществом также является смола (или гудрон, битум). Если раздробить её на мелкие куски и получившейся сыпучей массой заполнить сосуд, то через некоторое время смола сольётся в единое целое и примет форму сосуда.
В зависимости от электрических свойств, разделяют аморфные металлы, аморфные неметаллы и аморфные полупроводники.
Литература[править | править код]
- Скрышевский А. Ф. Структурный анализ жидкостей и аморфных тел. — 2-е изд., перераб. и доп.. — М.: Высшая школа, 1980. — С. 302-324. — 328 с.
- Шульц М. М., Мазурин О. В. Современное представление о строении стёкол и их свойствах. — Л.: Наука, 1988. — 200 с. — ISBN 5-02-024564-X.
См. также[править | править код]
- Опыт с капающим пеком
- Неньютоновская жидкость
Источник
>>> Перейти на мобильный размер сайта >>>
Учебник для 10 класса
ФИЗИКА
- Не все твердые тела — кристаллы. Существует множество аморфных(1) тел. Чем они отличаются от кристаллов?
Тепловые, электрические и оптические свойства аморфных тел одинаковы по всем направлениям: аморфные тела изотропны. Признаком аморфного тела является неправильная форма поверхности при изломе. Кристаллы же при изломе дают плоские (или ступенчатые) поверхности.
В зависимости от условий отвердевания расплава (например, в зависимости от режима его охлаждения) в аморфном состоянии могут оказаться и такие вещества, которые обычно имеют кристаллическую структуру. Так, кристалл кварца, если его расплавить (это происходит при температуре около 1700 °С), при быстром охлаждении образует так называемый плавленый кварц. Этот кварц имеет меньшую плотность, чем кристаллический, и обладает одинаковыми свойствами по всем направлениям.
Сходство аморфных тел с жидкостями
Аморфные тела мы считаем твердыми, так как они, подобно кристаллическим телам, сохраняют свою форму. Однако по прошествии более или менее длительного промежутка времени аморфные тела все же изменяют свою форму под действием, например, силы тяжести. Это делает их похожими на жидкости. Так, длинная стеклянная трубка, положенная на опоры, в конце концов под действием силы тяжести прогибается. Куски вара(2) в воронке с течением времени очень медленно просачиваются в отверстие воронки и выходят из нее в виде стержня. Если на дно сосуда положить пробку, на нее кусочки вара, а сверху на вар положить кусок свинца, то через достаточно большой промежуток времени куски вара сольются в сплошное тело с горизонтальной поверхностью, свинец опустится на дно, а пробка всплывет на поверхность. При повышении температуры такие изменения формы происходят быстрее. Таким образом, вар можно рассматривать как очень вязкую жидкость.
Переход аморфных тел в кристаллические
Аморфное состояние неустойчиво, и рано или поздно вещество из аморфного состояния переходит в кристаллическое. По прошествии более или менее длительного промежутка, времени в аморфном стекле под влиянием ударных нагрузок образуются мелкие кристаллы — стекло мутнеет. Аморфный стекловидный сахарный леденец засахаривается — покрывается кристаллами сахара и т. д.
Иногда переход вещества из аморфного состояния в кристаллическое происходит достаточно быстро. Так, аморфная пластическая сера обретает кристаллические свойства за несколько часов. С другой стороны, археологи обнаруживают стеклянные украшения, не изменившие своего вида за несколько сотен лет.
Ближний порядок
В аморфных телах слагающие его частицы не имеют определенного расположения по всему объему тела, как в кристалле. В расположении атомов (молекул) аморфного тела наблюдается беспорядок. Только ближние атомы — соседи располагаются в относительном порядке. Но строгой повторяемости во всех направлениях одного и того же элемента структуры, которая характерна для кристаллов, в аморфных телах нет. Наблюдается лишь так называемый ближний порядок. На рисунке 8.13, а схематически изображен фрагмент кристаллической решетки кварца — совокупность правильных шестиугольников. Для сравнения на рисунке 8.13, б изображена решетка аморфного кварца. Решетка имеет неправильную форму: наряду с шестиугольниками встречаются пяти- и семиугольники и т. д.

Рис. 8.13
Объяснение свойств аморфных тел
Беспорядок в расположении атомов аморфных тел приводит к тому, что средние расстояния между атомами по разным направлениям оказываются одинаковыми. Поэтому аморфные тела изотропны.
Сходство аморфных тел с жидкостями объясняется тем, что атомы и молекулы аморфных тел, подобно молекулам жидкости, имеют определенное время «оседлой жизни» — конечное время колебаний около положения равновесия. Но в отличие от жидкостей это время велико. В этом отношении аморфные тела близки к кристаллическим, так как перескоки атомов из одного положения в другое происходят редко.
По мере повышения температуры аморфные тела постепенно размягчаются. Это происходит потому, что с ростом температуры учащаются перескоки атомов из одного положения равновесия в другое. Определенной температуры плавления у аморфных тел в отличие от кристаллических нет. Поэтому аморфные твердые тела можно рассматривать как переохлажденные жидкости с очень большой вязкостью.
Упорядоченному расположению атомов кристаллических тел соответствует минимум потенциальной энергии, когда атомы сближаются на минимально возможные расстояния. Отсутствие дальнего порядка в расположении атомов аморфных тел приводит к тому, что вещество в аморфном состоянии имеет меньшую плотность, чем в кристаллическом. И этому состоянию соответствует большая потенциальная энергия взаимодействия. Вот почему аморфное состояние неустойчиво и вещество из аморфного состояния переходит в кристаллическое. Течение процессов в природе направлено в сторону уменьшения энергии.
Образование аморфного вещества из расплава при быстром охлаждении связано с тем, что за это время молекулы (или атомы) не успевают выстроиться в строгом порядке (процесс кристаллизации может требовать много времени) и образовать кристаллическую решетку. Однако для большинства веществ даже быстрого охлаждения недостаточно, чтобы помешать образованию кристаллов. Эти вещества существуют только в кристаллическом состоянии.
Аморфные твердые тела занимают промежуточное положение между кристаллическими твердыми телами и жидкостями. Их атомы или молекулы располагаются в относительном порядке.
(1) От греческого слова amorphos — бесформенный.
(2) Вар — легкоплавкое смолистое вещество.
Источник
