Какое свойство может характеризовать простое вещество

Просты́е вещества́ — химические вещества, состоящие исключительно из атомов одного химического элемента (из гомоядерных молекул)[1][2], в отличие от сложных веществ. Являются формой существования химических элементов в свободном виде[1][3]; или, иначе говоря, химические элементы, не связанные химически ни с каким другим элементом, образуют простые вещества[3]. Известно свыше 400 разновидностей простых веществ[2].
В зависимости от типа химической связи между атомами простые вещества могут быть металлами (Na, Mg, Al, Bi и др.) и неметаллами (H2, N2, Br2, Si и др.)[2].
Примеры простых веществ: молекулярные (O2, O3, H2, Cl2) и атомарные (He, Ar) газы; различные формы углерода, иод (I2), металлы (не в виде сплавов).
Аллотропные модификации[править | править код]
Один и тот же химический элемент зачастую может образовывать несколько типов простых веществ (аллотропия), называемых аллотропными модификациями. Явление аллотропии может быть обусловлено либо различным составом молекул данного элемента (аллотропия состава), либо различным строением молекул и способом размещения молекул (атомов) в кристаллах (аллотропия формы). Способность элемента к образованию соответствующих аллотропных модификаций обусловлена строением атома, которое определяет тип химической связи, строение молекул и кристаллов[2].
Различные аллотропные модификации могут переходить друг в друга. Для данного химического элемента его аллотропные модификации всегда различаются по физическим свойствам и химической активности (например, озон активнее кислорода, температура плавления алмаза больше, чем фуллерена)[4].
Агрегатное состояние[править | править код]
При нормальных условиях соответствующие простые вещества для 11 элементов являются газами (H, He, N, O, F, Ne, Cl, Ar, Kr, Xe, Rn), для 2 — жидкостями (Br, Hg), для остальных элементов — твёрдыми телами.
При комнатной температуре (либо близкой к ней) 5 металлов находятся в жидком либо полужидком состоянии, так как их температура плавления близка к комнатной:
- Ртуть (−39 °C)
- Франций (27 °C)
- Цезий (28 °C)
- Галлий (30 °C)
- Рубидий (39 °C)
Отношение понятий[править | править код]
Понятия «атом», «химический элемент» и «простое вещество» имеют каждый своё индивидуальное смысловое значение. Применение этих понятий возможно только в учебных целях. В научной и практической работе эта информация крайне недостаточна.
В таблице приведена классификация материальных объектов, в части масса-габаритных размеров и их вероятные соответствующие характеристики, см. таблицу ниже[4]:
Широта и правильность применения этих понятий базируется на знании русского языка и предмета Вашего изучения.
См. также[править | править код]
- Сложные вещества
Примечания[править | править код]
- ↑ 1 2 Редкол.:Кнунянц И. Л. (гл. ред.). Химическая энциклопедия: в 5 т. — М.: Советская энциклопедия, 1987. — Т. 1. — С. 361. — 623 с. — 100 000 экз.
- ↑ 1 2 3 4 Ахметов Н. С. Общая и неорганическая химия. — 4 изд., испр. — М.: Высшая школа, Издательский центр «Академия», 2001. — С. 253-269. — 743 с. — 15 000 экз. — ISBN 5-06-003363-5, ISBN 5-7695-0704-7.
- ↑ 1 2 Глинка Н. Л. Общая химия. — 24 изд., испр. — Л.: Химия, 1985. — С. 18-19. — 702 с.
- ↑ 1 2 Врублевский А. И. Химия: базовый школьный курс. — Мн.: Юнипресс, 2009. — С. 11-12. — 576 с. — 3100 экз. — ISBN 978-985-507-813-6.
Литература[править | править код]
- Ахметов Н. С. Общая и неорганическая химия. — 4 изд., испр. — М.: Высшая школа, Издательский центр «Академия», 2001. — 743 с. — 15 000 экз. — ISBN 5-06-003363-5, ISBN 5-7695-0704-7.
- Врублевский А. И. Химия: базовый школьный курс. — Мн.: Юнипресс, 2009. — 576 с. — 3 100 экз. — ISBN 978-985-507-813-6.
Ссылки[править | править код]
- Простые и сложные вещества. Аллотропия
Источник
Все вокруг нас состоит из каких-либо веществ. В зависимости от своего состава, они могут быть простыми и сложными. Но что это означает? Что такое простые вещества? Какими свойствами они обладают? Давайте это выясним.
Что такое простое вещество?
Разъяснения о веществах лучше всего начинать с понятия «атом». Это микроскопическая частица, обладающая конкретным размером, массой и другими свойствами. Каждый вид атома представляет определенный химический элемент. Но сами по себе они не могут существовать в природе и обязательно объединяются с другими атомами, формируя вещества.
Что такое простые вещества? Это структуры, образованные атомами одного вида элемента. При нормальных условиях они чаще всего являются твердыми, однако 11 из них пребывают в газообразном состоянии, а два – в жидком. В зависимости от того, какой тип связи образовался между атомами, их разделяют на две большие группы: металлы и неметаллы.
Понять, что такое простые вещества, иногда бывает затруднительно, ведь их названия могут совпадать с названиями химических элементов. Одинаково именуются: кислород, железо, медь, сера, фосфор и другие.

Свойства простых веществ
Основные качества, по которым характеризуют вещества:
- цвет;
- запах;
- твердость/мягкость;
- вязкость;
- растворимость;
- тепло- и электропроводность;
- магнитные свойства;
- температуры плавления и кипения и т. д.
Многие свойства веществ зависят от того, как и в каком количестве соединены их атомы. При этом может возникать аллотропия. Это явление, при котором одно простое химическое вещество существует в нескольких формах или модификациях. Так, атомы кислорода (О), объединяясь в пару, образуют О2 или вещество кислород – прозрачного цвета, без запаха и вкуса. Если же объединятся три атома, то получится озон или О3 – голубой газ с резким специфическим запахом.
Аллотропные модификации есть у селена, фосфора, водорода, кремния, сурьмы, олова, железа и других веществ. Формы могут переходить друг в друга при изменении температуры или давления. При этом существуют переходы обратимые, в которых вещество может вернуться к прежнему состоянию, и необратимые, в которых возврат уже невозможен.
Металлы
Простые вещества металлы характеризуются целым рядом общих свойств. Они в той или иной степени пластичны, а значит, поддаются ковке, растягиванию и сгибанию, не разрываясь и ломаясь. Самыми пластичными считаются золото, медь, серебро. А вот марганец, цинк или висмут сразу же ломаются при механическом воздействии.
Металлы хорошо проводят тепло и электричество. Наилучшим в этой области является серебро, хуже всего себя проявляет ртуть и висмут. Кстати, ртуть – единственный металл, который при нормальных условиях не твердый. Застывает она только при температуре -39 °C.

Другие представители этой группы простых веществ изначально твердые. Они переходят в жидкое состояние (плавятся) при определенных температурах, как правило, высоких. Так, франций плавится при 27 °C, свинец – при 1170 °C, алюминий – при 1554 °C, индий – при 156,6 °C , а вольфраму нужно целых 3410 °C.
Практически все металлы обладают блеском и серой окраской. Отличаются лишь их оттенки: у одних он темный и практически матовый, у других серебристо-белый и очень блестящий. Есть, конечно, и исключения. Например, золото и цезий окрашены в желтый, медь – в красноватый.
Неметаллы
Простых веществ неметаллов гораздо меньше. Их 118 известных элементов их образует только 22. Сходных черт между этими веществами тоже немного. Объединяет их в основном то, что они не принадлежат к металлам и не обладают характерным для них блеском (кроме йода и графита).
Все они имеют либо молекулярное, либо атомное строение. В первом случае неметаллы могут быть газами (хлор, азот, водород, кислород), твердыми телами (сера, фосфор, йод) или жидкостями (бром). Их атомы связаны тесно, а вот молекулы – нет. Поэтому такие вещества летучи, в твердом состоянии легко плавятся и крошатся.
Во втором случае они образованы длинными цепочками атомов. Их частицы связаны между собой очень тесно, поэтому вещества обладает твердостью, слабой пластичностью и летучестью, высокими температурами плавления и кипения. Графит, например, плавится только при 3800 °C, что выше, чем у самого тугоплавкого металла.

Фтор
Фтор – химический элемент под номером 9. В качестве простого вещества он является двухатомным газом (F2) желтоватого оттенка. Он имеет ярко выраженный запах, который немного напоминает хлор.
Фтор является самым активным неметаллом. Он вступает в реакцию со всеми элементами, кроме неона и гелия. Он также реагирует с большинством существующих веществ, которые при этом загораются или взрываются. Даже вода в атмосфере наполненной фтором начинает гореть. Водород, соединяясь с фтором, взрывается и при минусовых температурах.

Элемент фтор содержится в зубной эмали и костях нашего организма. Он необходим нам ежедневно в количестве 2,5—3,5 мг. Вместе с тем газ фтор очень токсичен и агрессивен. Он способен вызывать раздражение слизистых и ожоги II степени.
Сера
Химический элемент сера как простое вещество тоже проявляет неметаллические свойства. Он образует огромное количество аллотропных модификаций, основные из которых это: моноклинная, ромбическая, пластическая.
В природе встречается в свободном виде, поэтому человек знаком с ней давно. В таком состоянии она часто образуется в местах вулканических извержений и геотермальных источников. Кроме того, входит в состав многих минералов, например, пиритов.
Многим сера известна как вещество светло-желтого цвета с жирным блеском и высокой хрупкостью. Это моноклинная сера, которую часто производят в виде порошка. При нагревании такого порошка до 160 °C он расплавляется и приобретает темно-коричневый цвет. Остывая, он вновь становится желтого цвета.

Если расплавленную коричневую массу опустить в воду, то образуется пластическая сера. Она похожа на резину или пластилин. В таком виде она отлично растягивается и формируется. Однако через несколько дней опять превращается в моноклинную серу, обладающую хрупкостью.
При высоких вулканических температурах вещество образует красивые полупрозрачные кристаллы. На их образования уходят несколько тысяч лет, поэтому в природе они встречаются нечасто.
При сильной влажности измельченная сера может самовозгораться. С хлоратами, нитратами, маслами и жирами она реагирует очень бурно, возгораясь или взрываясь. Сера хорошо горит на воздухе, образуя бесцветный сернистый газ, обладающий резким запахом.
Источник
Об
атомах и химических элементах
Другого
ничего в природе нет
ни
здесь, ни там, в космических глубинах:
все
— от песчинок малых до планет —
из
элементов состоит единых.
С.
П. Щипачев, «Читая Менделеева».
В
химии кроме терминов “атом” и “молекула” часто
употребляется понятие “элемент”. Что общего и чем эти понятия различаются?
Химический
элемент – это
атомы одного и того же вида. Так, например, все атомы водорода –
это элемент водород; все атомы кислорода и ртути – соответственно элементы
кислород и ртуть.
В
настоящее время известно более 107 видов атомов, то есть более 107 химических
элементов. Нужно различать понятия “химический элемент”, “атом” и “простое
вещество”
Простые
и сложные вещества
По
элементному составу различают простые вещества, состоящие из атомов
одного элемента (H2, O2, Cl2, P4,
Na, Cu, Au), и сложные вещества, состоящие из атомов разных
элементов (H2O, NH3, OF2, H2SO4,
MgCl2, K2SO4).
К 70-м гг. XIX в. было уже известно более 60 химических элементов. Их условно классифицировали на металлы и неметаллы
ХИМИЧЕСКИЕ ЭЛЕМЕНТЫ | |
МЕТАЛЛЫ | НЕМЕТАЛЛЫ |
ОТЛИЧИТЕЛЬНЫЕ ФИЗИЧЕСКИЕ СВОЙСТВА СООТВЕТСТВУЮЩИХ ПРОСТЫХ ВЕЩЕСТВ | |
Железо Fe, медь Cu, алюминий Al, ртуть Hg, золото Au, серебро Ag и другие | Уголь С, сера S, фосфор P, йод I2, кислород O2, водород H2 и другие. |
1. Твёрдое агрегатное состояние (исключение – ртуть) 2. Металлический блеск 3. Хорошие проводники тепла и электричества. 4. Пластичные и ковкие. | 1. Твёрдые (Уголь С, сера S, фосфор P, йод I2), жидкие (бром Br2) и газообразные (кислород O2, водород H2). 2. Металлическим блеском не обладают (исключение йод) 3. Не проводят тепло и электрический ток – ИЗОЛЯТОРЫ. 4. Хрупкие |
На
2019 год в периодической таблице – 118 химических элементов, которые
образуют около 500 простых веществ.

Самородное
золото – простое вещество
Способность
одного элемента существовать в виде различных простых веществ, отличающихся по
свойствам, называется аллотропией. Например, элемент кислород O
имеет две аллотропные формы – кислород O2 и
озон O3 с различным числом атомов в молекулах. Аллотропные
формы элемента углерод C – алмаз и графит – отличаются строение их кристаллов. Существуют
и другие причины аллотропии.
| Название элемента | Аллотропные формы | Пример простого вещества |
| Углерод С | Графит
|
|
| Углерод С |
|
Сложные
вещества часто называют химическими соединениями, например, оксид
ртути(II) HgO (получается путем соединения атомов простых веществ – ртути Hg и
кислорода O2), бромид натрия (получается путем соединения атомов
простых веществ – натрия Na и брома Br2).
Итак,
подытожим вышесказанное. Молекулы вещества бывают двух видов:
1. Простые –
молекулы таких веществ состоят из атомов одного вида. В химических реакциях не
могут разлагаться с образованием нескольких более простых веществ.
2. Сложные –
молекулы таких веществ состоят из атомов разного вида. В химических реакциях
могут разлагаться с образованием более простых веществ.
Различие
понятий “химический элемент” и “простое вещество”
Отличить
понятия “химический элемент” и “простое вещество” можно
при сравнении свойств простых и сложных веществ. Например, простое вещество
– кислород – бесцветный газ, необходимый для дыхания,
поддерживающий горение. Мельчайшая частица простого вещества кислорода –
молекула, которая состоит из двух атомов. Кислород входит также в состав оксида
углерода (угарный газ) и воды. Однако, в состав воды и оксида углерода входит
химически связанный кислород, который не обладает свойствами простого вещества,
в частности он не может быть использован для дыхания. Рыбы, например, дышат не
химически связанным кислородом, входящим в состав молекулы воды, а свободным,
растворенным в ней. Поэтому, когда речь идет о составе каких – либо химических
соединений, следует понимать, что в эти соединения входят не простые вещества,
а атомы определенного вида, то есть соответствующие элементы.
При
разложении сложных веществ, атомы могут выделяться в свободном состоянии и
соединяясь, образовывать простые вещества. Простые вещества состоят из атомов
одного элемента. Различие понятий «химический элемент» и «простое вещество»
подтверждается и тем, что один и тот же элемент может образовывать несколько
простых веществ. Например, атомы элемента кислорода могут образовать
двухатомные молекулы кислорода и трехатомные – озона. Кислород и озон – совершенно
различные простые вещества. Этим объясняется тот факт, что простых веществ
известно гораздо больше, чем химических элементов.
Пользуясь
понятием «химический элемент», можно дать такое определение простым и сложным
веществам:
Простыми
называют такие вещества, которые состоят из атомов одного химического элемента.
Сложными
называют такие вещества, которые состоят из атомов разных химических элементов.
Отличие
понятий «смесь» и «химическое соединение»
Сложные
вещества часто называют химическими соединениями.
Осуществите
переход по ссылке и просмотрите опыт взаимодействия простых веществ железа и серы.
Попробуйте
ответить на вопросы:
1.Чем
отличаются по составу смеси от химических соединений?
2. Сопоставьте
свойства смесей и химических соединений?
3. Какими
способами можно разделить на составляющие компоненты смеси и химического
соединения?
4. Можно
ли судить по внешним признакам об образовании смеси и химического соединения?
Сравнительная
характеристика смесей и химических
Вопросы для сопоставления смесей с химическими соединениями | Сопоставление | |
Смеси | Химические соединения | |
Чем отличаются по составу смеси от химических соединений? | Вещества можно смешивать в любых соотношениях, т.е. состав смесей | Состав химических соединений постоянный. |
Сопоставьте свойства смесей и химических соединений? | Вещества в составе смесей сохраняют свои свойства | Вещества, образующие соединения, свои свойства не сохраняют, так как |
Какими способами можно разделить на составляющие компоненты смеси и | Вещества можно разделить физическими способами | Химические соединения можно разложить только с помощью химических |
Можно ли судить по внешним признакам об образовании смеси и химического | Механическое смешивание не сопровождается выделением теплоты или | Об образовании химического соединения можно судить по признакам |
Задания
для закрепления
I.
Поработайте с тренажёрами
Тренажёр №1
Тренажёр №2
Тренажёр №3
Тренажёр №4
Тренажёр №5
II.
Решите задание
Из предложенного списка веществ выпишите отдельно
простые и сложные вещества:
NaCl, H2SO4, K, S8, CO2, O3,
H3PO4, N2, Fe. Объясните ваш выбор, в каждом
из случаев.
III.
Ответьте на вопросы
№1. Сколько простых веществ записано в ряду
формул:
H2O, N2, O3, HNO3,
P2O5, S, Fe, CO2, KOH.
№2. К сложным относятся оба
вещества:
А) С (уголь) и S (сера);
Б) CO2 (углекислый газ) и H2O
(вода);
В) Fe (железо) и CH4 (метан);
Г) H2SO4 (серная кислота)
и H2 (водород).
№3. Выберите правильное
утверждение: простые вещества состоят из атомов одного вида.
А) Верно; Б) Неверно
№4. Для смесей характерно то, что
А) Они имеют постоянный состав;
Б) Вещества в составе “смеси” не сохраняют
свои индивидуальные свойства;
В) Вещества в “смесях” можно разделить
физическими свойствами;
Г) Вещества в “смесях” можно разделить при
помощи химической реакции.
№5. Для “химических соединений”
характерно следующее:
А) Переменный состав;
Б) Вещества, в составе “химического соединения
«можно разделить физическими способами;
В) Об образовании химического соединения можно
судить по признакам химических реакций;
Г) Постоянный состав.
№6. В каком случае идёт речь
о железе как о химическом элементе?
А) Железо – это металл, который притягивается
магнитом;
Б) Железо входит с состав ржавчины;
В) Для железа характерен металлический блеск;
Г) В состав сульфида железа входит один атом железа.
№7.
В каком случае идёт речь о кислороде как о простом веществе?
А) Кислород – это газ, поддерживает дыхание и
горение;
Б) Рыбы дышат кислородом, растворённым в воде;
В) Атом кислород входит в состав молекулы воды;
Г) Кислород входит в состав воздуха.
Источник
«Вещества и их свойства. Чистые вещества и смеси»
Ключевые слова конспекта: предмет химии, вещества и их свойства, чистые вещества и смеси, способо разделения смесей.
Химия – это наука о веществах, их свойствах, превращениях веществ и явлениях, сопровождающих эти превращения. Химия является одной из наук, изучающих природу. Вместе с биологией и физикой химия принадлежит к числу естественных наук.
Вещество — это то, из чего состоит физическое тело. Вещество характеризуется определенными физическими свойствами.
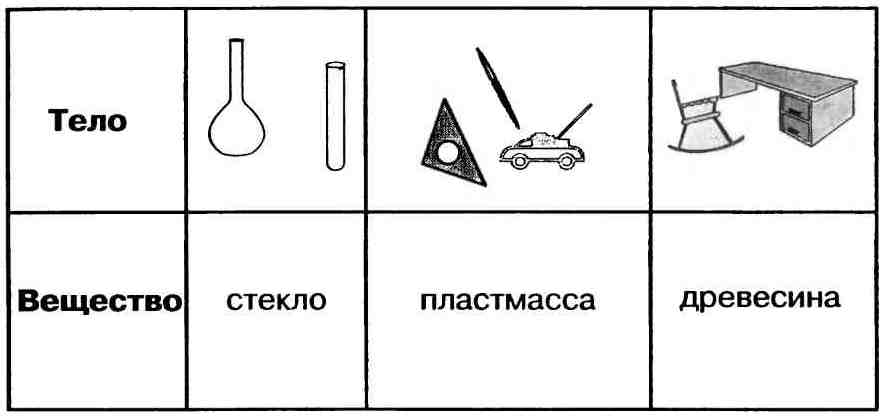
Свойства веществ — это признаки, по которым вещества отличаются друг от друга или сходны между собой, например:
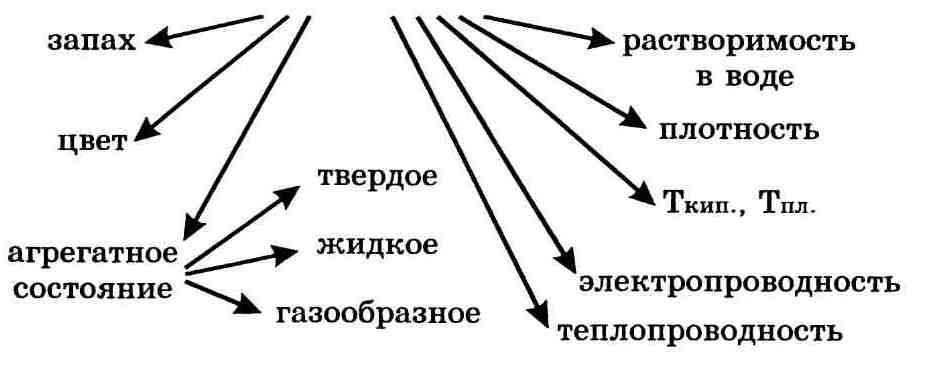
Важнейшие физические свойства вещества следующие: агрегатное состояние, цвет, запах, плотность, растворимость в воде, тепло-и электропроводность, температуры плавления и кипения.
Например, всем известное вещество алюминий можно охарактеризовать так: Алюминий — металл серебристо-белого цвета, сравнительно лёгкий (р = 2,7 г/см3), плавится при температуре 600°С. Алюминий очень пластичен. По электрической проводимости уступает лишь золоту, серебру и меди. Из-за лёгкости алюминий в виде сплавов широко используют в самолёто- и ракетостроении. Его также используют для изготовления электрических проводов и предметов быта.
Чистые вещества и смеси
Чистыми называются вещества, состоящие из одинаковых молекул. Смесь состоит из молекул разных веществ.
Каждое вещество имеет прежде всего свои, характерные именно для него свойства. Они в наибольшей степени проявляются, только если вещество является практически чистым, т. е. содержит мало примесей.
В природе чистых веществ не бывает, они встречаются преимущественно в виде смесей. Во многих случаях смеси нелегко отличить от чистых веществ. Например, сахар, растворяясь в воде, образует однородную по внешнему виду смесь. Даже с помощью микроскопа нельзя обнаружить частицы веществ, входящих в эту смесь. Такие смеси называют гомогенными (однородными).
Молоко на первый взгляд тоже кажется однородным веществом. Однако, если рассмотреть каплю молока под микроскопом, можно увидеть, что в ней плавает множество мельчайших капелек жира. Если дать молоку постоять, то эти капельки соберутся в верхнем слое, образуя сливки. Подобные неоднородные смеси называют гетерогенными смесями.
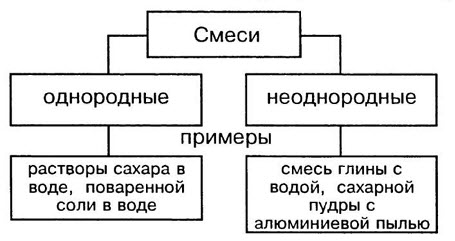
Однородные смеси — это смеси, в которых даже с помощью микроскопа нельзя обнаружить частицы веществ, входящих в смесь. Неоднородные смеси — это смеси, в которых невооруженным глазом или с помощью микроскопа можно заметить частицы веществ,составляющие смесь.
Способ разделения смесей
В смеси сохраняются свойства составляющих их веществ компонентов. На основании этих свойств выбирают рациональный способ разделения смесей.
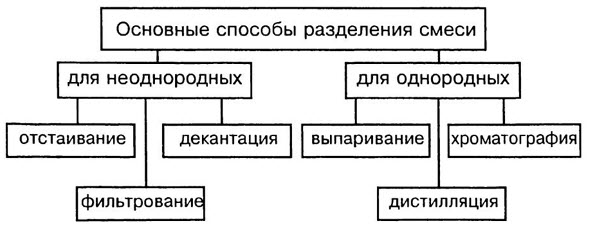
Способы разделения смесей основаны на различии свойств веществ-компонентов, их составляющих: плотности, растворимости в воде и других жидкостях-растворителях, способности плавиться и испаряться.
Способы разделения смесей: неоднородные смеси — отстаивание и фильтрование, действие магнитом; однородные смеси — перегонка, выпаривание, кристаллизация и хроматография.
Отстаивание. Прием разделения смеси твердого и жидкого вещества путем осаждения твердого на дно под действием сил тяжести.
- а) При выдерживании воды, содержащей частички глины, в емкостях глина медленно осаждается на дно, отстаивается. Применяется при очистке питьевой воды.
- б) Чтобы разделить смесь поваренной соли и речного песка, надо поместить ее в колбу и добавить воды. Соль растворится, а песок опустится на дно. Затем осторожно слить раствор, чтобы песок остался в колбе. Соль из раствора получают выпариванием воды.
- в) Для разделения смеси малорастворимых друг в друге жидкостей с различной плотностью используют делительную воронку. Это цилиндрический сосуд с краником внизу. Помещенная в эту воронку смесь бензина с водой или растительного масла с водой быстро расслаивается, причем водный слой оказывается внизу. Открывая кран, сливаем воду, а когда вода заканчивается, закрываем кран. В воронке — бензин или масло.
Фильтрование. Чтобы избавиться от нерастворимых в воде примесей, воду пропускают через фильтр. Материал фильтра — бумага, ткань, пористая керамика. Примеси остаются на фильтре, а вода очищается.
Действие магнитом. Выделение из неоднородной смеси веществ, способных к намагничиванию. К магниту притягиваются железные опилки.
Перегонка. Прием разделения однородных жидких смесей путем испарения летучих жидкостей, различающихся температурами кипения, с последующей конденсацией паров. Так из нефти, представляющей собой смесь жидких, газообразных и твердых углеводородов, получают попутные газы, бензин, керосин, дизельное топливо и другие продукты.
Выпаривание. Способ извлечения растворенного в жидком растворителе твердого или жидкого вещества. Например, упаривая воду из сладкого сиропа, получают сахар.
Кристаллизация. Избирательное извлечение одного из нескольких твердых веществ, содержащихся в растворе. Частичное упаривание воды с последующим охлаждением раствора приводит к осаждению кристаллов главного компонента. Так из морской воды выделяют поваренную соль NaCl, а другие соли, присутствующие в меньшем количестве, остаются в растворе.
Хроматография. Метод разделения смесей, основанный на различиях относительной растворимости веществ в используемом растворителе (жидкая фаза) и прочности связывания этих веществ поверхностью сорбента (твердая фаза).
Бумажная хроматография. Нанесем каплю раствора смеси двух веществ на расстоянии 2 см от края длинной полоски фильтровальной бумаги. Подвесим полоску в стеклянном цилиндре, на дне которого находится растворитель. Нижнюю часть полоски погрузим в растворитель, при этом пятно со смесью находится чуть выше. Верхняя часть полоски удерживается проволокой у отверстия цилиндра. Сверху цилиндр закроем стеклом, чтобы не испарялся растворитель. Боковые стороны полоски не касаются стенок цилиндра. Растворитель смачивает полоску, и жидкий фронт движется вверх за счет капиллярных сил. Вместе с растворителем по бумаге движутся и растворенные вещества. Если они цветные, то за движением можно наблюдать визуально. Вещество, которое лучше растворимо и менее прочно удерживается сорбентом (бумагой), поднимется выше. Когда фронт поднимется достаточно высоко и пятна разделятся, полоску вынимают и разрезают.
Колоночная хроматография — процесс, родственный рассмотренному. В качестве твердой фазы служит силикагель, помещенный в колонку. Только в этом случае смесь наносят равномерно вверху колонки, а потом добавляют растворитель. Разделенные вещества собирают внизу в разные стаканчики.
Конспект урока «Вещества и их свойства. Чистые вещества и смеси».
Следующая тема: «Физические и химические явления».
Источник


