Какое свойство декальцинированной кости
Костные образцы считаются одними из трудных объектов для гистологического исследования, так как межклеточное вещество содержит избыток различных солей кальция. Минерализация обусловливает опорно-механическую функцию костной ткани, но именно это обстоятельство представляет известную трудность в практической гистологии.
Для рутинного гистологического исследования наиболее употребимыми являются фиксация в 10% нейтральном забуференном формалине, заливка в парафин и окраска гематоксилином и эозином. Образцы костной ткани требуют удаления кальция и изменения технологии получения парафиновых срезов. Чрезвычайно важным этапом в технологии изготовления гистологических препаратов является фиксация. Предпочтительное использование формалина для фиксации определяется следующими соображениями:
1) это самый часто используемый фиксатор; подавляющее большинство гистологических лабораторий используют один и тот же фиксатор практически для всех гистологических объектов;
2) любой из рутинных образцов может быть подвергнут иммуногистохимическому исследованию, а использование подавляющего большинства первичных антител требует фиксации материала в 10% нейтральном забуференном формалине.
Наличие солей кальция не позволяет приготовить срезы тканей на обычных микротомах, поэтому кальций необходимо удалить перед проводкой ткани (декальцинация). Этой процедуре подвергают не только костные образцы, но любые ткани, содержащие патологические участки обызвествления.
Ниже описаны детали процедуры декальцинации и способы контроля окончания декальцинации, пригодные для современной гистологической лаборатории.
Выбор декальцинирующего агента
Все декальцинирующие агенты можно условно разделить на кислотные и бескислотные.
P. Gray [6] приводит 65 рецептов декальцинирующих жидкостей, каждый из которых включает, как минимум, одну из кислот.
К бескислотным декальцинаторам относятся ионообменные смолы, но они не столь широко используются в гистологии.
Считалось, что для удаления кальция из компактных костей лучше всего подходят декальцинирующие жидкости на основе сильных минеральных кислот (соляная, азотная). Они действительно быстро извлекают кальций (2—3 сут), но такие объекты совершенно не пригодны для иммуногистохимического (ИГХ) исследования.
Считается, что губчатые кости лучше декальцинировать растворами на основе слабых органических кислот (муравьиная, уксусная), но и в этом случае могут возникнуть трудности при проведении ИГХ-окрасок. Процедура декальцинации слабыми кислотами занимает 7—10 дней и более.
В любом случае, когда в лаборатории исследуются опухоли костей и трепанобиоптаты костного мозга, нужно использовать растворы на основе этилендиаминтетраацетата (ЭДТА) с рН 7,0. Если данная технология недоступна в лаборатории и используется метод декальцинации сильными кислотами, необходимо один репрезентативный кусочек опухоли вместе с костной тканью зафиксировать до процедуры декальцинации и сохранить его либо в 70% этаноле, либо в 70% изопропаноле, но не в формалине.
Процедура декальцинации
Выпиленные образцы толщиной 3 мм помещают в 10% нейтральный забуференный формалин на 24—48 ч при комнатной температуре в объеме фиксатора в 10—20 раз больше образца.
I. Dimmenstein [5] приводит описание некоторых приспособлений и вспомогательных приемов для вырезки костного материала. Перед проводкой избыток формалина отмывается в течение 20—30 мин в проточной воде.
Материал для декальцинации помещают в гистологические кассеты. Декальцинация каждого случая проводится в отдельной пластиковой емкости объемом не менее 200 мл, для контроля выбирают наиболее крупный образец. Процедура проводится без использования каких-либо приспособлений. Подогрев, мешалки, вакуум, микроволны, ультразвук и воздействие электрического поля могут изменить структуру белковых молекул и повредить антигены.
Объем декальцинатора по отношению к объему ткани должен быть, как минимум, в 50 раз больше, поскольку процесс извлечения происходит путем диффузии кальция в раствор. В свежем растворе декальцинация проходит сильнее. Необходимо заменять раствор на свежий ежедневно.
Определение окончания декальцинации
Это очень важный момент, так как он позволяет предотвратить необратимое разрушение тканей. Имеется несколько способов определения окончания процесса декальцинации.
1. Сгибание кусочка. Образец ткани пробуют согнуть пальцами. Пока в нем остается кальций, его очень трудно или невозможно согнуть, а при отсутствии кальция он легко гнется. Это быстрый и простой, но субъективный тест. При сгибании не полностью декальцинированной кости мягкие ткани могут отделяться от твердых, а также происходит повреждение структуры костной ткани. При слишком сильном сгибании ткани ломаются, даже если кальция в них уже нет [2, 11].
2. Проба образца тонкой иглой. Если игла проходит через образец без хруста, декальцинация считается законченной. При этом от иглы остаются следы, и это заметно под микроскопом. Нередко картина нарушается в самых ценных для диагностики местах. Тем не менее игла может проходить без затруднений и в тех случаях, когда в образце кальций еще остается в небольшом количестве [9].
3. Углекислотный тест. При помещении кусочка в декальцинирующую жидкость на поверхности раствора начинают появляться пузырьки углекислого газа. Отсутствие пузырьков газа свидетельствует об окончании процесса декальцинации. Это неточный тест, поскольку при наличии мелких кальцинатов пузырьки газа не визуализируются. Особенно трудно этот тест выполним на мелких костных фрагментах [10].
4. Всплывание образца на поверхность. Образец всплывает на поверхность, когда кальция в нем не остается. Это утверждение неверно, поскольку образец может всплывать независимо от наличия кальция или когда плотность образцов меньше плотности декальцинирующего раствора.
5. Оксалатный тест. Достаточно информативный и чувствительный метод [2, 4], который подходит для сильных и органических кислот, если их концентрация не превышает 10%. Он не подходит для растворов с ЭДТА. Продолжительность теста — 35 мин.
6. Рентгенографический метод. Впервые был описан в 1930 г. [7]. С помощью рентгеновского аппарата (обычного или специального, например, Faxitron) определяются даже минимальные количества кальция в исследуемом объекте. Можно определять отложения кальция и в парафиновых блоках [3]. Недостатки метода — дорогостоящая специальная аппаратура, а также влияние рентгеновского излучения на персонал. Преимущество — возможность тестирования большого количества объектов за короткое время.
7. Гравиметрический тест. Надежный тест, не требующий затрат реактивов, дорогостоящей аппаратуры и времени. Подходит для любого декальцинатора и любого объекта. Если масса объектов мала и они многочисленны, можно взвешивать их вместе. Исследуемый фрагмент промокают фильтровальной бумагой для удаления избытка воды и взвешивают его с точностью до миллиграмма. Массу фиксируют. В дальнейшем образец ткани после просушивания кусочками фильтровальной бумаги ежедневно взвешивают и сравнивают массу с предшествующим результатом. Пока удаляется кальций, масса образца будет убывать [1]. Имеется промежуток времени, когда масса остается постоянной. Как только кальций полностью будет удален, вода начинает замещать кальций, и масса образца начинает увеличиваться. Важно зафиксировать тот момент, когда кальций полностью удален из образца — декальцинация может считаться законченной [8]. После окончания декальцинации исследуемые образцы промывают в воде в течение 30—60 мин и начинают проводку по обычной схеме. Особенно важно выполнить промывку после использования жидкостей на основе ЭДТА, поскольку он при взаимодействии со спиртами образует осадки, значительно затрудняющие микротомию.
Определение момента окончания декальцинации является обязательным, но требует определенного навыка. Эти тесты рационально проводить на каком-либо одном (большем) образце от одного пациента, а не тестировать каждый объект.
Гравиметрический тест является наиболее быстрым, простым, удобным и дешевым. Для крупной лаборатории, постоянно работающей с костным материалом, целесообразно рассмотреть возможность приобретения портативной рентгеновской установки для тестирования момента окончания декальцинации. Оба метода оправдывают себя по затрате времени и простоте исполнения тестов, воспроизводимости и надежности результатов.
Прерывание декальцинации
Возможность прерывания процесса декальцинации является неоспоримым преимуществом в случае, когда процесс близок к окончанию, а возможность завершить его отсутствует (выходные и праздничные дни, ночь и др.). В этом случае кусочки костей извлекают из декальцинирующего раствора, промывают в проточной воде в течение 20—30 мин и помещают в 10% нейтральный забуференный формалин на нужный срок. Возобновляют декальцинацию после извлечения образцов из фиксатора и промывки в проточной воде в течение 20—30 мин.
Необходимо помнить, что декальцинации не подлежат хрящевые образцы, ткани с резко выраженным фиброзом, ногти, ороговевшая кожа и любые другие образцы, не содержащие солей кальция.
Декальцинирующие жидкости не обладают размягчающим действием и приводят к повреждению белковых структур. Декальцинаторы на основе минеральных кислот не могут применяться в тех случаях, когда может возникнуть необходимость в проведении ИГХ-исследований. Особенно это касается трепанобиоптатов костного мозга.
Поэтому группа декальцинаторов на основе сильных минеральных и органических кислот может использоваться только в тех случаях, например, когда нет подозрения на наличие опухолевого процесса, когда исследуют компактную кость.
Органические кислоты (муравьиная и ее соли, уксусная, трихлоруксусная, пикриновая, лимонная и ее соли) обладают более мягким действием, но требуют для полной декальцинации от нескольких дней до нескольких недель. В современных условиях, когда клиницисты требуют сократить сроки исследования, это вряд ли удобно.
Хелатирующие агенты (ЭДТА и ее соли) — отдельная группа декальцинирующих агентов. Механизм связывания кальция в зависимости от рН раствора можно представить следующим образом. ЭДТА связывает кальций в зависимости от рН за счет четырех карбоксильных кислотных групп (СООН) и двух аминогрупп (NH). При рН ниже 3,0 декальцинация не происходит вообще. При увеличении рН раствора протоны диссоциируют из этих групп. Этот процесс известен как депротонирование, и декальцинация становится возможной. При рН выше 10,0 группы СООН полностью депротонированы, эта форма ЭДТА быстро связывает кальций, и декальцинация происходит очень быстро. Однако при рН более 7,4 происходит необратимый щелочной гидролиз некоторых белков. При рН 7,0 декальцинация будет происходить достаточно эффективно. Детали эксперимента описываются в обзоре G. Callis, D. Sterchi [4].
К сожалению, в большинстве российских лабораторий чаще других используются декальцинаторы на основе сильных минеральных кислот (азотной, соляной), в которых концентрация кислот не превышает 10%. Более высокая концентрация не сокращает время извлечения кальция, а лишь ускоряет гидролиз белков ткани. Поэтому эта группа декальцинаторов подходит для извлечения больших масс кальция за короткое время, например для образцов компактной кости. Обычно время эффективного воздействия таких кислот ограничивается несколькими часами.
В формулах ЭДТА и ЭДТА с солями натрия более растворимы те, в которых больше натрия. Динатриевая соль ЭДТА менее растворима, чем тетранатриевая ЭДТА, но важно заметить, что их рН также отличаются.
Порошки ЭДТА, используемые для декальцинации, бывают нескольких видов.
А. ЭДТА (эдетовая кислота) имеет молекулярную массу 292 моль, она растворима в воде на 10%, концентрация ее полезна для декальцинации. Чтобы достичь высокой концентрации ЭДТА в растворе, ее нагревают и добавляют гидроксид натрия, который помогает «депротонировать» молекулу. Эта ЭДТА, растворенная в воде, имеет кислую рН (около 4,0) до добавки гидроксида натрия.
Б. Динатриевая соль ЭДТА имеет молекулярную массу 372 моль. 5% раствор имеет рН 4,0—5,0 при комнатной температуре. Соль растворяется в воде в концентрации до 10%, но при приготовлении раствора могут возникнуть трудности, пока рН раствора доводится до 7,0 с помощью гидроксида натрия. Наиболее часто применяется динатриевая соль ЭДТА, имеющая молекулярную массу 372,5 моль, раствор при комнатной температуре имеет рН 4,0—5,0:
вода дистиллированная, мл 850,0
ЭДТА динатриевая соль, г 125,0
натрия гидроксид, г 23,0.
Следует растворить динатриевую соль ЭДТА в воде, затем прибавить гидроксид натрия. Все процессы проводить, непрерывно помешивая. рН конечного раствора должен соответствовать 7,0, что достигается прибавлением по каплям 40% водного раствора гидроксида натрия, при помешивании и контроле рН с помощью предварительно откалиброванного рН-метра. Должен получиться совершенно прозрачный раствор, без каких-либо осадков и взвесей.
В. Тетранатриевая соль ЭДТА имеет молекулярную массу 380 моль и хорошо растворима в воде (14% или более), рН раствора 9,5—12,0. Эта молекула ЭДТА полностью «депротонирована», но высокий рН повреждает чувствительные к щелочам белки. При этом декальцинация будет очень быстрой, однако необходимо снизить рН уксусной кислотой до 7,4 (или до уровня, рекомендуемого для работы с ферментами) для гарантии качественных результатов при ИГХ-окрасках. Также рН можно снизить добавкой трис-гидроксиметиламинометана.
Приготовление растворов ЭДТА требует достаточного опыта, времени и четкого контроля рН с помощью рН-метра, что затруднительно в большинстве гистологических лабораторий. Поэтому целесообразно приобретать декальцинаторы, готовые к употреблению. Примерами могут служить Osteodec («Bio-Optica», Италия), бескислотный декальцинатор БМП («БМП», Россия) и др.
В итоге, находясь перед выбором декальцинирующего агента, лаборатория оказывается под влиянием следующих обстоятельств:
— неизвестно заранее, какой объект впоследствии будет подвергнут гистохимическому, иммуногистохимическому или молекулярному исследованию;
— клиницисты требуют выдачи результата в максимально короткие сроки;
— декальцинирующий раствор должен быть прост и эффективен, дешев и доступен и не повреждать элементы тканей.
По этим соображениям компромиссным представляется выбор декальцинатора на основе ЭДТА с нейтральной рН.
Костные образцы, фиксированные в 10% нейтральном забуференном формалине, могут быть декальцинированы с использованием разных декальцинирующих жидкостей, но с обязательным контролем окончания декальцинации. Такой подход позволяет контролировать качество декальцинации ткани, которая впоследствии будет подвергнута как рутинным, так и ИГХ-исследованиям. Декальцинацию для таких случаев важно проводить растворами на основе солей ЭДТА с нейтральной рН. Если в данной лаборатории ИГХ-методы не выполняются, то макроскопически репрезентативный образец, зафиксированный в 10% нейтральном забуференном формалине, должен сохраняться в 70% этиловом или изопропиловом спирте до тех пор, пока не потребуется ИГХ-исследование. Это чрезвычайно важно для выбора лечебной тактики при гематологических заболеваниях и опухолях костной ткани.
Источник
Цель урока:изучить химический состав,
строение и свойства костей.
Задачи урока:
- образовательная:
- развивающая:
- воспитательная:
- модель скелета человека;
- проектор, экран, компьютер, презентация
Power Point, фильм созданный в Windows Movie Maker; - выставка продуктов питания, необходимых для
укрепления костной системы; - подарки учащимся (молоко и творожные сырки);
- на столах учащихся раздаточный материал:
прокаленные, декальцинированные и
мацерированные кости, кусочек мрамора, салфетки;
печатный материал: инструкционные карты для
опыта, оценочный лист, кроссворд, рабочая
тетрадь; на столе учителя: стакан с надписью
“НСl” (в нем находились декальцинированные
кости); карточки с формулами солей: карбонатов и
ортофосфатов кальция и магния.
обобщить знания об основных
функциях скелета; сформировать у учащихся знания
об особенностях химического состава, строения и
свойств кости, обеспечивающих выполнение
функций опорно-двигательной системы.
развивать умения анализировать,
сравнивать, делать выводы; развивать логическое
мышление (устанавливать причинно-следственные
связи, подтверждая на данном предметном
материале зависимость свойств объекта от его
состава и строения); убедить учащихся в единстве
живой и неживой природы, целостности научного
мировоззрения, используя интеграцию
химико-биологических знаний.
воспитывать чувство
ответственности за сохранение своего здоровья
(формировать представления учащихся о
необходимости следить за своей осанкой и
питанием).
Проблема, которую призван решить урок: От чего
зависит прочность кости?
Планируемые результаты обучения. В
результате изучения данной темы учащиеся должны
знать: а) химический состав кости, влияние
органических и неорганических веществ на
свойства кости; б) особенности строения кости;
определение и значение понятий: надкостница,
костное вещество, губчатое вещество, красный
костный мозг, желтый костный мозг; уметь:
характеризовать зависимость свойств кости от её
состава и строения.
Подготовка к уроку. Учащиеся вместе с
учителем химии заранее готовят прокалённые и
декальцинированные кости для опыта. Часть костей
прокаливают в муфельной печи (или в духовке),
другую часть костей помещают в раствор соляной
кислоты (10%) для растворения неорганических
веществ.
Оборудование:
Оформление доски.
Структура урока:
- Актуализация знаний учащихся и целеполагание.
- Проверка знаний учащихся. Воспроизводящая
беседа и тест.
А.Просмотр видеофильма.(Приложение
3). Целеполагание.
Учитель биологии. Здравствуйте,
ребята! Как вы уже догадались из просмотренного
фильма, тема нашего урока напрямую связана со
строением опорно-двигательной системы. И вы,
конечно же, правы! Девизом урока мы выбрали слова
Вольтера: “Движение – это жизнь”. Урок не совсем
обычный – мы подготовили его совместно с
учителем химии, для того, чтобы лучше разобраться
в особенностях свойств и строения кости со
стороны двух смежных предметов. <Слайд 1>. Откройте
рабочие тетради и запишите тему урока:
“Химический состав, строение и свойства
костей”. <Слайд 2>.

Слайд 1

Слайд 2
Б. Формулировка цели урока. Попробуйте
самостоятельно сформулировать цель нашегоурока.(Учащиеся формулируют цель урока, исходя из
названия темы урока).
Цель урока: изучить строение, свойства
и химический состав костей. <Слайд 3>

Слайд 3
Сегодня при изучении нового материала, нам
понадобятся знания предыдущего урока.
- Каковы основные функции опорно-двигательного
аппарата? - Назовите отделы скелета и покажите их на модели
скелета человека. - Тест. <Слайд 4> Задание (2 мин.). Вам
необходимо соотнести перечисленные названия
костей с соответствующим отделом скелета.
Листочки с заданием лежат у вас на столе.
Сегодня мы предлагаем вам самим
оценить свою работу на уроке. Нам предстоит
выполнить три задания: тест, лабораторный опыт и
разгадать кроссворд. Перед вами оценочный лист (приложение 1а), в него вы
будете вносить оценки. В конце урока нужно
поставить итоговую оценку, а так же оценить урок
в целом и написать отзыв о нем. Подпишите свой
оценочный лист и приступайте к выполнению теста.

Слайд 4
Отделы скелета: | Названия костей |
| а) затылочная кость |
| б) грудина |
| в) лучевая кость |
г) скуловая кость | |
д) ребро | |
е) бедренная кость. |
Ответы: 1……; 2……….; 3 ……… .
Взаимопроверка. Учащиеся проверяют
правильность выполнения задания по слайду
<Слайд 5>. Переходим к главному
этапу урока.

Слайд 5
III.Изучение нового материала.
Целеосуществление.
Учитель химии. Биология и химия –
естественные науки. Они тесно взаимосвязаны и
сегодня мы убедимся в этом на примере данного
урока. <Слайд 6>.

Слайд 6
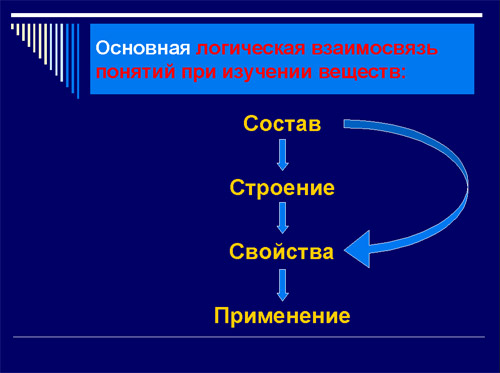
Для химиков очень важна логическая
взаимосвязь понятий:
она является для химиков основной при
изучении веществ (учитель прикрепляет карточки
схемы на доске, учащиеся записывают в тетради).
Интересно проследить эту взаимосвязь на примере
веществ, из которых состоит костная ткань. И
химия нам в этом первая помощница, ведь химия –
это наука о чем? – О веществах. Кость состоит из
чего? – Из веществ. Учёные установили, что в
состав кости входят многие вещества, химический
состав её очень сложен. Кость состоит из воды,
органических и неорганических веществ.
Слайд 7
<Слайд 8>. Обезжиренная, и
обезвоженная кость (мацерированная) состоит на 1/3
из органических веществ, получивших название
“оссеин”, и на 2/3 из неорганических. Химики
установили, что в состав кости входят соли
кальция и магния, среди них – известные нам: CaCO3;
MgCO3; Ca3(PO4)2; Mg3(PO4)2.
(Учитель показывает карточки с формулами
солей – ученики называют вещества). Итак, кость
состоит из многих веществ и обладает
определёнными свойствами.

Слайд 8
– Какие свойства кости позволяют ей
выполнять свои функции?
– Твердость, прочность, гибкость. И
очень важным свойством кости является прочность.
<Слайд 9>. По прочности кость
сравнивают с некоторыми металлами (медью,
железом). Прочность кости относится к прочности
стали, как 1:10. Например, короткий сегмент
большеберцовой кости может выдержать вес
легкового автомобиля!

Слайд 9
Кость очень прочна, а почему?
(Постановка проблемы урока.)
А. Лабораторный опыт: “Свойства
прокалённой и декальцинированной кости”
Мы постараемся ответить на этот вопрос
с точки зрения состава. И для этого проведём
лабораторный опыт, ведь “опыт – кратчайший путь
познания истины”, а народная мудрость гласит:
“Лучше один раз увидеть, чем сто раз услышать”, а
я бы ещё добавила: “А ещё лучше потрогать”, ведь
чтобы определить свойства (твёрдость, гибкость,
хрупкость), нужно косточки потрогать
(используйте салфетки).
<Слайд 10>. Цель опыта – найти
ответы на вопросы: “Чем определяется прочность
кости? Влияет ли состав кости на её свойства? ”.

Слайд 10
Вы знаете, что для опыта нам нужны три
кости животных: нормальная, прокаленная и
декальцинированная. Спасибо всем, кто принял
участие в подготовке опыта. Мы выяснили, что
кость состоит из органических (ОВ) и
неорганических веществ (НВ).
– Давайте вспомним: как мы получили
прокаленную кость?
– Мы прокалили её длительное время в
духовом шкафу.
– Что происходило с органическими
веществами кости при прокаливании?
– Органические вещества сгорали,
остались неорганические.
Запись на доске:
– Из каких веществ состоит прокалённая
кость?
– Из неорганических.
– Как мы получили декальцинированную
кость?
– Мы поместили кость в раствор соляной
кислоты.
– Что произошло с неорганическими
веществами в соляной кислоте?
– Неорганические вещества
растворились, а органические остались.
Запись на доске:
– Как вы понимаете слово
“декальцинированная кость?” Из каких веществ
состоит декальцинированная кость?
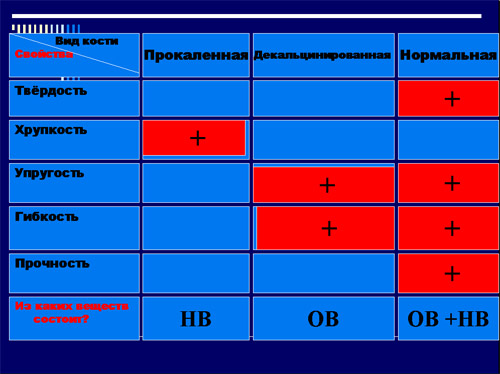
Итак, сравним свойства прокаленной,
декальцинированной и нормальной кости и ответим
на вопрос: какие вещества определяют прочность
кости? Перед вами инструкционная карта (приложение 1б). Читаем
задание и выполняем его. Заполняем таблицу и
делаем вывод, у вас есть возможность выбрать
уровень сложности (на “5” или на “4”).
Проверяем заполнение таблицы по слайду. <Слайды
11, 12>. <Далее Слайд 13>

Слайд 11
Слайд 12
Слайд 13
– Какое свойство наиболее характерно для
прокалённой кости?
– Хрупкость.
– Какие свойства характерны для
декальцинированной кости?
– Упругость, гибкость.
– Для нормальной?
– Твёрдость, упругость, гибкость, прочность.
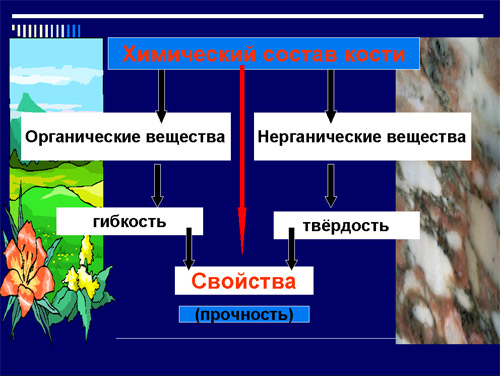
– Какие вещества входят в состав кости?
– Органические и неорганические.
– Какое свойство кости зависит от
органических веществ?
– Гибкость.
– Какое свойство кости зависит от
неорганических веществ?
– Твёрдость.
– Уместно сказать о единстве живой и
неживой природы, ведь в состав кости входит
карбонат кальция, он же – мрамор, потрогайте,
какой он твердый!
– Сочетание твёрдости и гибкости
определяют прочность кости.
Вывод. Свойства кости определяются её
составом. Прочность кости определяется
единством органических и неорганических
веществ. Оцените свою работу. Итак, мы убедились,
что свойства кости зависят от состава. Но только
ли состав влияет на свойства?
– От чего еще зависят уникальные
свойства кости?
– От строения.
Б. Объяснение нового материала по теме:
“Строение кости”.
Учитель биологии. Рассмотрим
строение кости, и докажем что ее свойства зависят
от строения. По ходу моего объяснения вы будете
выполнять задание № 61 на стр. 27 в рабочих
тетрадях на печатной основе (обозначение частей
кости на рисунке).
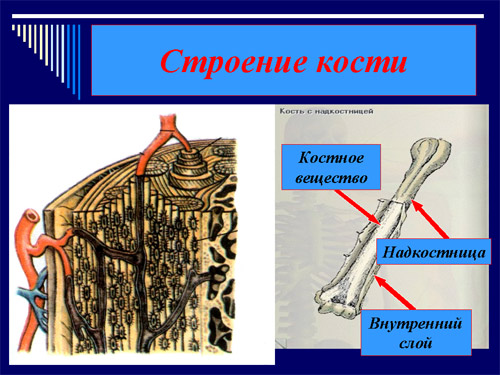
– Ребята, назовите основную ткань, из
которой построена кость?
Костная ткань построена из костных
клеток и межклеточного вещества, имеющего у
человека пластинчатое строение. <Слайды 14,
15>.
Слайд 14
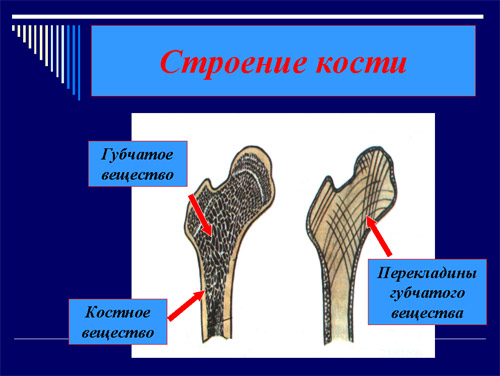
Слайд 15
Снаружи кость покрыта надкостницей
– тонкой, но весьма прочной оболочкой. Ее толщина
у разных костей колеблется от 0,1 до 0,8 мм. В
надкостнице можно выделить 2 слоя: внешний –
более грубый, волокнистый, с множеством
кровеносных сосудов и нервов, и внутренний –
тонкий, нежный. Внешний слой выполняет функцию
связи кости с сухожилиями, связками, мышцами, а
внутренний – образует собственно кость. Именно
этот слой восстанавливает ее при повреждениях и
переломах, участвует в росте кости. Под
надкостницей находится плотное компактное
вещество – костное. В нем находятся кровеносные
каналы и нервы. Ученые установили, что костные
пластинки, входящие в состав костной ткани,
располагаются не хаотично, а по направлению сил
сжатия и растяжения, возникающих в связи с
нагрузками на кость, это объясняет уникальную
прочность кости.
За компактным веществом прячется губчатое.
В губчатом веществе есть ячейки, в которых
расположен красный костный мозг. У взрослых он
содержится в плоских костях, в губчатых, и на
концах (эпифизах) трубчатых костей. Приведите
примеры указанных типов костей. В красном
костном мозге находятся клетки крови и их
предшественники, жировые клетки, кровеносные
сосуды и межклеточное вещество. Красный
костный мозг – орган кроветворения и орган
иммунной системы человека. Полость в диафизах
заполнена желтым костным мозгом, в котором много
жировых клеток.
Губчатое вещество – более пористое
по строению, и состоит из тонких перекладин. Они в
основном параллельны костной оси и многократно
соединяются друг с другом. Именно такие костные
трубочки работают на сжатие и на изгиб, поэтому
кости обладают значительным запасом прочности.
Данные особенности строения были использованы
Эйфелем при создании всемирно известной башни –
Эйфелевой. <Слайд 16>.

Слайд 16
Повторим основные понятия по строению кости:
надкостница, костное вещество, губчатое
вещество, красный костный мозг, желтый костный
мозг. <Слайд 17>.

Слайд 17
4 Итак, мы рассмотрели строение кости, и
теперь можем ответить на вопрос: “Зависят ли
свойства кости от ее строения?”.
4 Вывод: Сегодня на уроке мы убедились,
что свойства кости зависят не только от состава,
но и от строения.
IV.Закрепление.
Учитель химии. Переходим к
заключительному этапу урока. Мы предлагаем вам
разгадать кроссворд, в который входят основные
понятия урока. Впишите по вертикали нужные слова
и по горизонтали вы получите слово, расшифруйте
его смысл. Вариант 1 – отвечает на вопросы 1-5,
вариант 2 – 6-10.
Кроссворд к уроку по теме: “Состав,
строение и свойства костей”.
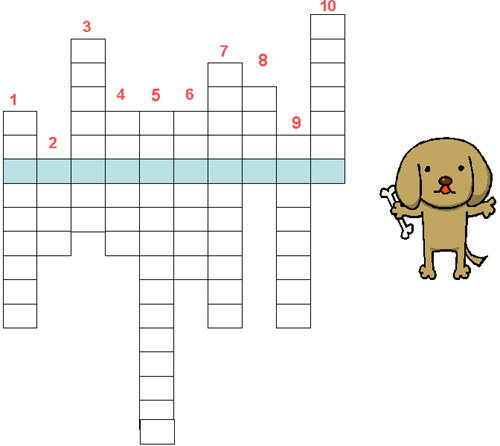
З а д а н и е
Впишите нужные слова по вертикали. В выделенных
клетках по горизонтали вы прочитаете слово,
расшифруйте его смысл.
- Свойство кости, обусловленное единством
органических и неорганических веществ. - Неорганические вещества, состоящие из атомов
металла и кислотного остатка. - Вещество кости, состоящее из костных перемычек
и балок, которые образуют многочисленные ячейки.
В ячейках находится красный костный мозг. - Совокупность костей, хрящей и укрепляющих их
связок. - Вещества, которые обеспечивают твёрдость кости.
- Химический элемент, входящий в состав костей.
- Наружный слой кости.
- Красный костный ………… .
- Свойство кости, которое зависит от органических
веществ. - Разновидность соединительной ткани, из которой
образован скелет.
Кто первым разгадает кроссворд,
поднимите руку. Вас ожидает приз! После ответа
“остеология” учащиеся проверяют кроссворд по
слайду. <Слайд 18>.
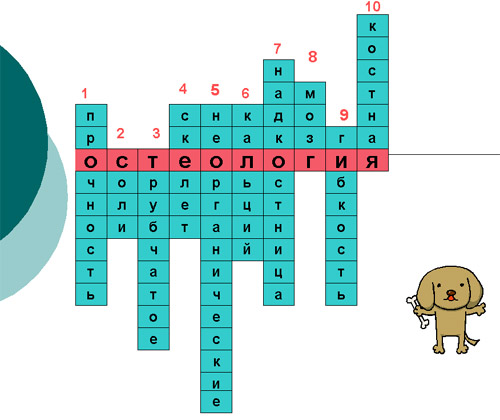
Слайд 18
– А как вы думаете, что означает слово
“остеология”?
– Учение о костях.
Победителям вручается приз – молоко.
– Как вы думаете, изменяется ли состав
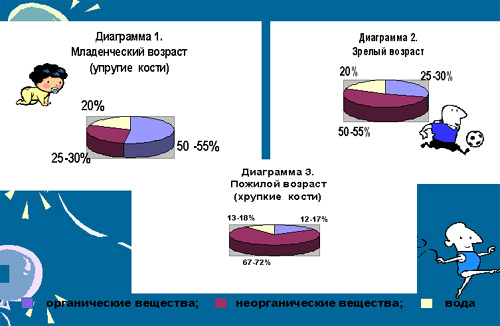
костей с возрастом? Каким образом? Рассмотрим
диаграммы “Возрастные изменения состава
костей”. <Слайд 19>.
Слайд 19
С возрастом увеличивается содержание
в кости неорганических веществ и уменьшается
содержание органических.
– Почему у детей часто встречаются
искривления костей, а у пожилых людей переломы?
– Почему в вашем возрасте нужно
постоянно следить за осанкой?
– Детские кости достаточно гибкие, и
неправильная осанка может привести к
искривлению позвоночника. В нашей школе по
данным медосмотра у 36 учащихся нарушение осанки,
в среднем звене – 18 человек уже испортили свою
осанку. Не попадайте в их число! Здоровье – самое
большое богатство человека, и его нужно беречь
смолоду. Установлено, что умеренная нагрузка на
кость увеличивает её прочность, поэтому очень
важно заниматься физической культурой. Здоровье
кости зависит от многих факторов, немаловажное
значение имеет сбалансированное питание. Об этом
расскажет учитель биологии. <Слайд 20>.

Слайд 20
Учитель биологии. Выдающийся
русский анатом П.Ф. Лесгафт проделал интересный
опыт. Он кормил четыре группы щенков разной
пищей: молочной, мясной, смешанной и
растительной. В костях щенков, которых кормили
молоком и мясом, соотношение неорганических и
органических веществ было примерно 1:1. Несколько
меньше неорганических веществ в кости при
смешанном питании, и особенно при питании
растительной пищей, где это соотношение
выражается 1:2. При недостатке неорганических
веществ в кости, а именно солей фосфора и кальция,
развивается заболевание, которое носит название
– рахит. Соли не усваиваются из-за недостатка
витамина D и солнечного света. В результате в
такой кости соотношение неорганических веществ
к органическим составляет 1:4, тогда как в
нормальной кости 3:1. Кости ребенка, страдающего
рахитом, мягкие, гибкие. Кости черепа, таза,
грудной клетки, нижних конечностей
деформируются. Профилактикой такого заболевания
служит правильное сбалансированное питание,
направленное на нормализацию нарушенных
обменных процессов. Необходимо вводить в питание
овощные продукты, белки и жиры, также употреблять
фруктовые и овощные соки, крупяные каши, яйца и
витамины группы B и D. Все перечисленные продукты
представлены на нашей выставке здорового
питания.
VI. Подведение итогов урока.
Подведем итог урока. Как вы считаете,
цель урока нами достигнута? Если да, то ответьте
на вопрос: “Так от чего же зависят свойства
кости?”.
– Свойства кости определяются
физико-химическим единством состава и строения.
<Слайд 21>.

Слайд 21
VI. Домашнее задание: стр. 93, ответить
на вопросы и найти дополнительную информацию об
опорно-двигательной системе под рубрикой “Это
интересно”.
А сейчас заполните лист учета,
поставьте себе оценку за урок, а так же напишите
отзыв об интегрированном уроке.
VII. Заключение, просмотр фрагмента
фильма, вручение подарков.
Учитель химии. На память об этом
уроке мы угощаем вас творожными сырками.
Победителю викторины мы вручили молоко. Как вы
думаете, почему мы выбрали такие подарки?
– Молочные продукты содержат кальций,
он необходим для укрепления костей.
Надеемся, что старания химиков и
биологов не напрасны. Следите за своей осанкой,
занимайтесь физической культурой и правильно
питайтесь. Желаем, чтобы ваши косточки были
здоровы, а вы были всегда такими гибкими и
пластичными.
Урок заканчивается демонстрацией фрагмента
фильма, где показана красота и пластичность
танца или спортивных упражнений (приложение 4).
Источник
