Какое свойство альдегидов лежит в основе реакции серебряного зеркала

Очень наглядным является опыт с красивым эффектом образования на стекле зеркального покрытия. Для этой реакции необходимо запастись опытом и терпением. В этой статье вы узнаете о необходимых реактивах и особенностях подготовки оборудования, а также увидите, по каким уравнениям реакций протекает этот процесс.
Суть реакции серебряного зеркала — в образовании металлического серебра в результате окислительно-восстановительной реакции при взаимодействии аммиачного раствора серебряного оксида в присутствии альдегидов.
«Серебряное зеркало» (пробирка слева)
[Wikipedia]
Для создания стойкого серебристого слоя понадобится:
- стеклянная колба емкостью до 100 мл;
- раствор аммиака (2,5—4%);
- нитрат серебра (2%);
- водный раствор формальдегида (40%).
Вместо растворов аммиака и нитрата серебра можно взять готовый реактив Толленса — аммиачный раствор оксида серебра. Для его создания нужно добавить 1 грамм нитрата серебра в 10 капель воды (если жидкость будет храниться долго, надо поместить ее в темное место или в стеклянную емкость с темными стенками). Непосредственно перед опытом раствор (около 3 мл) надо смешать в пропорции 1:1 с 10%-ным водным раствором гидроксида натрия. Серебро может выпасть в осадок, поэтому его разводят, медленно добавляя аммиачный раствор. Рекомендуем провести еще один зрелищный опыт с аммиачным раствором и напечатать «химическую фотографию».
Реакция проводится при комнатной температуре. Обязательное условие успешного финала — это идеально чистые и гладкие стенки стеклянного сосуда. Если на стенках будут малейшие частички загрязнений, осадок, получаемый в результате опыта, станет рыхлым слоем черного или темно-серого цвета.
Для очистки колбы нужно использовать разные виды растворов щелочей.Так, для обработки можно взять раствор едкого натра, который после очистки приходится смывать дистиллированной водой. Промывать колбу от чистящего средства необходимо много раз.
Почему так важна чистота сосуда
Дело в том, что коллоидные частицы серебра, образующиеся в конце опыта, должны прочно сцепиться с поверхностью стекла. На его поверхности не должно быть жиров и механических частиц. Дистиллированная вода не содержит солей и идеально подходит для финишной очистки колбы. Ее можно приготовить в домашних условиях, но проще купить готовую жидкость.
Уравнение реакции серебряного зеркала:
Ag₂O + 4 NH₃·Н₂О ⇄ 2[Ag(NН₃)₂]ОН + 3Н₂О,
где [Ag(NН₃)₂]ОН — это гидроксида диамминсеребра, получившийся при растворении оксида металла в водном растворе аммиака.
Молекула комплекса диамминсеребра
[Wikipedia]
Важно! Реакция работает при слабых концентрациях аммиака — внимательно соблюдайте пропорции!
Так протекает окончательный этап реакции:
R (какой-либо альдегид)-CH=O + 2[Ag(NH₃)₂]OH → 2Ag (коллоид серебра, выпавший в осадок) ↓ + R-COONH₄ + 3NH₃ + H₂O
Второй этап реакции лучше проводить, аккуратно нагревая колбу над пламенем горелки — это увеличит шансы, что опыт пройдет успешно.
Что может показать реакция серебряного зеркала
Эта интересная химическая реакция демонстрирует не только определенные состояния вещества — с ее помощью можно выполнить качественное определение альдегидов. То есть подобная реакция решит вопрос: есть ли в растворе альдегидная группа или нет.
Общая структурная формула альдегидов
[Wikipedia]
Например, в подобном процессе можно узнать, что содержится в растворе: глюкоза или фруктоза. Глюкоза даст положительный результат — получится «серебряное зеркало», а фруктоза содержит кетоновую группу и получить осадок серебра нельзя. Для того чтобы провести анализ, вместо раствора формальдегида необходимо добавлять 10%-ный раствор глюкозы. Рассмотрим, почему и как растворенное серебро превращается в твердый осадок:
2[Ag(NH₃)₂]OH + 3H₂O + C₆H₁₂O₆ (глюкоза) = 2Ag↓+ 4NH₃∙H₂O + C₆H₁₂O₇ (образуется глюконовая кислота).
Источник
Альдегиды – летучие жидкости органического состава, являющиеся продуктом неполного окисления спиртов. Карбонильная группа
в молекулах альдегидов связана с одним атомом водорода и одной группой R.
Не часто встречаются в природе в отдельном виде, но, несомненно, играют важную роль в физиологических процессах растений и животных.
Общая формула альдегидов CnH2nO.
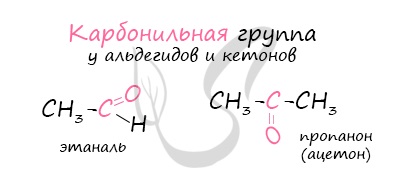
Многие альдегиды имеют специфический запах. Высшие альдегиды, в особенности непредельные, используются в пищевой промышленности и парфюмерии.
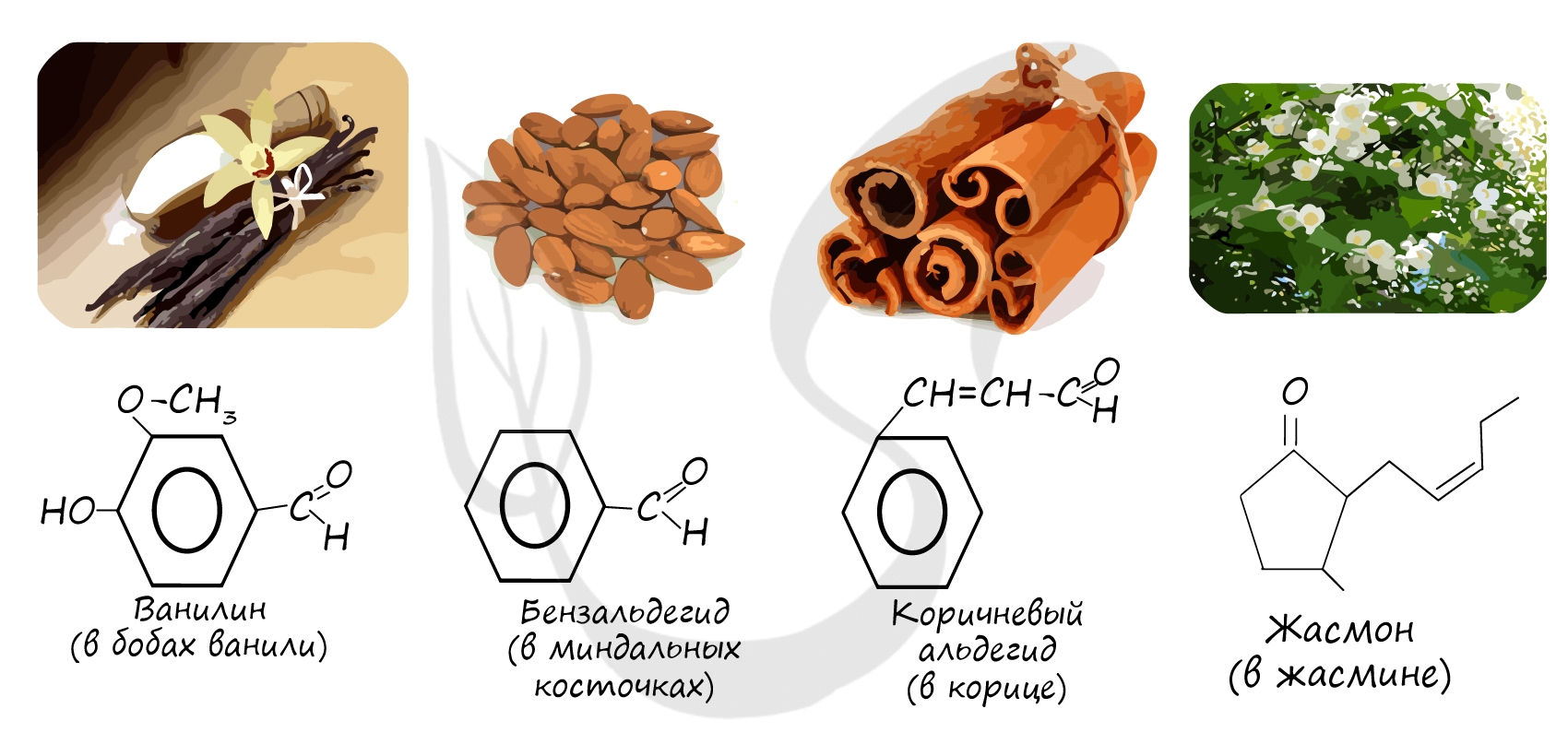
Номенклатура и изомерия альдегидов
Названия альдегидов формируются путем добавления суффикса “аль” к названию алкана с соответствующим числом атомов углерода: метаналь,
этаналь, пропаналь, бутаналь, пентаналь и т.д.
Вы можете встретить их молекулярные формулы, где группа OH записана наоборот – HO. Например: метаналь – HCHO, этаналь –
CH3CHO, пропаналь – C2H5CHO. Это делают специально для того, чтобы их было легче отличить от спиртов.
Многие альдегиды имеют тривиальные названия. Наиболее известные: метаналь – формальдегид, этаналь – ацетальдегид. Замечу, что формалином
называется 40% раствор формальдегида.
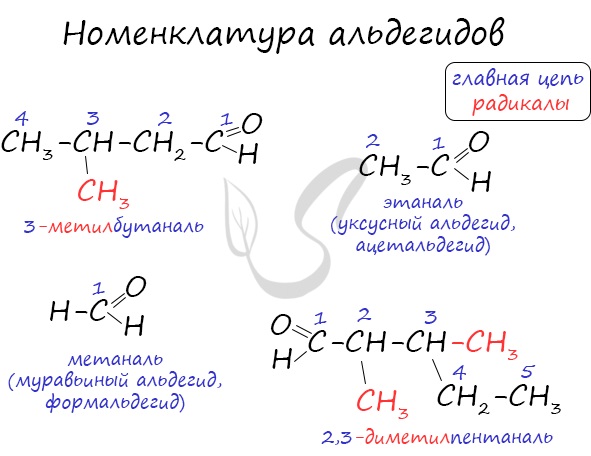
Для альдегидов характерна структурная изомерия: углеродного скелета, межклассовая изомерия с кетонами.
Получение альдегидов и кетонов
- Окисление спиртов
- Пиролиз солей карбоновых кислот
- Каталитическое дегидрирование спиртов
- Реакция Кучерова
- Гидролиз дигалогеналканов
- Окисление метана
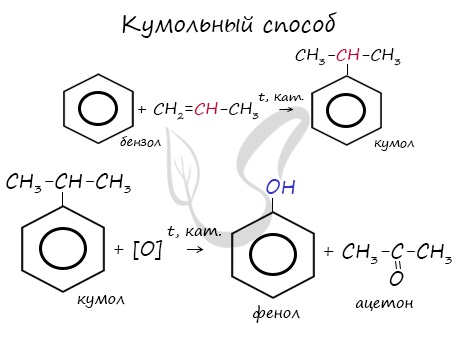
- Кумольный способ получения ацетона (и фенола)
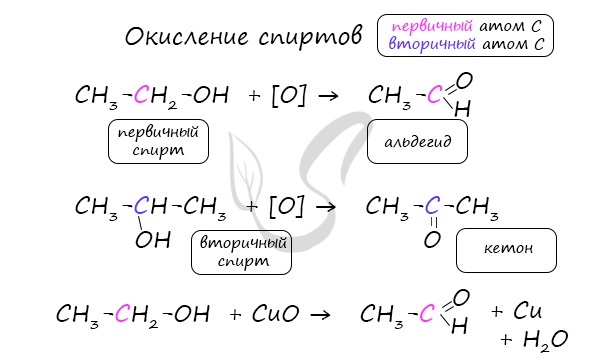
Важно заметить, что при окислении первичных спиртов образуются альдегиды, при окислении вторичных спиртов – кетоны.
Окисление с помощью оксида меди относится к лабораторным способам получения альдегидов.
Этот способ также просто осуществить в лабораторных условиях. При пиролизе (нагревании без доступа кислорода) кальциевых или
бариевых солей карбоновых кислот возможно получение кетонов.

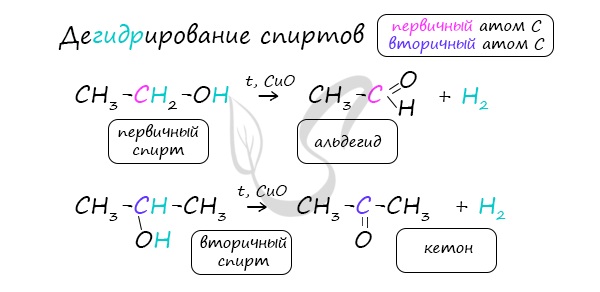
В присутствии катализатора и при нагревании спиртов от гидроксогруппы и прилежащего к ней атома углерода отщепляется по
атому водорода. В результате образуется карбонильная группа.
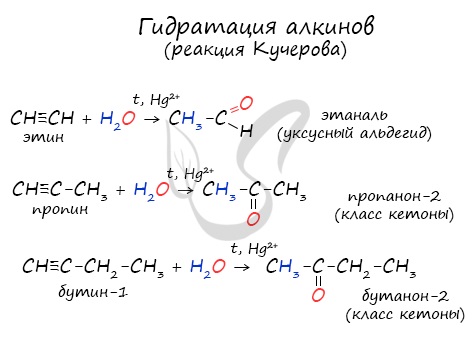
Реакцией Кучерова называют гидратацию алкинов в присутствии солей двухвалентной ртути.
В результате такой реакции ацетилен превращается в уксусный альдегид. Все остальные его гомологи: пропин, бутин, пентин и т.д. превращаются в
соответствующие кетоны.
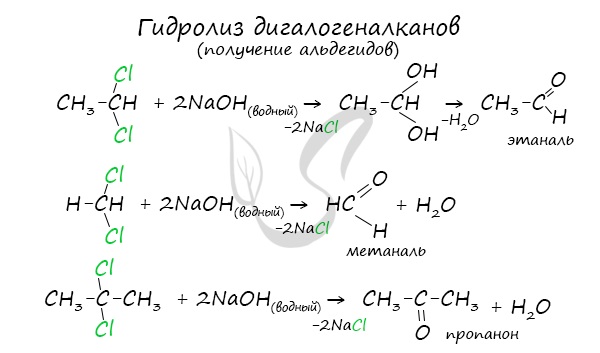
Для получения альдегида два атома галогена должны находиться у первичного атома углерода, для получения кетонов – у вторичного.
В результате такого гидролиза образуются двухатомные спирты, в которых две OH-группы прилежат к одному атому углерода. Такие соединения неустойчивы
и распадаются на карбонильное соединение (альдегид или кетон) и воду.
В промышленности окислением метана при температуре 500 °C и в присутствии катализатора получают формальдегид.

В прошлой теме, посвященной фенолам, мы касались данного способа. В результате такой реакции образуется не только фенол, но и ацетон.
Химические свойства альдегидов и кетонов
Запомните, что для альдегидов и кетонов характерны реакции присоединения по карбонильной группе. Это является важным отличием альдегидов от карбоновых кислот, для которых реакции присоединения не характерны.
- Реакции присоединения
- Окисление альдегидов
Для понимания механизма реакции важно вспомнить об электроотрицательности. В карбонильной группе кислорд, как более электроотрицательный
элемент, тянет электронную плотность на себя от углерода. На атоме кислорода возникает частичный отрицательный заряд (δ-), а на атоме
углерода частичный положительный (δ+).
Основы школьного курса физики подсказывают, что отрицательный заряд притягивает положительный: именно так и будет происходить
при присоединении различных молекул к карбонильной группе альдегидов и кетонов.
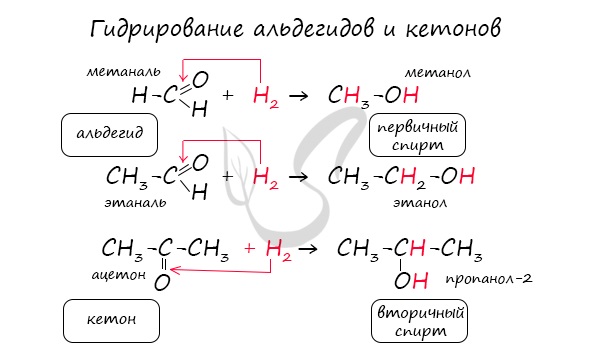
Реакция гидрирования альдегидов происходит по типу присоединения, сопровождается разрывом двойной связи в карбонильной группе.
Гидрирование альдегидов приводит к образованию первичных, а гидрирование кетонов – вторичных спиртов.
В результате полного окисления, горения, образуется углекислый газ и вода.
2CH3CHO + 5O2 → 4CO2 + 4H2O
Альдегиды легко окисляются до карбоновых кислот в лабораторных условиях. Это осуществляется с помощью известной реакции
серебряного зеркала. Данная реакция является качественной для альдегидов.
Кетоны, в отличие от альдегидов, в реакции окисления не вступают.

Обратите особое внимание, что при написании реакции с аммиачным раствором серебра в полном виде, правильнее будет указать не кислоту, а ее аммиачную соль. Это связано с тем, что выделяющийся аммиак, который обладает основными свойствами, реагирует с кислотой с образованием соли

Важно заметить, что при окислении метаналя, образовавшаяся муравьиная кислота тут же окисляется до угольной кислоты, которая
распадается на углекислый газ и воду. Это связано с интересным фактом – наличием альдегидной группы у муравьиной кислоты.

Окисление также возможно другим реагентом – гидроксидом меди II. Эта реакция также относится к качественным для
альдегидов, в результате образуется кирпично-красный осадок оксида меди I.

© Беллевич Юрий Сергеевич 2018-2020
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение
(в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов
без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования,
обратитесь, пожалуйста, к Беллевичу Юрию.
Источник
Реакция серебряного зеркала — это красивое название химической реакции, результатом которой является выпадение тонкого слоя серебра на стенках того сосуда, где проходил процесс. Когда-то так и обрабатывались все поверхности, где нужен был зеркальный налет.
Сейчас этот способ получения тонкого металлического налета на стекле или керамике применяется только в том случае, если необходимо создать токопроводящий слой на диэлектриках, а также при производстве оптики для телескопов, фотоаппаратов и т. п. Использовать эту реакцию можно и для получения чистого серебра. Столь поэтичное название простой химической реакции основано на ажиотаже, который возникает там, где речь заходит о драгоценных металлах — золоте и серебре.
Как провести реакцию в домашних условиях
Для того чтобы провести восстановление серебра из его оксида не в лабораторных условиях, необходимо в воде растворить азотнокислое серебро. Взять его можно в аптеке. Это ляписный карандаш. Воду лучше использовать дистиллированную. Получить ее можно простой конденсацией воды, испаряющейся из кипящего чайника. Если исходить из полулитровой емкости, то в таком количестве раствора азотнокислого серебра необходимо растворить еще нашатырный спирт (1 ч. л.). Сюда же нужно добавить 2-3 капли формальдегида — формалина.
Все реактивы вступают в реакцию не сразу, поэтому взболтайте как следует раствор и оставьте его в покое примерно на сутки. Если все пройдет успешно, то за этот срок ваша банка покроется тонким металлическим слоем. Таким же слоем покроется тот предмет, который вы поместите в банку.
Иногда что-то идет неправильно и вместо зеркала реакция дает серые осажденные хлопья. Это говорит о том, что реактивы были не совсем чистые. Чаще всего претензии нужно предъявлять к воде и чистоте посуды. Особенно следует обратить внимание на кислотность воды, поскольку больше всего неожиданностей происходит в щелочной среде.
Индикаторная функция реакции
С помощью этой реакции определяют наличие в растворе альдегидов. К этой группе относятся такие органические вещества, которые имеют альдегидную группу. Иначе их называют спиртами, лишенными водорода. Присутствие альдегида в растворе и дает эффект зеркала.
Аммиачный раствор оксида серебра используется для определения моносахаридов и дисахаридов. К первой группе относится глюкоза во всех ее изомерных состояниях, ко второй — лактоза и мальтоза. Особенно реакция серебряного зеркала характерна для глюкозы, что и нашло свое отражение в методах выявления глюкозы и фруктозы.
Несмотря на сходство этих веществ и на то, что фруктоза изомерна глюкозе, они все же разные. В открытой форме альдегидная группа присутствует только у глюкозы. Соответственно, осаждаться серебро будет только в присутствии глюкозы, фруктоза же такой реакции не даст. Но в щелочной среде и фруктоза может дать положительную реакцию.
Таким образом, оксид серебра как реактив может быть применен в качестве индикатора наличия в растворе определенной группы веществ. Кроме того, с помощью описанной реакции вы можете получить чистое серебро, серебряное зеркало и пластинку, с двух сторон покрытую металлическим налетом, что не только забавно, но и часто полезно.
Источник
Добрый день, дорогие подписчики и гости моего канала. Сегодня вас ждет еще одна статья из цикла «школьный курс химии». На написание этой статьи, меня вдохновили пособия для подготовки учеников старшей школы к ЕГЭ, в которых основные классы органических соединений описаны очень слабо и приведены далеко не все реакции встречающиеся на экзамене. В сегодняшней статье, я постараюсь, как можно более подробно разобрать два класса органических веществ – Альдегиды и Кетоны. И начнем мы как всегда с определений.
Альдегиды – это органические вещества, которые содержат карбонильную группу (=С=O), соединенную с атомом водорода и углеводородным радикалом.
Таким образом, общая формула альдегидов:
Кетоны — это органические вещества, в молекулах которых карбонильная группа (=С=O) связана с двумя углеводородными радикалами.
Общая формула кетонов:
Таким образом, карбонильная группа (=С=O) определяет принадлежность вещества к классу альдегидов или кетонов. Частный случай фунциональной карбонильной группы – это альдегидная группа (-COH) и она уже определяет принадлежность вещества лишь к классу альдегидов.
Гомологический ряд альдегидов следующий:
Гомологический ряд кетонов несколько сложнее, в виду изомерии, однако его можно представить так:
Как вы видете, всем известный растворитель краски ацетон, является простейшим кетоном.
Ацетон – это бесцветная летучая жидкость с характерным запахом. В последнее время он широко применяется в различных сферах производства, таких как:
– Синтез поликарбонатов и полиуретанов.
– Производство эпоксидных смол.
– Производство лаков.
– Производство взрывчатых веществ.
– Производство лекарственных препаратов.
– Используется при экстракции многих растительных веществ.
Так же, более подробно стоит поговорить и о некоторых простейших представителях класса альдегидов.
Формальдегид (от лат. formica — «муравей») — это бесцветный газ с резким запахом, хорошо растворимый в воде и других органических растворителях, очень ядовит. Его применяют для:
– Производства фенолформальдегидных пластмасс.
– Для производства многих лекарственных препаратов, например уротропина. Кстати, спресованый в виде брикетов уротропин применяют в качестве горючего (сухой спирт).
– Раствор формальдегида в воде называют формалином. Его используют для хранения биопрепаратов, протравливания семян перед посевом, дубления кож.
Ацетальдегид (Уксусный альдегид) – это летучая жидкость, хорошо растворимая в воде, с характерным запахом. Основные сферы применения уксусного альдегида:
– Производство уксусной кислоты.
– Получение ацетатного волокна.
– Получение альдегидных полимеров (различных пластмасс).
Получение альдегидов и кетонов:
Существует большое колличество способов получения альдегидов и кетонов перечислим некоторые из них.
1. Окисление спиртов на медном катализаторе:
C2H5OH + CuO → CH3CHO + Cu + H2O
Окисление вторичных спиртов по этому же методу, приводит к образованию кетонов:
2. Реакция Кучерова.
При гидратации ацетилена получается уксусный альдегид:
При гидратации любых других алкинов получаются кетоны:
3. При окисление вторичных спиртов перманганатом калия получаем кетоны:
5CH3CH(OH)CH3 + 2KMnO4 + 3H2SO4 = CH3-C(O)-CH3 + K2SO4 + 2MnSO4 + 8H2O
4. В промышленности формальдегид получают путем окисления метана при 500 градусах Цельсия, с участием различных катализаторов.
CH4 + O2 = H-COH + H2O
Химические свойства Альдегидов и Кетонов:
1. Взаимодействие с водородом (Гидрирование)
Слово Альдегиды, происходит от латинских слов «alcohol dehydrogenatus» – «алкоголь дегидрированый» или «спирт лишенный водорода», а дегидрированый продукт способен вернуть себе водород. Таким образом альдегиды востанавливаются до первичных спиртов, а кетоны до вторичных:
2. Гидратация.
Данная реакция характерна только для формальдегида и ацетальдегида.
Для кетонов данная реакция не характерна.
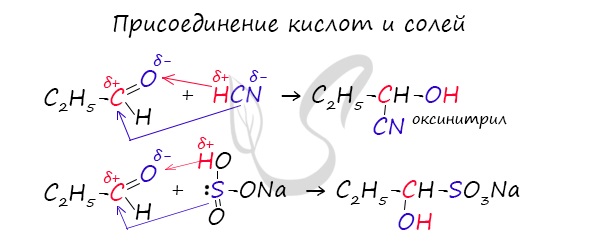
3. Присоединение синильной кислоты:
Кстати, необходимо знать, что синильная кислота или же цианистоводородная кислота – это бесцветная, очень летучая, легкоподвижная ядовитая жидкость, имеющая характерный запах горького миндаля.
4. Присоединение спиртов:
5. Взаимодействие с гидросульфитом натрия:
Данная реакция является качественной, так как образующаяся в результате нее соль выпадает в виде осадка.
6. Реакция «серебряного зеркала».
Это взаимодействие альдегида с аммиачным раствором оксида серебра или реактивом Толленса.
Данную реакцию можно записать так:
Однако, по факту кислота не может существовать с образовавшимся раствором аммиака, поэтому правильнее будет записать ее таким образом:
Данная реакция является качественной и для других веществ содержащих альдегидную группу, например для муравьинной кислоты, ее эфиров или для глюкозы.
Кетоны в реакцию серебряного зеркала не вступают.
7. Взаимодействие со свежеполученым осадком гидроксида меди II.
Эта реакция так же не характерна для кетонов.
Для альдегидов, эту реакцию можно записать так:
В результате реакции сначала произойдет образование желтого осадка, который затем постепенно начнет приобретать красно – оранжевый оттенок.
8. Взаимодействие с подкисленным раствором перманганата калия.
Надо отметить, что окисление формальдегида идет до углекислого газа:
HCOH + KMnO4 + H2SO4 = K2SO4 + MnSO4 + CO2 + H2O
Во всех остальных случаях образуется карбоновая кислота:
5CH3COH + 2KMnO4 + 3H2SO4 = 5CH3COOH + 2MnSO4 + K2SO4 + 3H2O
9. Реакция Тищенко.
Диспропорционирование альдегида – получение сложного эфира из альдегида – в присутствии алкоголята алюминия (1906 г.)
10. Реакция Фаворского.
Конденсация карбонильных соединений с алкинами с образованием ацетиленовых спиртов:
11. Реакция Бутлерова.
Получение углеводов из формальдегида в присутствие известкового раствора:
12. Галогенирование по альфа-атому углерода:
13. Полимеризация.
Полимериза́ция — это процесс образования высокомолекулярного вещества (полимера) путём многократного присоединения молекул низкомолекулярного вещества (мономера) к активным центрам в растущей молекуле.
Кетоны в эти реакции не вступают, а среди альдегидов имеет смысл лишь полимеризация формальдегида:
14. Поликонденсация.
Поликонденсация — процесс синтеза полимеров из органических соединений, обычно сопровождающийся выделением низкомолекулярных побочных продуктов (чаще всего воды).
Нам, особенно интересна поликонденсация формальдегида с фенолом, приводящая к образованию фенолформальдегидной смолы:
15. Реакция горения.
2 CH3COH + 5 O2 = 4 CO2 + 4 H2O
Вот пятнадцать химических реакций, которые могут встречаться на ЕГЭ по теме альдегидов. А я сейчас держу пособие для подготовки к ЕГЭ, где химических реакций перечислено только пять. К тому же забыли написать способы получения альдегидов. Так что качественно ищите материалы для подготовки к экзаменам.
Сдающим ЕГЭ, так же рекомендую к прочтению:
Карбоновые кислоты.
Фенолы.
То, что нужно знать о Спиртах.
Высоких балов тем, кто сдает ЕГЭ!
Источник
