Какое количество вещества содержится в одном грамме воды

Цель: Познакомить учащихся с понятиями «количество вещества», «молярная масса» дать представление о постоянной Авогадро. Показать взаимосвязь количества вещества, числа частиц и постоянной Авогадро, а также взаимосвязь молярной массы, массы и количества вещества. Научить производить расчёты.
Тип урока: урок изучения и первичного закрепления новых знаний.
Ход урока
I. Организационный момент
II. Проверка д/з по теме: «Типы химических реакций»
III. Изучение нового материала
1. Количество вещества – моль
Вещества вступают в реакцию в строго определённых соотношениях. Например, чтобы получить вещество вода нужно взять столько водорода и кислорода, чтобы на каждые две молекулы водорода приходилась одна молекула кислорода:
2Н2 + O2 = 2Н2О
Чтобы получить вещество сульфид железа, нужно взять столько железа и серы, чтобы на каждый атом железа приходился один атом серы.
Fe + S = FeS
Чтобы получить вещество оксид фосфора, нужно взять столько молекул фосфора и кислорода, чтобы на четыре молекулы фосфора приходилось пять молекул кислорода.
4P + 5O2 = 2P2O5
Определить количество атомов, молекул и других частиц на практике невозможно – они слишком малы и не видны невооружённым глазом. Для определения числа структурных единиц (атомов, молекул) в химии применяют особую величину – количество вещества (v – ню). Единицей количества вещества является моль.
- Моль – это количество вещества, которое содержит столько структурных частиц (атомов, молекул), сколько атомов содержится в 12 г углерода.
Экспериментально установлено, что 12 г углерода содержит 6·1023 атомов. Значит один моль любого вещества, независимо от его агрегатного состояния содержит одинаковое число частиц – 6· 1023 .
- 1 моль кислорода (O2) содержит 6·1023 молекул.
- 1 моль водорода (Н2) содержит 6·1023 молекул.
- 1 моль воды (Н2O) содержит 6·1023 молекул.
- 1 моль железа (Fe) содержит 6·1023 молекул.
Задание: Используя полученную информацию, ответьте на вопросы:
а) сколько атомов кислорода содержится в 1 моле кислорода?
– 6·1023·2 = 12· 1023 атомов.
б) сколько атомов водорода и кислорода содержится в 1 моле воды (Н2O)?
– 6·1023·2 = 12· 1023 атомов водорода и 6·1023 атомов кислорода.
Число 6·1023 названо постоянной Авогадро в честь итальянского учёного 19 века и обозначается NА. Единицы измерения атомы/моль или молекулы/моль.
2. Решение задач на нахождение количества вещества
Часто нужно знать, сколько частиц вещества содержится в определённом количестве вещества. Или же найти количество вещества по известному числу молекул. Эти расчёты можно сделать по формуле:
где N – число молекул, NА – постоянная Авогадро, v – количество вещества. Из этой формулы можно выразить количество вещества.
Задача 1. Сколько атомов содержится в 2 молях серы?
N = 2·6·1023 = 12·1023 атомов.
Задача 2. Сколько атомов содержится в 0,5 молях железа?
N = 0,5·6·1023 = 3·1023 атомов.
Задача 3. Сколько молекул содержится в 5 молях углекислого газа?
N = 5·6·1023 = 30·1023 молекул.
Задача 4. Какое количество вещества составляет 12·1023 молекул этого вещества?
v = 12·1023/ 6·1023 = 2 моль.
Задача 5. Какое количество вещества составляет 0,6·1023 молекул этого вещества?
v = 0,6·1023/ 6·1023 = 0,1 моль.
Задача 6. Какое количество вещества составляет 3·1023 молекул этого вещества?
v = 3·1023/ 6·1023 = 0,5 моль.
3. Молярная масса
Для химических реакций нужно учитывать количество вещества в молях.
В: Но как на практике отмерить 2, или 2,5 моль вещества? В каких единицах лучше всего измерять массу веществ?
Для удобства в химии используют молярную массу.
Молярная масса – это масса одного моля вещества.
Обозначается – М. Измеряется в г/моль.
Молярная масса равна отношению массы вещества к соответствующему количеству вещества.
где М – молярная масса вещества, v – количество вещества, т – масса вещества.
Молярная масса – величина постоянная. Численное значение молярной массы соответствует значению относительной атомной или относительной молекулярной массы.
В: Как можно найти значения относительной атомной или относительной молекулярной массы?
Мr (S) = 32; M (S) = 32 г/моль – что соответствует 1 молю серы
Мr (Н2О) = 18; М (Н2О) = 18 г/моль – что соответствует 1 молю воды.
Следует отличать понятия «моль молекул» и «моль атомов».
Например, Н2О соответствует одному молю молекулы воды.
В: Сколько молей атомов кислорода и водорода содержится в одном моле молекулы воды?
В одном моле молекулы воды содержится два моля атомов водорода и один моль атомов кислорода.
4. Решение задач на нахождение массы вещества
Задача 7. Определить массу 0,5 моль железа.
m = 0,5·56 = 28 г
Задача 8. Определить массу 0,25 моль меди
m = 0,25·64 = 16 г
Задача 9. Определить массу 2 моль углекислого газа (СO2)
m = 2·44 = 88 г
Задача 10. Сколько молей оксида меди – CuО составляют 160 г оксида меди?
v = 160 / 80 = 8 моль
Задача 11. Сколько молей воды соответствуют 30 г воды
v =30/18 = 1,66 моль
Задача 12. Сколько молей магния соответствует его 40 граммам?
v = 40 /24 = 1,66 моль
IV. Закрепление
Фронтальный опрос:
- Что такое количество вещества?
- Чему равен 1 моль любого вещества?
- Что такое молярная масса?
- Отличается ли понятия «моль молекул» и «моль атомов»?
- Объясните на примере молекулы аммиака NН3.
- Зачем необходимо знать формулы при решении задач?
Задачи:
- Сколько молекул содержится в 180 граммах воды?
- Сколько молекул составляет 80 г углекислого газа?
V. Домашнее задание
Изучить текст параграфа, составить две задачи: на нахождение количества вещества; на нахождение массы вещества.
Литература:
- Гара Н.Н. Химия. Уроки в 8 классе: пособие для учителя. _ М.: Просвещение, 2009.
- Рудзитес Г.Е., Фельдман Ф.Г. Химия. 8 класс.: Учебник для общеобразовательных учебных учреждений – М.: Просвещение, 2009.
Источник
Решениие задач по химии на закон Авогадро
Задача 53.
Сопоставить числа молекул, содержащихся в 1г NH3 и в 1г N2. В каком случае и во сколько раз число молекул больше?
Решение:
В одном моле любого вещества содержится 6,02 . 1023 молекул этого вещества.
Рассчитаем содержание количества вещества в 1г NH3 и N2 по формуле:
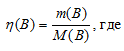
 (B) – количество вещества (В);
(B) – количество вещества (В);
m(B)- масса вещества (В);
M(B) – Молярная масса вещества (В).
М(NH3) = 17г/моль, M(N2) = 28г/моль.
Тогда
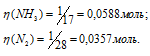
Число молекул NH3 больше числа молекул N2, так как  (NH3) >
(NH3) > (N2) . Теперь рассчитаем, во сколько раз число молекул NH3 больше числа молекул N2:
(N2) . Теперь рассчитаем, во сколько раз число молекул NH3 больше числа молекул N2:
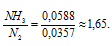
Ответ: в 1,65 раз число молекул NH3 больше числа молекул N2.
Задача 54.
Выразить в граммах массу одной молекулы диоксида серы.
Решение:
Находим молекулярную массу диоксида серы:
M(SO2) = 32 + (16 . 2) = 64г/моль.
Молекулярная масса численно составляет массу одного моля вещества, а значит, вес одного моля численно равен молекулярной массе и составляет 64г. Известно, что в одном моле любого вещества содержится 6,02 . 1023 молекул данного вещества. Исходя из этого, рассчитаем массу в граммах одной молекулы диоксида серы:
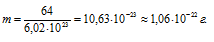
Ответ: масса одной молекулы диоксида серы равна.
Задача 55.
Одинаково ли число молекул в 0,001кг Н2 и в 0,001кг О2? В 1 моле Н2 и в 1 моле 02? В 1л Н2 и в 1л О2 при одинаковых условиях?
Решение:
Молекулярные массы водорода и кислорода равны соответственно 2г/моль и 32г/моль. Отсюда находим количество водорода и кислорода, зная их массы:
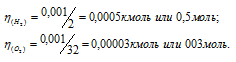
Один моль любого вещества содержит 6,02 .1023 молекул. Следовательно, в 0,001кг водорода и в 0,001кг кислорода содержится разное число молекул:

Так как имеется по одному молю водорода и кислорода, то количество молекул веществ будет одинаково:
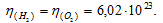
Согласно закону Авогадро в равных объёмах любых газов, взятых при одинаковых условиях, содержится одинаковое число молекул, Один моль любого газа занимает 22,4л, В которых содержится 6,02 . 1023 молекул. Отсюда рассчитаем количество молекул вещества, содержащихся в 1л водорода и в 1л кислорода:
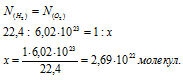
Ответ: а) в 0,001кг водорода и в 0,001кг кислорода содержится разное число молекул; б) в одном моле водорода и в одном моле кислорода содержится одинаковое число молекул: в) в одном литре водорода и в одном литре кислорода содержится одинаковое число молекул.
Задача 56.
Сколько молекул содержится в 1,00 мл водорода при нормальных условиях?
Решение:
Согласно закону Авогадро в равных объёмах любых газов, взятых при одинаковых условиях, содержится одинаковое число молекул, Один моль любого газа занимает 22,4л, В которых содержится 6,02 .1023 молекул. Отсюда рассчитаем количество молекул вещества, содержащихся в 1мл водорода из пропорции:
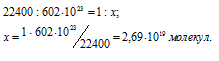
Ответ: 2,69 .1019 молекул.
Задача 57.
Какой объем при нормальных условиях занимают 27 .1021 молекул газа?
Решение:
Согласно закону Авогадро в равных объёмах любых газов, взятых при одинаковых условиях, содержится одинаковое число молекул, Один моль любого газа занимает 22,4л, В которых содержится 6,02 . 1023 молекул. Отсюда находим какой объём при нормальных условиях занимают 27 .1021 молекул газа, составив пропорцию:
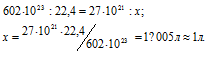
Ответ: V=1л.
Задача 58.
Каково соотношение объемов, занимаемых 1 молем О2 и 1 молем О3 (условия одинаковые)?
Решение:
Согласно закону Авогадро в равных объёмах любых газов, взятых при одинаковых условиях, содержится одинаковое число молекул, Один моль любого газа занимает 22,4л. Следовательно соотношение объёмов, занимаемых одним молем О2 и одним молем О3 иметь вид:
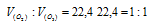
Ответ: 1:1
Задача 59.
Взяты равные массы кислорода, водорода и метана при одинаковых условиях. Найти отношение объемов взятых газов.
Решение:
Согласно закону Авогадро в равных объёмах любых газов, взятых при одинаковых условиях, содержится одинаковое число молекул, Один моль любого газа занимает 22,4л. Мольные массы кислорода, водорода и метана, соответственно равны 32 г/моль; 2г/моль; 16 г/моль.
Так как массы кислорода, водорода и метана одинаковы при одинаковых условиях, то отношение объёмов взятых газов находим из пропорции:
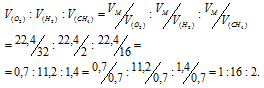
Ответ: 1:16:2.
Задача 60.
На вопрос, какой объем займет 1моль воды при нормальных условиях, получен ответ: 22,4л. Правильный ли это ответ?
Решение:
Согласно закону Авогадро в равных объёмах любых газов, взятых при одинаковых условиях, содержится одинаковое число молекул, Один моль любого газа занимает 22,4л. Так как вода при нормальных условиях находится в жидкой, а не в газообразной фазе, то ответ, что 1моль воды займёт 22,4л не правильный. Учитывая, что молярная масса воды равна 18г/моль, а плотность равна единице, то правильный ответ будет равен:
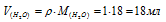
Ответ: 18мл.
Задача 61.
Сколько молекул диоксида углерода находится в 1л воздуха, если объемное содержание СО2 составляет 0,03% (условия нормальные)?
Решение:
При нормальных условиях углекислый газ, содержащийся в 1л воздуха, занимает объём 0,0003л. Зная, что мольный объём любого газа занимает 22,4л, рассчитаем число молей углекислого газа в 0,0003л из пропорции:
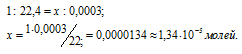
Учитывая, что в одном моле вещества содержится 6,02 . 1023 молекул, находим число молекул в 0,0003л газа:

Ответ: 8,07 .1018 молекул.
Источник
§5.4 Количество вещества. Моль. Молярная масса.
В начале главы мы “записали” уравнение реакции горения метана в виде моделей молекул. На картинке хорошо видно, что для полного протекания реакции на каждую молекулу метана СН4 потребуется израсходовать две молекулы кислорода О2:

В воздухе всегда содержится достаточно кислорода для того, чтобы горение метана протекало именно так, как записано в уравнении реакции. Но представим на минуту, что нам надо сконструировать газовую горелку для подводных работ или двигатель космического корабля. Эти устройства должны работать без доступа атмосферного воздуха. Поэтому в таких конструкциях не обойтись без точного подсчета молекул реагентов, поступающих в зону горения (то есть в химическую реакцию). Например, если в камеру сгорания космического двигателя попадает больше молекул топлива, чем может прореагировать с окислителем, то это ведет к снижению тяги двигателя и к бесполезному расходованию части драгоценного топлива.
Но для начала возьмем не “космическую” реакцию, а что-нибудь попроще. Допустим, мы знаем, что вещества А и Б реагируют между собой с образованием продукта В. Другими словами, нам известно уравнение химической реакции:
А + Б = В
Примером может послужить уже встречавшаяся нам простая реакция:
СаО + Н2О = Са(ОН)2
Остается взять нужные количества А (CaO) и Б (H2O) и провести реакцию. Итак, сколько нужно взвесить А и сколько Б, чтобы реакция прошла до конца и не осталось никаких исходных веществ?
Если мы возьмем одинаковые по весу образцы А и Б, то цели не достигнем – продукт В обязательно будет загрязнен одним из исходных веществ. Почему это произойдет?
Дело в том, что простейшие структурные единицы веществ А и Б состоят из разных наборов атомов – CaO и Н2О.Эти наборы атомов различаются по массе. Значит, в 1 г СаО окажется одно количество частиц, а в 1 г Н2О – другое. При реакции между ними останутся неизрасходованными частицы одного из исходных веществ.
Оксид кальция – ионное соединение и в твердом виде состоит не из молекул (как Н2О), а из набора ионов Ca2+ и O2–. Однако его сокращенная формула СаО по своей сути ничем не отличается от молекулярной формулы – она так же отражает качественный и количественный состав вещества. Поэтому в дальнейшем мы будем называть СаО “молекулой”, а суммарную массу атомов Са и О – “молекулярной массой” этого вещества. Что касается Н2О, то здесь кавычки не нужны – вода действительно состоит из молекул в любом состоянии: твердом, жидком, газообразном.
Для работы химикам удобно брать вещества такими порциями, которые содержали бы одинаковое количество молекул. Допустим, химик взял порцию СаО, в которой содержится N “молекул” этого вещества. Затем берется некая порция воды, в которой тоже N молекул. Смешав эти две порции реагентов, химик получает порцию продукта, в которой будет тоже ровно N “молекул” Са(ОН)2:

Здесь N “молекул” СаО, N молекул Н2О, N “молекул” Са(ОН)2
После окончания реакции не останется ни СаО, ни Н2О – они полностью превратились в Са(ОН)2.
Легко сосчитать определенное количество яблок, конфет или монеток, но молекулы отсчитывать затруднительно. Впрочем, это можно делать путем взвешивания вещества. Например, работники банков знают, что в 1 кг 10-копеечных монет окажется 540 таких монет. То же самое можно проделать с молекулами. Допустим, нам известно, что N молекул весят М г. Достаточно взвесить на весах М г этого вещества, чтобы быть уверенным, что мы отмерили N молекул этого вещества. Но как узнать величину М в граммах?
Масса молекул складывается из масс составляющих ее атомов. Атомные массы (атомные веса) элементов мы можем узнать из Периодической таблицы. Атомный вес Са – 40 а.е.м., а атомный вес кислорода – 16 а.е.м. Следовательно, молекулярный вес (молекулярная масса) СаО составит:
40 а.е.м. (Ca) + 16 а.е.м. (O) = 56 а.е.м. (CaO)
Допустим, мы решили взять для проведения реакции 10 “молекул” СаО и 10 молекул Н2О. Удобно ли нам будет работать с такими малыми количествами вещества? Разумеется, нет.
Тогда попробуем взвесить на весах по миллиону (1000000) молекул каждого реагента. В принципе, можно сосчитать, сколько весит порция из миллиона “молекул” СаО. Мы знаем, что 1 а.е.м. = 1,67.10-27 кг (это значение нам встречалось в таблице 2-1 из главы 2).
Перейдем для удобства из килограммов в граммы. В граммах масса 1 а.е.м. составляет 1,67.10-24 г. Нетрудно умножить эту величину на 56 (число а.е.м. в “молекуле” СаО).
Получим: 56.(1,67.10-24 г) = 93,5.10-24 г. Теперь умножим массу одной молекулы на число самих молекул (миллион). Мы получим вес (в граммах) порции из миллиона “молекул” СаО:
93,5.10-24 г×
1 000 000 = 93,5×
10-18 г.
Если вспомнить, что наибольшая точность обычных лабораторных весов составляет 1 мг (это всего лишь 10-3 г), то обнаружится, что и миллион “молекул” СаО – совсем неудобная “порция” для взвешивания на весах.
Значит, надо выбрать для работы не миллион, а какую-то другую, более удобную порцию из N молекул. Видимо, это число N должно быть намного больше миллиона.
** Попробуем найти такое число молекул (
N), с которым было бы удобно работать. Это может быть не обязательно число молекул именно СаО или Н2О. Число N должно быть таким, чтобы с его помощью было удобно “отмерять” взвешиванием ЛЮБЫЕ молекулы, атомы и вообще частицы, масса которых очень мала (измеряется в атомных единицах массы).
Возьмем одну из таких частиц – протон. Он имеет массу 1 а.е.м. (округленно). Такую же массу имеет нейтрон.
Посчитаем, какое количество протонов (или нейтронов) окажется в 1 г этих частиц. Для этого составим пропорцию:
1 частица (массой 1 а.е.м.) – весит 1,67.10-24 г
N частиц – весят 1 г.
Отсюда:
частиц.
Оказывается, очень удобной является порция из 6.1023 частиц (молекул, атомов, ионов и т.д.). Обозначим ее буквой N (чтобы отличать от любых других порций N. Если N равно именно такому числу частиц (6.1023), то их вес в граммах числено равен весу этих частиц в а.е.м.
Другими словами, чтобы перейти от измерений в а.е.м. к измерениям в граммах, достаточно увеличить шкалу измерений в 6.1023 раз!
6× 1023а.е.м. = 1 г
Число N = 6.1023 является как бы переводным коэффициентом из шкалы а.е.м. в шкалу граммов. Например, молекулярный вес CaO составляет 56 а.е.м. Взвесив на весах 56 г оксида кальция СаО, мы тем самым “отсчитали” 6.1023 структурных единиц (“молекул”) СаО. Чтобы теперь отсчитать для нашей реакции точно такое же количество молекул Н2О, следует взвесить на весах ровно 18 г воды:
1+1 а.е.м (вес двух атомов Н) + 16 а.е.м. (вес одного атома О) = 18 а.е.м. (H2O)
18 а.е.м. .6.1023 = 18 г.
Понятно, что взвесив 18 г воды, мы тем самым берем нужные нам 6.1023 молекул воды.
 Смешав точно 56 г СаО и 18 г Н
Смешав точно 56 г СаО и 18 г Н
2О, мы смешиваем порции веществ, в которых число структурных единиц CaO и H2O абсолютно одинаково. Тем самым мы обеспечиваем полное протекание реакции. В продукте реакции – Са(ОН)2 – не должно остаться непрореагировавших CaO и H2O.
Такие порции из 6.1023 структурных единиц вещества (атомов, молекул, ионов) называются МОЛЕМ вещества. Таким образом, МОЛЬ – это мера количества вещества. Более точное, не округленное количество частиц вещества в 1 моле составляет 6,022045.1023 частиц. С точностью до второго знака после запятой (6,02.1023) эту величину нужно хорошенько запомнить.
МОЛЬ – это КОЛИЧЕСТВО ВЕЩЕСТВА, равное 6,02.1023 структурных единиц данного вещества – молекул (если вещество состоит из молекул), атомов (если это атомарное вещество), ионов (если вещество является ионным соединением).
Примеры:
1 моль (1 М) воды = 6.1023 молекул Н2О,
1 моль (1 М) железа = 6.1023 атомов Fe,
1 моль (1 М) хлора = 6.1023 молекул Cl2,
1 моль (1 М) ионов хлора Cl- = 6.1023 ионов Cl-.
1 моль (1 М) электронов е- = 6.1023 электронов е-.
Теперь мы имеем удобную единицу количества вещества моль, с помощью которой легко отмерять равные порции молекул или атомов простым взвешиванием.
Разумеется, если мы увеличим или уменьшим взятое нами количество воды (18 г) и оксида кальция (56 г) в одинаковое количество раз, то и порции реагирующих молекул уменьшатся или возрастут во столько же раз.
Допустим, 1,8 г воды полностью прореагируют с 5,6 г СаО, а 180 г Н2О тоже без остатка прореагируют с 560 г СаО. Другими словами 0,1 моль воды прореагирует с 0,1 моль СаО, а 10 моль воды прореагируют с 10 моль СаО и т.д.
Как мы видим, масса одного моля какого-нибудь вещества (в граммах) числено совпадает с молекулярной или атомной массой этого вещества (в а.е.м. или в безразмерном выражении – как в случае относительной атомной или молекулярной массы). Это очень удобно для химических расчетов.
Например, молекулярная масса (молекулярный вес) метана CH4 составляет (12 + 4) = 16 а.е.м. Тогда для реакции горения метана:
CH4 + 2O2 = CO2 + 2H2O
справедливо, что из 1 моля метана получаются 2 моля воды и что из 16 г метана получается 2.18 = 36 г воды.
Масса одного моля вещества называется МОЛЯРНОЙ МАССОЙ. Она бозначается буквой М и имеет размерность г/моль. Количество молей вещества n находят из отношения массы m этого вещества (г) к его молярной массе М (г/моль).
Например, число молей в m г воды составляет: n = m/18. Для m г металлического натрия: n = m/23, и так далее.
И наоборот, массу вещества определяют как произведение молярной массы на количество вещества: m = n . M. Так, масса 0,1 моля Na составляет 0,1 моль×23 г/моль = 2,3 г.
Молярная масса численно всегда совпадает с молекулярной массой (или атомной массой – если вещество состоит не из молекул, а из атомов). В таблице 5-1 для иллюстрации приведены молярные массы М для нескольких веществ разного строения.
Таблица 5-1. Молярные массы различных веществ.
Вещество | Молекулярная или атомная масса (округлена) | молярная масса М |
Вода Н 2О | 18 а.е.м | 18 г/моль |
СаО | 56 а.е.м. | 56 г/моль |
Углерод 12С | 12 а.е.м. | 12 г/моль |
Медь Cu | 63,5 a.e.м. | 63,5 г/моль |
Атом хлора Сl | 35,5 а.е.м. | 35,5 г/моль *) |
Ион хлора Cl– | 35,5 а.е.м | 35,5 г/моль |
Молекула хлора Cl 2 | 71 а.е.м | 71 г/моль *) |
*) Атомарный хлор и молекулярный хлор – разные вещества, обладающие разными физическими и химическими свойствами.
Как мы видим, термины “молекулярная масса” и “молярная масса” применимы не только к веществам молекулярного строения, но и к атомарным и ионным веществам. В таблице 5-1 каждая из указанных в правой колонке “порций” вещества содержит 6,02×1023 структурных единиц этих веществ.
Молярная масса М – постоянная величина для каждого конкретного вещества. Без неё не обойтись при вычислении количества молей (n). Однако в дальнейшем для нас основным рабочим инструментом будет именно МОЛЬ вещества.
Термины “моль” и “молекула” отдаленно связаны между собой. Моль происходит от латинского
moles, что означает количество, счетное множество, а также масса. Термин “молекула” является уменьшительной формой этого слова и означает “маленькая масса”. Таким образом моль – это такое количество вещества, которое можно считать “большой массой”, состоящей из 6,02×
1023 “маленьких масс”.
Задачи.
5.7. Пользуясь значениями атомных весов элементов из Периодической таблицы, рассчитайте с точностью до целых чисел молекулярный вес (а.е.м) и молярную массу (г) для следующих веществ: NaF, N
2, NaOH, SO2. Сколько молекул содержится в 1 моле каждого из этих веществ?
5.8. Сколько молей кислорода содержится в 128 г кислорода?
5.9. При грозовых разрядах в атмосфере происходит следующая реакция: N
2 + O2®
NO2. Уравняйте реакцию. Сколько молей кислорода потребуется для полного превращения 1 моля азота в NO2? Cколько это будет граммов кислорода? Сколько граммов NO2 образуется?
5.10. В стакан налили 180 г воды. Сколько молекул воды в стакане? Сколько это молей H
2O?
5.11. Между собой прореагировали 1 моль кальция и 1 моль хлора. Сколько молей CaCl
2 получилось? Какова масса получившегося хлорида кальция CaCl2 ?
** 5.12. Между собой реагируют 4,0 г Ca и 14,2 г Cl
2. Какие вещества и в каком количестве (в молях и в граммах) останутся после окончания реакции?
5.13. Смешали 2 моля водорода и 1 моль кислорода. Смесь взорвали. Сколько молей воды получилось? А сколько граммов?
** 5.14. Смешали 4 г водорода и 64 г кислорода. Смесь взорвали. Сколько граммов воды получилось? Сколько граммов кислорода осталось не израсходованным?
** 5.15 (НГУ). Определите количество вещества (моль) и массу порции пропина C3H4, которая содержит 6,02.1021 атомов углерода. Какова масса одной молекулы пропина?
- В следующий параграф.
_________________
Источник
