Какое количество вещества и сколько молекул содержится в кислороде
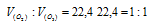
Решениие задач по химии на закон Авогадро
Задача 53.
Сопоставить числа молекул, содержащихся в 1г NH3 и в 1г N2. В каком случае и во сколько раз число молекул больше?
Решение:
В одном моле любого вещества содержится 6,02 . 1023 молекул этого вещества.
Рассчитаем содержание количества вещества в 1г NH3 и N2 по формуле:
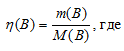
 (B) – количество вещества (В);
(B) – количество вещества (В);
m(B)- масса вещества (В);
M(B) – Молярная масса вещества (В).
М(NH3) = 17г/моль, M(N2) = 28г/моль.
Тогда
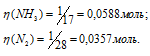
Число молекул NH3 больше числа молекул N2, так как  (NH3) >
(NH3) > (N2) . Теперь рассчитаем, во сколько раз число молекул NH3 больше числа молекул N2:
(N2) . Теперь рассчитаем, во сколько раз число молекул NH3 больше числа молекул N2:
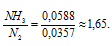
Ответ: в 1,65 раз число молекул NH3 больше числа молекул N2.
Задача 54.
Выразить в граммах массу одной молекулы диоксида серы.
Решение:
Находим молекулярную массу диоксида серы:
M(SO2) = 32 + (16 . 2) = 64г/моль.
Молекулярная масса численно составляет массу одного моля вещества, а значит, вес одного моля численно равен молекулярной массе и составляет 64г. Известно, что в одном моле любого вещества содержится 6,02 . 1023 молекул данного вещества. Исходя из этого, рассчитаем массу в граммах одной молекулы диоксида серы:
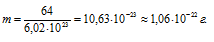
Ответ: масса одной молекулы диоксида серы равна.
Задача 55.
Одинаково ли число молекул в 0,001кг Н2 и в 0,001кг О2? В 1 моле Н2 и в 1 моле 02? В 1л Н2 и в 1л О2 при одинаковых условиях?
Решение:
Молекулярные массы водорода и кислорода равны соответственно 2г/моль и 32г/моль. Отсюда находим количество водорода и кислорода, зная их массы:
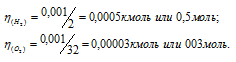
Один моль любого вещества содержит 6,02 .1023 молекул. Следовательно, в 0,001кг водорода и в 0,001кг кислорода содержится разное число молекул:

Так как имеется по одному молю водорода и кислорода, то количество молекул веществ будет одинаково:
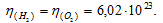
Согласно закону Авогадро в равных объёмах любых газов, взятых при одинаковых условиях, содержится одинаковое число молекул, Один моль любого газа занимает 22,4л, В которых содержится 6,02 . 1023 молекул. Отсюда рассчитаем количество молекул вещества, содержащихся в 1л водорода и в 1л кислорода:
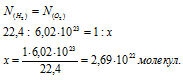
Ответ: а) в 0,001кг водорода и в 0,001кг кислорода содержится разное число молекул; б) в одном моле водорода и в одном моле кислорода содержится одинаковое число молекул: в) в одном литре водорода и в одном литре кислорода содержится одинаковое число молекул.
Задача 56.
Сколько молекул содержится в 1,00 мл водорода при нормальных условиях?
Решение:
Согласно закону Авогадро в равных объёмах любых газов, взятых при одинаковых условиях, содержится одинаковое число молекул, Один моль любого газа занимает 22,4л, В которых содержится 6,02 .1023 молекул. Отсюда рассчитаем количество молекул вещества, содержащихся в 1мл водорода из пропорции:
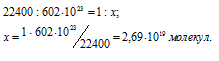
Ответ: 2,69 .1019 молекул.
Задача 57.
Какой объем при нормальных условиях занимают 27 .1021 молекул газа?
Решение:
Согласно закону Авогадро в равных объёмах любых газов, взятых при одинаковых условиях, содержится одинаковое число молекул, Один моль любого газа занимает 22,4л, В которых содержится 6,02 . 1023 молекул. Отсюда находим какой объём при нормальных условиях занимают 27 .1021 молекул газа, составив пропорцию:
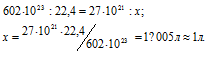
Ответ: V=1л.
Задача 58.
Каково соотношение объемов, занимаемых 1 молем О2 и 1 молем О3 (условия одинаковые)?
Решение:
Согласно закону Авогадро в равных объёмах любых газов, взятых при одинаковых условиях, содержится одинаковое число молекул, Один моль любого газа занимает 22,4л. Следовательно соотношение объёмов, занимаемых одним молем О2 и одним молем О3 иметь вид:
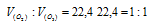
Ответ: 1:1
Задача 59.
Взяты равные массы кислорода, водорода и метана при одинаковых условиях. Найти отношение объемов взятых газов.
Решение:
Согласно закону Авогадро в равных объёмах любых газов, взятых при одинаковых условиях, содержится одинаковое число молекул, Один моль любого газа занимает 22,4л. Мольные массы кислорода, водорода и метана, соответственно равны 32 г/моль; 2г/моль; 16 г/моль.
Так как массы кислорода, водорода и метана одинаковы при одинаковых условиях, то отношение объёмов взятых газов находим из пропорции:
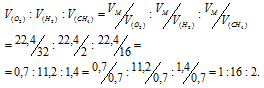
Ответ: 1:16:2.
Задача 60.
На вопрос, какой объем займет 1моль воды при нормальных условиях, получен ответ: 22,4л. Правильный ли это ответ?
Решение:
Согласно закону Авогадро в равных объёмах любых газов, взятых при одинаковых условиях, содержится одинаковое число молекул, Один моль любого газа занимает 22,4л. Так как вода при нормальных условиях находится в жидкой, а не в газообразной фазе, то ответ, что 1моль воды займёт 22,4л не правильный. Учитывая, что молярная масса воды равна 18г/моль, а плотность равна единице, то правильный ответ будет равен:
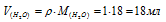
Ответ: 18мл.
Задача 61.
Сколько молекул диоксида углерода находится в 1л воздуха, если объемное содержание СО2 составляет 0,03% (условия нормальные)?
Решение:
При нормальных условиях углекислый газ, содержащийся в 1л воздуха, занимает объём 0,0003л. Зная, что мольный объём любого газа занимает 22,4л, рассчитаем число молей углекислого газа в 0,0003л из пропорции:
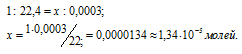
Учитывая, что в одном моле вещества содержится 6,02 . 1023 молекул, находим число молекул в 0,0003л газа:

Ответ: 8,07 .1018 молекул.
Источник
Цель: Познакомить учащихся с понятиями «количество вещества», «молярная масса» дать представление о постоянной Авогадро. Показать взаимосвязь количества вещества, числа частиц и постоянной Авогадро, а также взаимосвязь молярной массы, массы и количества вещества. Научить производить расчёты.
Тип урока: урок изучения и первичного закрепления новых знаний.
Ход урока
I. Организационный момент
II. Проверка д/з по теме: «Типы химических реакций»
III. Изучение нового материала
1. Количество вещества – моль
Вещества вступают в реакцию в строго определённых соотношениях. Например, чтобы получить вещество вода нужно взять столько водорода и кислорода, чтобы на каждые две молекулы водорода приходилась одна молекула кислорода:
2Н2 + O2 = 2Н2О
Чтобы получить вещество сульфид железа, нужно взять столько железа и серы, чтобы на каждый атом железа приходился один атом серы.
Fe + S = FeS
Чтобы получить вещество оксид фосфора, нужно взять столько молекул фосфора и кислорода, чтобы на четыре молекулы фосфора приходилось пять молекул кислорода.
4P + 5O2 = 2P2O5
Определить количество атомов, молекул и других частиц на практике невозможно – они слишком малы и не видны невооружённым глазом. Для определения числа структурных единиц (атомов, молекул) в химии применяют особую величину – количество вещества (v – ню). Единицей количества вещества является моль.
- Моль – это количество вещества, которое содержит столько структурных частиц (атомов, молекул), сколько атомов содержится в 12 г углерода.
Экспериментально установлено, что 12 г углерода содержит 6·1023 атомов. Значит один моль любого вещества, независимо от его агрегатного состояния содержит одинаковое число частиц – 6· 1023 .
- 1 моль кислорода (O2) содержит 6·1023 молекул.
- 1 моль водорода (Н2) содержит 6·1023 молекул.
- 1 моль воды (Н2O) содержит 6·1023 молекул.
- 1 моль железа (Fe) содержит 6·1023 молекул.
Задание: Используя полученную информацию, ответьте на вопросы:
а) сколько атомов кислорода содержится в 1 моле кислорода?
– 6·1023·2 = 12· 1023 атомов.
б) сколько атомов водорода и кислорода содержится в 1 моле воды (Н2O)?
– 6·1023·2 = 12· 1023 атомов водорода и 6·1023 атомов кислорода.
Число 6·1023 названо постоянной Авогадро в честь итальянского учёного 19 века и обозначается NА. Единицы измерения атомы/моль или молекулы/моль.
2. Решение задач на нахождение количества вещества
Часто нужно знать, сколько частиц вещества содержится в определённом количестве вещества. Или же найти количество вещества по известному числу молекул. Эти расчёты можно сделать по формуле:
где N – число молекул, NА – постоянная Авогадро, v – количество вещества. Из этой формулы можно выразить количество вещества.
Задача 1. Сколько атомов содержится в 2 молях серы?
N = 2·6·1023 = 12·1023 атомов.
Задача 2. Сколько атомов содержится в 0,5 молях железа?
N = 0,5·6·1023 = 3·1023 атомов.
Задача 3. Сколько молекул содержится в 5 молях углекислого газа?
N = 5·6·1023 = 30·1023 молекул.
Задача 4. Какое количество вещества составляет 12·1023 молекул этого вещества?
v = 12·1023/ 6·1023 = 2 моль.
Задача 5. Какое количество вещества составляет 0,6·1023 молекул этого вещества?
v = 0,6·1023/ 6·1023 = 0,1 моль.
Задача 6. Какое количество вещества составляет 3·1023 молекул этого вещества?
v = 3·1023/ 6·1023 = 0,5 моль.
3. Молярная масса
Для химических реакций нужно учитывать количество вещества в молях.
В: Но как на практике отмерить 2, или 2,5 моль вещества? В каких единицах лучше всего измерять массу веществ?
Для удобства в химии используют молярную массу.
Молярная масса – это масса одного моля вещества.
Обозначается – М. Измеряется в г/моль.
Молярная масса равна отношению массы вещества к соответствующему количеству вещества.
где М – молярная масса вещества, v – количество вещества, т – масса вещества.
Молярная масса – величина постоянная. Численное значение молярной массы соответствует значению относительной атомной или относительной молекулярной массы.
В: Как можно найти значения относительной атомной или относительной молекулярной массы?
Мr (S) = 32; M (S) = 32 г/моль – что соответствует 1 молю серы
Мr (Н2О) = 18; М (Н2О) = 18 г/моль – что соответствует 1 молю воды.
Следует отличать понятия «моль молекул» и «моль атомов».
Например, Н2О соответствует одному молю молекулы воды.
В: Сколько молей атомов кислорода и водорода содержится в одном моле молекулы воды?
В одном моле молекулы воды содержится два моля атомов водорода и один моль атомов кислорода.
4. Решение задач на нахождение массы вещества
Задача 7. Определить массу 0,5 моль железа.
m = 0,5·56 = 28 г
Задача 8. Определить массу 0,25 моль меди
m = 0,25·64 = 16 г
Задача 9. Определить массу 2 моль углекислого газа (СO2)
m = 2·44 = 88 г
Задача 10. Сколько молей оксида меди – CuО составляют 160 г оксида меди?
v = 160 / 80 = 8 моль
Задача 11. Сколько молей воды соответствуют 30 г воды
v =30/18 = 1,66 моль
Задача 12. Сколько молей магния соответствует его 40 граммам?
v = 40 /24 = 1,66 моль
IV. Закрепление
Фронтальный опрос:
- Что такое количество вещества?
- Чему равен 1 моль любого вещества?
- Что такое молярная масса?
- Отличается ли понятия «моль молекул» и «моль атомов»?
- Объясните на примере молекулы аммиака NН3.
- Зачем необходимо знать формулы при решении задач?
Задачи:
- Сколько молекул содержится в 180 граммах воды?
- Сколько молекул составляет 80 г углекислого газа?
V. Домашнее задание
Изучить текст параграфа, составить две задачи: на нахождение количества вещества; на нахождение массы вещества.
Литература:
- Гара Н.Н. Химия. Уроки в 8 классе: пособие для учителя. _ М.: Просвещение, 2009.
- Рудзитес Г.Е., Фельдман Ф.Г. Химия. 8 класс.: Учебник для общеобразовательных учебных учреждений – М.: Просвещение, 2009.
Источник
Решение задач на количественные характеристики вещества:
количества вещества, массу и объем
Количество вещества (ν) связано с числом структурных единиц (N) в образце вещества, его массой (m) и объемом (V) — для газообразных веществ при н. у. — следующими уравнениями:
 в которых
в которых
Vm = 22,4 л/моль (мл/ммоль, м3/кмоль) при н.у.,
NA = 6,02 • 1023 (постоянная Авогадро),
а молярная масса (М) численно равна относительной молекулярной массе вещества.
Цитаты из пособия «Задачи по химии 8-9 кл.» (авт. О.С. Габриелян и др.) использованы в учебных целях. Ссылка на покупку книги указана в конце конспекта.
ПРИМЕРЫ РЕШЕНИЯ ЗАДАЧ
№ 1.
Определите абсолютную массу (в г) одной молекулы воды.
 Ответ: m (молекулы Н2O) = 2,99 • 10–23 г.
Ответ: m (молекулы Н2O) = 2,99 • 10–23 г.
№ 2.
Определите массу порции оксида серы (VI), содержащей 7,224 • 1023 атомов кислорода.

Ответ: m(SO3) = 32 г.
№ 3.
Сколько атомов азота содержится в оксиде азота (I), объем которого (н. у.) равен 20,16 л?
 Ответ. N(N) = 10,836 • 1023.
Ответ. N(N) = 10,836 • 1023.
№ 4.
Определите объем (н. у.) оксида углерода (IV), в котором содержится столько же атомов кислорода, сколько их содержится в 48 г карбоната кальция.

Ответ. V(СO2) = 16,12 л.
№ 5.
Определите относительную плотность сероводорода по водороду и по воздуху.

Ответ: DH2(H2S) = 17; Dвозд(H2S) = 1,17.
№ 6.
Плотность газа по кислороду равна 0,875. Определите число молекул, содержащихся в 15,4 г этого газа.

Ответ. N(газа) = 3,311 • 1023.
ЗАДАЧИ с КРАТКИМ ОТВЕТОМ
№ 7. Сплав содержит 16 г меди и 11,2 г железа. Атомов какого метала будет больше в данном образце сплава?
№ 8. Смешали 16,8 г азота и 15,68 л (н. у.) водорода. Какое суммарное число молекул обоих газов будет содержаться в данной смеси?
№ 9. Чему равна масса порции хлорида бария, содержащая 1,3244 • 1024 ионов хлора?
№ 10. Какую массу должен иметь образец нитрата калия, чтобы в нем было столько же атомов кислорода, сколько их содержится в образце сульфата натрия массой 21,3 г?
№ 11. Сколько атомов хлора содержится в смеси, состоящей из 16,68 г хлорида фосфора (V) и 16,5 г хлорида фосфора (III)?
№ 12. Вычислите массу смеси, содержащей 672 мл (н. у.) оксида азота (I), 0,125 моль оксида азота (II) и 1,15 г оксида азота (IV). Сколько атомов азота будет содержаться в этой смеси?
№ 13. Молекула некоторого газа имеет массу 6,063* 10–23г. Определите плотность данного газа по гелию.
№ 14. Вычислите плотность газа по азоту, если 1 л (н. у.) этого газа имеет массу 1,7857 г.
№ 15. Плотность газа по воздуху равна 2,207. Найдите плотность этого газа по хлору и массу одной молекулы этого газа (в г).
№ 16. Масса порции оксида алюминия равна массе порции оксида кремния (IV). В какой порции будет содержаться больше атомов кислорода?
№ 17. Порции метана СН4 и аммиака NH3 содержат одинаковое число атомов водорода. Какая порция будет иметь большую массу?
№ 18. Десять молекул газа имеют массу 6,063 * 10–22г. Определите плотность данного газа по водороду.
№ 19. Определите массу и объем (н. у.) аммиака, содержащего столько же атомов водорода, сколько их содержится в 2,55 г сероводорода.
Решение задач на основные количественные характеристики вещества. Выберите дальнейшие действия:
- Перейти к следующей теме: Решение задач с долей вещества в смеси, в соединении.
- Вернуться к списку конспектов по Химии.
- Проверить знания по Химии.
- Купить книгу Задачи по химии и способы их решения. 8-9 кл. / О.С. Габриелян и др. — М.: Дрофа.
Источник
Решениие задач по химии на закон Авогадро
Задача 53.
Сопоставить числа молекул, содержащихся в 1г NH3 и в 1г N2. В каком случае и во сколько раз число молекул больше?
Решение:
В одном моле любого вещества содержится 6,02 . 1023 молекул этого вещества.
Рассчитаем содержание количества вещества в 1г NH3 и N2 по формуле:
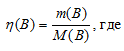
 (B) – количество вещества (В);
(B) – количество вещества (В);
m(B)- масса вещества (В);
M(B) – Молярная масса вещества (В).
М(NH3) = 17г/моль, M(N2) = 28г/моль.
Тогда
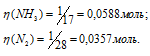
Число молекул NH3 больше числа молекул N2, так как  (NH3) >
(NH3) > (N2) . Теперь рассчитаем, во сколько раз число молекул NH3 больше числа молекул N2:
(N2) . Теперь рассчитаем, во сколько раз число молекул NH3 больше числа молекул N2:
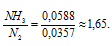
Ответ: в 1,65 раз число молекул NH3 больше числа молекул N2.
Задача 54.
Выразить в граммах массу одной молекулы диоксида серы.
Решение:
Находим молекулярную массу диоксида серы:
M(SO2) = 32 + (16 . 2) = 64г/моль.
Молекулярная масса численно составляет массу одного моля вещества, а значит, вес одного моля численно равен молекулярной массе и составляет 64г. Известно, что в одном моле любого вещества содержится 6,02 . 1023 молекул данного вещества. Исходя из этого, рассчитаем массу в граммах одной молекулы диоксида серы:
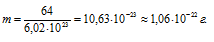
Ответ: масса одной молекулы диоксида серы равна.
Задача 55.
Одинаково ли число молекул в 0,001кг Н2 и в 0,001кг О2? В 1 моле Н2 и в 1 моле 02? В 1л Н2 и в 1л О2 при одинаковых условиях?
Решение:
Молекулярные массы водорода и кислорода равны соответственно 2г/моль и 32г/моль. Отсюда находим количество водорода и кислорода, зная их массы:
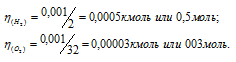
Один моль любого вещества содержит 6,02 .1023 молекул. Следовательно, в 0,001кг водорода и в 0,001кг кислорода содержится разное число молекул:

Так как имеется по одному молю водорода и кислорода, то количество молекул веществ будет одинаково:
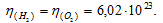
Согласно закону Авогадро в равных объёмах любых газов, взятых при одинаковых условиях, содержится одинаковое число молекул, Один моль любого газа занимает 22,4л, В которых содержится 6,02 . 1023 молекул. Отсюда рассчитаем количество молекул вещества, содержащихся в 1л водорода и в 1л кислорода:
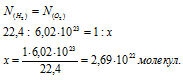
Ответ: а) в 0,001кг водорода и в 0,001кг кислорода содержится разное число молекул; б) в одном моле водорода и в одном моле кислорода содержится одинаковое число молекул: в) в одном литре водорода и в одном литре кислорода содержится одинаковое число молекул.
Задача 56.
Сколько молекул содержится в 1,00 мл водорода при нормальных условиях?
Решение:
Согласно закону Авогадро в равных объёмах любых газов, взятых при одинаковых условиях, содержится одинаковое число молекул, Один моль любого газа занимает 22,4л, В которых содержится 6,02 .1023 молекул. Отсюда рассчитаем количество молекул вещества, содержащихся в 1мл водорода из пропорции:
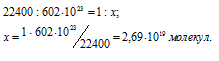
Ответ: 2,69 .1019 молекул.
Задача 57.
Какой объем при нормальных условиях занимают 27 .1021 молекул газа?
Решение:
Согласно закону Авогадро в равных объёмах любых газов, взятых при одинаковых условиях, содержится одинаковое число молекул, Один моль любого газа занимает 22,4л, В которых содержится 6,02 . 1023 молекул. Отсюда находим какой объём при нормальных условиях занимают 27 .1021 молекул газа, составив пропорцию:
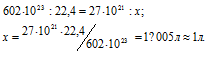
Ответ: V=1л.
Задача 58.
Каково соотношение объемов, занимаемых 1 молем О2 и 1 молем О3 (условия одинаковые)?
Решение:
Согласно закону Авогадро в равных объёмах любых газов, взятых при одинаковых условиях, содержится одинаковое число молекул, Один моль любого газа занимает 22,4л. Следовательно соотношение объёмов, занимаемых одним молем О2 и одним молем О3 иметь вид:
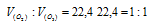
Ответ: 1:1
Задача 59.
Взяты равные массы кислорода, водорода и метана при одинаковых условиях. Найти отношение объемов взятых газов.
Решение:
Согласно закону Авогадро в равных объёмах любых газов, взятых при одинаковых условиях, содержится одинаковое число молекул, Один моль любого газа занимает 22,4л. Мольные массы кислорода, водорода и метана, соответственно равны 32 г/моль; 2г/моль; 16 г/моль.
Так как массы кислорода, водорода и метана одинаковы при одинаковых условиях, то отношение объёмов взятых газов находим из пропорции:
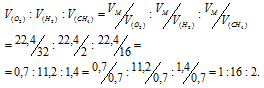
Ответ: 1:16:2.
Задача 60.
На вопрос, какой объем займет 1моль воды при нормальных условиях, получен ответ: 22,4л. Правильный ли это ответ?
Решение:
Согласно закону Авогадро в равных объёмах любых газов, взятых при одинаковых условиях, содержится одинаковое число молекул, Один моль любого газа занимает 22,4л. Так как вода при нормальных условиях находится в жидкой, а не в газообразной фазе, то ответ, что 1моль воды займёт 22,4л не правильный. Учитывая, что молярная масса воды равна 18г/моль, а плотность равна единице, то правильный ответ будет равен:
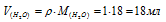
Ответ: 18мл.
Задача 61.
Сколько молекул диоксида углерода находится в 1л воздуха, если объемное содержание СО2 составляет 0,03% (условия нормальные)?
Решение:
При нормальных условиях углекислый газ, содержащийся в 1л воздуха, занимает объём 0,0003л. Зная, что мольный объём любого газа занимает 22,4л, рассчитаем число молей углекислого газа в 0,0003л из пропорции:
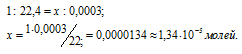
Учитывая, что в одном моле вещества содержится 6,02 . 1023 молекул, находим число молекул в 0,0003л газа:

Ответ: 8,07 .1018 молекул.
Источник
