Какое из перечисленных свойств характерно для аморфных тел

Схема атомно-молекулярного строения кристаллов и аморфных тел
Амо́рфные вещества́ (тела́) (от др.-греч. ἀ «не-» + μορφή «вид, форма») — конденсированное состояние веществ, атомная структура которых имеет ближний порядок и не имеет дальнего порядка, характерного для кристаллических структур. В отличие от кристаллов, стабильно-аморфные вещества не затвердевают с образованием кристаллических граней, и, (если не были под сильным анизотропным воздействием — деформацией или электрическим полем, например) обладают изотропией свойств, то есть не обнаруживают различия свойств в разных направлениях.
Аморфные вещества не имеют определённой точки плавления: при повышении температуры стабильно-аморфные вещества постепенно размягчаются и выше температуры стеклования () переходят в жидкое состояние. Вещества, обычно имеющие (поли-)кристаллическую структуру, но сильно переохлаждённые при затвердевании, могут затвердевать в аморфном состоянии, которое при последующем нагреве или с течением времени переходит в кристаллическое (в твёрдом состоянии с небольшим выделением тепла).
Аморфное состояние многих веществ получается при высокой скорости затвердевания (остывания) жидкого расплава, или при конденсации паров на охлаждённую заметно ниже температуры плавления поверхность-подложку. Соотношение реальной скорости охлаждения () и характеристической скорости кристаллизации определяет долю поликристаллов в аморфном объёме. Скорость кристаллизации — параметр вещества, слабо зависящий от давления и от температуры около точки плавления и сильно зависящий от сложности состава.
У металлов и сплавов аморфное состояние формируется, как правило, если расплав охлаждается за время порядка сотни и тысячи лет[источник не указан 54 дня]; для стёкол достаточно намного меньшей скорости охлаждения — долей-десятков миллисекунд[источник не указан 54 дня].
Кварц () также имеет низкую скорость кристаллизации, поэтому отлитые из квацевого расплава изделия имеют аморфное строение. Природный кварц, имевший сотни и тысячи лет для кристаллизации при остывании земной коры или глубинных слоёв вблизи вулканов, имеет крупнокристаллическое строение, в отличие от вулканического стекла, застывшего на поверхности и поэтому аморфного.
Из обычных полимеров (пластмасс) только полиэтилен имеет заметную скорость кристаллизации при комнатной температуре — порядка двух лет для мягкого (ПВД) и нескольких лет (даже с добавками-замедлителями кристаллизации) для твёрдого (ПНД) — уже примерно наполовину кристаллизованного вида. Это одна из причин охрупчивания со временем изделий из полиэтилена, особенно при повышенной температуре.
К стабильно-аморфным веществам принадлежат стёкла (искусственные и вулканические), естественные и синтетические смолы, клеи, парафин, воск и др. Аморфные вещества могут находиться либо в стеклообразном состоянии (при низких температурах), либо в состоянии расплава (при высоких температурах). Аморфные вещества переходят в стеклообразное состояние при температурах заметно ниже температуры стеклования . При температурах намного выше аморфные вещества ведут себя как расплавы, то есть находятся в расплавленном состоянии. Вязкость аморфных материалов — непрерывная функция температуры: чем выше температура, тем ниже вязкость аморфного вещества.
Структура[править | править код]
Исследования показали, что структуры жидкостей и аморфных тел имеют много общего.
В аморфных и жидких телах наблюдается ближний порядок в упаковке частиц (атомов или молекул).
Также бывают промежуточные полуаморфные (полукристаллические) состояния.
Свойства[править | править код]
Все физические свойства аморфного и поликристаллического состояний одного и того же вещества, кроме плотности, заметно, иногда сильно отличаются.
Электрические и механические свойства аморфных веществ ближе к таковым для монокристаллов, чем для поликристаллов, из-за отсутствия резких и сильно загрязнённых примесями межкристаллических границ с зачастую абсолютно другим химическим составом. Немеханические свойства полуаморфных состояний обычно являются промежуточными между аморфными и кристаллическими и изотропны.
При внешних воздействиях аморфные вещества обнаруживают одновременно упругие свойства, подобно кристаллическим твёрдым веществам, и текучесть, подобно жидкости, поэтому моделируются в механике сплошных сред как вязкоупругие среды. Так, при кратковременных воздействиях (ударах) они ведут себя как твёрдые вещества и при сильном ударе раскалываются на куски. Но при очень продолжительном воздействии (например, растяжении) аморфные вещества текут. Такими аморфным веществом также является смола (или гудрон, битум). Если раздробить её на мелкие куски и получившейся сыпучей массой заполнить сосуд, то через некоторое время смола сольётся в единое целое и примет форму сосуда.
В зависимости от электрических свойств, разделяют аморфные металлы, аморфные неметаллы и аморфные полупроводники.
Литература[править | править код]
- Скрышевский А. Ф. Структурный анализ жидкостей и аморфных тел. — 2-е изд., перераб. и доп.. — М.: Высшая школа, 1980. — С. 302-324. — 328 с.
- Шульц М. М., Мазурин О. В. Современное представление о строении стёкол и их свойствах. — Л.: Наука, 1988. — 200 с. — ISBN 5-02-024564-X.
См. также[править | править код]
- Опыт с капающим пеком
- Неньютоновская жидкость
Источник
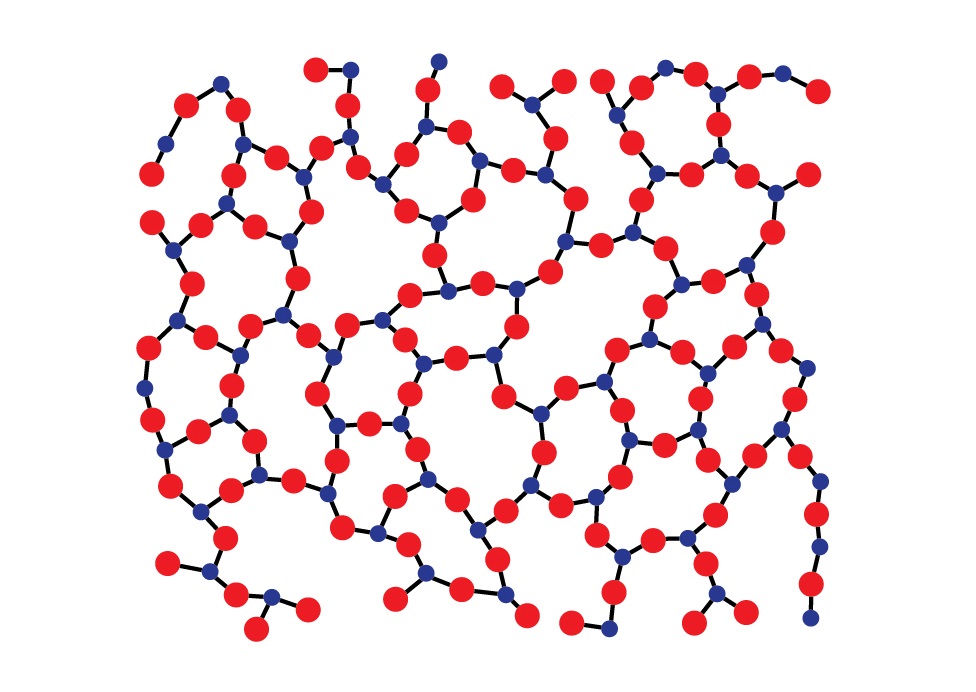
Аморфные тела (структура диоксида кремния)
Твердые тела разделяют на аморфные и кристаллические, в зависимости от их молекулярной структуры и физических свойств.
В отличие от кристаллов молекулы и атомы аморфных твердых тел не формируют решетку, а расстояние между ними колеблется в пределах некоторого интервала возможных расстояний. Иначе говоря, у кристаллов атомы или молекулы взаимно расположены таким образом, что формируемая структура может повторяться во всем объеме тела, что называется дальним порядком. В случае же с аморфными телами – сохраняется структура молекул лишь относительно каждой одной такой молекулы, наблюдается закономерность в распределении только соседних молекул – ближний порядок. Наглядный пример представлен ниже.
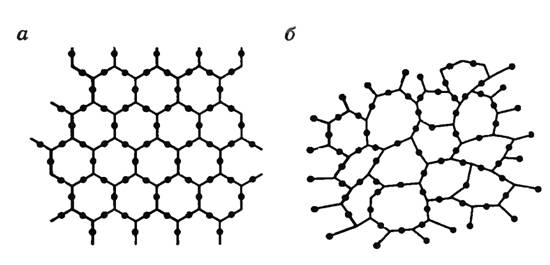
На рисунке слева (а) изображена решетка молекул кварца, а справа (б) расположение молекул кварцевого стекла, которое является аморфным телом.
К аморфным телам относится стекло и другие вещества в стеклообразном состоянии, канифоль, смолы, янтарь, сургуч, битум, воск, а также органические вещества: каучук, кожа, целлюлоза, полиэтилен и др.
Свойства аморфных тел
Особенность строения аморфных твердых тел придает им индивидуальные свойства:
- Слабо выраженная текучесть – одно из наиболее известных свойств таких тел. Примером будут потеки стекла, которое долгое время стоит в оконной раме.
- Аморфные твердые тела не обладают определенной температурой плавления, так как переход в состояние жидкости во время нагрева происходит постепенно, посредством размягчения тела. По этой причине к таким телам применяют так называемый температурный интервал размягчения.
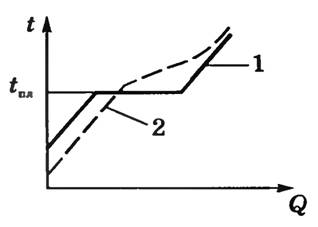
График перехода аморфного тела в жидкое состояние изображен пунктирной линией (2), а график перехода обычного твердого тела в жидкое состояние – сплошной (1).
- В силу своей структуры такие тела являются изотропными, то есть их физические свойства не зависят от выбора направления.
- Вещество в аморфном состоянии обладает большей внутренней энергией, нежели в кристаллическом. По этой причине аморфные тела способны самостоятельно переходить в кристаллическое состояние. Данное явление можно наблюдать как результат помутнения стекол с течением времени.
Стеклообразное состояние
В природе существуют жидкости, которые практически невозможно перевести в кристаллическое состояние посредством охлаждения, так как сложность молекул этих веществ не позволяет им образовать регулярную кристаллическую решетку. К таким жидкостям относятся молекулы некоторых органических полимеров.
Материалы по теме
Однако, при помощи глубокого и быстрого охлаждения, практически любое вещество способно перейти в стеклообразное состояние. Это такое аморфное состояние, которое не имеет явной кристаллической решетки, но может частично кристаллизироваться, в масштабах малых кластеров. Данное состояние вещества является метастабильным, то есть сохраняется при некоторых требуемых термодинамических условиях.
При помощи технологии охлаждения с определенной скоростью вещество не будет успевать кристаллизоваться, и преобразуется в стекло. То есть чем выше скорость охлаждения материала, тем меньше вероятность его кристаллизации. Так, например, для изготовления металлических стекол потребуется скорость охлаждения, равная 100 000 – 1 000 000 Кельвин в секунду.
В природе вещество существует в стеклообразном состоянии возникает из жидкой вулканической магмы, которая, взаимодействуя с холодной водой или воздухом, быстро охлаждается. В данном случае вещество зовется вулканическим стеклом. Также можно наблюдать стекло, образованная в результате плавления падающего метеорита, взаимодействующего с атмосферой – метеоритное стекло или молдавит.

Молдавит, естественное стекло, образованное ударом метеорита, из Беседин, Богемия, Чехия.
Источник
Твердые тела существуют в двух основных состояниях, отличающихся своим внутренним строением, что приводит различию их физических свойств. Это — кристаллическое и аморфное состояния твердых тел. Основным признаком кристаллов является строгий, повторяющийся порядок расположения атомов. Аморфные вещества (от греческого слова “аморфос” — бесформенный) не имеют упорядоченной, кристаллической структуры.

Структура аморфных тел
В телах, находящихся в аморфном состоянии, отсутствует четкий порядок расположения атомов. Существует только, так называемый ближний порядок, когда ближайшие атомы располагаются относительно упорядоченно. По своей структуре аморфные вещества похожи на жидкости.
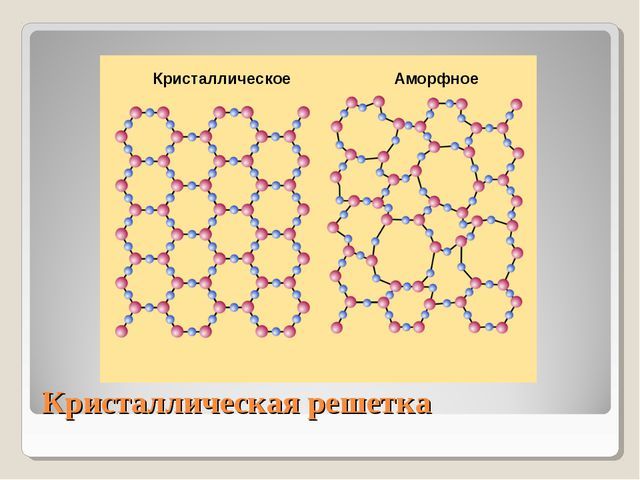
Рис. 1. Внутреннее строение (решетка) кристаллического твердого тела и структура аморфного тела.
Аморфное состояние вещества, в отличие от кристаллического, не является устойчивым. По прошествии некоторого времени аморфное вещество постепенно переходит в кристаллическое. Правда, это время измеряется годами и десятилетиями.
В аморфном состоянии могут находиться и такие вещества, которые обычно имеют кристаллическую структуру. Например, кристалл кварца SiO2 если его расплавить (при температуре 17000С), при охлаждении образует плавленый кварц, имеющий меньшую плотность, чем кристаллический, и обладающий свойствами одинаковыми по всем направлениям, притом сильно отличающимися от свойств кристаллического кварца.
Примеры аморфных тел
Аморфными являются огромное количество веществ. Вот только некоторые, хорошо известные вещества: парафин, воск, сургуч, эбонит, шоколад, канифоль, смола, стекло, плексиглас, каучук, стекло, различные пластмассы.

Рис. 2. Примеры аморфных веществ.
Свойства аморфных тел
В силу своего строения, в отличие от кристаллических тел, аморфные тела обладают следующими основными свойствами:
- Аморфные вещества изотропны по всем направлениям. Это означает, что все физические свойства (тепловые, электрические, оптические, механические) аморфных тел оказываются абсолютно одинаковы независимо от направления.
- Текучесть — это пример свойства этих тел, который визуально можно наблюдать в виде потеков на стекле, долго простоявшем в окне.
- Отсутствие определенной температуры плавления. Фазовый переход в жидкое состояние происходит постепенно, по мере размягчения аморфного тела.
- В аморфном состоянии вещество обладает большей внутренней энергией, чем в кристалле. Поэтому аморфные тела обладают способностью переходить в кристаллическое состояние. Хорошо известный пример этого явления — помутнение стекла с течением времени. Это помутнение связано с появлением внутри стекла мелких кристалликов, оптические параметры которых иные, чем окружающей их аморфной среды.

Рис. 3. Графики перехода аморфного и кристаллического тел в жидкое состояние.
Есть вещества, обладающие одновременно свойствами и жидкости и кристалла, а именно текучестью и анизотропией. Такое состояние вещества называется жидкокристаллическим. В основном жидкими кристаллами являются органические вещества, молекулы которых имеют форму плоских пластин или нитевидную форму. Эти вещества являются основой для жидкокристаллических экранов телевизоров.
Что мы узнали?
Итак, мы узнали, что из себя представляют твердые тела в аморфном состоянии. Структура этих веществ не имеет упорядоченного порядка размещения атомов. Физические свойства аморфных тел не зависят от направления воздействия и ориентации тела.
Тест по теме
Оценка доклада
Средняя оценка: 4.3. Всего получено оценок: 114.
Источник
Твердое тело является одним из трех основных состояний материи, наряду с жидкостью и газом. Материя – это вещество вселенной, атомы, молекулы и ионы, которые составляют все физические вещества. В твердом теле, эти частицы плотно упакованы вместе и не могут свободно перемещаться внутри вещества. Молекулярное движение для частиц в твердом теле ограничено очень малыми колебаниями атомов вокруг их фиксированных положений; поэтому твердые тела имеют фиксированную форму, которую трудно изменить. Твердые тела также имеют определенный объем, то есть они сохраняют свой размер независимо от того, как вы пытаетесь их изменить.
Твердые вещества делятся на две основные категории: кристаллические твердые вещества и аморфные твердые вещества, основанные на том, как расположены частицы.
Кристаллические твердые вещества
Кристаллические твердые вещества или кристаллы рассматриваются как настоящие твердые тела. Минералы представляют собой кристаллические твердые вещества. Обычная поваренная соль является одним из примеров такого твердого вещества. В кристаллических твердых телах атомы, ионы или молекулы расположены упорядоченно и симметрично во всем кристалле. Самая маленькая повторяющаяся структура твердого тела называется элементарной ячейкой, которая похожа на кирпич в стене. Элементарные ячейки объединяются в сеть, называемую кристаллической решеткой. Существует 14 типов решеток, называемых решетками Браве (названных в честь Августа Браве, французского физика 19-го века), и они классифицируются на семь кристаллических систем, основанных на расположении атомов – кубическую, гексагональную, тетрагональную, ромбоэдрическую, орторомбическую, моноклинную и триклинную.
Кроме регулярного расположения частиц, твердые тела обладают несколькими другими характерными свойствами. Они, как правило, вообще несжимаемы, а это означает то, что их нельзя сжать в более мелкую форму. Из-за повторяющейся геометрической структуры кристалла, все связи между частицами имеют равную силу. Это значит, что кристаллическое твердое тело будет иметь определенную точку плавления, поскольку применение тепла одновременно разрушит все связи.
Кристаллические твердые вещества также проявляют анизотропию. Это означает, что такие свойства, как показатель преломления (сколько света изгибается при прохождении вещества), проводимость (насколько хорошо он проводит электричество) и прочность на растяжение (сила, необходимая для его разрыва), будут варьироваться в зависимости от направления, от которого была применена сила. Кристаллические твердые вещества также проявляют свойство расщепления – при разрыве части будут иметь выровненную поверхность или прямые края.
Типы кристаллических твердых веществ
Существует четыре типа кристаллических твердых тел: ионные твердые тела, молекулярные твердые тела, сетевые ковалентные твердые тела и металлические твердые тела.
Ионные твердые тела
Ионные соединения образуют кристаллы, которые состоят из противоположно заряженных ионов – положительно заряженного катиона и отрицательно заряженного аниона. Из-за сильного притяжения между противоположными зарядами требуется много энергии для преодоления ионных связей. Это означает, что ионные соединения имеют очень высокую температуру плавления, часто между 300 и 1000 градусов по Цельсию.
Хотя сами кристаллы являются твердыми, хрупкими и непроводящими, большинство ионных соединений можно растворить в воде, образуя раствор свободных ионов, который будет проводить электричество. Они могут быть простыми двойными солями, такими как хлорид натрия NaCl или поваренная соль, где один атом металлического элемента – натрия, связан с одним атомом неметаллического элемента – хлора. Они также могут состоять из многоатомных ионов, таких как нитрат аммония NH4NO3. Многоатомные ионы представляют собой группы атомов, которые разделяют электроны – это называется ковалентная связь, они функционируют в соединении, как если бы они составляли один заряженный ион.
Молекулярные твердые вещества
Молекулярные твердые вещества состоят из ковалентно связанных молекул, притягиваемых друг к другу электростатическими силами – это называется Силы Ван–дер–Ваальса. Поскольку ковалентная связь предполагает совместное использование электронов, а не прямой перенос этих частиц, общие электроны могут проводить больше времени в электронном облаке более крупного атома, вызывая слабую или смещающуюся полярность. Это электростатическое притяжение между двумя полюсами – диполями, значительно слабее, чем ионное или ковалентное связывание, поэтому молекулярные твердые тела, как правило, мягче, чем ионные кристаллы, и имеют более низкие точки плавления – многие из них будут плавиться при температуре менее 100°C. Большинство молекулярных твердых веществ неполярны. Эти неполярные молекулярные твердые вещества не будут растворяться в воде, но будут растворяться в неполярном растворителе, таком как бензол и октан. Полярные молекулярные твердые вещества, такие как сахар, легко растворяются в воде. Молекулярные твердые тела являются непроводящими.
Примеры молекулярных твердых веществ – лед, сахар, галогены, такие как твердый хлор Cl2, соединения, состоящие из галогена и водорода, такие как хлористый водород HCl. Фуллерены также являются молекулярными твердыми веществами.
Ковалентные твердые вещества
В сплошной структуре твердого тела нет отдельных молекул. Атомы ковалентно связаны в непрерывной сети, что в свою очередь приводит к кристаллической структуре. Каждый атом ковалентно связан со всеми окружающими атомами. Ковалентные твердые тела обладают свойствами, аналогичными свойствам ионных твердых тел. Они очень твердые с чрезвычайно высокими температурами плавления, обычно выше 1000 градусов по Цельсию. В отличии от ионных соединений, они не растворяются в воде и не проводят электричество.
Примеры ковалентные твердых веществ – алмазы, аметисты и рубины.
Металлические твердые вещества
Металлы представляют собой непрозрачные, блестящие твердые вещества, которые являются пластичными. Они мягкие и могут быть сформированы или спрессованы в тонкие листы, или даже втянуты в провода. Валентные электроны не передаются и не распределяются, поскольку находятся в ионной и ковалентной связи. Электронные облака соседних атомов перекрываются, так что электроны становятся делокализованными. Электроны перемещаются с относительной свободой от одного атома к другому по всему кристаллу.
Металл можно описать как решетку положительных катионов в “море” отрицательных электронов. Эта подвижность электронов означает, что металлы обладают высокой проводимостью тепла и электричества. Металлы, как правило, имеют высокие точки плавления, хотя заметными исключениями являются ртуть, температура плавления которой составляет минус 38,8 градуса по Цельсию, и фосфор с температурой плавления 44 градуса по Цельсию.
Сплав представляет собой твердую смесь металлического элемента с другим веществом. Хотя чистые металлы могут быть чрезмерно податливыми и тяжелыми, сплавы являютсяболее используемыми. Бронза – сплав меди и олова, а сталь – сплав железа, углерода и других добавок.
Аморфные твердые вещества
В аморфных твердых телах (“твердые тела без формы”) частицы не имеют повторяющейся структуры решетки. Примерами аморфных твердых веществ являются стекло, резина, гели и большинство пластмасс. Аморфное твердое вещество не имеет определенной температуры плавления. Оно плавится постепенно в определенном диапазоне температур, потому что связи не разрываются все сразу. Аморфное твердое вещество расплавится в мягкое, податливое состояние (свечной воск или расплавленное стекло), прежде чем полностью превратиться в жидкость.
Аморфные твердые тела не имеют характерной симметрии, поэтому они не имеют ровных плоскостей при разрезании – края могут быть изогнуты. Они называются изотропными, поскольку такие свойства, как показатель преломления, проводимость и прочность на растяжение, равны независимо от направления, в котором применяется сила.
???? ???? ????
Источник
