Какое число молекул содержится в 1 л воды и сколько в нем содержится молей
Анонимный вопрос
10 января 2018 · 4,8 K
Книги, звери и еда – это хобби навсегда.
1 моль любого вещества содержит Na=6*10^23 молекул. Формула воды H2O, ее молярная масса составляет М=18 г, следовательно, в m=180 мг=0.18 г содержится N=Na*m/M=6*10^23*0.18/18=6*10^21 молекул.
Примерно сколько атомов гелия содержится в 4 кг гелия?
Молодой-исследовать в области химии и ядерной физики ускорителей частиц, г. Падуя, Италия. · tele.click/real_italy
К уже правильному ответу предложу свое решение, для тех кто предпочитает формульные решения.
n = m/M = N / Na = V / Vm
где n – кол моль вещества
m – масса вещества – в г
M – молекулярная масса (в нашем случаи атомная масса) в г/моль
N – колл. составляющих (атомов или молекул)
Na – число Авгодаро 6,022 * 10^23
V – обьем в л
Vm – молекулярный обьем 22,4 л/моль
С помощью этой формулы можно решить очень много задач школьной химии
Подставляем известные и выражаем неизвестную величины:
N = (m * Na)/M = 4000г * 6,022 * 10^23 ) / 4 г/моль = 6,022 * 10^26
Прочитать ещё 2 ответа
Сколько молекул содержится в 2,5 моль кислорода?
Инженер по профессии, люблю спорт, музыку, кино.
В одном моле любого вещества всегда содержится одно и тоже число молекул, называемое числом Авогадро:
Na = 6.02*10^23
Тогда в n=2,5 моль кислорода содержится молекул:
N = n*Na = 2.5*6.02*10^23 = 15.05*10^23
Как определить массу одной молекулы,если известно что молярная масса кислорода 0.032 кг моль?
Образование: высшее (бакалавр + магистр). Увлечения: спорт, путешествие, кофе:)
Решение: Массу одной молекулы кислорода можно рассчитать по формуле: m = М/Na, где M – молярная масса кислорода (М = 0,032 кг/моль), Na – число Авогадро (Na = 6*10^23 моль^-1). Рассчитаем массу одной молекулы кислорода: m = М/Na = 0,032/6*10^23 = 5,33*10^-26 кг.
Ответ: Масса одной молекулы кислорода равна 5,33*10^-26 кг.
Если броуновское движение – это хаотичное движение молекул, что эти молекулы “толкает”?
Копирайтер для B2B. Пишу яркие продающие тексты на сложные темы.
Под броуновским движением обычно понимают движение мелких частиц в газе или жидкости. Однако из Вашего вопроса следует, что Вы говорите, скорее, об атомах и молекулах самого газа или жидкости. Давайте посмотрим.
Молекулы “толкает” их кинетическая энергия. Для отдельных молекул считать ее было бы слишком долго и не слишком целесообразно, поэтому в реальности вместо подсчета энергий отдельных молекул или атомов используют такой параметр как температура. Т.е. температура – это мера усредненной внутренней энергии молекул или атомов вещества в некотором объеме. Сам по себе атом, конечно, никакой температуры не имеет. Это статистический параметр.
У твердых веществ движение атомов ограничивается межатомными связями. Поэтому атомы твердых тел просто колеблются туда-сюда в рамках кристаллической решетки.
Что касается расхода энергии. Энергия на собственно броуновское движение не расходуется. Но она расходуется в момент столкновения атомов и молекул друг с другом или с атомами сосуда, в котором заключен этот газ или жидкость. Расходуется на что? Она передается молекуле или атому, с которым произошло столкновение. Примерно как бильярдный шар после удара кием приводит в движение другие шары, с которыми сталкивается – передает им энергию. Как следствие, если газ не изолирован от среды, то он постепенно остывает до тех пор, пока его температура не сравняется с температурой среды, потому что выравниваются энергии молекул газа и среды.
Считается, что броуновское движение прекращается, если опустить температуру – т.е. внутреннюю энергию атомов – до минимума. Однако в этом случае в ход вступают квантовые эффекты, поэтому даже при абсолютном нуле атомы в покое находиться не смогут.
Прочитать ещё 1 ответ
Источник
Решениие задач по химии на закон Авогадро
Задача 53.
Сопоставить числа молекул, содержащихся в 1г NH3 и в 1г N2. В каком случае и во сколько раз число молекул больше?
Решение:
В одном моле любого вещества содержится 6,02 . 1023 молекул этого вещества.
Рассчитаем содержание количества вещества в 1г NH3 и N2 по формуле:
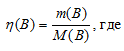
 (B) – количество вещества (В);
(B) – количество вещества (В);
m(B)- масса вещества (В);
M(B) – Молярная масса вещества (В).
М(NH3) = 17г/моль, M(N2) = 28г/моль.
Тогда
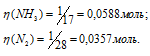
Число молекул NH3 больше числа молекул N2, так как  (NH3) >
(NH3) > (N2) . Теперь рассчитаем, во сколько раз число молекул NH3 больше числа молекул N2:
(N2) . Теперь рассчитаем, во сколько раз число молекул NH3 больше числа молекул N2:
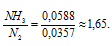
Ответ: в 1,65 раз число молекул NH3 больше числа молекул N2.
Задача 54.
Выразить в граммах массу одной молекулы диоксида серы.
Решение:
Находим молекулярную массу диоксида серы:
M(SO2) = 32 + (16 . 2) = 64г/моль.
Молекулярная масса численно составляет массу одного моля вещества, а значит, вес одного моля численно равен молекулярной массе и составляет 64г. Известно, что в одном моле любого вещества содержится 6,02 . 1023 молекул данного вещества. Исходя из этого, рассчитаем массу в граммах одной молекулы диоксида серы:
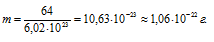
Ответ: масса одной молекулы диоксида серы равна.
Задача 55.
Одинаково ли число молекул в 0,001кг Н2 и в 0,001кг О2? В 1 моле Н2 и в 1 моле 02? В 1л Н2 и в 1л О2 при одинаковых условиях?
Решение:
Молекулярные массы водорода и кислорода равны соответственно 2г/моль и 32г/моль. Отсюда находим количество водорода и кислорода, зная их массы:
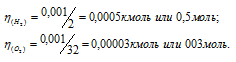
Один моль любого вещества содержит 6,02 .1023 молекул. Следовательно, в 0,001кг водорода и в 0,001кг кислорода содержится разное число молекул:

Так как имеется по одному молю водорода и кислорода, то количество молекул веществ будет одинаково:
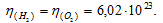
Согласно закону Авогадро в равных объёмах любых газов, взятых при одинаковых условиях, содержится одинаковое число молекул, Один моль любого газа занимает 22,4л, В которых содержится 6,02 . 1023 молекул. Отсюда рассчитаем количество молекул вещества, содержащихся в 1л водорода и в 1л кислорода:
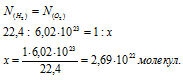
Ответ: а) в 0,001кг водорода и в 0,001кг кислорода содержится разное число молекул; б) в одном моле водорода и в одном моле кислорода содержится одинаковое число молекул: в) в одном литре водорода и в одном литре кислорода содержится одинаковое число молекул.
Задача 56.
Сколько молекул содержится в 1,00 мл водорода при нормальных условиях?
Решение:
Согласно закону Авогадро в равных объёмах любых газов, взятых при одинаковых условиях, содержится одинаковое число молекул, Один моль любого газа занимает 22,4л, В которых содержится 6,02 .1023 молекул. Отсюда рассчитаем количество молекул вещества, содержащихся в 1мл водорода из пропорции:
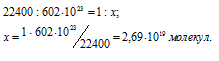
Ответ: 2,69 .1019 молекул.
Задача 57.
Какой объем при нормальных условиях занимают 27 .1021 молекул газа?
Решение:
Согласно закону Авогадро в равных объёмах любых газов, взятых при одинаковых условиях, содержится одинаковое число молекул, Один моль любого газа занимает 22,4л, В которых содержится 6,02 . 1023 молекул. Отсюда находим какой объём при нормальных условиях занимают 27 .1021 молекул газа, составив пропорцию:
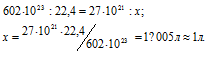
Ответ: V=1л.
Задача 58.
Каково соотношение объемов, занимаемых 1 молем О2 и 1 молем О3 (условия одинаковые)?
Решение:
Согласно закону Авогадро в равных объёмах любых газов, взятых при одинаковых условиях, содержится одинаковое число молекул, Один моль любого газа занимает 22,4л. Следовательно соотношение объёмов, занимаемых одним молем О2 и одним молем О3 иметь вид:
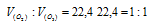
Ответ: 1:1
Задача 59.
Взяты равные массы кислорода, водорода и метана при одинаковых условиях. Найти отношение объемов взятых газов.
Решение:
Согласно закону Авогадро в равных объёмах любых газов, взятых при одинаковых условиях, содержится одинаковое число молекул, Один моль любого газа занимает 22,4л. Мольные массы кислорода, водорода и метана, соответственно равны 32 г/моль; 2г/моль; 16 г/моль.
Так как массы кислорода, водорода и метана одинаковы при одинаковых условиях, то отношение объёмов взятых газов находим из пропорции:
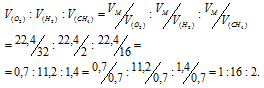
Ответ: 1:16:2.
Задача 60.
На вопрос, какой объем займет 1моль воды при нормальных условиях, получен ответ: 22,4л. Правильный ли это ответ?
Решение:
Согласно закону Авогадро в равных объёмах любых газов, взятых при одинаковых условиях, содержится одинаковое число молекул, Один моль любого газа занимает 22,4л. Так как вода при нормальных условиях находится в жидкой, а не в газообразной фазе, то ответ, что 1моль воды займёт 22,4л не правильный. Учитывая, что молярная масса воды равна 18г/моль, а плотность равна единице, то правильный ответ будет равен:
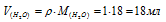
Ответ: 18мл.
Задача 61.
Сколько молекул диоксида углерода находится в 1л воздуха, если объемное содержание СО2 составляет 0,03% (условия нормальные)?
Решение:
При нормальных условиях углекислый газ, содержащийся в 1л воздуха, занимает объём 0,0003л. Зная, что мольный объём любого газа занимает 22,4л, рассчитаем число молей углекислого газа в 0,0003л из пропорции:
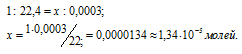
Учитывая, что в одном моле вещества содержится 6,02 . 1023 молекул, находим число молекул в 0,0003л газа:

Ответ: 8,07 .1018 молекул.
Источник
Анонимный вопрос
10 января 2018 · 2,4 K
Сколько молекул содержится в 210 граммах азота?
Образование: высшее (бакалавр + магистр). Увлечения: спорт, путешествие, кофе:)
Решение:
Молярная масса азота равна 28г/моль, это масса 6,02 х 10 в 23 степени молекул. По условию азота 210г, находим вещества 210 г : 28 г/моль = 7,5 моль. Это 7,5×6,02×10^23=4.515×10^24 молекул.
Ответ: 4.515×10^24 молекул.
Какое количество вещества содержит 5 молекул селена?
Работал инженером по обслуживанию военных авиационных двигателей, увлекаюсь…
Количество вещества = общее колличество молекул разделить на N = 6,02*10 ^ 23 моль – постаянную Авогадро
v = 5 / 6.02 *10^23 = 83 * 10^(-25) моль
Чему равно количество вещества в молях содержащегося в воде массой 5г?
Чтобы найти количество вещества в молях нужно массу вещества в граммах разделить на молекулярную массу этого вещества. Молекулярная масса вещества равна сумме атомных весов элементов входящих в состав этого вещества. В воде два элемента: два атома водорода с атомной массой 1 г/моль и один атом кислорода с атомной массой 16 г/моль. Молекулярная масса воды равна 2*1+16=18 г/моль. Тогда в 5 г воды содержится 5/18=0.278 моль Н2О
Почему молекула воды H2O?
@Андрей 40, тут важен механизм сцепления атомов в молекулы. Начать надо, наверное, со строения атома. Как Вы, наверное, знаете, если не углубляться в квантовую механику, а пользоваться простой планетарной моделью, то атомы состоят из ядер (положительно заряженных) и отрицательно заряженных электронов, которые вращаются вокруг ядер. Но вся штука в том, что они не просто так вращаются, а могут занимать только определенные орбиты, причем на каждой орбите может быть только определенное количество электронов. Сначала электроны занимают ближние к ядру орбиты, если на данную орбиту нельзя пустить больше электронов, то начинает заполняться следующая и т.д. Не будем сейчас обсуждать почему подходит не каждая орбита, а лишь строго определенные и почему для каждой орбиты существует предельно допустимое количество электронов – это отдельная тема. Для нас важно, что при таком заполнении орбит (или как их называют электронных оболочек), все внутренние оболочки оказываются заполенными, а если и остается свободное место для электронов, то только на внешней оболочке. Если внешняя оболочка оказывается заполнена полностью, то такие атомы очень трудно вступают в связь с другими. Пример – благородные газы (аргон, криптон, ксенон, неон, гелий). А вот если во внешней оболочке остаются вакансии, то атом может попробовать посадить на нее электрон из внешней оболочки другого атома, т.е. как бы занять из его оболочки электрон, чтобы заполнить свою оболочку. Тогда получается, что этот самый электрон начинает разрываться между двумя атомами и т.о. между этими атомами образуется связь, объединяющая их в молекулу. Так вот у атома кислорода есть вакансии для двух электронов во внешней оболочке, а у атома водорода всего один электрон. Вообще один. Он же, естественно во внешней оболочке. Вот и получается, что чтобы полностью заполнить внешнюю оболочку, атому кислорода надо позаимствовать электроны у двух атомов водорода. Один – слишком мало, оболочка еще не будет заполнена и будет стремиться занять электрон еще где-нибудь, три – перебор, потому что завершив заполнение внешней оболочки атом кислорода теряет активность и третий атом водорода ему уже не нужен. Надеюсь, ответил на Ваш вопрос.
Источник
Цель: Познакомить учащихся с понятиями «количество вещества», «молярная масса» дать представление о постоянной Авогадро. Показать взаимосвязь количества вещества, числа частиц и постоянной Авогадро, а также взаимосвязь молярной массы, массы и количества вещества. Научить производить расчёты.
Тип урока: урок изучения и первичного закрепления новых знаний.
Ход урока
I. Организационный момент
II. Проверка д/з по теме: «Типы химических реакций»
III. Изучение нового материала
1. Количество вещества – моль
Вещества вступают в реакцию в строго определённых соотношениях. Например, чтобы получить вещество вода нужно взять столько водорода и кислорода, чтобы на каждые две молекулы водорода приходилась одна молекула кислорода:
2Н2 + O2 = 2Н2О
Чтобы получить вещество сульфид железа, нужно взять столько железа и серы, чтобы на каждый атом железа приходился один атом серы.
Fe + S = FeS
Чтобы получить вещество оксид фосфора, нужно взять столько молекул фосфора и кислорода, чтобы на четыре молекулы фосфора приходилось пять молекул кислорода.
4P + 5O2 = 2P2O5
Определить количество атомов, молекул и других частиц на практике невозможно – они слишком малы и не видны невооружённым глазом. Для определения числа структурных единиц (атомов, молекул) в химии применяют особую величину – количество вещества (v – ню). Единицей количества вещества является моль.
- Моль – это количество вещества, которое содержит столько структурных частиц (атомов, молекул), сколько атомов содержится в 12 г углерода.
Экспериментально установлено, что 12 г углерода содержит 6·1023 атомов. Значит один моль любого вещества, независимо от его агрегатного состояния содержит одинаковое число частиц – 6· 1023 .
- 1 моль кислорода (O2) содержит 6·1023 молекул.
- 1 моль водорода (Н2) содержит 6·1023 молекул.
- 1 моль воды (Н2O) содержит 6·1023 молекул.
- 1 моль железа (Fe) содержит 6·1023 молекул.
Задание: Используя полученную информацию, ответьте на вопросы:
а) сколько атомов кислорода содержится в 1 моле кислорода?
– 6·1023·2 = 12· 1023 атомов.
б) сколько атомов водорода и кислорода содержится в 1 моле воды (Н2O)?
– 6·1023·2 = 12· 1023 атомов водорода и 6·1023 атомов кислорода.
Число 6·1023 названо постоянной Авогадро в честь итальянского учёного 19 века и обозначается NА. Единицы измерения атомы/моль или молекулы/моль.
2. Решение задач на нахождение количества вещества
Часто нужно знать, сколько частиц вещества содержится в определённом количестве вещества. Или же найти количество вещества по известному числу молекул. Эти расчёты можно сделать по формуле:
где N – число молекул, NА – постоянная Авогадро, v – количество вещества. Из этой формулы можно выразить количество вещества.
Задача 1. Сколько атомов содержится в 2 молях серы?
N = 2·6·1023 = 12·1023 атомов.
Задача 2. Сколько атомов содержится в 0,5 молях железа?
N = 0,5·6·1023 = 3·1023 атомов.
Задача 3. Сколько молекул содержится в 5 молях углекислого газа?
N = 5·6·1023 = 30·1023 молекул.
Задача 4. Какое количество вещества составляет 12·1023 молекул этого вещества?
v = 12·1023/ 6·1023 = 2 моль.
Задача 5. Какое количество вещества составляет 0,6·1023 молекул этого вещества?
v = 0,6·1023/ 6·1023 = 0,1 моль.
Задача 6. Какое количество вещества составляет 3·1023 молекул этого вещества?
v = 3·1023/ 6·1023 = 0,5 моль.
3. Молярная масса
Для химических реакций нужно учитывать количество вещества в молях.
В: Но как на практике отмерить 2, или 2,5 моль вещества? В каких единицах лучше всего измерять массу веществ?
Для удобства в химии используют молярную массу.
Молярная масса – это масса одного моля вещества.
Обозначается – М. Измеряется в г/моль.
Молярная масса равна отношению массы вещества к соответствующему количеству вещества.
где М – молярная масса вещества, v – количество вещества, т – масса вещества.
Молярная масса – величина постоянная. Численное значение молярной массы соответствует значению относительной атомной или относительной молекулярной массы.
В: Как можно найти значения относительной атомной или относительной молекулярной массы?
Мr (S) = 32; M (S) = 32 г/моль – что соответствует 1 молю серы
Мr (Н2О) = 18; М (Н2О) = 18 г/моль – что соответствует 1 молю воды.
Следует отличать понятия «моль молекул» и «моль атомов».
Например, Н2О соответствует одному молю молекулы воды.
В: Сколько молей атомов кислорода и водорода содержится в одном моле молекулы воды?
В одном моле молекулы воды содержится два моля атомов водорода и один моль атомов кислорода.
4. Решение задач на нахождение массы вещества
Задача 7. Определить массу 0,5 моль железа.
m = 0,5·56 = 28 г
Задача 8. Определить массу 0,25 моль меди
m = 0,25·64 = 16 г
Задача 9. Определить массу 2 моль углекислого газа (СO2)
m = 2·44 = 88 г
Задача 10. Сколько молей оксида меди – CuО составляют 160 г оксида меди?
v = 160 / 80 = 8 моль
Задача 11. Сколько молей воды соответствуют 30 г воды
v =30/18 = 1,66 моль
Задача 12. Сколько молей магния соответствует его 40 граммам?
v = 40 /24 = 1,66 моль
IV. Закрепление
Фронтальный опрос:
- Что такое количество вещества?
- Чему равен 1 моль любого вещества?
- Что такое молярная масса?
- Отличается ли понятия «моль молекул» и «моль атомов»?
- Объясните на примере молекулы аммиака NН3.
- Зачем необходимо знать формулы при решении задач?
Задачи:
- Сколько молекул содержится в 180 граммах воды?
- Сколько молекул составляет 80 г углекислого газа?
V. Домашнее задание
Изучить текст параграфа, составить две задачи: на нахождение количества вещества; на нахождение массы вещества.
Литература:
- Гара Н.Н. Химия. Уроки в 8 классе: пособие для учителя. _ М.: Просвещение, 2009.
- Рудзитес Г.Е., Фельдман Ф.Г. Химия. 8 класс.: Учебник для общеобразовательных учебных учреждений – М.: Просвещение, 2009.
Источник
