Какое число молекул двухатомного газа содержится в сосуде объемом 20 см3 при давлении

Источник
Бесплатные решения контрольных работ из методички Чертова 1987 г. издания для студентов-заочников.
Смотрите также решения задач по молекулярной физике и термодинамике в “большом” задачнике Чертова (c примерами решений), Савельеве, Иродове.
Будьте внимательны: символы физических величин в условии и решении задачи могут отличаться.
201. Определить количество вещества ν и число N молекул кислорода массой m=0,5 кг.
202. Сколько атомов содержится в ртути: 1) количеством вещества ν=0,2 моль; 2) массой m=1 г?
203. Вода при температуре t=4° C занимает объем V=1 см3. Определить количество вещества ν и число N молекул воды.
204. Найти молярную массу М и массу mм одной молекулы поваренной соли.
205. Определить массу mм одной молекулы углекислого газа.
206. Определить концентрацию n молекул кислорода, находящегося в сосуде вместимостью V=2 л. Количество вещества ν кислорода равно 0,2 моль.
207. Определить количество вещества ν водорода, заполняющего сосуд объемом V=3 л, если концентрация молекул газа в сосуде n=2*1018 м-3…
208. В баллоне объемом V=3 л содержится кислород массой m=10 г. Определить концентрацию n молекул газа.
209. Определить относительную молекулярную массу Mr: 1) воды; 2) углекислого газа; 3) поваренной соли.
210. Определить количество вещества ν и число N молекул азота массой m=0,2 кг.
211. В цилиндр длиной l=1,6 м, заполненный воздухом при нормальном атмосферном давлении p0, начали медленно вдвигать поршень площадью основания S=200…
212. В баллоне находится газ при температуре Т1=400 К. До какой температуры T2 надо нагреть газ, чтобы его давление увеличилось в 1,5…
213. Баллон вместимостью V=20 л заполнен азотом при температуре T=400 К. Когда часть газа израсходовали, давление в баллоне понизилось на Δp=200 кПа…
214. В баллоне вместимостью V=15 л находится аргон под давлением p1=600 кПа и при температуре Т1=300 К. Когда из баллона было взято некоторое…
215. Два сосуда одинакового объема содержат кислород. В одном сосуде давление p1=2 МПа и температура T1=800 К, в другом p2=2,5…
216. Вычислить плотность ρ азота, находящегося в баллоне под давлением p=2 МПа и имеющего температуру T=400 К.
217. Определить относительную молекулярную массу Mr газа, если при температуре Т=154 К и давлении p=2,8 МПа он имеет плотность ρ=6,1 кг/м3…
218. Найти плотность ρ азота при температуре T=400 К и давлении p=2 МПа.
219. В сосуде объемом V=40 л находится кислород при температуре Т=300 К. Когда часть кислорода израсходовали, давление в баллоне понизилось на Δр=100…
220. Определить плотность ρ водяного пара, находящегося под давлением p=2,5 кПа и имеющего температуру Т=250 К.
221. Определить внутреннюю энергию U водорода, а также среднюю кинетическую энергию <ε> молекулы этого газа при температуре T=300 К, если количество…
222. Определить суммарную кинетическую энергию Ек поступательного движения всех молекул газа, находящегося в сосуде вместимостью V=3 л под давлением…
223. Количество вещества гелия ν=1,5 моль, температура T=120 К. Определить суммарную кинетическую энергию Ек поступательного движения всех молекул…
224. Молярная внутренняя энергия Um некоторого двухатомного газа равна 6,02 кДж/моль. Определить среднюю кинетическую энергию <εвр>…
225. Определить среднюю кинетическую энергию <ε> одной молекулы водяного пара при температуре Т=500 К.
226. Определить среднюю квадратичную скорость <vкв> молекулы газа, заключенного в сосуд вместимостью V=2 л под давлением p=200 кПа. Масса газа…
227. Водород находится при температуре T=300 К. Найти среднюю кинетическую энергию <εвр> вращательного движения одной молекулы, а также…
228. При какой температуре средняя кинетическая энергия <εп> поступательного движения молекулы газа равна 4,14*10-21 Дж?…
229. В азоте взвешены мельчайшие пылинки, которые движутся так, как если бы они были очень крупными молекулами. Масса каждой пылинки равна 6*10-10…
230. Определить среднюю кинетическую энергию <εк> поступательного движения и <εвр> вращательного движения…
231. Определить молярную массу М двухатомного газа и его удельные теплоемкости, если известно, что разность cp-cV удельных теплоемкостей…
232. Найти удельные cp и cV, а также молярные Cp и CV теплоемкости углекислого газа.
233. Определить показатель адиабаты γ идеального газа, который при температуре T=350 К и давлении p=0,4 МПа занимает объем V=300 л и имеет теплоемкость…
234. В сосуде вместимостью V=6 л находится при нормальных условиях двухатомный газ. Определить теплоемкость CV этого газа при постоянном объеме.
235. Определить относительную молекулярную массу Mr и молярную массу газа M, если разность его удельных теплоемкостей cp-cV=2,08…
236. Определить молярные теплоемкости газа, если его удельные теплоемкости cV=10,4 кДж/(кг*К) и cp=14,6 кДж/(кг*К).
237. Найти удельные cV и cp и молярные CV и Cp теплоемкости азота и гелия.
238. Вычислить удельные теплоемкости газа, зная, что его молярная масса M=4*10-3 кг/моль и отношение теплоемкостей Cp/CV=1,67…
239. Трехатомный газ под давлением p=240 кПа и температуре t=20° C занимает объем V=10 л. Определить теплоемкость Cp этого газа при постоянном…
240. Одноатомный газ при нормальных условиях занимает объем V=5 л. Вычислить теплоемкость CV этого газа при постоянном объеме.
241. Найти среднее число <z> столкновений за время t=1 с и длину свободного пробега <l> молекулы гелия, если газ находится под давлением p=2 кПа…
242. Определить среднюю длину свободного пробега <l> молекулы азота в сосуде вместимостью V=5 л. Масса газа m=0,5 г.
243. Водород находится под давлением p=20 мкПа и имеет температуру T=300 К. Определить среднюю длину свободного пробега <l> молекулы такого газа.
244. При нормальных условиях длина свободного пробега <l> молекулы водорода равна 0,160 мкм. Определить диаметр d молекулы водорода.
245. Какова средняя арифметическая скорость <v> молекул кислорода при нормальных условиях, если известно, что средняя длина свободного пробега <l>…
246. Кислород находится под давлением p=133 нПа при температуре T=200 К. Вычислить среднее число <z> столкновений молекулы кислорода при этих условиях…
247. При каком давлении p средняя длина свободного пробега <l> молекул азота равна 1 м, если температура газа t=10° С?
248. В сосуде вместимостью V=5 л находится водород массой m=0,5 г. Определить среднюю длину свободного пробега <l> молекулы водорода в этом сосуде.
249. Средняя длина свободного пробега <l> молекулы водорода при некоторых условиях равна 2 мм. Найти плотность ρ водорода при этих условиях.
250. В сферической колбе вместимостью V=3 л, содержащей азот, создан вакуум с давлением p=80 мкПа. Температура газа T=250 К. Можно ли считать вакуум в колбе…
251. Определить количество теплоты Q, которое надо сообщить кислороду объемом V=50 л при его изохорном нагревании, чтобы давление газа повысилось на Δp=0,5…
252. При изотермическом расширении азота при температуре Т=280 К объем его увеличился в два раза. Определить: 1) совершенную при расширении газа работу А; 2)…
253. При адиабатном сжатии давление воздуха было увеличено от p1=50 кПа до p2=0,5 МПа. Затем при неизменном объеме температура воздуха…
254. Кислород массой m=200 г занимает объем V1=100 л и находится под давлением p1=200 кПа. При нагревании газ расширился при постоянном…
255. Объем водорода при изотермическом расширении при температуре T=300 К увеличился в n=3 раза. Определить работу А, совершенную газом, и теплоту Q, полученную…
256. Азот массой m=0,1 кг был изобарно нагрет от температуры T1=200 К до температуры Т2=400 К. Определить работу А, совершенную газом,…
257. Во сколько раз увеличится объем водорода, содержащий количество вещества ν=0,4 моль при изотермическом расширении, если при этом газ получит теплоту…
258. Какая работа А совершается при изотермическом расширении водорода массой m=5 г, взятого при температуре Т=290 К, если объем газа увеличивается в три раза?…
259. Какая доля w1 количества теплоты Q, подводимого к идеальному двухатомному газу при изобарном процессе, расходуется на увеличение ΔU внутренней…
260. Определить работу А, которую совершит азот, если ему при постоянном давлении сообщить количество теплоты Q=21 кДж. Найти также изменение ΔU внутренней…
261. Идеальный газ совершает цикл Карно при температурах теплоприемника T2=290 К и теплоотдатчика T1=400 К. Во сколько раз увеличится…
262. Идеальный газ совершает цикл Карно. Температура Т1 теплоотдатчика в четыре раза (n=4) больше температуры теплоприемника. Какую долю w количества…
263. Определить работу А2 изотермического сжатия газа, совершающего цикл Карно, КПД которого η=0,4, если работа изотермического расширения равна…
264. Газ, совершающий цикл Карно, отдал теплоприемнику теплоту Q2=14 кДж. Определить температуру Т1 теплоотдатчика, если при температуре…
265. Газ, являясь рабочим веществом в цикле Карно, получил от теплоотдатчика теплоту Q1=4,38 кДж и совершил работу A=2,4 кДж. Определить температуру…
266. Газ, совершающий цикл Карно, отдал теплоприемнику 67% теплоты, полученной от теплоотдатчика. Определить температуру T2 теплоприемника, если…
267. Во сколько раз увеличится коэффициент полезного действия η цикла Карно при повышении температуры теплоотдатчика от T1=380 К до T1’=560…
268. Идеальная тепловая машина работает по циклу Карно. Температура теплоотдатчика Т1=500 К, температура теплоприемника T2=250 К. Определить…
269. Газ, совершающий цикл Карно, получает теплоту Q1=84 кДж. Определить работу А газа, если температура T1 теплоотдатчика в три раза…
270. В цикле Карно газ получил от теплоотдатчика теплоту Q1=500 Дж и совершил работу A=100 Дж. Температура теплоотдатчика T1=400 K. Определить…
271. Найти массу m воды, вошедшей в стеклянную трубку с диаметром канала d=0,8 мм, опущенную в воду на малую глубину. Считать смачивание полным.
272. Какую работу А надо совершить при выдувании мыльного пузыря, чтобы увеличить его объём от V1=8 см3 до V2=16 см3?…
273. Какая энергия Е выделится при слиянии двух капель ртути диаметром d1=0,8 мм и d2=1,2 мм в одну каплю?
274. Определить давление p внутри воздушного пузырька диаметром d=4 мм, находящегося в воде у самой ее поверхности. Считать атмосферное давление нормальным…
275. Пространство между двумя стеклянными параллельными пластинками с площадью поверхности S=100 см2 каждая, расположенными на расстоянии l=20 мкм…
276. Глицерин поднялся в капиллярной трубке с диаметром канала d=1 мм на высоту h=20 мм. Определить поверхностное натяжение α глицерина. Считать смачивание…
277. В воду опущена на очень малую глубину стеклянная трубка с диаметром канала d=1мм. Определить массу m воды, вошедшей в трубку.
278. На сколько давление р воздуха внутри мыльного пузыря больше нормального атмосферного давления р0, если диаметр пузыря d=5 мм?
279. Воздушный пузырек диаметром d=2,2 мкм находится в воде у самой ее поверхности. Определить плотность ρ воздуха в пузырьке, если воздух над поверхностью…
280. Две капли ртути радиусом r=1,2 мм каждая слились в одну большую каплю. Определить энергию Е, которая выделится при этом слиянии. Считать процесс изотермическим…
Источник

IV. МОЛЕКУЛЯРНАЯ ФИЗИКА И ТЕРМОДИНАМИКА
7.ЗАКОНЫ ИДЕАЛЬНЫХ ГАЗОВ.
МОЛЕКУЛЯРНО-КИНЕТИЧЕСКАЯ ТЕОРИЯ ГАЗОВ
Основные формулы
1. Количество вещества
ν m , или ν N ,
NA
где N – число структурных элементов системы (молекул, атомов, ионов и т. д.); NA – постоянная Авогадро; – молекулярная масса.
2. Уравнение состояния идеальных газов (уравнение Менделеева– Клапейрона)
pV m RT ,
где т – масса газа; – молярная масса газа; R – универсальная газовая постоянная; Т – термодинамическая температура.
3. Закон Дальтона
p p1 p2 … pn,
где р – давление смеси газов; рi – парциальное давление i-го компонента смеси;
п – число компонентов смеси. 4. Молярная масса смеси газов
cм m1 m2 … mn . ν1 ν2 … νn
5. Концентрация частиц (молекул, атомов и т.п.) однородной системы
n N V NA
V NA  .
.
где V – объем системы; – плотность вещества.
6. В МКТ пользуются физической (идеализированной) моделью, называемой идеальным газом, согласно которой:
а) собственный объем молекул газа пренебрежимо мал по сравнению с объемом сосуда.
б) пренебрегают силами взаимодействия между молекулами. Следовательно, потенциальная энергия взаимодействия молекул принимается равной нулю, а внутренняя энергия идеально газа – равной средней кинетической энергии молекул.
в) столкновения молекул газа между собой и со стенками сосуда абсолютно упругие.
68

Заметим, что понятие идеального газа не применимо при очень низких температурах (близких к температуре конденсации данного газа) и при очень высоких давлениях.
Макропараметры газа р, V, T.
Основное уравнение МКТ идеального газа – уравнение, которое связывает макропараметры идеального газа с микропараметрами:
р | 1 | nm V 2 , | (3.1) | ||||||||||||||||||||||||||||||||
3 | ср | ||||||||||||||||||||||||||||||||||
где р – давление газа; m0 – масса молекулы газа m0 | ; n – число моле- | ||||||||||||||||||||||||||||||||||
кул газа в единице объема; Vср2 | NA | ||||||||||||||||||||||||||||||||||
– среднеквадратичная скорость молекул. | |||||||||||||||||||||||||||||||||||
р | 1 | nm V 2 | 2 | nm | Vср2 | 2 | n E | , | (3.2) | ||||||||||||||||||||||||||
2 | |||||||||||||||||||||||||||||||||||
3 | 0 ср | 3 | 3 | кин | |||||||||||||||||||||||||||||||
где Eкин | – средняя кинетическая энергия поступательного движения моле- | ||||||||||||||||||||||||||||||||||
кулы. | 3 | ||||||||||||||||||||||||||||||||||
Eкин | kT, | (3.3) | |||||||||||||||||||||||||||||||||
R | 2 | ||||||||||||||||||||||||||||||||||
где k | – постоянная Больцмана (k = 1,38 · 10–23 Дж/К). | ||||||||||||||||||||||||||||||||||
NA | |||||||||||||||||||||||||||||||||||
Основное управление МКТ можно записать в виде | |||||||||||||||||||||||||||||||||||
р nkT. | (3.4) | ||||||||||||||||||||||||||||||||||
Из уравнения (3.3) следует, что кинетическая энергия не зависит от ро- | |||||||||||||||||||||||||||||||||||
да вещества, а зависит только от температуры. | |||||||||||||||||||||||||||||||||||
7. Скорость молекул: средняя квадратичная | |||||||||||||||||||||||||||||||||||
vкв | , | или | vкв | ; | |||||||||||||||||||||||||||||||
3kT m1 | 3RT | ||||||||||||||||||||||||||||||||||
средняя арифметическая | |||||||||||||||||||||||||||||||||||
v | , | или | v | ; | |||||||||||||||||||||||||||||||
8kT m1 | 8RT | ||||||||||||||||||||||||||||||||||
наиболее вероятная | |||||||||||||||||||||||||||||||||||
v | , | или | v | 2RT | , | ||||||||||||||||||||||||||||||
в | 2kT m | в | |||||||||||||||||||||||||||||||||
1 | |||||||||||||||||||||||||||||||||||
где т1 – масса одной молекулы. | |||||||||||||||||||||||||||||||||||
69
Примеры решения задач
Задача 1. Сколько молекул содержится в 1 м3 водорода при нормальных условиях? Какова масса одной молекулы водорода?
Д а н о:
V = 1 м3
T = 273 ºК р = 1·105 Па
= 2·10–3 кг/моль
п0 = ? т = ?
Р е ш е н и е
Число молекул в одном моле любого газа (число Авогадро) NА = 6,02·1023 1/моль. Объем одного моля любого газа (в том числе и водорода) при нормальных условиях V0 = 22, 4 л/моль = 22,4·10–3 м3/моль.
Следовательно, число молекул водорода, содержащихся в 1 м3 при нормальных условиях, определяется соотношением
n0 NA 2,69 1025 1/моль.
V0
Эта величина одинакова для любого газа и называется числом Лошмидта. Масса одной молекулы водорода
NA
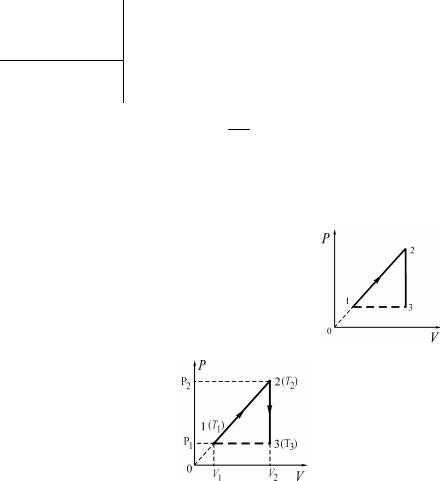
Задача 2. Моль одноатомного идеального газа участвует в процессе 1–2–3, представленном на p–V диаграмме.
Всостоянии 1 температура газа равна Т1 =
=100 ºК, а в состоянии 2 – Т2 = 400 ºК. Определите температуру газа Т3 в точке 3.
Т1 | Дано: | Решение |
= 100 ºК | ||
Т2 | = 400 ºК | V1 p1; |
Т3 = ? | ||
V2 p2. | ||
Запишем уравнение Менделеева–Клапейрона для состояний газа 1 и2:
pV RT ; | p2 RT ; | |||||
1 | 1 | 1 | 1 | 1 | ||
p2 RT | p2 | T | ||||
p V RT , | или | 1 | 1 | . | ||
p2 | ||||||
2 2 | 2 | 2 | 2 | T | ||
2 | 2 | |||||
70 | ||||||
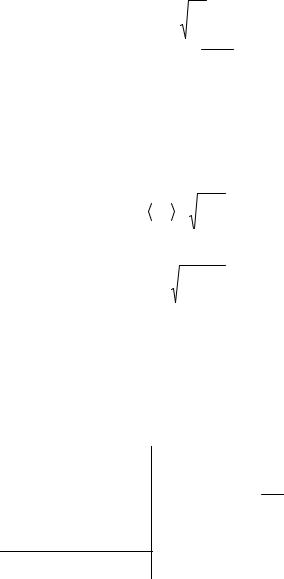
Для изохорического процесса (2–3) можно записать:
p1 | T3 | ; | T1 | T3 | , следовательно, | ||
p2 | T2 | T2 | T2 | ||||
T3 
 T1 T2 200К.
T1 T2 200К.
Задача 3. Температур поверхностного слоя Солнца (фотосферы) – около 6000 ºК. Почему с поверхности Солнца не улетают атомы водорода, из которых в основном состоит фотосфера?
Р е ш е н и е
Средняя квадратичная скорость атомов водорода в фотосфере
Вторая космическая скорость
Как видно, средняя квадратичная скорость в 51 раз меньше второй космической скорости, поэтому большинство атомов водорода не могут вырваться из поля тяготения Солнца.
Задача 4. Определить плотность смеси 4 г водорода и 32 г кислорода при температуре 7 ºС и давлении 700 мм рт.ст.
Д а н о:
m1 = 4 г = 0,004 кг1 = 2·10–3 кг/моль m2 = 32 г = 0,032 кг
2 = 32·10–3 кг/моль T = 280 0К
рсм = 700 мм рт.ст. = = 700·133 = 9,31·104 Па
см = ?
отсюда
Р е ш е н и е
Чтобы найти плотность смеси, необходимо знать ее массу и объем, тогда
cм mсм ; mсм m1 m2 .
V
Объем смеси можно найти, используя уравнение Менделеева–Клапейрона:
p | см | p p | 2 | ; p V | m1 | RT; | p V | m2 | RT ; | |||||||
1 | 1 | 1 | 2 | 2 | ||||||||||||
m | m | 2 | RT | |||||||||||||
pсм | 1 | , | ||||||||||||||
V | ||||||||||||||||
2 | ||||||||||||||||
1 | ||||||||||||||||
71

m | m | ||||||||||
1 | 2 | ||||||||||
1 | 2 | RT | |||||||||
V | , | ||||||||||
и тогда | pсм | ||||||||||
4 10 3 | 32 10 3 9,31 104 | ||||||||||
m1 | m2 pсм | 3 | |||||||||
см | 0,48 кг/м . | ||||||||||
m | m | 2 | 4 10 | 3 | 32 10 | 3 | |||||
1 | RT | 8,31 280 | |||||||||
3 | 3 | ||||||||||
1 | 2 10 | 32 10 | |||||||||
2 | |||||||||||
Задача 5. На осях р-V изображены графически процессы, с помощью которых идеальный газ был переведен из состояния 1 в состояние 4. Начертить, как будут выглядеть эти же процессы 1-2, 2-3 и
3-4 на осях р-Т и V-Т, если 1-2 – изотерма. Расшифруем, графики каких процессов пока-
заны на осях:
1-2 – изотермическое сжатие;
2-3 – изобарическое сжатие;
3-4 – изохорический процесс с понижением давления.
Вычертим графики этих же процессов на других осях.
72
Задачи
7-1. В баллоне объемом 22,4 л находится водород при нормальных условиях. После того как в баллон было дополнительно введено некоторое количество гелия, давление в баллоне возросло до р2 = 0,25 МПа, а температура не изменилась. Определить массу гелия, введенного в баллон.
7-2. Смесь водорода и азота общей массой т = 290 г при температуре Т = 600 ºК и давлении р = 2,46 МПа занимает объем V = 30 л. Определить массу т1 водорода и массу т2 азота.
7-3. Оболочка воздушного шара имеет объем V = 1 600 м3. Найти подъемную силу FП водорода, наполняющего оболочку, на высоте, где давление р = 60 кПа и температура Т = 280 ºК. При подъеме шара водород может выходить через отверстиев нижней части.
7-4. Водород находится при температуре Т = 300 ºК. Найти среднюю кинетическую энергию вращательного движения одной молекулы, а также суммарную кинетическую энергию всех молекул этого газа; количество вещества водорода = 0,5 моль.
7-5. В баллоне объемом 10 л находится гелий под давлением р1 = 1 МПа при температуре Т1 = 300 ºК. После того как из баллона было взято 10 г гелия, температура в баллоне понизилась до Т2 = 290 ºК. Определить давление р2 гелия, оставшегося в баллоне.
7-6. Баллон содержит т1 = 80 г кислорода и т2 = 320 г аргона. Давление смеси р = 1 МПа, температура 300 ºК. Принимая данные газа за идеальные, определить объем баллона.
7-7. Какой объем занимает смесь азота массой т1 = 1 кг и гелия массой т2 = 1 кг при нормальных условиях?
7-8. В баллоне емкостью 15 л находится смесь, содержащая т1 = 10 г водорода, т2 = 54 г водяного пара и т3 = 60 г окиси углерода. Температура смеси 27 ºС. Определить давление.
7-9. Количество вещества гелия = 1,5 моль, температура Т = 120 ºК. Определить суммарную кинетическую энергию поступательного движения всех молекул этого газа.
7-10. Теплоизолированный сосуд объемом V = 2 м3 разделен пористой перегородкой на две равные части. Атомы гелия могут свободно проникать через поры в перегородке, а атомы аргона – нет. В начальный момент в одной части сосуда находится m = 1 кг гелия, а в другой – m = 1 кг аргона, а средняя квадратичная скорость атомов аргона игелия одинакова и составляет1000 м/с.
Определить температуру гелий-аргоновой смеси после установления равновесия в системе.
7-11. Найти плотность газовой смеси водорода и кислорода, если их массовые доли 1 и 2 равны соответственно 1/9 и 8/9. Давление смеси равно 100 кПа, температура Т = 300 ºК.
7-12. В сосуде объемом 2,24 л при нормальных условиях находится кислород. Определить количество вещества и массу т кислорода, а также концентрацию п0 его молекул в сосуде.
73

7-13. В сосуде находится смесь 10 г углекислого газа (СО2) и 15 г азота (N2). Найти плотность этой смеси при температуре 27 0С и давлении 1,5·105 Па.
7-14. Сосуд объемом 20 л содержит смесь водорода и гелия при температуре t = 20 ºС и давлении 2 атм. Масса смеси т = 5 г. Найти отношение массы водорода к массе гелия в данной смеси.
7-15. В баллон емкостью V = 12 л поместили т1 = 1,5 кг азота при температуре t1 = 327 ºС. Какое давление р2 будет создавать азот в баллоне при температуре t2 = 50 ºС, если 35 % азота будет выпущено. Каково было начальное дав-
ление р1?
7-16. На дне сосуда, заполненного воздухом, лежит полыйстальной шарик радиусом r = 2 см. Масса шарика 5 г. До какого давления р надо сжать воздух в сосуде, чтобы шарик поднялся вверх? Считать, что воздух при больших давлениях подчиняется уравнению газового состояния. Температура воздуха t = 20 ºС = = const (сжатие воздуха происходитдостаточно медленно).
7-17. На какой глубине радиус пузырька воздуха вдвое меньше, чем у поверхности воды, если давление у поверхности равно р0?
7-18. Определить температуру газа, находящегося в закрытом баллоне, если его давление увеличилось на 0,4 % первоначально при нагревании на
T = 1 К.
7-19. Тонкостенный резиновый шар собственным весом 0,6 Н наполнен неоном и погружен в озеро на глубину h = 120 м. Найти массу неона, если шар находится в положении равновесия. Атмосферное давление р0 = 1,03·105 Па, температура на глубине озера t = + 4 ºС. Натяжением резины пренебречь.
7-20. В закрытом сосуде емкостью V = 2 м3 находится т1 = 2,7 кг воды и т2 = 3,2 кг кислорода. Найти давление в сосуде при температуре t = 527 ºС, зная, что в этих условиях вся вода превращается в пар (считать, что пар в данном случае подчиняется законам идеального газа).
7-21. В теплоизолированный сосуд объемом V = 2 л, содержащий одноатомный идеальный газ при температуре Т1 = 300 К, помещают кусочек железа массой m = 100 г, нагретый до температуры Т2 = 500 К. Определить давление р2 газа после установления теплового равновесия, если его начальное давление равно р1 = 105 Па. Объемом железа по сравнению с объемом сосуда пренебречь. Удельная теплоемкость железа с = 0,46 · 103 Дж/кг·К.
7-22. В идеальном газе происходят процессы 1-2; 2-3; 3-4. Изобразить эти процессы на координатных осях р–T, р–V.
7-23. В лифте, движущимся с ускорением а = 5 м/с2, направленным вверх, находится цилиндрический сосуд, закрытый поршнем массой М = 20 кг и площадью S = 100 см2. Под поршнем находится идеальный газ. Поршень расположен на расстоянии h = 22 см от дна сосуда. Определите, на
74

какую величину h переместится поршень, если лифт будет перемещаться с тем же по модулю ускорением, направленным вниз. Температура газа не изменяется, атмосферное давление p0 = 105 Па. Ускорение свободного падения поршня g = 10 м/с2. Трением поршня о стенки сосуда пренебречь.
7-24. В цилиндре под невесомым поршнем площадью S = 100 см2 находится 1 моль идеального газа при температуре t1 = 100 ºС. К поршню через два блока на невесомой нерастяжимой нити подвешен груз массой М = 17 кг. На какую высоту h поднимется груз, если охладить газ до температуры t2 = 0 ºС. Атмосферное давление p0 = 105 Па. Трением пренебречь.
7-25. В вертикально расположенном цилиндрическом сосуде находится идеальный газ массой m с молярной массой . Газ отделен от атмосферы поршнем, соединенным с дном сосуда с пружиной жесткости k. При температуре T1 поршень расположен н?
