Какими свойствами обладают вещества с ионной кристаллической решеткой
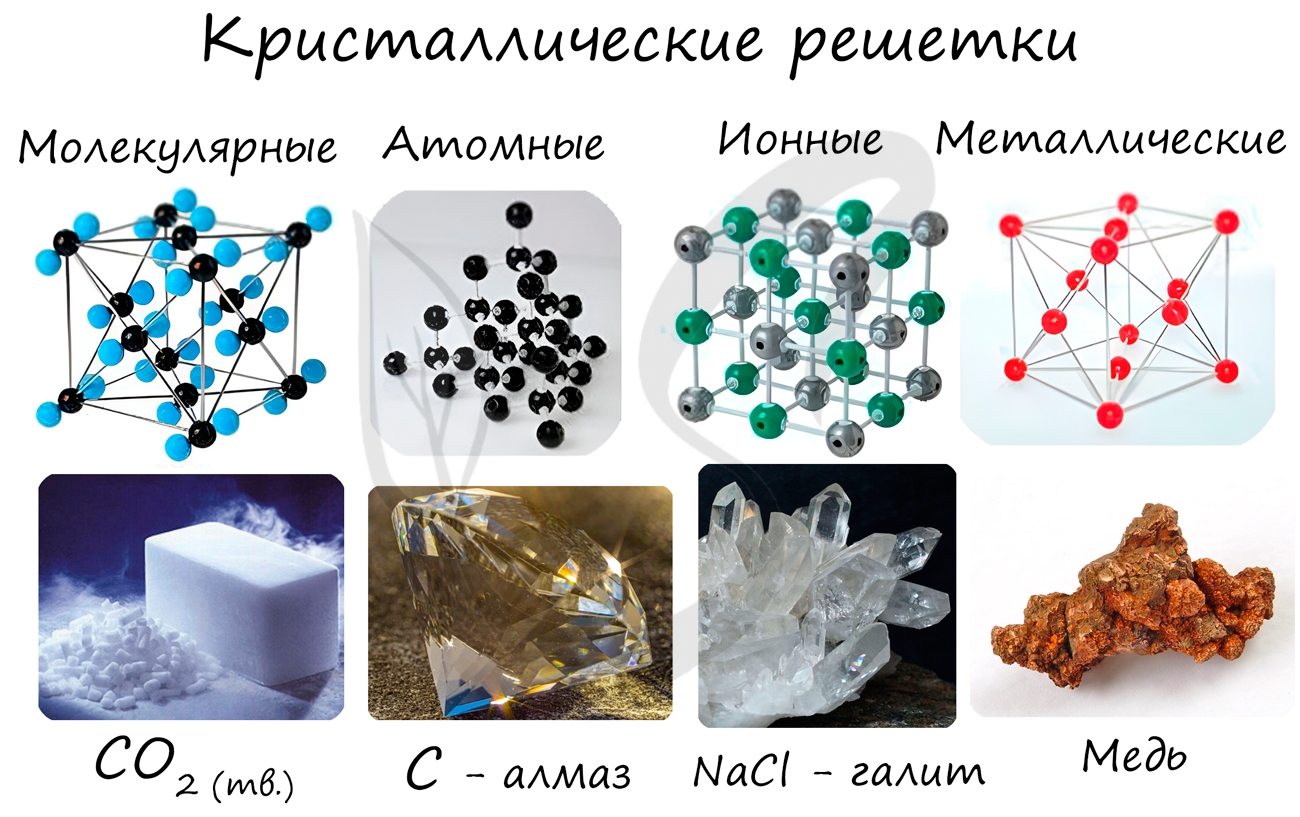
Кристаллические решетки
Твердые вещества бывают аморфные или кристаллические (чаще всего имеют кристаллическое строение).
Кристаллическое строение характеризуется правильным расположением частиц в определенных точках пространства. При соединении этих точек воображаемыми прямыми линиями образуется так называемая кристаллическая решетка Точки, в которых размещены частицы, называются узлами кристаллической решетки.
В узлах кристаллической решетки могут находиться ионы, атомы или молекулы.
В зависимости от вида частиц, расположенных в узлах кристаллической решетки, и характера связи между ними различают четыре типа кристаллических решеток: ионные, атомные, молекулярные и металлические.
Ионная решетка
Эту решетку образуют все вещества с ионным типом связи — соли, щелочи, бинарные соединения активных металлов с активными неметаллами (оксиды, галогениды, сульфиды), алкоголяты, феноляты, соли аммония и аминов. Примеры: КОН, СаСО$_3$, СН$_3$СООК, NH$_4$NO$_3$, [CH$_3$NH$_3$]Cl, С$_2$Н$_5$ОК. В узлах решетки — ионы, между которыми существует электростатическое притяжение. Ионная связь очень прочная.

Свойства ионных кристаллов:
твердые, но хрупкие;
отличаются высокими температурами плавления;
нелетучи, не имеют запаха;
расплавы ионных кристаллов обладают электропроводностью;
многие растворимы в воде. При растворении в воде диссоциируют на катионы и анионы, и образующиеся растворы проводят электрический ток.
Атомная решетка
В узлах решетки — атомы, связанные ковалентными связями. Химическая связь — ковалентная полярная или неполярная. Атомная кристаллическая решетка характерна для углерода (алмаз, графит — рисунок), бора, кремния, германия, оксида кремния SiO$_2$ (кремнезем, кварц, речной песок), карбида кремния SiC (карборунд), нитрида бора BN. Свойства: высокая твердость, высокие температуры плавления, нерастворимость, нелетучесть, отсутствие запаха.
Свойства веществ с атомной кристаллической решеткой:
высокая твердость;
высокие температуры плавления;
нерастворимость;
нелетучесть;
отсутствие запаха.
Металлическая решетка
Реализуется в простых веществах — металлах и их сплавах. В узлах решетки — атомы и катионы металла, при этом электроны металла обобществляются и образуют так называемый электронный газ, который движется между узлами решетки, обеспечивая ее устойчивость.

Молекулярные решетки
В узлах — молекулы веществ, которые удерживаются в узлах решетки с помощью слабых межмолекулярных сил.
Молекулярное строение имеют:
все органические вещества (кроме солей);
вещества — газы и жидкости;
легкоплавкие и летучие твердые вещества, в молекулах которых ковалентные связи (полярные и неполярные).
Подобные вещества часто имеют запах.
Обобщающая таблица
Кристаллические решетки, вид связи и свойства веществ
| Тип решетки | Виды частиц в узлах решетки | Вид связи между частицами | Примеры веществ | Физические свойства веществ |
| Ионная | Ионы | Ионная — связь прочная | Соли, галогениды (IA, IIA), оксиды и гидроксиды щелочных и щел.-зем. металлов | Твердые, прочные, нелетучие, хрупкие, тугоплавкие, многие растворимы в воде, расплавы проводят электрический ток |
| Атомная | Атомы | 1. Ковалентная неполярная — очень прочная 2. Ковалентная полярная связь — очень прочная. Простые вещества: алмаз (C), графит (C), бор (B), кремний (Si) | Сложные вещества:оксид алюминия (Al$_2$O$_3$), оксид кремния (IV) SiO$_2$ | Очень твердые, очень тугоплавкие, прочные, нелетучие, нерастворимы в воде |
| Молекулярная | Молекулы | Между молекулами слабые силы межмолекулярного притяжения, внутри молекул прочная ковалентная связь | При обычных условиях – газы, жидкости или летучие твердые вещества (О$_2$, Н$_2$, Cl$_2$, N$_2$, Br$_2$, H$_2$O, CO$_2$, HCl); сера, белый фосфор, иод; органические вещества | Непрочные, летучие, легкоплавкие, способны к возгонке, имеют небольшую твердость |
| Металлическая | Атом-ионы | Металлическая разной прочности | Металлы и сплавы | Ковкие, обладают блеском, пластичностью, тепло- и электропроводны |
Источник
Ионными называют кристаллические решетки, в узлах которых находятся ионы. Их образуют вещества с ионной связью. Ионные кристаллические решётки имеют соли, некоторые оксиды и гидроксиды металлов. Рассмотрим строение кристалла поваренной соли, в узлах которого находятся ионы хлора и натрия.
Связи между ионами в кристалле очень прочные и устойчивые.Поэтому вещества с ионной решёткой обладают высокой твёрдостью и прочностью, тугоплавки и нелетучи.
Вещества с ионной кристаллической решеткой обладают следующими свойствами:
1. Относительно высокой твердостью и прочностю;
2. Хрупкостью;
3. Термостойкостью;
4. Тугоплавкостью;
5. Нелетучестью.
Примеры: соли – хлорид натрия, карбонат калия, основания – гидрооксид кальция, гидрооксид натрия.
4. Механизм образования ковалентной связи (обменный и донорно-акцепторный).
Каждый атом стремится завершить свой внешний электронный уровень, чтобы уменьшить потенциальную энергию. Поэтому ядро одного атома притягивается к себе электронную плотность другого атома и наоборот, происходит наложение электронных облаков двух соседних атомов.
Демонстрация аппликации и схемы образования ковалентной неполярной химической связи в молекуле водорода. (Учащиеся записывают и зарисовывают схемы).
Вывод: Связь между атомами в молекуле водорода осуществляется за счет общей электронной пары. Такая связь называется ковалентной.
Прочитать стр. 33 в учебнике и записать определение.
Какую связь называют ковалентной неполярной? (Учебник стр. 33).
Составление электронных формул молекул простых веществ неметаллов:
•• ••
•• CI •• CI •• – электронная формула молекулы хлора,
•• ••
CI — CI – структурная формула молекула хлора.
••
•• N •• N •• – электронная формула молекулы азота,
••
N ≡ N – структурная формула молекулы азота.
Электроотрицательность. Ковалентные полярная и неполярная связи. Кратность ковалентной связи.
Но молекулы могут образовывать и разные атомы неметаллов и в этом случае общая электронная пара будет смещаться к более электроотрицательному химическому элементу.
Изучить материал учебника на стр. 34
Вывод: Металлы имеют более низкое значение электроотрицательности, чем неметаллы. И между ними она сильно отличается.
Демонстрация схемы образования полярной ковалентной связи в молекуле хлороводорода.
Общая электронная пара смещена к хлору, как более электроотрицательному. Значит это ковалентная связь. Она образована атомами, электроотрицательности которых несильно отличаются, поэтому это ковалентная полярная связь.
Составление электронных формул молекул йодоводорода и воды:
••
H •• J •• – электронная формула молекулы йодоводорода,
••
H → J – структурная формула молекулы йодоводорода.
••
H •• O •• – электронная формула молекулы воды,
••
H
Н →О – структурная формула молекулы воды.
↑
Н
Самостоятельная работа с учебником: выписать определение электроотрицательности.
Молекулярные и атомные кристаллические решетки. Свойства веществ с молекулярными и атомными кристаллическими решетками
Самостоятельная работа с учебником.
Вопросы для самоконтроля
– Атом, какого химического элемента имеет заряд ядра +11
– Записать схему электронного строения атома натрия
– Внешний слой завершен?
– Как добиться завершения заполнения электронного слоя?
– Составить схему отдачи электрона
– Сравнить строение атома и иона натрия
– Сравнить строение атома и иона инертного газа неона.
– Определить атом, какого элемента с количеством протонов 17.
– Запишите схему электронного строения атома.
– Слой завершен? Как этого добиться.
– Составить схему завершения электронного слоя хлора.
Задание по группам:
1-3 группа: Cоставьте электронные и структурные формулы молекул веществ и укажите тип связи Br2 ; NH3.
4-6 группы: Cоставьте электронные и структурные формулы молекул веществ и укажите тип связи F2 ; HBr.
Два ученика работают у дополнительной доски с этим же заданием для образца к самопроверке.
Устный опрос.
1. Дайте определение понятия «электроотрицательность».
2. От чего зависит электроотрицательность атома?
3. Как изменяется электроотрицательность атомов элементов в периодах?
4. Как изменяется электроотрицательность атомов элементов в главных подгруппах?
5. Сравните электроотрицательность атомов металлов и неметаллов. Отличаются ли способы завершения внешнего электронного слоя, характерные для атомов металлов и неметаллов? Каковы причины этого?
7. Какие химические элементы способны отдавать электроны, принимать электроны?
Что происходит между атомами при отдаче и принятии электронов?
Как называют частицы, образовавшиеся из атома в результате отдачи или присоединения электронов?
8. Что произойдет при встрече атомов металла и неметалла?
9. Как образуется ионная связь?
10. Химическая связь, образуемая за счет образования общих электронных пар называется …
11. Ковалентная связь бывает … и …
12. В чем сходство ковалентной полярной и ковалентной неполярной связи? От чего зависит полярность связи?
13. В чем различие ковалентной полярной и ковалентной неполярной связи?
ПЛАН ЗАНЯТИЯ № 8
Дисциплина: Химия.
Тема:Металлическая связь. Агрегатные состояния веществ и водородная связь.
Цель занятия: Сформировать понятие об химических связях на примере металлической связи. Добиться понимания механизма образования связи.
Планируемые результаты
Предметные: формировании кругозора и функциональной грамотности человека для решения практических задач; умение обрабатывать, объяснять результаты; готовность и способность применять методы познания при решении практических задач;
Метапредметные: использование различных источников для получения химической информации, умение оценить ее достоверность для достижения хороших результатов в профессиональной сфере;
Личностные: умение использовать достижения современной химической науки и химических технологий для повышения собственного интеллектуального развития в выбранной профессиональной деятельности;
Норма времени:2 часа
Вид занятия:Лекция.
План занятия:
1. Металлическая связь. Металлическая кристаллическая решетка и металлическая химическая связь.
2. Физические свойства металлов.
3. Агрегатные состояния веществ. Переход вещества из одного агрегатного состояния в другое.
4. Водородная связь
Оснащение: Периодическая система химических элементов, кристаллическая решетка, раздаточный материал.
Литература:
1. Химия 11 класс: учеб. для общеобразоват. организаций Г.Е. Рудзитис, Ф.Г. Фельдман. – М.:Просвещение, 2014. -208 с.: ил..
2. Химия для профессий и специальностей технического профиля: учебник для студ. учреждений сред. проф. образования / О.С.Габриелян, И.Г. Остроумов. – 5 – изд., стер. – М.: Издательский центр «Академия», 2017. – 272с., с цв. ил.
Преподаватель: Тубальцева Ю.Н.
Источник
Кристаллической решеткой называют пространственное расположение атомов или ионов в кристалле. Точки
кристаллической решетки, в которых расположены атомы или ионы, называют узлами кристаллической решетки.
Кристаллические решетки подразделяют на молекулярные, атомные, ионные и металлические.

Очень важно не перепутать вид химической связи и кристаллической решетки. Помните, что кристаллические решетки отражают
пространственное расположение атомов.
Молекулярная кристаллическая решетка
В узлах молекулярной решетки расположены молекулы. При обычных условиях молекулярную решетку имеют большинство газов и жидкостей.
Связи чаще всего ковалентные полярные или неполярные.
Классическим примером вещества с молекулярной решеткой является вода, так что ассоциируйте свойства этих веществ с водой. Вещества с
молекулярной решеткой непрочные, имеют небольшую твердость, летучие, легкоплавкие, способны к возгонке, для них характерны небольшие
температуры кипения.
Примеры: NH3, H2O, Cl2, CO2, N2, Br2, H2, I2.
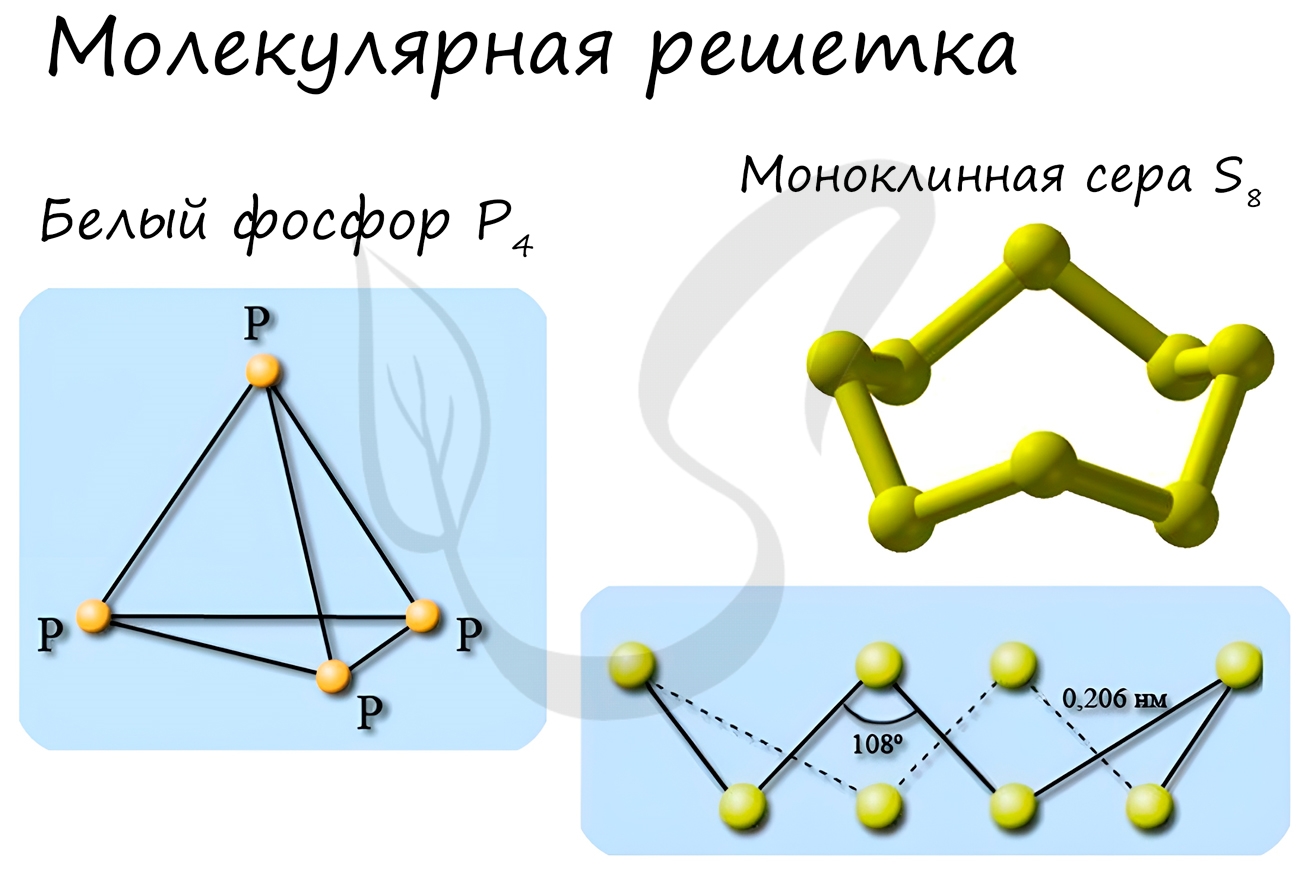
Особо хочется отметить красный и белый фосфор, ромбическую, пластическую и моноклинную серу, фуллерен. Эти аллотропные модификации мы
подробно изучили в статье, посвященной классификации веществ.
Ионная кристаллическая решетка
В узлах ионной решетки находятся атомы, связанные ионной связью. Этот тип решетки характерен для веществ, обладающих ионной связь: соли,
оксиды и гидроксиды металлов.
Ассоциируйте этот ряд веществ с поваренной солью – NaCl. Веществе с ионной решеткой имеют высокие температуры плавления и кипения, легко
растворимы в воде, хрупкие, твердые, их растворы и расплавы проводят электрический ток.
Примеры: NaCl, MgCl2, NH4Br, KNO3, Li2O, Na3PO4.

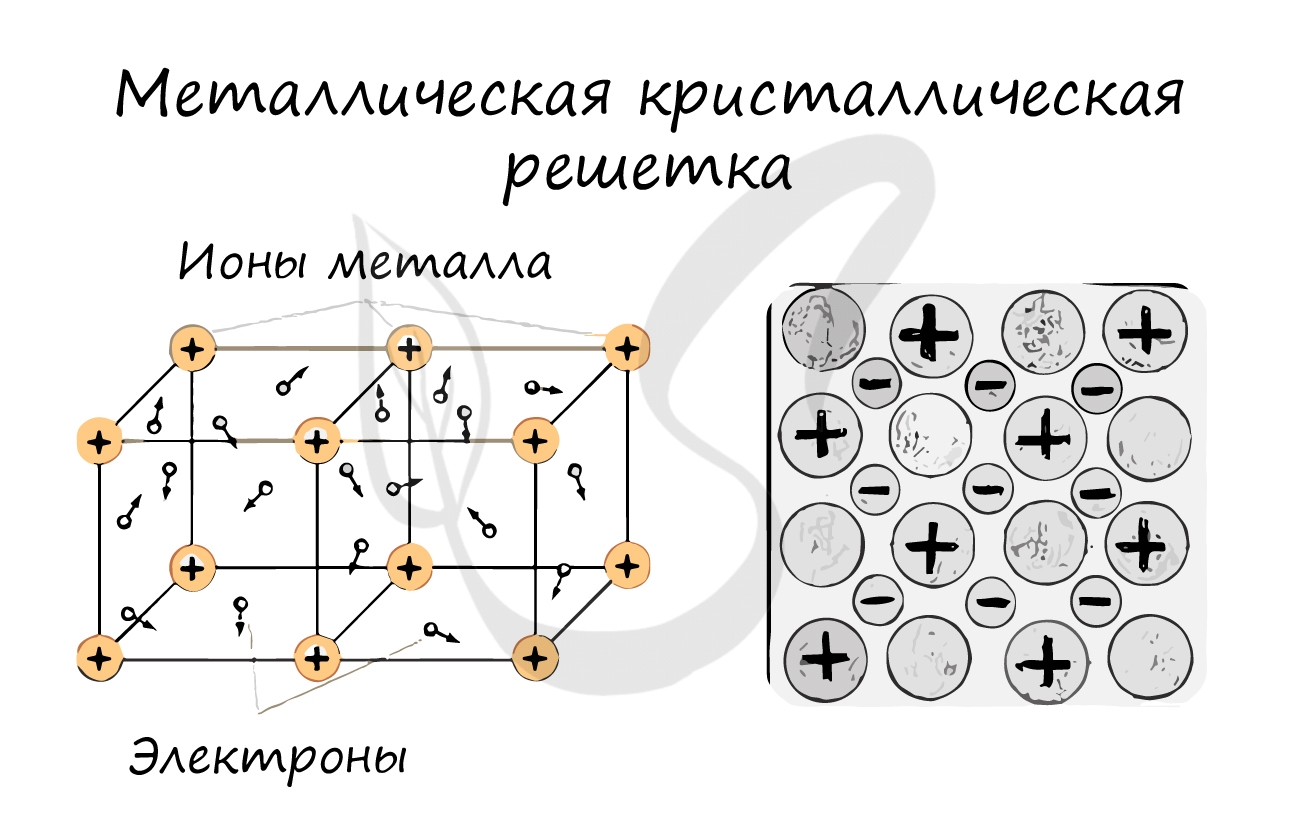
Металлическая кристаллическая решетка
В узлах металлической решетки находятся атомы металла. Этот тип решетки характерен для веществ, образованных металлической связью.
Ассоциируйте свойства этих веществ с медью. Они обладают характерным металлическим блеском, ковкие и пластичные, хорошо проводят
электрический ток и тепло, имеют высокие температуры плавления и кипения.
Примеры: Cu, Fe, Zn, Al, Cr, Mn.
Атомная кристаллическая решетка
В узлах атомной решетки находятся атомы, связанные ковалентной полярной или неполярной связью.
Ассоциируйте эти вещества с песком. Они очень твердые, очень тугоплавкие (высокая температура плавления), нелетучие, прочные,
нерастворимы в воде.
Примеры: SiO2, B, Ge, SiC, Al2O3. Особенно хочется выделить: алмаз и графит (C), черный фосфор (P).

© Беллевич Юрий Сергеевич 2018-2020
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение
(в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов
без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования,
обратитесь, пожалуйста, к Беллевичу Юрию.
Источник
Взаимосвязь
типа химической связи с видом кристаллической решеткиВещества и кристаллические решетки
Твердые вещества бывают аморфные или кристаллические (чаще
всего имеют кристаллическое строение).Кристаллическое строение характеризуется
правильным расположением частиц в определенных точках пространства. При
соединении этих точек воображаемыми прямыми линиями образуется так называемая
кристаллическая решетка. Точки, в которых размещены частицы, называются узлами кристаллической решетки.В узлах кристаллической решетки могут
находиться ионы, атомы или молекулы.В зависимости от вида частиц,
расположенных в узлах кристаллической решетки, и характера связи между ними
различают четыре типа кристаллических решеток:
·
ионные,·
атомные,·
молекулярные и·
металлические.Ионная решетка
Эту решетку образуют все вещества с
ионным типом связи — соли, щелочи, бинарные соединения активных металлов с
активными неметаллами (оксиды, галогениды, сульфиды), алкоголяты, феноляты,
соли аммония и аминов. В узлах решетки — ионы, между которыми существует
электростатическое притяжение. Ионная связь очень прочная.Примеры:
КОН, СаСО3, СН3СООК, NH4NO3, [CH3NH3]Cl,
С2Н5ОК.Свойства ионных кристаллов:
· твердые, но хрупкие;
· отличаются высокими температурами
плавления;· нелетучи, не имеют запаха;
· расплавы ионных кристаллов обладают
электропроводностью;· многие растворимы в воде; при растворении
в воде диссоциируют на катионы и анионы, и образующиеся растворы проводят
электрический ток.Металлическая решетка
Характерна для веществ с металлической
связью. Реализуется в простых веществах — металлах и их сплавах. В узлах
решетки — атомы и катионы металла, при этом электроны металла обобществляются и
образуют так называемый электронный газ, который движется между узлами решетки,
обеспечивая ее устойчивость. Именно свободно перемещающимися электронами и
обусловлены свойства веществ с
металлической решеткой:·
тепло- и электропроводность;·
обладают металлическим блеском;·
высокие температуры плавления.Атомная решетка
В узлах решетки — атомы, связанные
ковалентными связями. Химическая связь — ковалентная полярная или неполярная.
Атомная кристаллическая решетка характерна для углерода (алмаз, графит),
бора, кремния, германия, оксида кремния SiO2(кремнезем, кварц,
речной песок), карбида кремния SiC (карборунд), нитрида бора BN.Свойства веществ с атомной решеткой:
·
высокая твердость;·
высокие температуры плавления;·
нерастворимость;·
нелетучесть;·
отсутствие запаха.Молекулярная решетка
В узлах — молекулы веществ, которые
удерживаются в решетке с помощью слабых межмолекулярных сил.Молекулярное
строение имеют:o все органические вещества (кроме солей);
o вещества — газы и жидкости;
o легкоплавкие и летучие твердые вещества, в молекулах
которых ковалентные связи (полярные и неполярные).Подобные вещества часто имеют запах.
Обобщающая таблица
Кристаллические решетки, вид связи и
свойства веществ
Тип решетки
Виды частиц в узлах решетки
Вид связи между частицами
Примеры веществ
Физические свойства веществ
Ионная
Ионы
Ионная связь — прочная
Соли, галогениды (IA,IIA), оксиды и гидроксиды щелочных и щел.-зем.
металловТвердые, прочные, нелетучие, хрупкие, тугоплавкие, многие растворимы в
воде, расплавы проводят электрический токАтомная
Атомы
1. Ковалентная неполярная -очень прочная
2. Ковалентная полярная связь — очень прочная
Простые вещества: алмаз (C), графит (C), бор (B), кремний (Si)
Сложные вещества: оксид алюминия (Al2O3), оксид кремния
(IV) SiO2Очень твердые, очень тугоплавкие, прочные, нелетучие, нерастворимы в воде
Молекулярная
Молекулы
Между молекулами — слабые силы межмолекулярного притяжения, внутри
молекул — прочная ковалентная связьПри обычных условиях — газы, жидкости или летучие твердые вещества:
(О2,Н2,Cl2,N2,Br2,
H2O, CO2, HCl); сера, белый фосфор, йод; органические
веществаНепрочные, летучие, легкоплавкие, способны к возгонке, имеют небольшую
твердостьМеталлическая
Атом-ионы
Металлическая связь — разной прочности
Металлы и сплавы
Ковкие, обладают блеском, пластичностью, тепло- и электропроводны
источник информации: https://foxford.ru/wiki/himiya/vzaimosvyaz-tipa-himicheskoy-svyazi-s-vidom-kristallicheskoy-reshetki
Источник


