Какими свойствами обладают почвенные коллоиды
Высокодисперсная часть почвы состоит преимущественно из коллоидов. Почвенные коллоиды – совокупность почвенных частичек размером от 1 до 100 нм. Таким образом, коллоидные растворы занимают промежуточное положение между истинными, или молекулярными растворами (размер частичек 100 нм), с другой.

Почву относят к сложной полидисперсной системе – в ее состав входят частицы различного размера. Исключительно важную роль играет высокодисперсная часть почвы. Она представлена частицами, имеющими размер меньше 0,001 мм. Их содержание в почве может колебаться от 1–2% до 30–40% к массе почвы. Значение высокодисперсной части почвы состоит в том, что она во многом определяет физические и водно-физические свойства почвы, режим питания растений, поглотительную способность почвы.
Происхождение почвенных коллоидов может быть связано с лиспегацией (раздроблением) более крупных частичек, что происходит при выветривании пород. Другой путь образования коллоидов – в результате активизации поликонденсации и полимеризации низкомолекулярных органических соединений.
По составу бывают минеральные, органические и органоминеральные коллоиды.
Минеральные коллоиды представлены преимущественно глинистыми, а также некоторыми первичными минералами (например, кварц), измельченными до коллоидного состояния. Кроме того, минеральные коллоиды образуют гидрооксиды кремния SiO2 • пН2О; железа Fe(OH)3 • пН2О, алюминия А1(ОН)3 • п Н2О, марганца Мп2О3 • пН2О. На долю минералов коллоидов приходится около 80–90 % от массы всех коллоидов почвы.
Органические коллоиды образуются при гумификации органического вещества. Представлены в почве гумусовыми кислотами и их солями: гуматами, фульватами, алюмо-железогумусовыми соединениями.
При взаимодействии гумуса с высокодисперсными минералы частичками почвы образуются комплексные соединения сложного состава – органо-минеральные коллоиды.
Количество коллоидов в почве может сильно колебаться в зависимости от содержания в ней гумусовых веществ и частичек физической глины, с их увеличением возрастает количество коллоидов.
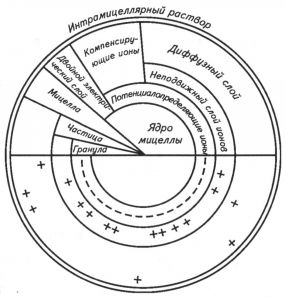
Коллоидная система почвы состоит из дисперсной фазы (масса коллоидных частичек) и дисперсионной среды (почвенного раствора), они взаимодействуют, в результате этого вокруг коллоидной частички создается двойной ионогенный слой. Коллоидную частичку с двойным ионогенным слоем называют мицеллой. Общая схема ее строения дана на рисунке 1.

Рис. 1. Схема строения коллоидной мицеллы (по Н.И. Горбунову)
Внутри мицеллы находится ядро – масса недисоциированных молекул коллоидообразующего вещества. К ядру примыкает потенциал-определяющий (внутренний) слой ионов определенного электрического заряда. Он неподвижный, прочно связан с ядром. Ядро вместе с потен-циалопределяюшим слоем образует гранулу. Вокруг нее формируется слой компенсирующих ионов, имеющих противоположный заряд по сравнению с ионами внутреннего слоя. Часть его ионов образует неподвижный слой компенсирующих ионов, другая часть отходит от внутреннего слоя на значительное расстояние, теряет с ним прочную связь и образует диффузный слой. Ионы диффузионного слоя способны к различным обменным реакциям с почвенным раствором. При потере диффузным слоем части ионов между зарядами слоя потенциалопределяющих ионов и слоем компенсирующих ионов возникает определенная разность потенциалов, называемая дзета-потенциалом. Величина его колеблется от 0 до 40–60 мВ.
Основная масса мицеллы принадлежит грануле, поэтому заряд последней рассматривается как заряд всего коллоида. Коллоиды, имеющие во внутреннем слое отрицательно заряженные ионы и диссоциирующие в раствор Н-ионы, называются ацидоидами. Они способны к поглощению и обмену катионов. Положительным зарядом характеризуются базоиды – их потенциалопределяющий слой состоит из катионов, а диффузный – из ОН-ионов (анионов). Базоиды способны поглощать и обменивать анионы.
Некоторые коллоиды (гидроксиды железа, алюминия) при изменении реакции среды меняют и знак заряда: в кислой среде они заряжены положительно, а в щелочной – отрицательно. Такие коллоиды называют амфолитоидами. Большинство почвенных коллоидов являются ацидоидами – это коллоиды гумусовых веществ, глинистых минералов и кремнекислоты. К базидам можно отнести гидрооксиды алюминия, железа.
Взаимодействию и соединению коллоидных частиц препятствуют водные пленки, образующиеся на их поверхности. По количеству воды, которую удерживают коллоиды, они подразделяются на гидрофильные и гидрофобные. Первые сильно гидротируются, набухают в воде. К ним относятся коллоиды гумуса, глинистых минералов. Гидрофобные коллоиды удерживают небольшое количество воды – это минералы каолинитовой группы и др.
Почвенные коллоиды могут находиться в двух состояниях: золя или коллоидного раствора, и геля или студенистого, комковатого или аморфного осадка. Под влиянием тех или других факторов коллоиды из состояния раствора могут переходить в осадок и наоборот. Процесс соединения отдельных коллоидных частичек и выпадения осадка называется коагуляцией. Осадок, образующийся при коагуляции, называется гелем. Переход геля в золь – пептизация.
При снижении дзета-потенциала и гидротированности частичек состояние золя делается неустойчивым, и как только коллоид теряет заряд или он уменьшается настолько, что силы притяжения превышают силы отталкивания, коллоидные частички начинают сцепляться, образовывать комочки и выпадать в осадок. Коагуляция коллоидов происходит главным образом при взаимодействии с электролитами (растворами солей, кислот, щелочей). При этом ацидоиды коагулируются под влиянием катионов электролита, базоиды – под влиянием анионов. Коагулирующая способность двух-трехвалентных катионов более сильная, чем одновалентных катионов, за исключением Н-.
Коагуляцию почвенных коллоидов могут вызывать и такие явления, как старение коллоидов, обезвоживание и замораживание почв. Скоагулированные коллоиды могут переходить от состояния геля в золь. Обычно это происходит с гидрофильными коллоидами, насыщенными одновалентными катионами – Н-, NH4+,Na+, и др. В этих условиях не может образоваться водопрочная структура почвы. Коллоиды передаются вниз по профилю, что может ухудшить физико-химические свойства почвы.
Переход геля в золь затруднен или вообще невозможен для гидрофобных коллоидов, насыщенных двух- и трехвалентными катионами – Са2+, Mg2+, A13+, Fe3+. В таких условиях пептизации коллоидов почти не наблюдается, образуются водопрочные структурные агрегаты, в почве закрепляются гумусовые вещества.
Почвенные коллоиды являются носителями сорбционных свойств почвы. Они способны поглощать и обменивать ионы диффузного слоя мицеллы на ионы почвенного раствора.
Адсорбционные свойства коллоидов обусловлены большой удельной поверхностью, благодаря которой коллоидные частички приобретают силы электростатического притяжения – вокруг их могут концентрироваться молекулы воды, газов и др.
Источник
Накопление в почве элементов питания растений связано с поглотительной способностью почв. Академик К. К. Гедройц предложил под поглотительной способностью почвы понимать способность ее поглощать жидкости, газы, солевые растворы и удерживать твердые частички, а также живыемикроорганизмы. Поглотительные процессы в почве обусловлены преимущественно тонкодисперсной частью почвы и особенно коллоидами. Содержание коллоидов в почве редко превышает 30 % почвенной массы, но влияние их на свойства почвы и уровень плодородия исключительно велико.
Почва состоит из частиц различного размера. Почвенными коллоидами называют частицы диаметром от 0,2 до 0,001 мкм. Они образуются при диспергировании (раздроблении) крупных частиц или при конденсации вследствие физического или химического соединения молекул.
По происхождению почвенные коллоиды бывают минеральные, органические и органо-минеральные.
Минеральные коллоиды образуются при выветривании горных пород. Это глинистые минералы, коллоидные формы кремнезема и полуторные оксиды.
К органическим коллоидам относятся гумусовые вещества почвы, сформированные в процессе гумификации растительных и животных остатков.
Органо-минеральные коллоиды образуются при взаимодействии минеральных и органических коллоидов.
В различных почвах содержание коллоидов составляет от 1…2 до 30…40 % массы почвы. Наибольшее количество коллоидов отмечено в глинистых и суглинистых почвах с высоким содержанием гумуса, наименьшее — в песчаных и супесчаных почвах, бедных гумусом.
Строение коллоидной частицы (мицеллы). На рисунке показано строение коллоидной мицеллы. Ядро мицеллы — это внутренняя ее часть, состоящая из недиссоциированных молекул. Оно может быть аморфным или кристаллическим. На поверхности ядра находится двойной электрический слой ионов, соприкасающийся с дисперсной средой (почвенным раствором): внутренний — потенциал определяющий слой неподвижных ионов, прочно связанных с ядром, и внешний — компенсирующий слой ионов, имеющий противоположный заряд.

Рис. Схема строения коллоидной мицеллы (по Н. И. Горбунову)
Заряд коллоидной мицеллы определяют ионы, непосредственно связанные с поверхностью ядра. Этот заряд возникает в результате диссоциации молекул на поверхности ядра. Например, молекулы гидроксида алюминия Аl(ОН)з, составляющие ядро мицеллы, в кислой среде диссоциируют на ионы Al(OH)2+ и ОН-, а в щелочной — на АlO(OН)2- и Н+. Сложные ионы удерживаются на поверхности ядра и определяют знак заряда коллоидной мицеллы. Поэтому коллоидная частица гидроксида алюминия в кислой среде имеет положительный заряд, а в щелочной — отрицательный.
Коллоиды, имеющие кристаллическое строение, приобретают заряд иным путем. Известно, что ионы кристаллических частиц, находящиеся на поверхности, не насыщены связями и поэтому могут притягивать ионы из растворов. При этом притягиваются ионы противоположного заряда, вследствие чего образуется диффузный слой коллоидной мицеллы.
Ядро мицеллы и потенциалопределяющий слой ионов образуют гранулу. За потенциалопределяющим слоем гранулы расположены компенсирующие ионы. Прочносвязанные ионы этого слоя образуют неподвижный слой компенсирующих ионов. Затем следует внешний, или диффузный, слой ионов, способных обмениваться на ионы почвенного раствора. Таким образом, коллоидная мицелла состоит из ядра и двух противоположно заряженных слоев ионов.
Почвенные коллоиды по знаку заряда потенциал определяющего слоя подразделяются на отрицательные (ацидоиды) и положительные (базоиды). К отрицательным коллоидам относятся кремниевая кислота, глинистые минералы и гумусовые кислоты, к положительным — гидроксиды железа и алюминия.
Потенциал почвенных коллоидов зависит от их природы и реакции среды. Поскольку почвенные частицы имеют заряд, они способны притягивать дипольные молекулы воды из окружающего раствора, образуя гидратные пленки. Толщина этой пленки зависит от величины заряда. В связи с этим различают гидрофильные коллоиды (кремниевая кислота, гумусовые кислоты), удерживающие многослойные пленки воды, и гидрофобные, то есть слабогидратированные коллоиды (гидроксид железа, каолинит). Гидрофильные коллоиды имеют сродство с водой и способны сильно набухать, что предотвращает их слипание. Гидрофобные коллоиды набухают слабо, поэтому у них выражена способность свертываться и выпадать в осадок.
Коагуляция и пептизация коллоидов. Коллоиды могут находиться в двух состояниях: золя (коллоидного раствора) и геля (коллоидного осадка).
Коагуляцией называется процесс перехода коллоидов из состояния золя в состояние геля. Слипание коллоидов в агрегаты происходит под влиянием электролитов. Коагуляция ацидоидов вызвана катионами электролита, базоидов — анионами. Свертывание (слипание) коллоидов может происходить при взаимодействии противоположно заряженных коллоидных систем. При высушивании или замораживании почвы наблюдаются дегидратация (обезвоживание) гидрофильных коллоидов и повышение концентрации электролита почвенного раствора, что также вызывает коагуляцию коллоидов.
При коагуляции коллоидов происходит склеивание элементарных почвенных частиц в комочки, в результате чего улучшаются физические свойства почвы. Коагуляцию вызывают двухвалентные катионы, особенно Са2+. Кальций называют «стражем почвенного плодородия», так как он способствует образованию структуры и уменьшает кислотность почв.
Пептизация — это обратный процесс коагуляции, при котором коллоиды переходят из геля в золь. Пептизация происходит при воздействии растворов щелочных солей. Например, под влиянием одновалентного катиона натрия наблюдается усиленная гидратация коллоидов и переход их в состояние золя. При пептизации почвенных коллоидов разрушается ценная структура и ухудшаются свойства почвы. Так, столбчатый горизонт солонцовых почв, насыщенный гидратированными катионами натрия, во влажном состоянии набухает, а при высыхании растрескивается на крупные отдельности.
Роль коллоидов в почве исключительно велика: от содержания коллоидной фракции зависят связность, водопроницаемость, буферность и другие свойства почвы.
Источник:https://www.zoodrug.ru/topic3543.html
39. Почвенный поглощающий комплекс. Насыщенные и ненасыщенные основаниями почвы. Кислотность и буферность почв.
Материальным носителем обменной способности почв является почвенный поглощающий комплекс (ППК) — совокупность минеральных, органических и органо-минеральных соединений высокой степени дисперсности, нерастворимых в воде и способных к обменным реакциям. Поглотительной способностью обладала коллоидные частицы (0,001—0,200 мкм) и в меньшей степени предколлоидная фракция (0,2—1,0 мкм). Основным механизмом обменной поглотительной способности почв является процесс сорбции. Природа и состав ППК связаны с типом почвообразования. Общее количество поглощенных (обменных) катионов называется емкостью поглощения, или емкостью катионного обмена (ЕКО). Она зависит от содержания в почве илистой фракции, природы ППК и реакции среды. Емкость катионного обмена больше в почвах тяжелого гранулометрического состава, чем в легких. Органические коллоиды обладают более высокой ЕКО, чем минеральные. Минеральные коллоиды в почвах, содержащих монтмориллонит, характеризуются большим ЕКО, чем в почвах с преобладанием каолинита и гидрослюд. В обменной форме находятся многие макро — и микроэлементы минерального питания растений. Наиболее важны для диагностики процессов почвообразования и плодородия почв обменные катионы почвенного поглощающего комплекса: Са2+, Mg2+, Na+, Н+, Аl3+.
Кислотность почвы,одно из важнейших свойств многих почв, обусловленное наличием водородных ионов в почвенном растворе, а также обменных ионов водорода и алюминия в почвенном поглощающем комплексе. Повышенная К. п. отрицательно влияет на развитие растений и многих полезных микроорганизмов. Различают 2 формы К. п.: актуальную, или активную, — кислотность почвенного раствора, почвенной суспензии или водной вытяжки из почв, и потенциальную, или пассивную, “скрытую”, — кислотность твёрдой фазы почвы. Актуальная К. п. обусловлена наличием ионов водорода. Выражается условной величиной pH (отрицательный логарифм концентрации водородных ионов); при pH 7 реакция почвенного раствора нейтральная, ниже 7 — кислая; чем ниже числовое значение рН, тем выше К. п. Потенциальную К. п. делят на обменную и гидролитическую. Обменная К. п. вызывает значительное подкисление почвенного раствора при взаимодействии почвы с нейтральной солью, что наблюдается при внесении физиологически кислых удобрений (хлористый калий, сернокислый аммоний и др.). По представлениям русского учёного К. К. Гедройца и некоторых других исследователей, обменная К. п. обусловлена присутствием в твердой фазе почвы ионов водорода, не вытесняемых нейтральными солями из поглощаемого комплекса, но способных к замещению (обмену) на другие катионы при обработке почвы растворами щелочей или гидролитически щелочных солей (например, раствором ацетата натрия, который и применяется при определении гидролитической кислотности). Степень К. п. необходимо учитывать при выборе минеральных удобрений, подготовке их перед внесением в почву. Основной способ борьбы с повышенной К. п. — известкование почв
Буферность почвы
свойство почвы препятствовать изменению её реакции (pH) под действием кислот и щелочей. Чем больше в почвенном растворе солей сильных оснований и слабых кислот, тем более буферна почва по отношению к кислым удобрениям; соли слабых оснований и сильных кислот буферны к щелочным удобрениям. Так как раствор находится в постоянном взаимодействии с твёрдой фазой почвы, то последняя также оказывает существенное влияние на буферность. Чем больше коллоидных частиц и гумуса в почве (например, чернозёмы) и чем больше они содержат поглощённых оснований, тем буфернее почва по отношению к кислым удобрениям; поглощённый коллоидами водород (подзолистые почвы, краснозёмы) способствует увеличению Б. п. к щелочным удобрениям. Наиболее буферны почвы тяжёлого (глинистого) механического состава. Атмосферные осадки, грунтовая и оросительная вода могут изменить реакцию почвы, если последняя не обладает буферностью, и наоборот. Растения реагируют на изменение реакции почвы, поэтому Б. п. играет большую роль в их росте и развитии. Б. п. можно повысить внесением органических удобрений
40. систематика почв, ее цели и задачи. Таксономия почв. Номенклатура почв и диагностика почв.
Источник
ЛЕКЦИЯ 8 КОЛЛОИДНАЯ ЧАСТЬ ПОЧВЫ И ЕЕ ПОГЛОТИТЕЛЬНАЯ СПОСОБНОСТЬ
Вопросы
1. Коллоиды и их роль в почвообразовании
2. Виды поглотительной способности почвы
3. Состав обменных катионов различных типов почв
4. Понятие о кислотности и щелочности почв
Почва – это живое тело, живой организм, поскольку представляет собой не только среду, в которой происходят различные физические, химические и биологические явления, но она испытывает постоянное изменение, имеет такой же регулируемый обмен веществ, как и организованное тело, поэтому эта формация является переходным мостиком между областью инертных пород и миром организованных индивидуумов – жизнью. Почва является полидисперсной системой, субстратом, состоящим из 4х фаз: твердой, жидкой, газообразной и живой. Соотношения этих фаз могут колебаться даже в пределах одной разновидности почвы в зависимости от климатических условий и уровня хозяйствования.
Твердая фаза почвы состоит из частиц различного размера, начиная от крупинок песка до коллоидальных частиц. Отдельные фракции почвы отличаются между собой не только по размеру частиц, но и по минералогическому составу и целому ряду химических и физических свойств.
Пример. Грубый песок в основном состоит из кварца (с примесью обломков разных пород), это связанно с большой стойкостью кварца против выветривания и значительной твердостью, которая предохраняет кварц от механического измельчения.
В более тонких фракциях, кроме кварца, присутствуют и другие первичные минералы – полевые шпаты, слюды, отличающиеся малой твердостью.
Фракция пыли содержит уже некоторое количество вторичных минералов, а в иле – вторичные минералы преобладают.
Соответственно минералогическому составу изменяется и химический состав почвенных фракций. Крупные фракции в основном состоят из SiО2 , мелкие фракции – богаты рядом питательных для растений веществ (Al2O3, MgO, K2O, P2O5).
Почвенный гумус сосредоточен в наиболее высокодисперсной части почв, т.е. именно высокодисперсная часть почв играет наибольшую роль в питании растений. С высокодисперсными частицами нацело связана поглотительная способность почвы.
Кроме того, эти же наиболее мелкие частицы являются клеящим материалом в почве и принимают участие в создании почвенной структуры, определяющей ряд физических свойств почвы, от которых зависит и воздушный и водный и питательный режим почв, а также жизнедеятельность микроорганизмов, которые играют важнейшую роль в обеспечении растений минеральными и органическими компонентами обмена веществ.
Высокодисперсные частицы являются настоящими катализаторами почвы. Они играют важную роль в разрушении пестицидов, в динамике передвижения тяжелых металлов и других загрязнителей в почве.
Таким образом, высокодисперсные частицы почвы, точнее ее коллоиды, являются наиболее активной частью. Что же такое коллоиды? Коллоиды– это тонкодисперсные частицы почвы размером менее 0,0002мм. Образуются эти частицы путем диспергации (дробления) более крупных частиц или конденсации многих молекул в агрегаты молекул. Их количество в почве различно – от 1-2 до 30-40% к массе почвы.
По составу почвенные коллоиды подразделяют на минеральные, органические и органо-минеральные. Минеральные коллоиды представлены преимущественно вторичными минералами (монтмориллонит, каолинит, бейделит), гидроокисями Fe, Al, кремния и частично тонкодисперсной фракцией первичных минералов (кварц, слюда).
Органические коллоиды состоят из различных перегнойных веществ и имеют высокую степень дисперсности. Они представлены преимущественно веществами гумусовой и белковой природы.
Органо-минеральные коллоиды возникают при взаимодействии гумусовых веществ со вторичными минералами. Следовательно тяжелые и хорошо гумусированные почвы содержат больше почвенных коллоидов и обладают более высокой поглотительной способностью, чем почвы песчаные и бедные органическим веществом.
Всю совокупность коллоидов, обуславливающих поглотительную способность почвы, по предложению академика К. К. Гедройца называют почвенно – поглотительным комплексом (ППК). ППК характеризуется с химической стороны как комплекс нерастворимых в воде алюмосиликатных, органических и органо – минеральных соединений, а с физической стороны – как совокупность тех почвенных соединений, которые находятся в почве в мелкораздробленном состоянии; эта высокодисперсная часть почвы по всей вероятности близко совпадает с коллоидальной частью почвы. ППК удерживает питательные вещества и пополняет их запас. С ним связаны структурообразование и характер структуры. Он способен разрушаться в результате физико-химических и биологических процессов, а также водой. ППК размещен в почве не равномерно, большая часть находится в верхних горизонтах. В связи с процессом почвообразования и проявлением экзогенных факторов с течением времени ППК, изменяется. Содержание его может увеличиваться, благодаря чему повышается плодородие почвы. Влияя на ППК, можно воздействовать на плодородие почвы (гипсование, известкование).
Высокая дисперсность и большая поверхностная энергия обуславливают определенное строение почвенных коллоидов (рисунок 1).
Рисунок 1 – Схема строения коллоидной мицеллы (по Н.А. Горбунову)
Отдельная структурная единица называется коллоидной мицеллой. Внутри нее находится ядро – агрегаты недиссоциированных молекул основного вещества (аморфного или кристаллического). Вокруг ядра расположен внутренний слой ионов, который называют слоем потенциалопределяющих ионов. Эти ионы, несущие определенный электрический заряд, прочно удерживаются ядром и не могут быть отдиссоциированы.
Ядро со слоем потенциалопределяющих ионов называется гранулой. К поверхности гранулы примыкает слой компенсирующих ионов (противоионов), который прочно удерживается электростатическими силами. Часть ионов компенсирующего слоя неподвижна, т.к. прочно связана с внутренним слоем ионов (потенциалопределяющими), часть подвижна и образует внешний, или диффузный, слой. Этот слой образует рой (облако) ионов, способных к обменным реакциям. Диффузный слой вместе с коллоидной частице образует мицеллу; она электронейтральна но поскольку масса ее принадлежит грануле, то заряд последней считается зарядом коллоида. Мицелла (дисперсная фаза) окружена внешним интермицеллярным раствором (дисперсной средой).
В пределах диффузного слоя между неподвижным слоем ионов и дисперсной средой (раствором, окружающим коллоидную частицу) возникает разность потенциалов вследствие удаления части противоионов к внешней границе диффузного слоя. Эта разность потенциалов называется дзета – потенциалом и обуславливает свободный электрический заряд коллоидной частицы. Величина дзета – потенциала колеблется от 0 до 40-60 милливольт (МВ). При дзета – потенциале, равном 0, коллоид находится в незаряженном состоянии, оно называется изоэлектрической точкой коллоида [для Al(OH)3 соответствуют PH 8,1; а для Fe(OH)3 -PH 7,1].
По электрическому заряду частиц все коллоиды подразделяют на ацидоиды, базоиды и амфолитоиды. Ацидоиды – отрицательно заряженные коллоиды, они содержат в потенциалопределяющем слое анионы, а в диффузном – катионы. Базоиды – положительно заряженные коллоиды, несущие в потенциалопределяющем слое катионы, а в диффузном – анионы. Большинство почвенных коллоидов являются ацидоидами. К ним относятся гумусовые кислоты, глинистые минералы и кремнекислота в коллоидном состоянии. Ацидоиды способны отдиссоциировать в раствор ионы Н+, Na+, Ca++, Mg++ и др. Базоиды в почве представлены преимущественно гидратами окиси Al, Fe и белковыми веществами. Они способны отдиссоциировать в раствор анионы ОН- и содержат в диффузном слое различные анионы (Al+++, Cl`, SO4“, NO3` и др.)
Некоторые коллоиды при изменении реакции среды меняют знак заряда. Такие коллоиды называются амфолитоидами. Свойствами амфолитоидов обладают многие базоиды (полуторные окислы, почвенные белки).
Наличие электрического заряда обуславливает электрокинетические свойства, главнейшими из которых являются коагуляция и пептизация коллоидной системы.
Понятие о коагуляции и пептизации коллоидной системы. В почвах коллоиды могут находиться в двух состояниях: золя (коллоидного раствора) и геля (коллоидного осадка).
Переход коллоида из состояния золя в состояние геля называется коагуляцией.При этом коллоиды теряют заряд и происходит слипание их в агрегаты (аморфный осадок). Коагуляция – положительный процесс. Она вызывается действием электролитов (щелочей, солей, растворы кислот), ионы которых несут противоположный знак заряда. Ацидоиды коагулируют под действием катионов электролита, базоиды – под влиянием анионов. Коагуляция способствует образованию почвенной структуры, уменьшению связности тяжелых почв (глинистых), сохранению от вымывания коллоидов.
Пептизация– переход коллоида из состояния геля в золь. Этот процесс противоположен коагуляции. Пептизация вызывается восстановлением и повышением дзета -потенциала коллоидной системы. Она происходит при удалении избытка электролита и действием ионов ОН- , которые увеличивают заряд ацидоидов. Пептизация почвенных коллоидов происходит также при насыщении почвы высоко гидратированными катионами (Na и др.). При пептизации разрушается структура, коллоиды распыляются и приобретают способность к передвижению по почвенному профилю
Рассмотренные свойства коллоидов имеют большое значение в почвообразовании, т.к. обуславливают их способность к аккумуляции и передвижению в пределах почвенного профиля, а следовательно к их участию в формировании аккумулятивных, элювиальных и иллювиальных горизонтов почвы.
Источник
