Какими свойствами обладают химические соединения

Большинство людей не задумывается о составе окружающих их предметов, веществ, материи. Атомы, молекулы, электроны, протоны – эти понятия кажутся не только непонятными, но и далекими от действительности. Однако такое мнение ошибочно. Практически все, что нас окружает, состоит из химических связей. Химические соединения – это достаточно сложные формы веществ. В окружающем нас мире великое множество таких связей. Однако и соединения, состоящие только из одного элемента химического, могут относиться к ним, например, кислород или хлор. Поэтому стоит подробнее разобрать вопрос: “Химические соединения – это что?”

Сложный “химический” мир
Мало кто задумывается о том, что окружающий нас мир состоит из сложных структур, макромолекул и крошечных частиц. Удивительно, насколько разнородны даже размеры атомов у разных элементов. Различия в величинах атомных масс тоже впечатляют – бериллий со своими 9 а. е. м. – “легковес” по сравнению с “тяжеловесом” астатом: его атомный вес составляет 210 а. е. м. (а. е. м. – атомные единицы массы – единица измерения массы атомов, молекул, ядер, которая равна 1/12 массы атома углерода, находящегося в основном состоянии).
Многообразие элементов обуславливает и наличие множества химических соединений (это, простыми словами, комбинация соединенных между собой атомов различных и, в некоторых случаях, одинаковых частей). Большинство предметов, веществ представляют собой именно такого рода соединения. Необходимый для жизни кислород, поваренная соль, ацетон… Можно еще очень долго перечислять примеры и всем известные, и понятные только узким специалистам. Что же такое эти химические соединения?

Определение, отличие от смесей
Химические соединения – это сложные вещества, которые состоят из соединенных между собой атомов разных химических элементов, однако существуют исключения: к химическим соединениям относятся и простые вещества (то есть состоят из атомов одного элемента), если атомы этих веществ соединены ковалентной связью (она образована общими для обоих атомов электронами). К таким веществам относятся азот, кислород, большинство галогенов (в таблице Менделеева элементы седьмой группы главной подгруппы; фтор, хлор, бром, йод, предположительно и астат).
Зачастую путают между собой понятия “химическое соединение” и “смесь простых веществ”. Смесь веществ – это, как можно сделать вывод из названия, не самостоятельное вещество, а система двух и более компонентов. Сам состав этих двух единиц химических веществ является основным различием между ними. Как уже говорилось, соединение химических элементов и смесь простых (или сложных) веществ – это не одно и то же. Свойства, способы получения, методы разделения на компоненты также являются отличительными критериями смесей и соединений. Важно отметить, что ни получить, ни разделить химические соединения нельзя без проведения химических реакций, а смеси – можно.

Соединения веществ или элементов?
Очень многие люди также путают между собой словосочетания “соединение химических веществ” и “соединение элементов”. По непонятным причинам, но, скорее всего, в силу своей некомпетентности, большинство из них не видит разницы между первым и вторым научными понятиями. Стоит узнать и понимать, что не существует такой терминологии, как “соединение химических веществ”. Не стоит повторять за другими ошибки этимологии тех или иных не только выражений, но и слов.

Как определить свойства соединений
Зачастую свойства химических соединений разительно отличаются от свойств элементов, из которых они состоят. Например, молекула этилового спирта состоит из двух атомов углерода, шести атомов водорода и одного атома кислорода, однако его свойства разительно отличаются от свойств всех элементов своего состава. В связи с тем, что существуют разные классы соединений, то и свойства у каждого из них свои. Большинство реакций, безусловно, являются характерными для многих соединений, однако механизмы их проявления разные.

На какие классы делятся химические соединения
В зависимости от своей природы, существуют такие классы химических соединений, как органические и неорганические. Стоит сказать, что органическими называют вещества (соединения), в составе которых присутствует углерод (исключения составляют некоторые соединения, содержащие углерод, но относящиеся к неорганическим, ниже они приводятся). Основными группами органических соединений являются углеводороды, спирты, альдегиды, кетоны, эфиры, карбоновые кислоты, амиды и амины. Неорганические вещества (соединения) в своем составе не содержат атомов углерода, однако среди них можно выделить карбиды, цианиды, карбонаты и оксиды углерода, так как они, наравне с органическими соединениями, в своем составе содержат его атомы. И те, и другие соединения имеют свои особенности, свои свойства, причем разные группы соединений одного класса могут иметь разные характеристики.
Неорганические соединения: основные свойства
Все неорганические соединения можно разбить на несколько групп. У каждого из данных видов соединений есть общие свойства, зачастую не совпадающие с другими группами этого же класса. Итак, ответ на вопросы, какие химические соединения относятся к неорганическими, какие группы образуют и какими свойствами обладают, можно представить следующим образом:
- Первая группа – простые неорганические соединения неметаллической природы. Данную категорию соединений объединяют такие свойства, как возможность находиться в газообразном состоянии. Твердые соединения неметаллического характера обладают немолекулярным строением, в связи с чем способны к образованию кристаллов.
- Вторая группа – сложные неорганические соединения. Их можно разделить на четыре подгруппы.

Сложные неорганические соединения, их свойства
Как было сказано ранее, вторую группу неорганических соединений можно разделить на четыре подгруппы:
- Оксиды. Для этой подгруппы неорганических соединений характерны реакции взаимодействия с водой, кислотами и кислотными оксидами (у них есть соответствующая кислородсодержащая кислота).
- Кислоты. Эти соединения взаимодействуют с водой, щелочами и основными оксидами (у них есть соответствующее основание).
- Амфотерные соединения – соединения, которые могут вести себя и как кислоты, и как основания (обладают и теми, и теми свойствами). Такие соединения реагируют и с кислотными оксидами, и с основаниями.
- Гидроксиды. Эти вещества неограниченно растворяются в воде, изменяют окраску при воздействии на них щелочами.
Соединения органической природы
Большинство предметов, с которыми человек ежедневно сталкивается, изготовлены из органических соединений. Органические химические соединения представляют собой обширный класс связей, составы и свойства групп, при взаимодействии которых они отличаются завидной разнообразностью. Стоит подробнее рассмотреть группы этих соединений.

Группы органических соединений и их некоторые свойства
- Углеводороды. Они представляют собой соединения только атомов водорода и углерода. Можно выделить предельные и непредельные, линейные (ациклические) и карбоциклические, ароматические и не ароматические; алканы, алкены, алкины, диены, нафтены. Для всех перечисленных углеводородов является общим свойством их не смешиваемость с водой. Для предельных типичны реакции замещения, а для непредельных – присоединения.
- Спирты – соединения, содержащие в своем составе гидроксильную (-ОН) группу (конечно, органические соединения). Они обладают свойствами слабых кислот, для них характерны реакции нуклеофильного замещения и реакции окисления, а также спирты сами могут выступать в качестве нуклеофила.
- Простые и сложные эфиры. Простые эфиры малорастворимы в воде, обладают слабоосновными свойствами. Сложные эфиры выступают в качестве носителей электрофильных реагентов, вступают в реакции замещения.
- Альдегиды (содержат альдегидную -СНО группу). Они вступают в такие реакции, как присоединение, окисление, восстановление, сопряженного присоединения.
- Кетоны. Для них характерны гидрирование, конденсация, нуклеофильное замещение.
- Карбоновые кислоты. Они проявляют, конечно же, кислотные свойства. Восстановление, галогенирование, реакции нуклеофильного замещения у ацильного атома углерода, получение амидов и нитрилов, декарбоксилирование – основные характерные реакции.
- Амиды. Гидролизация, разложение, кислотность и основность – основные свойственные реакции для амидов.
- Амины. Являются основаниями; взаимодействуют с водой, с кислотами, с ангидридами, галогенами и галогеналканами.
Источник
Содержание:
Химическая связь, ее типы, свойства, наряду с химическими реакциями является одним из краеугольных камней интересной науки под названием химия. В этой статье мы разберем все аспекты химических связей, их значение в науке, приведем примеры и многое другое.
Что такое химическая связь
Под химической связью в химии понимается взаимное сцепление атомов в молекуле и кристаллической решетке, в результате действия силы притяжения, существующей между атомами. Именно благодаря химическим связям происходит образование различных химических соединений, в этом заключается природа химической связи.
Типы химических связей
Механизм образования химической связи сильно зависит от ее типа или вида, в целом различаются такие основные виды химической связи:
- Ковалентная химическая связь (которая в свою очередь может быть полярной и неполярной)
- Ионная связь
- Водородная связь
- Химическая связь металлов
подобных людям.
Что касается ковалентной химической связи, то на нашем сайте ей посвящена отдельная статья, и более детально вы можете почитать по ссылке. Далее же мы разберем более детально все другие основные типы химических связей.
Ионная химическая связь
Образование ионной химической связи возникает при взаимном электрическом притяжении двух ионов, имеющих разные заряды. Ионы обычно при таких химических связях простые, состоящие из одного атома вещества.
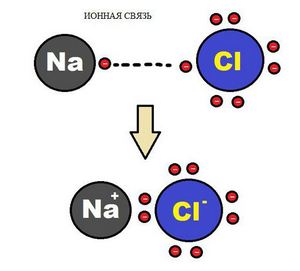
Схема ионной химической связи.
Характерной особенностью ионного типа химичечкой связи является отсутствие у нее насыщенности, и как результат, к иону или даже целой группе ионов может присоединиться самое разное количество противоположно заряженных ионов. Примером ионной химической связи может служить соединение фторида цезия CsF, в котором уровень «ионости» составляет практически 97%.
Водородная химическая связь
Еще задолго до появления современной теории химических связей в ее современном виде учеными химиками было замечено, что соединения водорода с неметаллами обладают различными удивительными свойствами. Скажем, температура кипения воды и вместе со фтороводородом гораздо выше, чем это могло бы быть, вот вам готовый пример водородной химической связи.
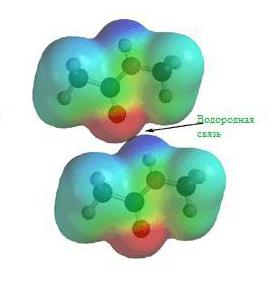
На картинке схема образования водородной химической связи.
Природа и свойства водородной химической связи обусловлены способностью атома водорода H образовывать еще одну химическую связь, отсюда собственно и название этой связи. Причиной образования такой связи являются свойства электростатических сил. Например, общее электронное облако в молекуле фтороводорода настолько смещено в сторону фтора, что пространство вокруг атома этого вещества насыщено отрицательным электрическим полем. Вокруг атома водорода, тем более лишенного своего единственного электрона, все с точностью до наоборот, его электронное поле значительно слабее и как следствие имеет положительный заряд. А положительные и отрицательные заряды, как известно, притягиваются, таким нехитрым образом и возникает водородная связь.
Химическая связь металлов
Какая химическая связь характерна для металлов? У этих веществ есть свой собственный тип химической связи – атомы всех металлов расположены не абы как, а определенным образом, порядок их расположения называется кристаллической решеткой. Электроны различных атомов образуют общее электронное облако, при этом они слабо взаимодействуют друг с другом.
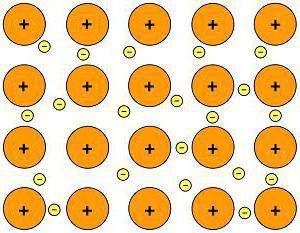
Так выглядит металлическая химическая связь.
В качестве примера металлической химической связи могут выступать любые металлы: натрий, железо, цинк и так далее.
Как определить вид химической связи
В зависимости от веществ, принимающих в ней участие, если метал и неметалл, то связь ионная, если два метала, то металлическая, если два неметалла то ковалентная.
Свойства химических связей
Чтобы провести сравнение разных химических реакций используются разные количественные характеристики, такие как:
- длина,
- энергия,
- полярность,
- порядок связей.
Разберем их подробнее.
Длина связи – равновесное расстояние между ядрами атомов, которые соединены химической связью. Обычно измеряется экспериментально.
Энергия химической связи определяет ее прочность. В данном случае под энергией подразумевается усилие, необходимое, для того, чтобы разорвать химическую связь и разъединить атомы.
Полярность химической связи показывает, насколько электронная плотность смещена к одному из атомов. Способность атомов смещать к себе электронную плотность или говоря простым языком «тянуть одеяло на себя» в химии называют электроотрицательностью.
Порядок химической связи (другими словами кратность химической связи) – это число электронных пар, вступающих в химическую связь. Порядок может быть, как целым, так и дробным, чем он выше, тем большее число электронов осуществляют химическую связь и тем труднее ее разорвать.
Химическая связь, видео
И в завершение познавательное видео об разных видах химической связи.

Автор: Павел Чайка, главный редактор журнала Познавайка
При написании статьи старался сделать ее максимально интересной, полезной и качественной. Буду благодарен за любую обратную связь и конструктивную критику в виде комментариев к статье. Также Ваше пожелание/вопрос/предложение можете написать на мою почту pavelchaika1983@gmail.com или в Фейсбук, с уважением автор.
Эта статья доступна на английском языке – Chemical Bonding: Definition, Types, Properties.
Источник
Причины образования химической связи
Известно, что электронные оболочки, содержащие восемь внешних электронов, два из которых находятся на s-орбитали, а шесть — на р-орбиталях, обладают повышенной устойчивостью. Они соответствуют инертным газам: неону, аргону, криптону, ксенону, радону (найдите их в периодической таблице). Еще более устойчив атом гелия, содержащий всего два электрона. Атомы всех других элементов стремятся приблизить свою электронную конфигурацию к электронной конфигурации ближайшего инертного газа. Это возможно сделать двумя путями — отдавая или присоединяя электроны внешнего уровня.
Атому натрия, имеющему всего один неспаренный электрон, выгоднее его отдать, тем самым атом получает заряд (становится ионом) и приобретает электронную конфигурацию инертного газа неона.
Атому хлора до конфигурации ближайшего инертного газа недостает всего одного электрона, поэтому он стремится приобрести электрон.
Каждый элемент в большей или меньшей степени обладает способностью притягивать электроны, которая численно характеризуется значением электроотрицательности. Соответственно, чем больше электроотрицательность элемента, тем сильнее он притягивает электроны и тем сильнее выражены его окислительные свойства.
Стремление атомов приобрести устойчивую электронную оболочку объясняет причину образования молекул.
Определение
Химическая связь — это взаимодействие атомов, обусловливающее устойчивость химической молекулы или кристалла как целого.
ТИПЫ химической связи
Различают 4 основных типа химической связи:

Рассмотрим взаимодействие двух атомов с одинаковыми значениями электроотрицательности, например двух атомов хлора. Каждый из них имеет по семь валентных электронов. До электронной конфигурации ближайшего инертного газа им не хватает по одному электрону.
Сближение двух атомов до определенного расстояния приводит к образованию общей электронной пары, одновременно принадлежащей обоим атомам. Эта общая пара и представляет собой химическую связь. Аналогично происходит и в случае молекулы водорода. У водорода всего один неспаренный электрон, и до конфигурации ближайшего инертного газа (гелия) ему не хватает еще одного электрона. Таким образом, два атома водорода при сближении образуют одну общую электронную пару.
Определение
Связь между атомами неметаллов, возникающая при взаимодействии электронов с образованием общих электронных пар, называется ковалентной.
В случае если взаимодействующие атомы имеют равные значения электроотрицательности, общая электронная пара в равной степени принадлежит обоим атомам, то есть находится на равном расстоянии от обоих атомов. Такая ковалентная связь называется неполярной.
Определение
Ковалентная неполярная связь — химическая связь между атомами неметаллов с равными или близкими значениями электроотрицательности. При этом общая электронная пара одинаково принадлежит обоим атомам, смещения электронной плотности не наблюдается.
Ковалентная неполярная связь имеет место в простых веществах-неметаллах: $mathrm{О}_2, mathrm{N}_2, mathrm{Cl}_2, mathrm{P}_4, mathrm{O}_3$. При взаимодействии атомов, имеющих различные значения электроотрицательности, например водорода и хлора, общая электронная пара оказывается смещенной в сторону атома с большей электроотрицательностью, то есть в сторону хлора. Атом хлора приобретает частичный отрицательный заряд, а атом водорода — частичный положительный. Это пример ковалентной полярной связи.
Определение
Связь, образованная элементами-неметаллами с разной электроотрицательностью, называется ковалентной полярной. При этом происходит смещение электронной плотности в сторону более электроотрицательного элемента.
Молекула, в которой разделены центры положительного и отрицательного зарядов, называется диполем. Полярная связь имеет место между атомами с различной, но не сильно различающейся электроотрицательностью, например между различными неметаллами. Примерами соединений с полярными ковалентными связями являются соединения неметаллов друг с другом, а также различные ионы, содержащие атомы неметаллов $(mathrm{NO}_3–, mathrm{CH}_3mathrm{COO}–)$. Особенно много ковалентных полярных соединений среди органических веществ.
В случае если разница электроотрицательностей элементов будет велика, произойдет не просто смещение электронной плотности, а полная передача электрона от одного атома к другому. Рассмотрим это на примере фторида натрия NaF. Как мы видели ранее, атом натрия стремится отдать один электрон, а атом фтора готов его принять. Это легко осуществляется при их взаимодействии, которое сопровождается переходом электрона.
При этом атом натрия полностью передает свой электрон атому фтору: натрий лишается электрона и становится заряженным положительно, а хлор приобретает электрон и становится заряженным отрицательно.
Определение
Атомы и группы атомов, несущие на себе заряд, называют ионами.
В образовавшейся молекуле — хлориде натрия $Na^+F^-$ — связь осуществляется за счет электростатического притяжения разноименно заряженных ионов. Такую связь называют ионной. Она реализуется между типичными металлами и неметаллами, то есть между атомами с сильно различающимися значениями электроотрицательности.
Определение
Ионная связь образована за счет сил электростатистического притяжения между разноименно заряженными ионами — катионами и анионами.
Существует еще один тип связи — металлическая, характерная для простых веществ — металлов. Она характеризуется притяжением частично ионизованных атомов металлов и валентных электронов, образующих единое электронное облако («электронный газ»). Валентные электроны в металлах являются делокализованными и принадлежат одновременно всем атомам металла, свободно перемещаясь по всему кристаллу. Таким образом, связь является многоцентровой. В переходных металлах металлическая связь носит частично ковалентный характер, так как дополнена перекрыванием частично заполненных электронами d-орбиталей предвнешнего слоя. Металлы образуют металлические кристаллические решетки. О ней подробно рассказывается в теме «Металлическая связь и ее характеристики».
межмолекулярные взаимодействия
Примером сильного межмолекулярного взаимодействия
является водородная связь, образующаяся между атомом водорода одной молекулы и атомом с высокой электроотрицательностью ($mathrm{F}$, $mathrm{O}$, $mathrm{N}$). Примером водородной связи является взаимодействие молекул воды $mathrm{O}_2mathrm{O}…mathrm{OH}_2$, молекул аммиака и воды $mathrm{H}_3mathrm{N}…mathrm{OH}_2$, метанола и воды $mathrm{CH}_3mathrm{OH}…mathrm{OH}_2$ , а также различных частей молекул белков, полисахаридов, нуклеиновых кислот.

Другим примером межмолекулярного взаимодействия являются ван-дер-ваальсовы силы, которые возникают при поляризации молекул и образовании диполей. Они обусловливают связь между слоями атомов в слоистых кристаллах (таких как структура графита).

Характеристики химической связи
Химическая связь характеризуется длиной, энергией, направленностью и насыщаемостью (каждый атом способен образовать ограниченное число связей). Кратность связи равна числу общих электронных пар. Форма молекул определяется типом электронных облаков, участвующих в образовании связи, а также фактом наличия или отсутствия неподеленных электронных пар. Так, например, молекула $mathrm{CO}_2$ является линейной (нет неподеленных электронных пар), а $mathrm{H}_2mathrm{O}$ и $mathrm{SO}_2$ – уголковыми (есть неподеленные пары). В случае если взаимодействующие атомы имеют сильно различающиеся значения электроотрицательностей, общая электронная пара практически полностью смещается в сторону атомов с наибольшей электроотрицательностью. Ионную связь, таким образом, можно рассматривать как предельный случай полярной ковалентной связи, когда электрон практически полностью перешел от одного атома к другому. В действительности полного смещения не происходит никогда, то есть абсолютно ионных веществ нет. Например, в $mathrm{NaCl}$ реальные заряды на атомах составляют +0,92 и –0,92, а не +1 и –1.
Ионная связь реализуется в соединениях типичных металлов с неметаллами и кислотными остатками, а именно в оксидах металлов ($mathrm{CaO}$, $mathrm{Al}_2mathrm{O}_3$), щелочах ($mathrm{NaOH}$, $mathrm{Ca(OH)}_2$) и солях ($mathrm{NaCl}$, $mathrm{K}_2mathrm{S}$, $mathrm{K}_2mathrm{SO}_4$, $mathrm{NH}_4mathrm{Cl}$, $mathrm{CH}_3mathrm{NH}_3^+$, $mathrm{Cl^–}$).
механизмы образования химической связи
Обменный.
Обменный механизм образования химической связи обусловлен обобществлением неспаренных электронов атомов. Подробно он был рассмотрен выше на примере образования молекулы хлора.Донорно-акцепторный.

Донор — элемент, предоставляющий пару электронов (например, азот или бор).
Акцептор — элемент, предоставляющий свободную орбиталь для пары электронов другого атома.
Источник
