Какими свойствами обладает азотная кислота

Строение молекулы и физические свойства
Азотная кислота HNO3 – это сильная одноосновная кислота-гидроксид. При обычных условиях бесцветная, дымящая на воздухе жидкость, температура плавления −41,59 °C, кипения +82,6 °C ( при нормальном атмосферном давлении). Азотная кислота смешивается с водой во всех соотношениях. На свету частично разлагается.
Валентность азота в азотной кислоте равна IV, так как валентность V у азота отсутствует. При этом степень окисления атома азота равна +5. Так происходит потому, что атом азота образует 3 обменные связи и одну донорно-акцепторную, является донором электронной пары.
Поэтому строение молекулы азотной кислоты можно описать резонансными структурами:


Обозначим дополнительные связи между азотом и кислородом пунктиром. Этот пунктир по сути обозначает делокализованные электроны. Получается формула:

Способы получения
В лаборатории азотную кислоту можно получить разными способами:
1. Азотная кислота образуется при действии концентрированной серной кислоты на твердые нитраты металлов. При этом менее летучая серная кислота вытесняет более летучую азотную.
Например, концентрированная серная кислота вытесняет азотную из кристаллического нитрата калия:
KNO3 + H2SO4(конц) → KHSO4 + HNO3
2. В промышленности азотную кислоту получают из аммиака. Процесс осуществляется постадийно.
1 стадия. Каталитическое окисление аммиака.
4NH3 + 5O2 → 4NO + 6H2O
2 стадия. Окисление оксида азота (II) до оксида азота (IV) кислородом воздуха.
2NO + O2 → 2NO2
3 стадия. Поглощение оксида азота (IV) водой в присутствии избытка кислорода.
4NO2 + 2H2O + O2 → 4HNO3
Химические свойства
Азотная кислота – это сильная кислота. За счет азота со степенью окисления +5 азотная кислота проявляет сильные окислительные свойства.
1. Азотная кислота практически полностью диссоциирует в водном растворе.
HNO3 → H+ + NO3–
2. Азотная кислота реагирует с основными оксидами, основаниями, амфотерными оксидами и амфотерными гидроксидами.
Например, азотная кислота взаимодействует с оксидом меди (II):
CuO + 2HNO3 → Cu(NO3)2 + H2O
Еще пример: азотная кислота реагирует с гидроксидом натрия:
HNO3 + NaOH → NaNO3 + H2O
3. Азотная кислота вытесняет более слабые кислоты из их солей (карбонатов, сульфидов, сульфитов).
Например, азотная кислота взаимодействует с карбонатом натрия:
2HNO3 + Na2CO3 → 2NaNO3 + H2O + CO2
4. Азотная кислота частично разлагается при кипении или под действием света:
4HNO3 → 4NO2 + O2 + 2H2O
5. Азотная кислота активно взаимодействует с металлами. При этом никогда не выделяется водород! При взаимодействии азотной кислоты с металлами окислителем всегда выступает азот +5. Азот в степени окисления +5 может восстанавливаться до степеней окисления -3, 0, +1, +2 или +4 в зависимости от концентрации кислоты и активности металла.
металл + HNO3 → нитрат металла + вода + газ (или соль аммония)
С алюминием, хромом и железом на холоду концентрированная HNO3 не реагирует – кислота «пассивирует» металлы, т.к. на их поверхности образуется пленка оксидов, непроницаемая для концентрированной азотной кислоты. При нагревании реакция идет. При этом азот восстанавливается до степени окисления +4:
Fe + 6HNO3(конц.) → Fe(NO3)3 + 3NO2 + 3H2O
Al + 6HNO3(конц.) → Al(NO3)3 + 3NO2 + 3H2O
Золото и платина не реагируют с азотной кислотой, но растворяются в «царской водке» – смеси концентрированных азотной и соляной кислот в соотношении 1 : 3 (по объему):
HNO3 + 3HCl + Au → AuCl3 + NO + 2H2O
Концентрированная азотная кислота взаимодействует с неактивными металлами и металлами средней активности (в ряду электрохимической активности после алюминия). При этом образуется оксид азота (IV), азот восстанавливается минимально:
4HNO3(конц.) + Cu → Cu(NO3)2 + 2NO2 + 2H2O
С активными металлами (щелочными и щелочноземельными) концентрированная азотная кислота реагирует с образованием оксида азота (I):
10HNO3 + 4Ca → 4Ca(NO3)2 + 2N2O + 5H2O
Разбавленная азотная кислота взаимодействует с неактивными металлами и металлами средней активности (в ряду электрохимической активности после алюминия). При этом образуется оксид азота (II).
8HNO3 (разб.) + 3Cu → 3Cu(NO3)2 + 2NO + 4H2O
С активными металлами (щелочными и щелочноземельными), а также оловом и железом разбавленная азотная кислота реагирует с образованием молекулярного азота:
12HNO3(разб) + 10Na → 10NaNO3 + N2 + 6H2O
При взаимодействии кальция и магния с азотной кислотой любой концентрации (кроме очень разбавленной) образуется оксид азота (I):
10HNO3 + 4Ca → 4Ca(NO3)2 + 2N2O + 5H2O
Очень разбавленная азотная кислота реагирует с металлами с образованием нитрата аммония:
10HNO3 + 4Zn → 4Zn(NO3)2 + NH4NO3 + 3H2O
Таблица. Взаимодействие азотной кислоты с металлами.
| Азотная кислота | ||||
| Концентрированная | Разбавленная | |||
| с Fe, Al, Cr | с неактивными металлами и металлами средней активности (после Al) | с щелочными и щелочноземельными металлами | с неактивными металлами и металлами средней активности (после Al) | с металлами до Al в ряду активности, Sn, Fe |
| пассивация при низкой Т | образуется NO2 | образуется N2O | образуется NO | образуется N2 |
6. Азотная кислота окисляет и неметаллы (кроме кислорода, водорода, хлора, фтора и некоторых других). При взаимодействии с неметаллами HNO3 обычно восстанавливается до NO или NO2, неметаллы окисляются до соответствующих кислот, либо оксидов (если кислота неустойчива).
Например, азотная кислота окисляет серу, фосфор, углерод, йод:
6HNO3 + S → H2SO4 + 6NO2 + 2H2O
Безводная азотная кислота – сильный окислитель. Поэтому она легко взаимодействует с красным и белым фосфором. Реакция с белым фосфором протекает очень бурно. Иногда она сопровождается взрывом.
5HNO3 + P → H3PO4 + 5NO2 + H2O
5HNO3 + 3P + 2H2O → 3H3PO4 + 5NO
Видеоопыт взаимодействия фосфора с безводной азотной кислотой можно посмотреть здесь.
4HNO3 + C → CO2 + 4NO2 + 2H2O
Видеоопыт взаимодействия угля с безводной азотной кислотой можно посмотреть здесь.
10HNO3 + I2 → 2HIO3 + 10NO2 + 4H2O
7. Концентрированная азотная кислота окисляет сложные вещества (в которых есть элементы в отрицательной, либо промежуточной степени окисления): сульфиды металлов, сероводород, фосфиды, йодиды, соединения железа (II) и др. При этом азот восстанавливается до NO2, неметаллы окисляются до соответствующих кислот (или оксидов), а металлы окисляются до устойчивых степеней окисления.
Например, азотная кислота окисляет оксид серы (IV):
2HNO3 + SO2 → H2SO4 + 2NO2
Еще пример: азотная кислота окисляет иодоводород:
6HNO3 + HI → HIO3 + 6NO2 + 3H2O
Азотная кислота окисляет углерод до углекислого газа, т.к. угольная кислота неустойчива.
3С + 4HNO3 → 3СО2 + 4NO + 2H2O
Сера в степени окисления -2 окисляется без нагревания до простого вещества, при нагревании до серной кислоты.
Например, сероводород окисляется азотной кислотой без нагревания до молекулярной серы:
2HNO3 + H2S → S + 2NO2 + 2H2O
При нагревании до серной кислоты:
2HNO3 + H2S → H2SO4 + 2NO2 + 2H2O
8HNO3 + CuS → CuSO4 + 8NO2 + 4H2O
Соединения железа (II) азотная кислота окисляет до соединений железа (III):
4HNO3 + FeS → Fe(NO3)3 + NO + S + 2H2O
8. Азотная кислота окрашивает белки в оранжево-желтый цвет («ксантопротеиновая реакция«).
Ксантопротеиновую реакцию проводят для обнаружения белков, содержащих в своем составе ароматические аминокислоты. К раствору белка прибавляем концентрированную азотную кислоту. Белок свертывается. При нагревании белок желтеет. При добавлении избытка аммиака окраска переходит в оранжевую.

Видеоопыт обнаружения белков с помощью азотной кислоты можно посмотреть здесь.
Источник
Определение и формула
Азотная кислота
Неорганическая сильная одноосновная кислота.
Формула
HNO3HNO_3HNO3
Свойства азотной кислоты
Физические свойства
Представляет собой бесцветную жидкость, дымящую на воздухе. С водой смешивается в любых соотношениях. Концентрированной азотной кислотой называют растворы с концентрацией HNO3, равной 60-70%, «дымящей азотной кислотой» 95-98%-ные растворы азотной кислоты.
| Свойство | Описание |
|---|---|
| плотность | 1,51 г/см3 |
| молярная масса | 63,01 г/моль |
| температура кипения | +82,6°C |
| температура плавления | -41,59 ᵒС |
Химические свойства
В химических реакциях азотная кислота может выступать в роли сильной одноосновной кислоты, либо окислителя. Азотная кислота высокой концентрации обычно окрашена в бурый цвет за счет присутствия в ней оксида азота (IV), образующегося по уравнению:
4HNO3⟶4NO2↑+2H2O+O24HNO_3 longrightarrow 4NO_2↑+ 2H_2O + O_24HNO3⟶4NO2↑+2H2O+O2↑
Такое же превращение азотная кислота претерпевает при нагревании.
Кислотные свойства
- Диссоциация в воде
HNO3⟷H++NO3−HNO3 longleftrightarrow H^+ + NO_3^-HNO3⟷H++NO3−
- Взаимодействие с основными и амфотерными оксидами
MgO+2HNO3⟶Mg(NO3)2+H2OMgO + 2HNO_3 longrightarrow Mg(NO_3)_2 + H_2OMgO+2HNO3⟶Mg(NO3)2+H2O
ZnO+2HNO3⟶Zn(NO3)2+H2OZnO + 2HNO_3 longrightarrow Zn(NO_3)_2 + H_2OZnO+2HNO3⟶Zn(NO3)2+H2O
- Взаимодействие с основаниями и амфотерными гидроксидами
NaOH+HNO3⟶NaNO3+H2ONaOH + HNO_3 longrightarrow NaNO_3 + H_2ONaOH+HNO3⟶NaNO3+H2O
Zn(OH)2+2HNO3⟶Zn(NO3)2+2H2OZn(OH)_2 + 2HNO_3 longrightarrow Zn(NO_3)_2 + 2H_2OZn(OH)2+2HNO3⟶Zn(NO3)2+2H2O
- Взаимодействие с солями слабых кислот (карбонатами, силикатами)
BaCO3+2HNO3⟶Ba(NO3)2+CO2↑+H2OBaCO_3 + 2HNO_3 longrightarrow Ba(NO_3)_2 + CO_2↑ + H_2OBaCO3+2HNO3⟶Ba(NO3)2+CO2↑+H2O
Окислительные свойства
В азотной кислоте атом азота находится в высшей степени окисления +5, благодаря чему азотная кислота любой концентрации может выступать в роли окислителя. Азот может восстанавливаться до степеней окисления от +4 до -3. Возможные продукты восстановления азотной кислоты при взаимодействии с металлами представлены в таблице 1.
Таблица 1. Типичные продукты восстановления азотной кислоты
| Степень окисления азота | +4 | +2 | +1 | -3 | |
|---|---|---|---|---|---|
| Формула вещества | NO2 | NO | N2O | N2 | NH4NO3 |
Закономерность
Увеличение активности металла и разбавление кислоты способствуют более полному восстановлению азотной кислоты.
- Взаимодействие с металлами
Железо (Fe), алюминий (Al), хром (Cr) пассивируются холодной концентрированной азотной кислотой.
Азотная кислота не взаимодействует с золотом, металлами платиновой группы и танталом. В остальных случаях продукты (табл. 2) зависят от концентрации HNO3:
Таблица 2. Зависимость продуктов реакции взаимодействия азотной кислоты с металлами от концентрации кислоты и активности металла
| Формула кислоты | Концентрация | Активность металла | Продукты взаимодействия с кислотой |
| HNO3 | Концентрированная | Независимо от активности металла | Соль + NO2 + Н2О |
| Разбавленная | Активный металл Li-Zn | Соль + N2 + Н2О | |
| Металл средней активности Fe-Pb | Соль + N2O + Н2О | ||
| Неактивный металл (после Н2) | Соль + NO + Н2О | ||
| Очень разбавленная | Активный металл | Соль + NH4NO3 + Н2О |
- Взаимодействие с неметаллами
При взаимодействии с неметаллами азотная кислота восстанавливается до NONONO или NO2NO_2NO2:
S+6HNO3S + 6HNO_3S+6HNO3(конц.) ⟶H2SO4+6NO2↑+2H2Olongrightarrow H_2SO_4 + 6NO_2↑ + 2H_2O⟶H2SO4+6NO2↑+2H2O
S+2HNO3S + 2HNO_3S+2HNO3(разб.) ⟶H2SO4+2NO↑longrightarrow H_2SO_4 + 2NO↑⟶H2SO4+2NO↑
- Взаимодействие со сложными веществами-восстановителями
FeS+4HNO3FeS + 4HNO_3FeS+4HNO3(разб.) ⟶Fe(NO3)3+S+NO↑+2H2Olongrightarrow Fe(NO_3)_3 +S + NO↑ + 2H_2O⟶Fe(NO3)3+S+NO↑+2H2O
Взаимодействие с органическими соединениями
Взаимодействие углеводородов с азотной кислотой используется для введения в молекулу органического вещества нитрогруппы –NO2NO_2NO2. В результате нитрования углеводородов образуются нитросоединения.
- Реакция Коновалова (взаимодействие разбавленной азотной кислоты с алканами):
CH4+HNO3⟶CH3NO2+H2OCH_4 + HNO_3 longrightarrow CH_3NO_2 + H_2OCH4+HNO3⟶CH3NO2+H2O
- Нитрование аренов
C6H6+HNO3⟶C6H5NO2+H2OC_6H_6 + HNO_3 longrightarrow C_6H_5NO_2 + H_2OC6H6+HNO3⟶C6H5NO2+H2O
Источники получения
В природе не встречается.
Способом производства является каталитическое окисление синтетического аммиака на платиновом катализаторе до смеси оксидов азота с дальнейшим поглощением их водой:
4NH3+5O2⟶4NO+6H2O4NH_3 + 5O_2 longrightarrow 4NO + 6H_2O4NH3+5O2⟶4NO+6H2O
2NO+O2⟶2NO22NO + O_2 longrightarrow 2NO_22NO+O2⟶2NO2
4NO2+O2+2H2O⟶4HNO34NO_2 + O_2 + 2H_2O longrightarrow 4HNO_34NO2+O2+2H2O⟶4HNO3
Применение
- Производство минеральных удобрений (нитратов);
- органический синтез (получение нитроалканов, анилиза, нитроцеллюлоз, тринитротолуола);
- производство лекарственных средств (нитроглицерин);
- военная промышленность (производство взрывчатых веществ, в качестве окислителя ракетного топлива, синтез отравляющих веществ);
- травление печатных форм в станковой графике;
- ювелирное дело (определение золота в сплаве).
Тест по теме «Азотная кислота»
Источник
Азотная кислота является одной из самых сильных минеральных кислот, в концентрированном виде выделяет пары
желтого цвета с резким запахом. За исключением золота и платины растворяет все металлы.
Применяют азотную кислоту для получения красителей, удобрений, органических нитропродуктов, серной и фосфорной
кислот. В результате ожога азотной кислотой образуется сухой струп желто-зеленого цвета.

Получение
В промышленности азотную кислоту получают в результате окисления аммиака на платино-родиевых катализаторах.
NH3 + O2 → (кат. Pt) NO + H2O
NO + O2 → NO2
NO2 + H2O + O2 → HNO3
Чистая азотная кислота впервые была получена действием на селитру концентрированной серной кислоты:
KNO3 + H2SO4(конц.) → KHSO4 + HNO3↑
Химические свойства
- Кислотные свойства
- Термическое разложение
- Реакции с неметаллами
- Реакции с металлами
Является одноосновной сильной кислотой, вступает в реакции с основными оксидами, основаниями. С солями реагирует при условии
выпадения осадка, выделения газа или образования слабого электролита.
CaO + HNO3 → Ca(NO3)2 + H2O
HNO3 + NaOH → NaNO3 + H2O
Na2CO3 + HNO3 → NaNO3 + H2O + CO2↑

При нагревании азотная кислота распадается. На свету (hv) также происходит подобная реакция, поэтому азотную кислоту следует хранить в
темном месте.
HNO3 → (hv) NO2 + H2O + O2
Азотная кислота способна окислить все неметаллы, при этом, если кислота концентрированная, азот обычно восстанавливается до NO2,
если разбавленная – до NO.
HNO3(конц.) + C → CO2 + H2O + NO2
HNO3(конц.) + S → H2SO4 + NO2 + H2O
HNO3(разб.) + S → H2SO4 + NO + H2O
HNO3(конц.) + P → H3PO4 + NO2 + H2O

В любой концентрации азотная кислота проявляет свойства окислителя, при этом азот восстанавливается до степени окисления от +5 до -3. На какой
именно степени окисления остановится азот, зависит от активности металла и концентрации азотной кислоты.
Для малоактивных металлов (стоящих в ряду напряжений после водорода) реакция с концентрированной азотной кислотой происходит с образованием
нитрата и преимущественно NO2.
Cu + HNO3(конц.) → Cu(NO3)2 + NO2 + H2O
С разбавленной азотной кислотой газообразным продуктом преимущественно является NO.
Cu + HNO3(разб.) → Cu(NO3)2 + NO + H2O
В реакциях с металлами, стоящими левее водорода в ряду напряжений, возможны самые разные газообразные (и не газообразные) продукты: бурый газ NO2,
NO, N2O, атмосферный газ N2, NH4NO3.
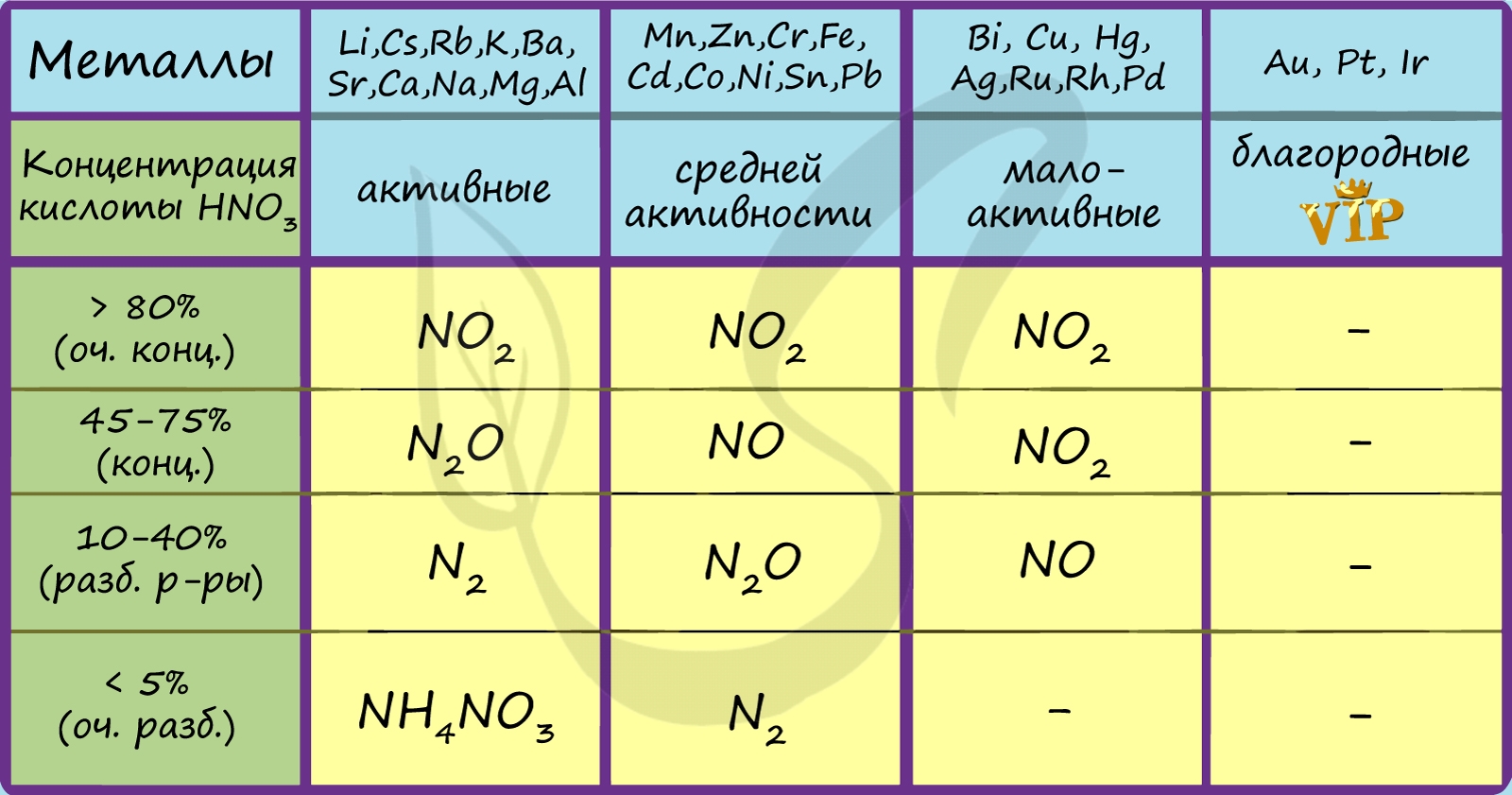
Помните о закономерности: чем более разбавлена кислота и активен металл, тем сильнее восстанавливается азот. Ниже представлены реакции цинка
с азотной кислотой в различных концентрациях.
Zn + HNO3(70% – конц.) → Zn(NO3)2 + NO2 + H2O
Zn + HNO3(35% – ср. конц.) → Zn(NO3)2 + NO + H2O
Zn + HNO3(20% – разб.) → Zn(NO3)2 + N2O + H2O

Zn + HNO3(10% – оч. разб.) → Zn(NO3)2 + N2 + H2O
Zn + HNO3(3% – оч. разб.) → Zn(NO3)2 + NH4NO3 + H2O
Посмотрите на таблицу ниже, в которой также отражены изученные нами закономерности.
Концентрированная холодная азотная кислота пассивирует хром, железо, алюминий, никель, свинец и бериллий. Это происходит
за счет оксидной пленки, которой покрыты данные металлы.
Al + HNO3(конц.) ⇸ (реакция не идет)
При нагревании или амальгамировании (покрытие ртутью) перечисленных металлов реакция с азотной кислотой идет, так
как оксидная пленка на поверхности металлов разрушается.
Al + HNO3 → (t) Al(NO3)3 + NO2 + H2O
Соли азотной кислоты – нитраты NO3-
Получение
Получают нитраты в ходе реакции азотной кислоты с металлами, их оксидами и основаниями.
Fe + HNO3(разб.) → Fe(NO3)2 + NH4NO3 + H2O
В реакциях с оксидами и основаниями газообразный продукт обычно не выделяется.
MgO + HNO3 → Mg(NO3)2 + H2O
Cr(OH)3 + HNO3 → Cr(NO3)3 + H2O

Нитрат аммония получают реакция аммиака с азотной кислотой.
NH3 + HNO3 → NH4NO3
Обратите внимание на следующую закономерность: концентрированная азотная кислота, как правило, окисляет железо и хром до +3. Разбавленная
кислота – до +2.
Fe + HNO3(разб.) → Fe(NO3)2 + NH4NO3 + H2O
Fe + HNO3(конц.) → Fe(NO3)3 + NO + H2O
Химические свойства
- Реакции с металлами, основаниями и кислотами
- Разложение нитратов
Как и для всех солей, из нитратов можно вытеснить металл другим более активным. Соли реагируют с основаниями и кислотами, если в результате
реакции выпадает осадок, выделяется газ или образуется слабый электролит (вода).
Hg(NO3)2 + Mg → Mg(NO3)2 + Hg
Pb(NO3)2 + LiOH → Pb(OH)2 + LiNO3
AgNO3 + KCl → AgCl↓ + KNO3

Ba(NO3)2 + Na2SO4 → BaSO4 + NaNO3
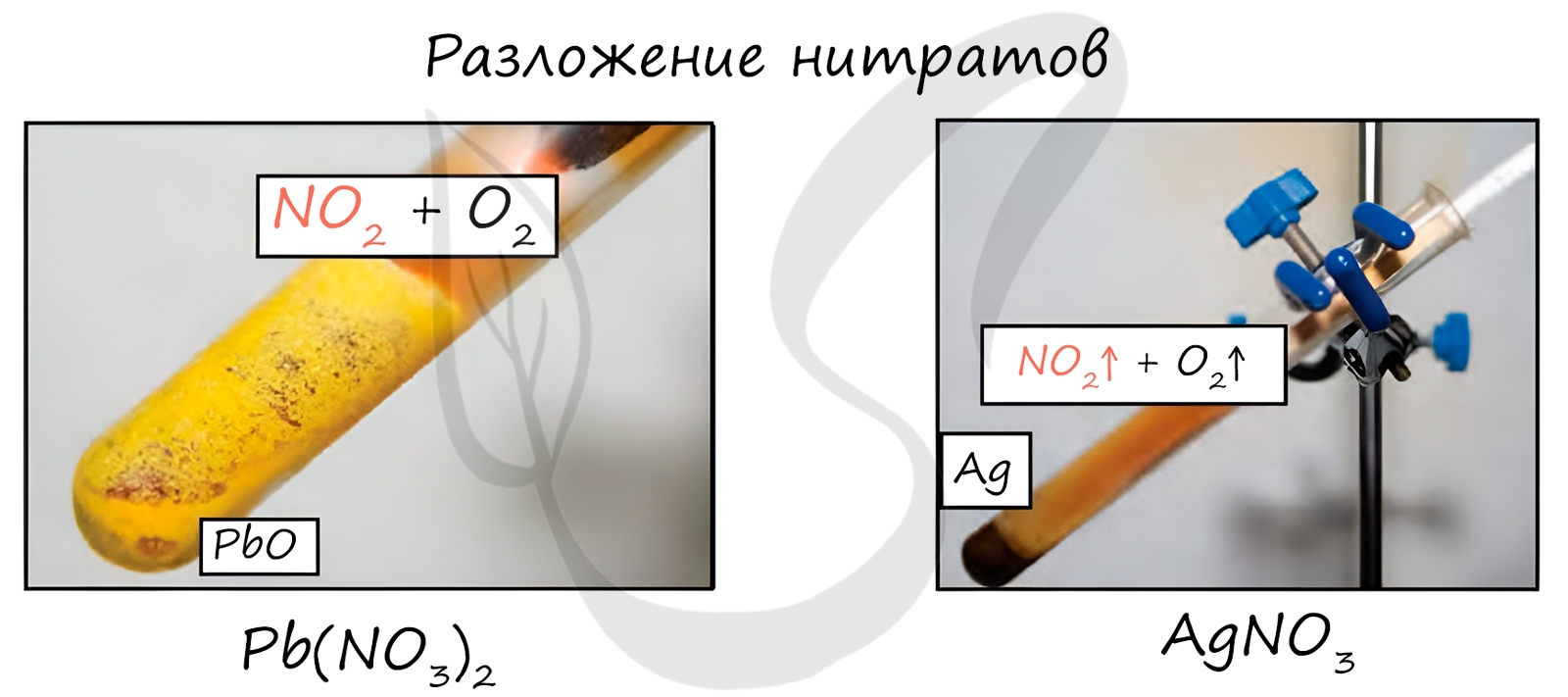
Нитраты разлагаются в зависимости от активности металла, входящего в их состав.

Pb(NO3)2 → (t) PbO + NO2 + O2
NaNO3 → (t) NaNO2 + O2
Cu(NO3)2 → (t) CuO + NO2 + O2
PtNO3 → (t) Pt + NO2 + O2
© Беллевич Юрий Сергеевич 2018-2020
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение
(в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов
без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования,
обратитесь, пожалуйста, к Беллевичу Юрию.
Источник
Строение молекулы азотной кислоты:
Связь N+-O- образуются по донорно-акцепторному механизму: атом азота отдает электрон, играя роль донора и приобретая положительный заряд, атом кислорода присоединяет электрон, выступая в роли акцептора и приобретая отрицательный заряд. Атомы азота проявляют степень окисления +5 (валентность 4).
Физические свойства азотной кислоты:
- бесцветная маслянистая жидкость с резким запахом;
- температура кипения 83°C
- плотность 1,4 г/см3 (63% HNO3);
- с водой смешивается в любых пропорциях, проявляя в водных растворах свойства сильной кислоты;
- легко разлагается на свету при длительном хранении, приобретая при этом желтый оттенок, в который ее окрашивает газ NO2, выделяющийся при разложении:
4HNO3 ↔ 2H2O+4NO2↑+O2↑
Химические свойства азотной кислоты
HNO3 является одной из самых сильных кислот – в водных растворах полностью диссоциирует на катионы водорода и нитрат-ионы:
HNO3 ↔ H++NO3-
Азотная кислота вступает в реакции:
- с оксидами металлов:
MgO+2H+NO3 = Mg2+(NO3)2+H2O - с основаниями:
Mg(OH)2+2H+NO3 = Mg2+(NO3)2+2H2O - с солями более слабых кислот:
Na2CO32-+2H+NO3 = 2NaNO3+CO2↑+H2O
Следует обратить внимание, что азотная кислота в обменных реакциях может взаимодействовать далеко не со всеми солями, а лишь только с теми, при реагировании с которыми образуются нерастворимые, слабодиссоциирующие и газообразные вещества, которые, по мере их образования, более не участвуют в реакции обмена. В обменных реакциях солями, при взаимодействии с которыми образуются растворимые в воде соли азотной кислоты, азотная кислота не участвует.
В окислительно-восстановительных реакциях азотная кислота выступает в роли сильного окислителя. Высокие окислительные свойства HNO3 объясняются тем, что в молекуле азотной кислоты атом азота в составе кислотного остатка NO3- имеет максимально возможную степень окисления +5. По этой причине окислительные свойства NO3- значительно превосходят “возможности” катионов водорода H+, из-за чего азотная кислота реагирует практически со всеми металлами за исключением золота,платины, родия, рутения, иридия и тантала, стоящими в конце ряда напряжений.

Характерной особенностью взаимодействия азотной кислоты с металлами является отсутствие выделения водорода, поскольку окислителями являются не катионы водорода, а нитрат-ионы NO3-, которые, при взаимодействии азотной кислоты с металлами восстанавливается тем полнее, чем более активным является металл и чем более разбавленной является HNO3.
По этой причине образование тех или иных продуктов реакции азотной кислоты и металла зависит от концентрации кислоты и активности металла.
Атом азота в молекуле азотной кислоты имеет степень окисления +5, и может принимать 1, 2, 3, 4, 5 или 8 электронов:
HN+5O3+1e- → N+4O2
HN+5O3+2e- → HN+3O2
HN+5O3+3e- → N+2O
HN+5O3+4e- → N2+1O
HN+5O3+5e- → N20
HN+5O3+8e- → N-3H3
HN+5O3+8e- → N-3H4NO3
Чем более концентрированной является азотная кислота, тем меньшей окислительной способностью по отношению к металлам она обладает.
С другой стороны, чем более активным является металл, тем в большей степени он восстанавливает азотную кислоту.
Примеры реакций азотной кислоты:
- концентрированная HN+5O3 с активными металлами (до алюминия в ряду напряжений) восстанавливается до N2O
10HN+5O3+4Ca0 = 4Ca+2(NO3)2+N2+1O↑+5H2O - концентрированная HN+5O3 с неактивными металлами (Ni, Cu, Ag, Hg) восстанавливается до NO2
4HN+5O3+Ni0 = Ni+2(NO3)2+2N+4O2↑+2H2O - концентрированная HN+5O3 с неметаллами (Ni, Cu, Ag, Hg) восстанавливается до NO2
4HN+5O3+P0 = HP+5O3+5N+4O2↑+2H2O - разбавленная HN+5O3 с активными металлами (до алюминия в ряду напряжений) образует аммиак или нитрат аммония
10HN+5O3+4Mg0 = 4Mg+2(NO3)2+N-3H4N+5O3+3H2O - разбавленная HN+5O3 с неактивными металлами образует оксид азота (II)
8HN+5O3+3Cu0 = 3Cu+2(NO3)2+2N+2O↑+4H2O - разбавленная HN+5O3 с неметаллами образует оксид азота (II)
2HN+5O3+S0 = H2S+6O4+2N+2O↑
Уравнения окислительно-восстановительных реакций азотной кислоты…
Концентрированная азотная кислота пассивирует алюминий, железо и хром, образуя на их поверхности очень прочную нерастворимую оксидную пленку:
2Al+6HNO3 = Al2O3+6NO2+3H2O
“Царская водка” (смесь концентрированной азотной кислоты с соляной в соотношении 1:3) окисляет золото и платину:
Au+3HNO3+3HCl = AuCl3+3NO2+3H2O
Получение и применение азотной кислоты
Промышленный способ получения азотной кислоты:
- окислением аммиака на платиновом катализаторе до оксида азота (II):
4N-3H3+5O20 = 4N+2O-2+6H2O - окислением оксида азота (II) до оксида азота (IV):
2N+2O-2+O20 = 2N+4O2-2 - растворением оксида азота (IV) в воде в присутствии кислорода (автор способа И.И.Андреев, 1916 г.):
4N+4O2+2H2O+O20 = 4HN+5O3-2
Лабораторный способ получения азотной кислоты:
- взаимодействием безводных нитратов с концентрированной серной кислотой:
NaNO3+H2SO4 = NaHSO4+HNO3
Применение азотной кислоты:
- производство азотных удобрений;
- в фармакологии для производства лекарственных препаратов;
- в производстве взрывчатых веществ.
Соли азотной кислоты
О солях азотной кислоты, наверняка, слышали многие, ведь в последнее время так много говорят о вреде нитратов в овощах и фруктах.
Нитраты калия, натрия, аммония и кальция называются селитрами (калийная селитра, натриевая селитра, аммонийная селитра, известковая селитра). Селитры нашли широкое применение в сельском хозяйстве в качестве минеральных азотных удобрений, что вполне логично, ибо азот является одним из основных элементов растений.
Нитраты хорошо растворяются в воде, при этом такие растворы не обладают окислительными свойствами, а вот расплавы нитратов являются хорошими окислителями.
Те нитраты, которые были образованы слабыми основаниями, гидролизуются, их водные растворы являются кислыми:
Cu2+(NO3)2+H2O ↔ CuOH+NO3+H+NO3
Соли азотной кислоты являются сильными окислителями.
Все нитраты, за исключением нитрата аммония разлагаются с выделением кислорода, при этом образующиеся продукты разложения зависят от электроотрицательности металла (см. таблицу выше):
- соли металлов, расположенных в ряду напряжений левее магния, при разложении образуют кроме кислорода еще и нитриты:
MeN+5O3 → MeN+3O2+O20↑
2KNO3 = 2KNO2+O2 - соли металлов, расположенных от магния до меди – образуют оксиды металла и азота (IV):
MeN+5O3 → MeO+N+4O2↑+O20↑
2Pb(NO3)2 = 2PbO+4NO2+O2 - соли металлов, расположенных правее меди – образуют свободный металл и оксид азота (IV):
MeN+5O3 → Me+N+4O2↑+O20↑
2AgNO3 = 2Ag+2NO2+O2 - нитрат аммония разлагается с образованием оксида азота (I) и воды:
NH4NO3 = N2O+2H2O
Нитраты вступают в реакции, типичные для всех солей:
- с металлами:
Hg(NO3)2+Zn = Zn(NO3)2+Hg - с щелочами:
Pb(NO3)2+2NaOH = Pb(OH)2↓+2NaNO3 - с кислотами:
Ba(NO3)2+H2SO4 = BaSO4↓+2HNO3 - с другими солями:
AgNO3+NaCl = AgCl↓+NaNO3
Получение и применение нитратов
Нитраты получают реакцией азотной кислоты:
- на металлы:
10HNO3(разб)+4Zn = 4Zn(NO3)2+NH4NO3+3H2O - на оксиды металлов:
2HNO3+CuO = Cu(NO3)2+H2O - на основания:
3HNO3+Al(OH)3 = Al(NO3)3+3H2O
Применение нитратов:
- Селитры используются в качестве минеральных удобрений:
- KNO3 – калийная или индийская селитра;
- NaNO3 – натриевая или чилийская селитра;
- NH4NO3 – аммонийная селитра;
- Ca(NO3)2 – известковая или норвежская селитра.
- Калийная селитра используется для изготовления “черного пороха”.
- Аммонийная селитра используют для изготовления взрывчатого вещества – аммонала.
Другие соединения азота:
- Аммиак
- Оксиды азота
Источник
