Какими свойствами характеризуется молекула

Одним из основополагающих понятий современной науки является понятие молекулы. Его введение европейскими учеными в 1860 г. дало толчок к развитию не только химии и физики, но и других естественных наук.
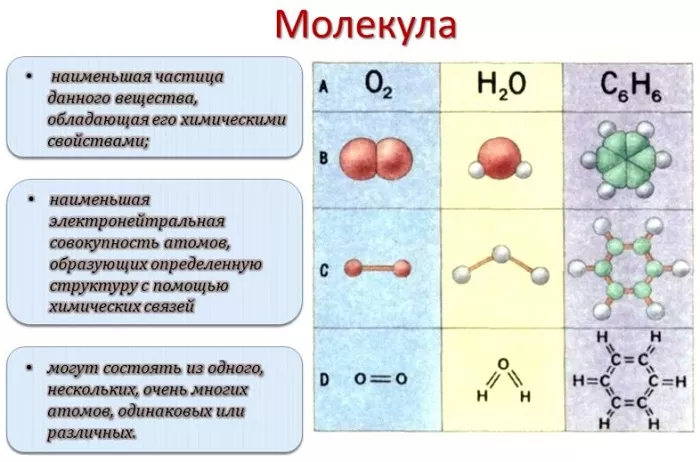
Молекулой, в наиболее общем определении, называется частица, образованная из нескольких (двух или более) атомов, объединенных между собой ковалентными связями. Она не имеет электрического заряда, все электроны в её составе имеют пару.
Молекулы, несущие заряд, называются ионами, неспаренные электроны – радикалами. Качественный и количественный состав их стабилен. Количество ядер атомов, электронов и их взаимное расположение позволяют отличать молекулы разных веществ друг от друга.
Что такое молекула в физике
В физике этим понятием оперируют при изучении свойств разных сред (газы, жидкости) и твердых тел.

Также их свойствами объясняются явления диффузии, теплопроводности и вязкость веществ.
Что такое молекула в химии
Учение о молекулах для химической науки является одним из самых главных. Именно химические исследования дали важнейшие сведения о составе и свойствах этой мельчайшей единицы вещества.
При прохождении химического превращения молекулы обмениваются атомами, распадаются. Поэтому знания о строении и состоянии этих частиц лежат в основе изучения химии веществ и их превращений.
На основании знаний о проходящей химической реакции можно предсказать строение молекул веществ, в ней участвующих. Противоположное заключение тоже будет верным: на основании сведений о строении молекулы вещества реально предсказать его поведение во время химической реакции.
Строение молекулы
Понятие о строении включает геометрическую структуру и распределение электронной плотности.
В качестве примера рассмотрим строение наименьшей частицы воды.
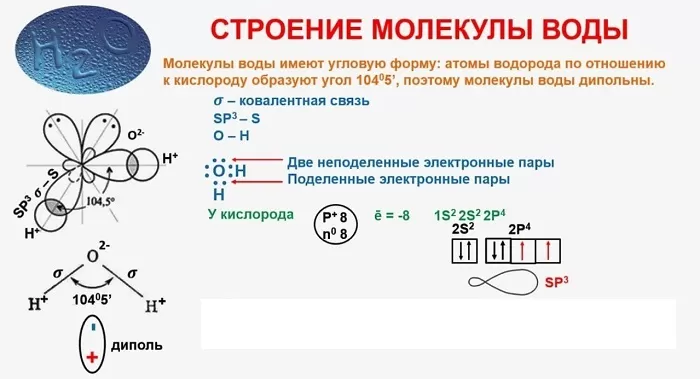
Существует несколько способов взаимодействия атомов. Основным способом являются химические связи, благодаря им поддерживается стабильное существование молекул. Прочие (неосновные) взаимодействия происходят между теми атомами, которые не связаны непосредственно.
Виды химической связи:
Металлическая – ядра атомов металлов, расположенные в узлах кристаллических решёток, объединены общим облаком электронов.
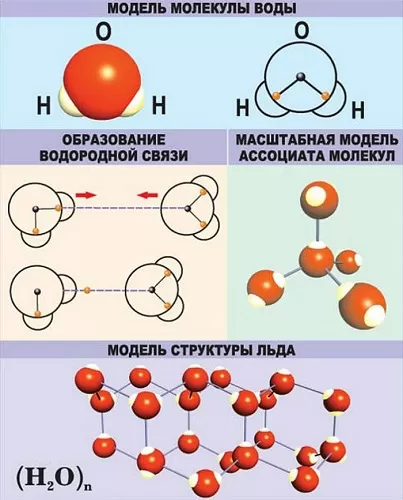
Водородная – основана на способности атома водорода образовывать дополнительную связь при смещении от него электронной плотности.
Ионная – имеет электрическую природу. Сильно поляризована. Возникает при притяжении ионов, несущих противоположный заряд.
Ковалентная – может быть полярной и неполярной. Образуется за счет пары электронов, совместно принадлежащей двум атомам. Отличается наибольшей устойчивостью и энергетической емкостью.
Связи характеризуются следующими показателями:
длина – степень удаления друг от друга ядер атомов, образовавших связь;
энергия – сила, прилагаемая для разрушения связи;
полярность – смещение электронного облака к одному из атомов;
порядок или кратность – количество пар электронов, образовавших связь.
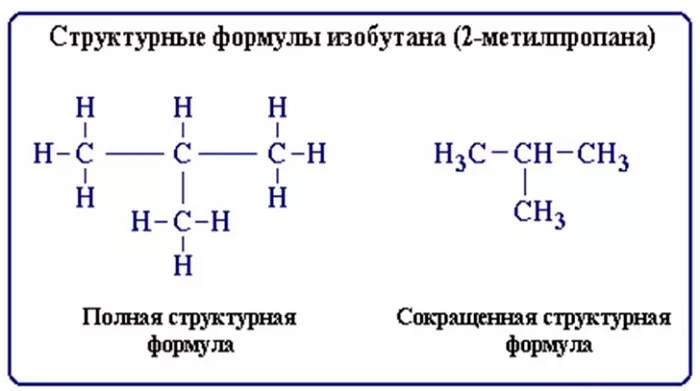
Строение молекул условно отражается структурными формулами. Основные взаимодействия атомов, при составлении таких формул, отображается черточками. В таких формулах связи образуют неразрывную цепь и иллюстрируют валентности образовавших их элементов (атомов).
Структурные формулы также отражают то, как выглядит молекула (линейная, циклическая, наличие радикалов и т. д.).
Строение частицы вещества активно изучается. Для этого используют различные экспериментальные и теоретические методы. К экспериментальным относят рентгеновский структурный анализ, спектроскопия, массспектрометрия и др. К теоретическим – расчётные методы квантовой химии.
Масса (размер) молекулы
В зависимости о количества ядер атомов, входящих в их состав, можно выделить молекулы двухатомные, трехатомные и т. д.

В том случае, если количество атомов велико, молекула носит название макромолекулы.
Путем сложения масс атомов, входящих в состав частицы, можно определить молекулярную массу. В зависимости от её величины, все вещества делят на высоко- и низкомолекулярные.
Свойства молекулы

Современная наука выделяет следующие свойства молекул:
Электрические – этими свойствами определяется то, как ведет себя вещество в электрическом поле. Атомы, входящие в состав молекулы, состоят, в свою очередь, из положительно заряженного ядра и электронов, несущих отрицательный заряд. Эти заряды внутри самой молекулы располагаются неравномерно, в связи с этим возникает так называемый дипольный момент и смещение электронной плотности в сторону одного из атомов.
Оптические – дают характеристику того, как ведет себя вещество в поле световой волны. К оптическим свойствам относят способность поляризовать свет, преломлять его и рассеивать.
Магнитные – объясняются распределением электронов в атомах.
Различают вещества:
диамагнитные – парных электронов нет;
парамагнитные – имеются непарные электроны.
Знания о свойствах и строении молекул являются основополагающими для развития теоретических и прикладных наук и играют важную роль в жизни человека.
Источник
Моле́кула (новолат. molecula, уменьшительное от лат. moles — масса[1]) — электрически нейтральная частица, образованная из двух или более связанных ковалентными связями атомов[2][3][4][5][6][7]. В физике к молекулам причисляют также одноатомные молекулы, то есть свободные (химически не связанные) атомы (например, инертных газов, ртути и т. п.). Причисление к молекулам одноатомных молекул, то есть свободных атомов, например одноатомных газов, приводит к совмещению понятий «молекула» и «атом»[8].
Обычно подразумевается, что молекулы нейтральны (не несут электрических зарядов) и не несут неспаренных электронов (все валентности насыщены); заряженные молекулы называют ионами, молекулы с мультиплетностью, отличной от единицы (то есть с неспаренными электронами и ненасыщенными валентностями) — радикалами.
Молекулы относительно высокой молекулярной массы, состоящие из повторяющихся низкомолекулярных фрагментов, называются макромолекулами[9].
С точки зрения квантовой механики[10] молекула представляет собой систему не из атомов, а из электронов и атомных ядер, взаимодействующих между собой.
Особенности строения молекул определяют физические свойства вещества, состоящего из этих молекул.
К веществам, сохраняющим молекулярную структуру в твёрдом состоянии, относятся, например, вода, оксид углерода (IV), многие органические вещества. Они характеризуются низкими температурами плавления и кипения. Большинство же твёрдых (кристаллических) неорганических веществ состоят не из молекул, а из других частиц (ионов, атомов) и существуют в виде макротел (кристалл хлорида натрия, кусок меди и т. д.).
Состав молекул сложных веществ выражается при помощи химических формул.
История
На международном съезде химиков в Карлсруэ в 1860 году были приняты определения понятий молекулы и атома. Молекула была определена как наименьшая частица химического вещества, обладающая всеми его химическими свойствами.
Классическая теория химического строения
Шаро-стержневая модель молекулы диборана B2H6. Атомы бора показаны розовым, водорода — серым.
Центральные «мостиковые» атомы одновалентного водорода образуют с соседними атомами бора трёхцентровые связи
Пространственная структура молекулы диборана.
Длины связей показаны серым, валентные углы — цветным.
Диэдральный угол между плоскостями периферических и мостиковых троек ядер H-B-H составляет 90°
В классической теории химического строения молекула рассматривается как наименьшая стабильная частица вещества, обладающая всеми его химическими свойствами.
Молекула данного вещества имеет постоянный состав, то есть одинаковое количество атомов, объединённых химическими связями, при этом химическая индивидуальность молекулы определяется именно совокупностью и конфигурацией химических связей, то есть валентными взаимодействиями между входящими в её состав атомами, обеспечивающими её стабильность и основные свойства в достаточно широком диапазоне внешних условий. Невалентные взаимодействия (например, водородные связи), которые зачастую могут существенно влиять на свойства молекул и вещества, образуемого ими, в качестве критерия индивидуальности молекулы не учитываются.
Центральным положением классической теории является положение о химической связи, при этом допускается наличие не только двухцентровых связей, объединяющих пары атомов, но и наличие многоцентровых (обычно трёхцентровых, иногда — четырёхцентровых) связей с «мостиковыми» атомами — как, например, мостиковых атомов водорода в боранах, природа химической связи в классической теории не рассматривается — учитываются лишь такие интегральные характеристики, как валентные углы, диэдральные углы (углы между плоскостями, образованными тройками ядер), длины связей и их энергии.
Таким образом, молекула в классической теории представляется динамической системой, в которой атомы рассматриваются как материальные точки и в которой атомы и связанные группы атомов могут совершать механические вращательные и колебательные движения относительно некоторой равновесной ядерной конфигурации, соответствующей минимуму энергии молекулы и рассматривается как система гармонических осцилляторов.
Молекула состоит из атомов, а если точнее, то из атомных ядер, окруженных определенным числом внутренних электронов, и внешних валентных электронов, образующих химические связи. Внутренние электроны атомов обычно не участвуют в образовании химических связей. Состав и строение молекул вещества не зависят от способа его получения.
Атомы объединяются в молекуле в большинстве случаев с помощью химических связей. Как правило, такая связь образуется одной, двумя или тремя парами электронов, находящихся в совместном владении двух атомов, образуя общее электронное облако, форма которого описывается типом гибридизации. Молекула может иметь положительно и отрицательно заряженные атомы (ионы).
Состав молекулы передается химическими формулами. Эмпирическая формула устанавливается на основе атомного соотношения элементов вещества и молекулярной массы.
Геометрическая структура молекулы определяется равновесным расположением атомных ядер. Энергия взаимодействия атомов зависит от расстояния между ядрами. На очень больших расстояниях эта энергия равна нулю. Если при сближении атомов образуется химическая связь, то атомы сильно притягиваются друг к другу (слабое притяжение наблюдается и без образования химической связи), при дальнейшем сближении начинают действовать электростатические силы отталкивания атомных ядер. Препятствием к сильному сближению атомов является также невозможность совмещения их внутренних электронных оболочек.
Каждому атому в определенном валентном состоянии в молекуле можно приписать определенный атомный, или ковалентный радиус (в случае ионной связи — ионный радиус), который характеризует размеры электронной оболочки атома (иона) образующего химическую связь в молекуле. Размер электронной оболочки молекулы, является условной величиной. Существует вероятность (хотя и очень малая) найти электроны молекулы и на большем расстоянии от её атомного ядра. Практические размеры молекулы определяются равновесным расстоянием, на которое они могут быть сближены при плотной упаковке молекул в молекулярном кристалле и в жидкости. На больших расстояниях молекулы притягиваются друг к другу, на меньших — отталкиваются. Размеры молекулы можно найти с помощью рентгеноструктурного анализа молекулярных кристаллов. Порядок величины этих размеров может быть определен из коэффициентов диффузии, теплопроводности и вязкости газов и с плотности вещества в конденсированном состоянии. Расстояние, на которое могут сблизиться валентно не связанные атомы одного и того же или разных молекул, может быть охарактеризована средними значениями так называемых ван дер ваальсовых радиусов (Ǻ).
Радиус Ван-дер-Ваальса существенно превышает ковалентный. Зная величины ван дер ваальсовых, ковалентных и ионных радиусов, можно построить наглядные модели молекул, которые бы отражали форму и размеры их электронных оболочек.
Ковалентные химические связи в молекуле расположены под определенными углами, которые зависят от состояния гибридизации атомных орбиталей. Так, для молекул насыщенных органических соединений характерно тетраэдральное (четырехгранное) расположение связей, образуемых атомом углерода, для молекул с двойной связью (С = С) — плоское расположение атомов углерода, для молекул соединений с тройной связью (С º С) — линейное расположение связей. Таким образом, многоатомная молекула имеет определенную конфигурацию в пространстве, то есть определенную геометрию расположения связей, которая не может быть изменена без их разрыва. Молекула характеризуется той или иной симметрией расположения атомов. Если молекула не имеет плоскости и центра симметрии, то она может существовать в двух конфигурациях, которые представляют собой зеркальные отражения друг друга (зеркальные антиподы, или стереоизомеры). Все важнейшие биологические функциональные вещества в живой природе существуют в форме одного определенного стереоизомера.
Молекулы, содержащие единичные связи, или сигма-связи, могут существовать в различных конформациях, возникающих при поворотах атомных групп вокруг единичных связей. Важные особенности макромолекул синтетических и биологических полимеров определяются именно их конформационными свойствами.
Квантохимическая теория химического строения
В квантохимической теории химического строения основными параметрами, определяющими индивидуальность молекулы, является её электронная и пространственная (стереохимическая) конфигурации. При этом в качестве электронной конфигурации, определяющей свойства молекулы принимается конфигурация с наинизшей энергией, то есть основное энергетическое состояние.
Представление структуры молекул
Молекулы состоят из электронов и атомных ядер, расположение последних в молекуле передаёт структурная формула (для передачи состава используется т. н. брутто-формула). Молекулы белков и некоторых искусственно синтезированных соединений могут содержать сотни тысяч атомов. Отдельно рассматриваются макромолекулы полимеров.
Молекулы являются объектом изучения теории строения молекул, квантовой химии, аппарат которых активно использует достижения квантовой физики, в том числе релятивистских её разделов. Также в настоящее время развивается такая область химии, как молекулярный дизайн. Для определения строения молекул конкретного вещества современная наука располагает колоссальным набором средств: электронная спектроскопия, колебательная спектроскопия, ядерный магнитный резонанс и электронный парамагнитный резонанс и многие другие, но единственными прямыми методами в настоящее время являются дифракционные методы, как то: рентгеноструктурный анализ и дифракция нейтронов.
Взаимодействие атомов при образовании молекулы
Природа химических связей в молекуле оставалась загадкой до создания квантовой механики — классическая физика не могла объяснить насыщаемость и направленность валентных связей. Основы теории химической связи были заложены в 1927 году Гайтлером и Лондоном на примере простейшей молекулы Н2. Позже, теория и методы расчетов были значительно усовершенствованы.
Химические связи в молекулах подавляющего большинства органических соединений является ковалентными. Среди неорганических соединений существуют ионные и донорно-акцепторные связи, которые реализуются в результате обобществления пары электронов атома. Энергия образования молекулы из атомов во многих рядах подобных соединений приближенно аддитивна. То есть можно считать, что энергия молекулы — это сумма энергий её связей, имеющих постоянные значения в таких рядах.
Аддитивность энергии молекулы выполняется не всегда. Примером нарушения аддитивности являются плоские молекулы органических соединений с так называемыми сопряженными связями, то есть с кратными связями, которые чередуются с единичными. Сильная делокализация p-состояний электронов приводит к стабилизации молекулы. Выравнивание электронной плотности вследствие коллективизации p-состояний электронов по связям выражается в укорочении двойных связей и удлинении одинарных. В правильном шестиугольнике межуглеродных связей бензола все связи одинаковы и имеют длину, среднюю между длиной одинарной и двойной связи. Сопряжение связей ярко проявляется в молекулярных спектрах. Современная квантовомеханическая теория химических связей учитывает делокализации не только p-, но и s-состояний электронов, которая наблюдается в любых молекулах.
В подавляющем большинстве случаев суммарный спин валентных электронов в молекуле равен нулю. Молекулы, содержащие неспаренные электроны — свободные радикалы (например, атомный водород Н, метил ·CH3), обычно неустойчивы, поскольку при их взаимодействии друг с другом происходит значительное снижение энергии вследствие образования ковалентных связей.
Межмолекулярное взаимодействие
Межмолекулярное взаимодействие — взаимодействие между электрически нейтральными молекулами в пространстве. В зависимости от полярности молекул характер межмолекулярного взаимодействия разный. Природа последнего оставалась неясной до создания квантовой механики.
Ориентационный тип межмолекулярного взаимодействия возникает между двумя полярными молекулами, то есть, такими, которые имеют собственный дипольный момент. Взаимодействие дипольных моментов и определяет результирующую силу — притяжения или отталкивания. В случае, если дипольные моменты молекул размещаются на одной линии, взаимодействие молекул будет интенсивней.
Индукционный тип межмолекулярного взаимодействия возникает между одной полярной и одной неполярной молекулами. При этом типе взаимодействия полярная молекула поляризует неполярную молекулу так, что заряд неполярной молекулы, противоположный действующему на неё заряда полярной молекулы, смещается до последнего: в общем, положительный заряд смещается по направлению электрического поля, которое создает полярная молекула, а отрицательный — против. Это обусловливает поляризацию неполярной молекулы, то есть явления смещения связанной электронной оболочки относительно центра положительного заряда.
Дисперсионный тип межмолекулярного взаимодействия возникает между двумя неполярными молекулами. В общем, дипольные моменты неполярных молекул равны нулю, однако в определенный момент времени, есть вероятность распределения электронов по всему объёму молекулы неравномерно. Вследствие этого возникает мгновенный дипольный момент. При этом, мгновенный диполь или поляризует соседние неполярные молекулы, или взаимодействует с мгновенным диполем другой нейтральной молекулы.
Электрические и оптические свойства молекул
Поведение вещества в электрическом поле определяется основными электрическими характеристиками молекул — постоянным дипольным моментом и поляризуемостью.
Дипольный момент означает несовпадение «центров тяжести» положительных и отрицательных зарядов в молекуле (электрическую асимметрию молекулы). То есть молекулы, имеющие центр симметрии, например H2, лишены постоянного дипольного момента, и наоборот.
Поляризуемость — это способность электронной оболочки любой молекулы перемещаться под действием электрического поля, в результате чего в молекуле образуется наведенный дипольный момент. Значение дипольного момента и поляризуемости находят экспериментально с помощью измерения диэлектрической проницаемости.
Оптические свойства вещества характеризуют его поведение в переменном электрическом поле световой волны и определяются поляризуемостью молекулы этого вещества. С поляризуемостью непосредственно связаны преломление и рассеяние света, оптическая активность и другие явления, изучаемые молекулярной оптикой.
Магнитные свойства молекул
Молекулы и макромолекулы подавляющего большинства химических соединений являются диамагнитными. Магнитная восприимчивость молекул (χ) для отдельных органических соединений может быть выражена как сумма значений χ для отдельных связей.
Молекулы, имеющие постоянный магнитный момент, является парамагнитными. К таковым относятся молекулы с нечётным количеством электронов на внешней оболочке (например, NO и любые свободные радикалы), молекулы, содержащие атомы с незаполненными внутренними оболочками (переходные металлы и т. д.). Магнитная восприимчивость парамагнитных веществ зависит от температуры, поскольку тепловое движение препятствует ориентации магнитных моментов в магнитном поле.
Спектры и строение молекул
Электрические, оптические, магнитные и другие свойства молекул связаны с волновыми функциями и энергиями различных состояний молекул. Информацию о состояниях молекул и вероятности перехода между ними дают молекулярные спектры.
Частоты колебаний в спектрах определяются массами атомов, их расположением и динамикой межатомных взаимодействий. Частоты в спектрах зависят от моментов инерции молекул, определение которых с спектроскопических данных позволяет получить точные значения межатомных расстояний в молекуле. Общее число линий и полос в колебательном спектре молекулы зависит от её симметрии.
Электронные переходы в молекулах характеризуют структуру их электронных оболочек и состояние химических связей. Спектры молекул, которые имеют большее количество связей, характеризуются длинноволновыми полосами поглощения, попадающими в видимую область. Вещества, которые построены из таких молекул, характеризуются окраской; к таким веществам относятся все органические красители.
Молекулы в химии, физике и биологии
Понятие молекулы является основным для химии, и большей частью сведений о строении и функциональность молекул наука обязана химическим исследованиям. Химия определяет строение молекул на основе химических реакций и, наоборот, на основе строения молекулы, определяет каким будет ход реакций.
Строением и свойствами молекулы определяются физические явления, которые изучаются молекулярной физикой. В физике понятие молекулы используется для объяснения свойств газов, жидкостей и твёрдых тел. Подвижностью молекул определяется способность вещества к диффузии, её вязкость, теплопроводность и т. д. Первое прямое экспериментальное доказательство существования молекул было получено французским физиком Жаном Перреном в 1906 году при изучении броуновского движения.
Поскольку все живые организмы существуют на основе тонко сбалансированного химического и нехимического взаимодействия между молекулами, изучение строения и свойств молекул имеет фундаментальное значение для биологии и естествознания в целом.
Развитие биологии, химии и молекулярной физики привели к возникновению молекулярной биологии, которая исследует основные явления жизни, исходя из строения и свойств биологически функциональных молекул.
См. также
- Химический элемент
- Молекулярные вещества
- Супрамолекула
- Теория молекулярных орбиталей
Примечания
- ↑ Молекула — статья из Большой советской энциклопедии.
- ↑ IUPAC Gold Book internet edition: (1994) “molecule”.
- ↑ Pauling, Linus. General Chemistry. — New York : Dover Publications, Inc., 1970. — ISBN 0-486-65622-5.
- ↑ Ebbin, Darrell, D. General Chemistry, 3rd Ed.. — Boston : Houghton Mifflin Co., 1990. — ISBN 0-395-43302-9.
- ↑ Brown, T.L. Chemistry – the Central Science, 9th Ed.. — New Jersey : Prentice Hall, 2003. — ISBN 0-13-066997-0.
- ↑ Chang, Raymond. Chemistry, 6th Ed.. — New York : McGraw Hill, 1998. — ISBN 0-07-115221-0.
- ↑ Zumdahl, Steven S. Chemistry, 4th ed.. — Boston : Houghton Mifflin, 1997. — ISBN 0-669-41794-7.
- ↑ Войшвалло Е.К. Понятие как форма мышления: логико-гносеологический анализ.. — М.: МГУ, 1989. — С. 181. — 238 с.
- ↑ macromolecule (polymer molecule) // IUPAC Gold Book
- ↑ Татевский В. М. Квантовая механика и теория строения молекул. — М.: Изд-во МГУ, 1965. — 162 с.
Литература
- Татевский В. М. Квантовая механика и теория строения молекул. — М.: Изд-во МГУ, 1965. — 162 с.
- Бейдер Р. Атомы в молекулах. Квантовая теория. — М.: Мир, 2001. — 532 c. ISBN 5-03-003363-7
- Минкин В. И., Симкин Б. Я., Миняев Р. М. Теория строения молекул. — М.: Высшая школа, 1979. — 408 с.
- Кук Д., Квантовая теория молекулярных систем. Единый подход. Пер с англ. М.: Интеллект, 2012. — 256с. ISBN 978-5-91559-096-9
Ссылки
- Молекула // Энциклопедический словарь Брокгауза и Ефрона : в 86 т. (82 т. и 4 доп.). — СПб., 1890—1907.
- Молекулы (видеурок, программа 7 класса)
- Molecule // IUPAC Gold Book
- Molecular entity // IUPAC Gold Book
- Молекула: Сайт о Химии
- Шредингер Э. Волновая теория механики атомов и молекул. УФН 1927
- Статья «Молекула» в Физической энциклопедии
Источник
