Какими особыми свойствами обладают вещества с межмолекулярной связью
Межмолекулярное взаимодействие — взаимодействие между молекулами и/или атомами, не приводящее к образованию ковалентных (химических) связей.
Межмолекулярное взаимодействие имеет электростатическую природу. Предположение о его существовании было впервые использовано Я. Д. Ван-дер-Ваальсом в 1873 году для объяснения свойств реальных газов и жидкостей. В наиболее широком смысле под ним можно понимать такие взаимодействия между любыми частицами (молекулами, атомами, ионами), при которых не происходит образования химических, то есть ионных, ковалентных или металлических связей. Иными словами, эти взаимодействия существенно слабее ковалентных и не приводят к существенной перестройке электронного строения взаимодействующих частиц.
На больших расстояниях преобладают силы притяжения, которые могут иметь ориентационную, поляризационную (индукционную) и дисперсионную природу (см. подробнее в статьях Силы Ван-дер-Ваальса и Дисперсионные силы). При усреднении по вращению частиц, происходящему вследствие теплового движения, потенциал межмолекулярных сил обратно пропорционален шестой степени расстояния, а ион-дипольных (как с постоянным, так и с наведенным диполем) — четвёртой степени. На малых расстояниях начинают преобладать силы отталкивания электронных оболочек частиц. Особым случаем является водородная связь — возникающее на малом расстоянии взаимодействие между атомом водорода одной молекулы и электроотрицательным атомом другой, когда эти атомы несут достаточно большой эффективный заряд.
Упаковку частиц и расстояние между ними в конденсированной фазе, определяющиеся равновесием между притяжением и отталкиванием, можно предсказать, исходя из ван-дер-ваальсовых радиусов составляющих молекулы атомов (ионных в случае ионов): расстояния между атомами разных молекул не должны превышать суммы радиусов этих атомов. Для моделирования межмолекулярных взаимодействий используют эмпирические потенциалы, среди которых наиболее известны потенциалы Леннард-Джонса (отталкивание описывается двенадцатой степенью обратного расстояния, притяжение — шестой) и Бакингема (с более физически обоснованным экспоненциальным отталкиванием), из которых первый более удобен для расчетов. В конденсированной фазе, где мультипольное разложение для молекул плохо применимо из-за близости молекул друг к другу, может применяться метод атом-атомных потенциалов, основанный на тех же потенциалах, но уже для парных взаимодействий атомов и с добавкой кулоновских членов, описывающих взаимодействие их эффективных зарядов.
Межмолекулярное взаимодействие, водородная связь[править | править код]
Дипольная молекула создает вокруг себя электростатическое поле и ориентирует остальные диполи системы, что приводит к снижению энергии. Рассчитанная П.Кизомом средняя энергия ориентационного диполь-дипольного взаимодействия между полярными молекулами составляет:
(формула 1) где – дипольный момент молекулы; r – расстояние между центрами молекул; k – константа Больцмана; T – температура по Кельвину.
Множитель (kT) в знаменателе отражает влияние флуктуации на ориентацию диполей вследствие теплового движения, которое возрастает с увеличением температуры. Кроме ориентационного, следует учитывать индукционный эффект (), то есть взаимодействие диполя с приведенным диполем, который, соответственно с П.Дебаем, равен:
(формула 2)
Ориентационные и индукционные силы возникают между полярными молекулами и не могут объяснить межмолекулярное взаимодействие между неполярными. Учитывание так сказать слабой квадруполь-квадруполь взаимодействия не решает проблему, тем более, что молекула типа и атомы инертных газов не имеют вообще квадрупольного момента (отметим, что квадрупольный момент (без дипольного) имеют молекулы типа квадруполями можно считать двухатомные гомоядерные молекулы – и т.д.).
Природа межмолекулярных сил в неполярных системах была определена Ф.Лондоном с помощью квантовой механики. Можно сказать лишь, что учитывание корреляции во время движения атомных электронов приводит к снижению энергии. Если движение электронов в разных атомах скоррелировано, то это также способствует снижению энергии. Атомы с подвижными электронами можно считать диполями, которые осциллируют с некоторой частотой . При синхронном движении электронов мгновенные диполи ориентируются всегда так, что это приводит к снижению энергии:
(формула 3)
Заменив на , где – энергия ионизации молекулы (атома), получим:
(формула 4) Эту формулу можно получить более последовательно (не применяя модель осциллирующих диполей) на основе теории возмущений.
Дж.Слетер и Дж.Кирквуд для взаимодействия многоэлектронных атомов вывели следующую формулу:
(формула 5) где N – количество электронов на внешней оболочке; m – масса электрона; е – его заряд.
Формулы (3) и (5) совпадают при N=1, если вместо подставить его выражение: Из приведенных формул можно сделать вывод о том, что основная характеристика, которая определяет величину сил Лондона, – это поляризованность () атомов (молекул). В связи с тем, что поляризованность тесно связана с коэффициентом преломления света и характеризует способность вещества к рассеиванию энергии (дисперсии) света, силы Лондона часто называют дисперсионными ().
Поляризованность зависит от размера частички, поэтому прочность молекулярных решеток должна возрастать с увеличением размеров атомов и молекул, которые взаимодействуют. Эта закономерность хорошо иллюстрируется увеличением температур кипения (аналогические зависимости наблюдаются для теплот и температур плавления, сублимации, испарения и т.д., то есть для величин, которые зависят от прочности молекулярных связей) в группе инертных газов в гомологическом ряду парафинов.
Атом Гелия настолько мал и дисперсионные силы при взаимодействии атомов Гелия такие слабые, что Гелий не может существовать в кристаллическом состоянии даже при обычном давлении и 0К. Причина этого – существование нулевой кинетической энергии, которая для гелия больше, чем энергия связи. Наличие кинетической энергии ядер в связанных атомах (при 0К) является следствием соотношения неопределенностей Гейзенберга.
Энергия связи для гелия кДж/моль, где m – масса атома Гелия.
Поэтому, и кристаллическое состояние не может реализоваться даже при 0К. Лишь при большом внешнем давлении гелий может перейти в кристаллическое состояние.
Все межмолекулярные взаимодействия (их часто объединяют общим названием – взаимодействие Ван дер Вальса) можно выразить в таком виде:
Ориентационное, индукционное и дисперсионное взаимодействия делают разный вклад в энергию связи. Для атомов и неполярных молекул и равны нулю и остается только дисперсионное взаимодействие. Вклад ориентационных и индукционных сил увеличивается с ростом дипольного момента молекул. В молекуле (1D-дебай= Кл * м) вносит 0,005%, а – 14,4%, – 4,2%; В – 3,3%, – 2,2%; – 14,4%, – 4,2%.
Благодаря приведенным формулам можно сделать вывод, что даже для очень полярных молекул дисперсионное взаимодействие делает огромный вклад.
См. также[править | править код]
- Силы Ван-дер-Ваальса
- Межатомное взаимодействие
Литература[править | править код]
- [www.xumuk.ru/encyklopedia/2477.html Межмолекулярные взаимодействия] // Химическая энциклопедия. Т. 3. — М.: Большая Российская энциклопедия, 1992. С. 12-15.
- Маррел Дж., Кеттл С., Теддер Дж. Химическая связь / Пер. с англ. С. В. Христенко. Под ред. И. В. Александрова. — М.: Мир, 1980.— 382 с.
- Бараш Ю. С. «Силы Ван-дер-Ваальса» М.: Наука, 1988. 344с.
- Каплан И. Г. «Введение в теорию межмолекулярных взаимодействий» М.: Наука, 1982. 312с.
- Каплан И. Г. Межмолекулярные взаимодействия. Физическая интерпретация, компьютерные расчеты и модельные потенциал М.: БИНОМ. Лаборатория знаний, 2012. — 400 с. ISBN 978-5-94774-939-7
- «Межмолекулярные взаимодействия; от двухатомных молекул до биополимеров» Пюльман Б. (ред) Пер. с англ., М.: Мир, 1981. — 592с.
- Израелашвили Дж. Межмолекулярные и поверхностные силы. М.: Научный мир, 2011. — 456 с. ISBN 978-5-91522-222-8
Ссылки[править | править код]
- Межмолекулярное взаимодействие в ФЭ
- [www.xumuk.ru/bse/1603.html Межмолекулярное взаимодействие] в БСЭ
Некоторые внешние ссылки в этой статье ведут на сайты, занесённые в спам-лист. Эти сайты могут нарушать авторские права, быть признаны неавторитетными источниками или по другим причинам быть запрещены в Википедии. Редакторам следует заменить такие ссылки ссылками на соответствующие правилам сайты или библиографическими ссылками на печатные источники либо удалить их (возможно, вместе с подтверждаемым ими содержимым). Список проблемных доменов |
Источник
Глава первая. Углеводороды и их природные источники
Необратимая денатурация белка вам хорошо известна по процессу варки яиц или приготовления мяса, рыбы и других белковых продуктов. О том, какие факторы могут привести к разрушению природной структуры белковых молекул, красноречиво расскажут несложные опыты. Если к раствору белка куриного яйца прилить немного этилового спирта или соли тяжёлого металла (медного купороса, нитрата свинца (II)), то нетрудно будет заметить выпадение осадка вследствие денатурации белка. Аналогичным действием обладает никотин. Может быть, эти опыты помогут вам понять, как губительны такие вредные привычки, как курение и употребление спиртного.
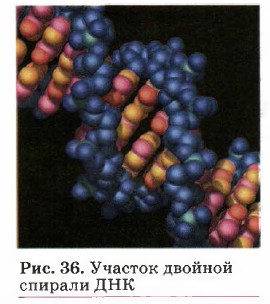
Водородная связь играет важнейшую роль в организации структуры и функционирования таких природных биополимеров, как нуклеиновые кислоты.
Так, двойная спираль (рис. 36) дезоксирибонуклеиновой кислоты — ДНК (из курса органической химии вспомните, из чего она состоит) — построена в полном соответствии с принципом комплементарности, или дополнительности. Он заключается в том, что напротив аденинового нуклеотида (А) одной полинукле- отидной цепи всегда располагается не любой, а только тиминовый нуклеотид (Т), а напротив гуанинового нуклеотида (Г) — обязательно цитозиновый нуклеотид (Ц) (рис. 37). Всё дело в том, что между этими нуклеотидами возникают водородные связи: между А и Т — две водородные связи, между Ц и Г — три.
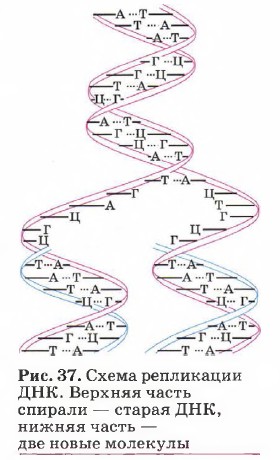
Аналогичную роль играют водородные связи и в процессе передачи наследственной информации. Так, при самоудвоении ДНК (этот процесс, как вы помните, называют репликацией) водородные связи разрываются, полинуклеотидные цепи раскручиваются и расходятся. Каждая цепь служит матрицей для образования на ней комплементарной цепи за счёт возникновения новых водородных связей.
Таким образом, после репликации образуются две дочерние молекулы ДНК, в каждой из которых одна спираль была взята из родительской ДНК, а вторая (комплементарная) спираль синтезирована заново (см. рис. 37).
Не менее важны водородные связи и в процессе транскрипции, т. е. переписывания информации о составе синтезируемого впоследствии белка на полинуклеотидную цепь ДНК.
Аналогична роль водородных связей и в трансляции, т. е. передаче информации о последовательности аминокислот в белковой молекуле в рибосомы, где происходит её сборка.

1. Что такое водородная связь? Какую точку зрения — физиков или химиков — вы разделяете по вопросу её природы?
2. Каков механизм образования водородной связи? Какие виды водородной связи вы знаете?
3. Какими особыми свойствами обладают вещества с межмолекулярной водородной связью?
4. Какую роль играет межмолекулярная водородная связь в природе?
5. Какую роль играет внутримолекулярная водородная связь в организации нативной (природной) структуры биополимеров — белков и нуклеиновых кислот?
6. Какую роль играет внутримолекулярная водородная связь в хранении и передаче наследственной информации? При ответе используйте знания по курсу общей биологии, а также консультации учителей биологии и химии.
7. Подготовьте сообщение и презентацию о социальной роли водородных связей, проиллюстрировав примерами. Воспользуйтесь ресурсами Интернета.
8. Подготовьте сообщение об открытии структуры дезоксирибонуклеиновых кислот лауреатами Нобелевской премии Дж. Уотсоном и Ф. Криком, используя ресурсы Интернета.
9. Подготовьте сообщение о химической природе негативных последствий для организма человека курения и употребления алкоголя, используя различные источники информации и ЦОРы.
Источник
В молекулах соединениях HF, H2O, NH3 существуют связи водорода с сильно электроотрицательным элементом (Н–F, Н–O, Н–N). Между молекулами таких соединений могут образовываться межмолекулярные водородные связи. В некоторых органических молекулах, содержащих связи Н–O, Н–N, могут возникать внутримолекулярные водородные связи.
Механизм образования водородной связи имеет частично электростатический, частично донорно – акцепторный характер. При этом донором электронной пары выступают атом сильно электроотрицательного элемента (F, O, N), а акцептором – атомы водорода, соединенные с этими атомами. Как и для ковалентной связи, для водородной связи характерны направленность в пространстве и насыщаемость.
Водородную связь принято обозначать точками: Н ··· F. Водородная связь проявляется тем сильнее, чем больше электроотрицательность атома-партнера и чем меньше его размеры. Она характерна прежде всего для соединений фтора, а также кислорода, в меньшей степени азота, в еще меньшей степени для хлора и серы. Соответственно меняется и энергия водородной связи (табл. 1).
Таблица 1. Средние значения энергий водородных связей
Тип водородной связи | Энергия связи, кДж/моль |
Н ··· F | 40 |
Н ··· О | 20 |
H ··· N | 8 |
Межмолекулярная и внутримолекулярная водородная связь
Благодаря водородным связям молекулы объединяются в димеры и более сложные ассоциаты. Молекулы воды образуют ассоциаты (Н2О)2, (Н2О)3, (Н2О)4; спирта (C2H5ОН)4. Этим и объясняется увеличение температуры кипения спиртов по сравнению с углеводородами, Наблюдается хорошее растворение метанола и этанола в воде. Водородная связь, возникшая между молекулами, называется межмолекулярной.
Например, образование димера парагидроксибензальдегида можно представить следующей схемой (рис. 1).
Рис. 1. Образование межмолекулярных водородных связей в парагидроксибензальдегиде.
Водородные связи могут возникать как между различными молекулами (межмолекулярная водородная связь), так и внутри молекулы (внутримолекулярная водородная связь). Внутримолекулярные водородные связи имеются в многоатомных спиртах, углеводах, белках и
других органических веществах.
Рис. 2. Образование внутримолекулярных водородных связей в салициловом альдегиде.
Влияние водородной связи на свойства веществ
Наиболее удобным индикатором существования межмолекулярной водородной связи является температура кипения вещества. Более высокая температура кипения воды (100oC по сравнению с водородными соединениями элементов подгруппы кислорода (H2S, H2Se, H2Te) объясняется наличием водородных связей: на разрушение межмолекулярных водородных связей в воде необходимо затратить дополнительную энергию.
Водородная связь существенным образом может влиять на структуру и свойства веществ. Существование межмолекулярной водородной связи повышает температуры плавления и кипения веществ. Наличие внутримолекулярной водородной связи приводит к тому, что молекула дезоксирибонуклеиновой кислоты (ДНК) оказывается свернутой в воде двойной спирали.
Водородная связь также играет важную роль в процессах растворения, поскольку растворимость зависит и от способности соединения давать водородные связи с растворителем. В результате содержащие ОН-группы такие вещества, как сахар, глюкоза, спирты, карбоновые кислоты, как правило, хорошо растворимы в воде.
Примеры соединений: одноатомные (метанол, этанол) и многоатомные спирты (глицерин, этиленгликоль), карбоновые кислоты, амины, аминокислоты, белки, вода, аммиак, фтороводород, кислородсодержащие карбоновые кислоты.
Источник
Внимание! Предварительный просмотр слайдов используется исключительно в ознакомительных целях и может не давать представления о всех возможностях презентации. Если вас заинтересовала данная работа, пожалуйста, загрузите полную версию.
Цели урока: актуализировать, обобщить и
расширить знания учащихся о водородной связи;
показать биологическое значение водородной
связи и действие различных факторов на
водородную связь.
Оборудование: компьтер, мультимедийный
проектор, презентация (Приложение 3);
штатив для пробирок, пробирки, стекляная
палочка.
Вещества и реактивы: вода, этиловый спирт,
уксусная кислота, глицерин, азотная кислота,
р-р сульфата меди, водный раствор куриного
белка.
Методы и методические приемы: словесный,
наглядный, демонстрационный.
Информационные источники: (Приложение
2)
Ход урока
I.Организация.
II.Проверка домашнего задания
Проверка домашенего задания проводится в форме
беседы по вопросам и выполнения отдельными
учащимися индивидуальных заданий.
Беседа по вопросам.
- Какими особенностями характеризуется строение
атомов металлов? - Что такое металлическая связь?
- Что представляет собой металлическая
кристаллическая решетка? - Как особенности строения металлов – простых
веществ сказываются на их физических свойствах?
Индивидуальные задания.
№1. Составить схему строения и записать
электронную конфигурацию атома индия.
Определить, к какому семейству химических
элементов принадлежит индий.
№2.Какой объем водорода выделится при
взаимодействии 0,7 моль цинка с соляной кислотой ?
№3.Найти массу 0,75 моль железа.
III.Изучение нового материала.
По ходу изучения материала учащиеся формируют
опорный конспект (Приложение 1).
– Мы продолжаем изучать типы химических
связей. Какие типы химических связей вы уже
знаете?
Предполагаемый ответ ученика.
– Ковалентная полярная, ковалентная
неполярная, ионная, металлическая.
– На сегодняшнем уроке мы рассмотрим еще один
вид химической связи – водородную связь.
Запишите тему урока (слайд №1). Сегодня мы
выясним, какие вещества образуют водородную
связь, определим виды водородной связи,
установим, как водородная связь влияет на
свойства веществ и каково её биологическое
значение, а также установим факторы, разрушающе
действующие на водородную связь.
Впервые с водородной связью вы познакомились,
когда изучали аммиак. При изучении этилового
спирта, уксусной и муравьиной кислот тоже
говорили о водородной связи. Дадим определение
водородной связи (слайд №2).
Задание.
Запишите в тетрадь определение водородной
связи.
– Какие виды водородной связи существуют?
Почему они так называются? (Слайд №3)
Задание.
Запишите в тетрадь виды водородной связи в виде
схемы. Лист разделите на две половины.
– Рассмотрим более подробно межмолекулярную
водородную связь. Она характерна для следующих
веществ: воды, спиртов, карбоновых кислот,
аммиака, фтороводорода.
(Слайды № №4-8)
Задание.
Запишите в левой колонке вещества, между
молекулами которых образуется водородная связь.
– При изучении других типов химической связи
мы говорили, какими характерными свойствами
обладают вещества, образованные той или иной
химической связью. Для веществ с межмолекулярной
связью также присущи особые свойства.
- Наличием водородной связи объясняется тот факт,
что даже вещества с небольшими относительными
молекулярными массами при обычных условиях
представляют собой жидкости (вода, спирты –
метанол, этанол, пропанол, карбоновые кислоты –
мураьиная, уксусная) или легко сжижаемые газы
(фтороводород, аммиак). (Слайд №9) - Некоторые спирты – метанол, этанол, глицерин,
этиленгликоль, уксусная и муравьиная кислоты
неограничеснно растворяются в воде. (Слайд №10)
(Демонстрация растворения в воде глицерина,
уксусной кислоты и этилового спирта). - Образованием водородных связей объясняется
аномально высокие температуры кипения (1000)
и температуры плавления (00) воды и других
веществ. (Слайд №11) - Водородные связи в немалой степени
способствуют образованию кристаллов в виде
снежинок и измороси. (Слайд №12)
Задание.
Запишите в тетрадь особенные свойства веществ,
образованных водородной связью.
– Теперь рассмотрим вещества с
внутримолекулярной водородной связью. Заполняем
правую колонку опорного конспекта.
К веществам с внутримолекулярной водородной
связью относятся природные биополимеры –
пептиды и нуклеиновые кислоты.
- В молекулах белков водородная связь определяет
вторичную структуру. (Слайд № 13)
Полипептидная цепь закручена в спираль, витки
которой удерживаются от раскручивания за счет
образования водородных связей между пептидными
фрагментами участков белковой молекулы. - Двойная спираль ДНК построена по принципу
комплементарности. (Слайд №14)
Напротив аденинового нуклеотида (А) одной
полунуклеотидной цепи всегда располагается
только тиминовый нуклеотид (Т) другой
полинуклеотидной цепи, а напротив гуанинового (Г)
нуклеотида – цитозиновый (Ц) нуклеотид. Между
этими нуклеотидами возникают водородные связи:
между А и Т – две водородные связи, между Ц и Г –
три.
Задание.
Запишите названия веществ с
внутримолекулярной водородной связью.
– Каково значение внутримолекулярной
водородной связи? (Слайд №15)
- Внутримолекулярная водородная связь имеет
большое значение в организации структур
белковых молекул. - Внутримолекулярная водородная связь
определяет функционирование нуклеиновых кислот:
хранение и передача наследственной информации
(репликация, транскрипция, трансляция).
Задание.
Запишите во второй колонке значение
внутримолекулярной водородной связи.
– Каков механизм образования водородной связи?
Механизм образования водородной связи имеет
двойную природу. (Слайд №16)
С одной стороны, он состоит в
электростатическом притяжении атома водорода,
имеющего частично положительный заряд, и атома
кислорода (фтора или азота), имеющего частично
отрицательный заряд. С другой стороны, в
образование водородной связи вносит свой вклад и
донорно-акцепторное взаимодействие между почти
свободной орбиталью атома водорода и
неподеленной электронной парой атома кислорода
(фтора или азота).
Задание.
Запишите соответствующую схему в тетрадь.
– Водородная связь непрочная. Она легко может
разрушаться в белковых молекулах. Белки
денатурируют. Денатурация бывает обратимой и
необратимой. Обратимая денатурация белков имеет
социальное значение. Денатурирующими факторами
белков человеческого организма могут служить
вибрации, высокие температуры, электромагнитное
излучение, химические вещества. (Слайд №17)
Демонстрация опыта: денатурация куриного белка
под действием азотной кислоты и под действием
сульфата меди.
Задание.
Запишите факторы, которые оказывают на белок
человеческого организма денатурирующее
воздействие.
IV.Закрепление.
Беседа по вопросам.
– Используя составленный опорный конспект,
ответьте на вопросы.
- Какая химическая связь называется водородной?
- Какие виды водородной связи существуют?
- Для каких веществ характерна межмолекулярная
водородная связь? - Какие особые свойства присущи веществам с
межмолекулрной водородной связью? - Для каких веществ характерна
внутримолекулярная водородная связь? - Каково значение внутримолекулярной связи?
- Каков механизм образования водородной связи?
V.Домашнее задание.
Выучить опорный конспект, ответить на вопросы
№№1, 2, 3, 4, 5, 6 параграфа 6.
Источник
