Какими химическими свойствами обладает соляная кислота
Получение. Соляную кислоту получают путем растворения хлороводорода в воде.
Обратите внимание на прибор изображенный на рисунке слева. Его используют для получения соляной кислоты. Во время процесса получения соляной кислоты, следят за газоотводной трубкой, она должна находиться вблизи уровня воды, а не быть погруженной в нее. Если за этим не следить, то из-за большой растворимости хлороводорода вода попадет в пробирку с серной кислотой и 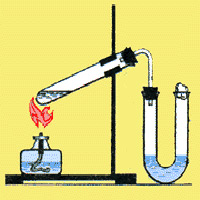 может произойти взрыв.
может произойти взрыв.
В промышленности соляную кислоту обычно получают путем сжигания водорода в хлоре и растворении продукта реакции в воде.
Физические свойства. Растворяя хлороводород в воде, можно получить даже 40% раствор соляной кислоты с плотностью 1,19 г/см3. Однако имеющаяся в продаже концентрированная соляная кислота содержит около 0,37 массовых долей, или около 37% хлороводорода. Плотность данного раствора составляет примерно 1,19 г/см3. Пр разбавлении кислоты плотность ее раствора уменьшается.
Концентрированная соляная кислота является бесценным раствором, сильно дымящая во влажном воздухе, обладающая резким запахом вследствие выделения хлороводорода.
Химические свойства. Соляная кислота обладает рядом общих свойств, которые характерны большинству кислот. Помимо этого, она обладает некоторыми специфическими свойствами.
Свойства HCL, общие с другими кислотами: 1) Изменение окраски индикаторов 2) взаимодействие с металлами 2HCL + Zn → ZnCL2 + H2↑ 3) Взаимодействие с основными и амфотерными оксидами: 2HCL + CaO → CaCl2 + H2O; 2HCL + ZnO → ZnHCL2 + H2O 4) Взаимодействие с основаниями: 2HCL + Cu (OH)2 → CuCl2 + 2H2O 5) Взаимодействие с солями: 2HCL + CaCO3 → H2O + CO2↑ + CaCL2
Специфические свойства HCL: 1) Взаимодействие с нитратом серебра (нитрат серебра является реактивом на соляную кислоту и ее соли); выпадет осадок белого цвета, который не растворяется в воде, ни в кислотах: HCL + AgNO3 → AgCL↓ + HNO3 2) Взаимодействие с окислителями (MnO2, KMnO, KCLO3 и др.): 6HCL + KCLO3 → KCL +3H2O + 3CL2↑
 Применение. Огромное количество соляной кислоты расходуется для удаления оксидов железа перед покрытием изделий из этого металла другими металлами (оловом, хромом, никелем). Для того чтобы соляная кислота реагировала только с оксидами, но не с металлом, к ней добавляют особые вещества, которые называются ингибиторами. Ингибиторы – вещества замедляющие реакции.
Применение. Огромное количество соляной кислоты расходуется для удаления оксидов железа перед покрытием изделий из этого металла другими металлами (оловом, хромом, никелем). Для того чтобы соляная кислота реагировала только с оксидами, но не с металлом, к ней добавляют особые вещества, которые называются ингибиторами. Ингибиторы – вещества замедляющие реакции.
Соляная кислота применяется для получения различных хлоридов. Ее используют для получения хлора. Очень часто, раствор соляной кислоты прописывают больным с пониженной кислотностью желудочного сока. Соляная кислота находится у каждого в организме, она входит в состав желудочного сока, который необходим для пищеварения.
В пищевой промышленности соляная кислота применяется только в виде раствора. Она используется для регулирования кислотности при производстве лимонной кислоты, желатина или фруктозы (Е 507).
Не стоит забывать, что соляная кислота опасна для кожи. Еще большую опасность она представляет для глаз. Воздействуя на человека, она может вызвать разрушение зубов, раздражение слизистых оболочек, удушье.
Помимо этого, соляная кислота активно применяется в гальванопластике и гидрометаллургии (удаление накипи, ржавчины, обработка кожи, химреактивы, в качестве растворителя породы при добыче нефти, при производстве каучуков, глутамината натрия, соды, Сl2). Соляная кислота используется для регенерации Сl2, в органическом синтезе (для получения винилхлорида, алкилхлоридов и т.д.) Она может использоваться в качестве катализатора при получении дифенилолпропана, алкилирование бензола.
© blog.tutoronline.ru,
при полном или частичном копировании материала ссылка на первоисточник обязательна.
Остались вопросы?
Задайте свой вопрос и получите ответ от профессионального преподавателя.
Источник
Характеристики и физические свойства соляной кислоты
Сильная кислота: pKa = -7,1. Концентрированная соляная кислота содержит около 37% HCl.
Основные физические свойства соляной кислоты приведены в таблице:
Температура плавления, oС | -30 |
Температура кипения, oС | 48 |
Энтальпия образования, кДж/моль | -605,22 |
Плотность, г/см3 | 1,19 |
Удельная теплоемкость, кДж/(кг×К) | 2,46 |
Вязкость, МПа×с | 1,99 |
Получение соляной кислоты
Соляная кислота получается растворением в воде хлороводорода. В настоящее время основным способом промышленного получения хлороводорода является синтез его из водорода и хлора:
H2 + Cl2 = 2HCl + 183 кДж.
Этот процесс осуществляют в специальных установках, в которых смесь водорода и хлора непрерывно образуется и тут же сгорает ровным пламенем. Тем самым достигается спокойное (без взрыва) протекание реакции. Исходным сырьем для получения хлороводорода служат хлор и водород, образующиеся при электролизе раствора хлорида натрия.
Большие количества соляной кислоты получают также в качестве побочного продукта хлорирования органических соединений согласно уравнению реакции, представленному ниже:
R-H + Cl2 = R-Cl + HCl,
где R – углеводородный радикал.
Химические свойства соляной кислоты
Соляная кислота – сильный электролит. Для нее характерны следующие химические свойства, общие для всех кислот:
— способность взаимодействовать с основаниями с образованием солей:
HCldilute + NaOHdilute = NaCl + H2O;
HCldilute + NH3×H2O = NH4Cl + H2O;
— способность взаимодействовать с некоторыми металлами с выделением водорода (разбавленный раствор):
2HCldilute + Fe = FeCl2 + H2↑;
2HCldilute + Zn = ZnCl2 + H2↑;
— способность вступать в реакции взаимодействия с основными и амфотерными оксидами с образованием солей и воды:
4HClconc + MnO2 = MnCl2 + 2H2O + Cl2↑;
4HClconc + PbO2 = PbCl2↓ + Cl2↑ + 2H2O;
— способность взаимодействовать с солями более слабых кислот:
2HCldilute + CaCO3 = CaCl2 + CO2↑ + H2O;
— способность изменять цвета индикаторов, в частности, вызывать красную окраску лакмуса;
— кислый вкус.
При диссоциации соляной кислоты образуются ионы водорода:
HCl↔H+ + Cl—.
Нагревание смеси растворов соляной и азотной кислот до температуры 100-150oС приводит к образованию очень сильного окислителя — соединения, которое называют «царская водка»:
6HClconc + 2HNO3 conc = 2NO↑ + 3Cl2↑ + 4H2O.
Соляная кислота в окислительно-восстановительных реакциях может выступать и как восстановитель (за счет хлорид-аниона Cl—) и как окислитель (за счет катиона водорода H+). Уравнения ОВР с участием соляной кислоты приведены ниже:
16HClconc + 2KMnO4 = 2MnCl2 + 5Cl2↑ + 8H2O + 2KCl;
14 HClconc + K2Cr2O7 = 2CrCl3 + 3Cl2↑ + 7H2O + 2KCl (t = 60 – 80oC);
4 HClconc + Ca(ClO)2 = 2Cl2↑ + CaCl2 + 2H2O;
6 HClconc + KClO3 = 3Cl2↑ + KCl + 3H2O.
Применение соляной кислоты
Соляная кислота – одна из важнейших кислот в химической практике. Ежегодное мировое производство соляной кислоты исчисляется миллионами тонн. Широкое применение находят также многие её соли.
Соляная кислота применяется в таких областях народного хозяйства как гидрометаллургия и гальванопластика, для травления, декапирования и лужения поверхности металлов; пищевом производстве, как регулятор кислотности (добавка Е507); в медицине, в качестве лекарства (смесь с ферментом пепсином) при недостаточной кислотности желудка.
Примеры решения задач
Источник
Раствор хлорводорода в воде, который является бесцветной прозрачной жидкостью.
Из-за присутствия единственного элемента (односоставной примеси) в воде считается едкой в силу своих химических свойств. При соприкосновении с воздухом исходит «дымок».
Формула
HCl
Техническая кислота (Cl – H) имеет такую же формулу, но отличается по цвету – из-за примесей железа и хлора отдает желтоватым оттенком. Концентрация раствора зависит от температурного режима хранения, и при 20 градусах она составляет 38% с плотностью 1,18 г/см3. Соль раствора называется хлоридом.
Альтернативные названия
Хлористоводородная кислота или хлористый водород.
Получение соляной кислоты
Соляную кислоту получают путём растворения газообразного хлороводорода в воде. Его сжигают в хлоре, в результате чего на выходе имеется синтетическая кислота. Также получение возможно из побочных газов при хлорировании углеводорода. В первом случае она будет иметь меньше примесей, а второй необходим в промышленности, когда спрос на абгазную кислоту увеличивается.
В лабораторных условиях используют серную кислоту и поваренную соль:
- При температуре в 550 градусов и выше поваренная соль дает избыток.
- При проведении гидролиза магния и алюминия хлоридов (нагревание гидратированной соли).
- При получении оксихлоридов, когда происходит неполное растворение солей (реакция не завершается).
Чем выше температура окружающей среды, тем ниже способность к растворению. Поэтому на практике используют 36%-ую кислоту, хотя при 0-1 градусе кислород поглотит больше половины примесей, что равно 45%-ой кислоте.
Свойства соляной кислоты
Физические свойства
Физические свойства кислоты зависят от степени концентрации растворенного хлороводорода. При повышении наблюдается:
• Увеличение плотности раствора;
• Увеличение молярности;
• Снижение водородного показателя (pH);
• Увеличение вязкости вещества;
• Снижение удельной теплоёмкости;
• Увеличение давления пара;
• Снижение температуры кипения;
• Вариации температуры плавления.
Последние меняются так: при минимальной и максимальной концентрации плавление достигает максимальных показателей. Средняя концентрация поддаётся плавлению в минимальных температурах. Затвердевшее вещество даёт кристаллогидраты – HCl·H2O, HCl·6H2O, HCl·3H2O, HCl·2H2O.
Химические свойства
- Взаимодействует с металлами (Ме) электрохимических потенциалов:
Mg+2HCl = MgCl2+H2.
Образуется соль с выделением водорода.
- Взаимодействует с оксидами Ме:
Na2O+2HCl = 2NaCl+H2O
с образованием соли и воды.
- Реакция нейтрализации с гидроксидами Ме:
NaOH+HCl = NaCl+H2O
с образованием растворимой соли и воды.
Также вступает в реакцию с солями Ме, окислителями с выделением хлорного газа и аммиаком с выделением густого белого дыма из кристаллов аммония хлорида.
Применение соляной кислоты
Применение широко распространено в сферах гидрометаллургии и гальванопластике. Проводится очистка поверхностей металлов при помощи кислот; для получения цинковых хлоридов. Иногда техническая соляная кислота необходима для чистки керамики и металлических изделий. Для этого берётся ингибированная кислота, предназначенная специально для дезинфекций.
В пищевой промышленности она необходима для урегулирования кислотности продуктов. Зарегистрировано вещество под кодом пищевой добавки Е507. Чаще всего используется при изготовлении зельтерской воды (содовая).
В фармацевтической промышленности соляная кислота нужна для изготовления лекарственных препаратов, предназначенных для смеси с ферментами пепсинов. При недостатке естественной кислоты в желудочном соке в концентрации 0,5% назначается приемом внутрь.
Тест по теме «Соляная кислота»
Источник
- Описание вещества
- Свойства
- Как получают
- Хранение и транспортировка
- Применение
Описание вещества
 Соляная кислота представляет из себя водный раствор хлористого водорода. Химическая формула данного вещества – HCl. В воде масса хлороводорода при наибольшей концентрации не может превышать 38%. При комнатной температуре хлороводород находится в газообразном состоянии. Для перехода его в жидкое состояние, он должен быть охлажден до минус 84 градуса по шкале Цельсия, в твердое – до минус 112 градусов. Плотность концентрированной кислоты при комнатной температуре составляет 1,19 г/см3. Данная жидкость входит в состав желудочного сока, который обеспечивает переваривание пищи. В этом состоянии ее концентрация не превышает 0,3%.
Соляная кислота представляет из себя водный раствор хлористого водорода. Химическая формула данного вещества – HCl. В воде масса хлороводорода при наибольшей концентрации не может превышать 38%. При комнатной температуре хлороводород находится в газообразном состоянии. Для перехода его в жидкое состояние, он должен быть охлажден до минус 84 градуса по шкале Цельсия, в твердое – до минус 112 градусов. Плотность концентрированной кислоты при комнатной температуре составляет 1,19 г/см3. Данная жидкость входит в состав желудочного сока, который обеспечивает переваривание пищи. В этом состоянии ее концентрация не превышает 0,3%.
Свойства соляной кислоты
Раствор хлористого водорода химически вреден, класс его опасности – второй.
Соляная жидкость – это сильная одноосновная кислота, которая может вступать в реакцию с множеством металлов, их солями, оксидами и гидрооксидами, она может взаимодействовать с нитратом серебра, аммиаком, гипохлоритом кальция и сильными окислителями:
Физические свойства и влияние на организм
При высоких концентрациях это едкое вещество, которое может вызвать ожоги не только слизистых оболочек, но и кожных покровов. Нейтрализовать его можно раствором пищевой соды. При открытии емкостей с концентрированным соляным раствором, его пары, соприкасаясь с находящейся в воздухе влагой, образовывают конденсат ядовитых паров в виде мельчайших капелек (аэрозоля), который раздражает дыхательные пути и глаза.
Концентрированное вещество имеет характерный резкий запах. Технические сорта раствора хлористого водорода делят на:
рыжий неочищенный, его цвет в основном обуславливается примесями хлорного железа;
очищенный, бесцветная жидкость, в которой концентрация HCl составляет порядка 25%;
дымящий, концентрированный, жидкость с концентрацией HCl в 35-38%.
Химические свойства

Как получают
Процесс производства соляной жидкости состоит из этапов получение хлорводорода и абсорбация (поглощение) его водой.
Существует три промышленных способа получения хлористого водорода:
синтетический
сульфатный
из побочных газов (абгазов) ряда технологических процессов. Последний способ является самым распространенным. Побочный HCl обычно образуется при дегихлорировании и хлорировании органических соединений, изготовлении калийных удобрений, пиролизе хлоридов металлов или органических отходов, содержащих хлор.
Хранение и транспортировка

Хранят и транспортируют соляную техническую кислоту в специализированных покрытых полимерами цистернах и контейнерах, бочках из полиэтилена, стеклянных бутылях, упаковываемых в ящики. Люки контейнеров и цистерн, пробки бочек и бутылей должны обеспечивать герметичность емкости. Кислотный раствор не должен контактировать с металлами, находящимися в линейке напряжения левее водорода, так как это может стать причиной возникновения взрывоопасных смесей.
Применение
в металлургии для извлечения руд, удаления ржавчины, окалин, грязи и окислов, паянии и лужении;
при изготовлении синтетических каучуков и смол;
в гальванопластике;
в качестве регулятора кислотности в пищевой промышленности;
для получения хлоридов металлов;
для получения хлора;
в медицине для лечения недостаточной кислотности желудочного сока;
в качестве чистящего и дезинфицирующего средства.
В нашей следующей статье мы подробно поговорить о классификации, свойствах и предназначении всасывающих рукавов.
← Назад к списку новостей
Источник
Соляная кислота (также хлороводородная, хлористоводородная кислота, хлористый водород) — раствор хлороводорода (HCl) в воде, сильная одноосновная кислота. Бесцветная, прозрачная, едкая жидкость, «дымящаяся» на воздухе (техническая соляная кислота — желтоватого цвета из-за примесей железа, хлора и пр.). В концентрации около ω = 0,5 % присутствует в желудке человека, что соответствует pH = pω − lg ( ρH2O / μHCl ) ≅ 0,86. Максимальная концентрация при 20 °C равна 38 % по массе, плотность такого раствора 1,19 г/см³. Соли соляной кислоты называются хлоридами.
Физические свойства
Физические свойства соляной кислоты сильно зависят от концентрации растворённого хлороводорода:
| Конц. (вес), кг HCl/кг | Конц. (г/л), кг HCl/м³ | Плотность, кг/л | Молярность M | Водородный показатель (pH) | Вязкость, мПа·с | Удельная теплоемкость, кДж/(кг·К) | Давление пара, Па | Температура кипения, °C | Температура плавления, °C |
| 10 % | 104,80 | 1,048 | 2,87 | −0,4578 | 1,16 | 3,47 | 0,527 | 103 | −18 |
| 20 % | 219,60 | 1,098 | 6,02 | −0,7796 | 1,37 | 2,99 | 27,3 | 108 | −59 |
| 30 % | 344,70 | 1,149 | 9,45 | −0,9754 | 1,70 | 2,60 | 1,410 | 90 | −52 |
| 32 % | 370,88 | 1,159 | 10,17 | −1,0073 | 1,80 | 2,55 | 3,130 | 84 | −43 |
| 34 % | 397,46 | 1,169 | 10,90 | −1,0374 | 1,90 | 2,50 | 6,733 | 71 | −36 |
| 36 % | 424,44 | 1,179 | 11,64 | −1,06595 | 1,99 | 2,46 | 14,100 | 61 | −30 |
| 38 % | 451,82 | 1,189 | 12,39 | −1,0931 | 2,10 | 2,43 | 28,000 | 48 | −26 |
При 20 °C, 1 атм (101 кПа)При затвердевании даёт кристаллогидраты составов HCl·H2O, HCl·2H2O, HCl·3H2O, HCl·6H2O.
Химические свойства
- Взаимодействие с металлами, стоящими в ряду электрохимических потенциалов до водорода, с образованием соли и выделением газообразного водорода:
2Na + 2HCl ⟶ 2NaCl + H2 ↑Mg + 2HCl ⟶ MgCl2 + H2 ↑
2Al + 6HCl ⟶ 2AlCl3 + 3H2 ↑
- Взаимодействие с оксидами металлов с образованием растворимой соли и воды:
Na2O + 2HCl ⟶ 2NaCl + H2O MgO + 2HCl ⟶ MgCl2 + H2OAl2O3 + 6HCl ⟶ 2AlCl3 + 3H2O
- Взаимодействие с гидроксидами металлов с образованием растворимой соли и воды (реакция нейтрализации):
NaOH + HCl ⟶ NaCl + H2O Ba(OH)2 + 2HCl ⟶ BaCl2 + 2H2OAl(OH)3 + 3HCl ⟶ AlCl3 + 3H2O
- Взаимодействие с солями металлов, образованных более слабыми кислотами, например угольной:
Na2CO3 + 2HCl ⟶ 2NaCl + H2O + CO2 ↑
- Взаимодействие с сильными окислителями (перманганат калия, диоксид марганца) с выделением газообразного хлора:
2KMnO4 + 16HCl ⟶ 5Cl2 ↑ + 2MnCl2 + 2KCl + 8H2O
- Взаимодействие с аммиаком с образованием густого белого дыма, состоящего из мельчайших кристалликов хлорида аммония:
NH3 + HCl ⟶ NH4Cl
- Качественной реакцией на соляную кислоту и её соли является её взаимодействие с нитратом серебра, при котором образуется белый творожистый осадок хлорида серебра, нерастворимый в азотной кислоте:
HCl + AgNO3 → AgCl ↓ + HNO3

Получение
Соляную кислоту получают растворением газообразного хлороводорода в воде. Хлороводород получают сжиганием водорода в хлоре, полученная таким способом кислота называется синтетической. Также соляную кислоту получают из абгазов — побочных газов, образующихся при различных процессах, например, при хлорировании углеводородов. Хлороводород, содержащийся в этих газах, называется абгазным, а полученная таким образом кислота — абгазной. В последние десятилетия доля абгазной соляной кислоты в объёме производства постепенно увеличивается, вытесняя кислоту, полученную сжиганием водорода в хлоре. Но полученная методом сжигания водорода в хлоре соляная кислота содержит меньше примесей и применяется при необходимости высокой чистоты.
В лабораторных условиях используется разработанный ещё алхимиками способ, заключающийся в действии концентрированной серной кислоты на поваренную соль:
NaCl + H2SO4 →150oC NaHSO4 + HCl
При температуре выше 550 °C и избытке поваренной соли возможно взаимодействие:
2NaCl + H2SO4 →550oC Na2SO4 + 2HCl
Возможно получение путём гидролиза хлоридов магния, алюминия (нагревается гидратированная соль):
MgCl2 ⋅ 6H2O →t,oC MgO + 2HCl + 5H2O
AlCl3 ⋅ 6H2O →t,oC Al(OH)3 + 3HCl + 3H2O
Эти реакции могут идти не до конца с образованием основных хлоридов (оксихлоридов) переменного состава, например:
MgCl2 + H2O → Mg2OCl2 + HCl
Хлороводород хорошо растворим в воде. Так, при 0 °C 1 объём воды может поглотить 507 объёмов HCl, что соответствует концентрации кислоты 45 %. Однако при комнатной температуре растворимость HCl ниже, поэтому на практике обычно используют 36-процентную соляную кислоту.
Применение

Перевозка соляной кислоты железнодорожным транспортом осуществляется в специализированных вагонах-цистернах
Промышленность
- Применяется в гидрометаллургии и гальванопластике (травление, декапирование), для очистки поверхности металлов при пайке и лужении, для получения хлоридов цинка, марганца, железа и др. металлов. В смеси с поверхностно-активными веществами используется для очистки керамических и металлических изделий (тут необходима ингибированная кислота) от загрязнений и дезинфекции.
- В пищевой промышленности зарегистрирована как регулятор кислотности (пищевая добавка E507). Применяется для изготовления зельтерской (содовой) воды.
Медицина
Основная статья: Кислотность желудочного сока
- Естественная составная часть желудочного сока человека. В концентрации 0,3—0,5 %, обычно в смеси с ферментом пепсином, назначается внутрь при недостаточной кислотности.
Особенности обращения
Высококонцентрированная соляная кислота — едкое вещество, при попадании на кожу вызывает сильные химические ожоги. Особенно опасно попадание в глаза. Для нейтрализации ожогов применяют раствор слабого основания, или соли слабой кислоты, обычно питьевой соды.
При открывании сосудов с концентрированной соляной кислотой пары хлороводорода, притягивая влагу воздуха, образуют туман, раздражающий глаза и дыхательные пути человека.
Реагируя с сильными окислителями (хлорной известью, диоксидом марганца, перманганатом калия) образует токсичный газообразный хлор.
В РФ оборот соляной кислоты концентрации 15 % и более — ограничен.

Источник

