Какие вещества называют органическими их свойства

История развития органической химии
В истории развития органической химии выделяют два периода: эмпирический (с середины XVII до конца XVIII века), в который познание органических веществ, способов их выделения и переработки происходило опытным путем и аналитический (конец XVIII – середина XIX века), связанный с появлением методов установления состава органических веществ. В аналитический период было установлено, что все органические вещества содержат углерод. Среди, других элементов, входящих в состав органических соединений были обнаружены водород, азот, сера, кислород и фосфор.
Важное значение в истории органической химии имеет структурный период (вторая половина XIX – начало XX века), ознаменовавшийся рождением научной теории строения органических соединений, основоположником которой был А.М. Бутлеров.
Основные положения теории строения органических соединений:
- атомы в молекулах соединены между собой в определенном порядке химическими связями в соответствии с их валентностью. Углерод во всех органических соединениях четырехваленнтен;
- свойства веществ зависят не только от их качественного и количественного состава, но и от порядка соединения атомов;
- атомы в молекуле взаимно влияют друг на друга.
Порядок соединения атомов в молекуле описывается структурной формулой, в которой химические связи изображаются черточками.
Характерные свойства органических веществ
Существует несколько важных свойств, которые выделяют органические соединения в отдельный, ни на что не похожий класс химических соединений:
- Органические соединения обычно представляют собой газы, жидкости или легкоплавкие твердые вещества, в отличие неорганических соединений, которые в большинстве своём представляют собой твердые вещества с высокой температурой плавления.
- Органические соединения большей частью построены ковалентно , а неорганические соединения — ионно.
- Различная топология образования связей между атомами, образующими органические соединения (прежде всего, атомами углерода), приводит к появлению изомеров — соединений, имеющих один и тот же состав и молекулярную массу, но обладающих различными физико-химическими свойствами. Данное явление носит название изомерии.
- Явление гомологии — существование рядов органических соединений, в которых формула любых двух соседей ряда (гомологов) отличается на одну и ту же группу — гомологическую разницу CH2. Органические вещества горят.
Классификация органических веществ
В классификации принимают за основу два важных признака – строение углеродного скелета и наличие в молекуле функциональных групп.
В молекулах органических веществ атомы углерода соединяются друг с другом, образуя т.н. углеродный скелет или цепь. Цепи бывают открытыми и замкнутыми
(циклическими), открытые цепи могут быть неразветвленными (нормальными) и разветвленными:

По строению углеродного скелета различают:
— алициклические органические вещества, имеющие открытую углеродную цепь как разветвленную, так и неразветвленную. Например,
СН3-СН2-СН2-СН3 (бутан)
СН3-СН(СН3)-СН3 (изобутан)
— карбоциклические органические вещества, в которых углеродная цепь замкнута в цикл (кольцо). Например,

— гетероциклические органические соединения, содержащие в цикле не только атомы углерода, но и атомы других элементов, чаще всего азота, кислорода или серы:

Функциональная группа – атом или группа атомов неуглеводородного характера, которые определяют принадлежность соединения к определенному классу. Признаком, по которому органическое вещество относят к тому или иному классу, является природа функциональной группы (табл. 1).
Таблица 1. Функциональные группы и классы.

Соединения могут содержать не одну, а несколько функциональных групп. Если эти группы одинаковые, то соединения называют полифункциональными, например хлороформ, глицерин. Соединения, содержащие различные функциональные группы, называют гетерофункциональными, их можно одновременно отнести к нескольким классам соединений, например молочную кислоту можно рассматривать, как карбоновую кислоту и как спирт, а коламин – как амин и спирт.
Примеры решения задач
Источник
Что такое органические вещества?
В прошлом ученые разделяли все вещества в природе на условно неживые и живые, включая в число последних царство животных и растений. Вещества первой группы получили название минеральных. А те, что вошли во вторую, стали называть органическими веществами.
Что под этим подразумевается? Класс органических веществ наиболее обширный среди всех химических соединений, известных современным ученым. На вопрос, какие вещества органические, можно ответить так – это химические соединения, в состав которых входит углерод.
Обратите внимание, что не все углеродсодержащие соединения относятся к органическим. Например, корбиды и карбонаты, угольная кислота и цианиды, оксиды углерода не входят в их число.
Почему органических веществ так много?
Ответ на этот вопрос кроется в свойствах углерода. Этот элемент любопытен тем, что способен образовывать цепочки из своих атомов. И при этом углеродная связь очень стабильная.
Кроме того, в органических соединениях он проявляет высокую валентность (IV), т.е. способность образовывать химические связи с другими веществами. И не только одинарные, но также двойные и даже тройные (иначе – кратные). По мере возрастания кратности связи цепочка атомов становится короче, а стабильность связи повышается.
А еще углерод наделен способностью образовывать линейные, плоские и объемные структуры.
Именно поэтому органические вещества в природе так разнообразны. Вы легко проверите это сами: встаньте перед зеркалом и внимательно посмотрите на свое отражение. Каждый из нас – ходячее пособие по органической химии. Вдумайтесь: не меньше 30% массы каждой вашей клетки – это органические соединения. Белки, которые построили ваше тело. Углеводы, которые служат «топливом» и источником энергии. Жиры, которые хранят запасы энергии. Гормоны, которые управляют работой органов и даже вашим поведением. Ферменты, запускающие химические реакции внутри вас. И даже «исходный код», цепочки ДНК – все это органические соединения на основе углерода.
Состав органических веществ
Как мы уже говорили в самом начале, основной строительный материал для органических веществ – это углерод. И практические любые элементы, соединяясь с углеродом, могут образовывать органические соединения.
В природе чаще всего в составе органических веществ присутствуют водород, кислород, азот, сера и фосфор.
Строение органических веществ
Многообразие органических веществ на планете и разнообразие их строения можно объяснить характерными особенностями атомов углерода.
Вы помните, что атомы углерода способны образовывать очень прочные связи друг с другом, соединяясь в цепочки. В результате получаются устойчивые молекулы. То, как именно атомы углерода соединяются в цепь (располагаются зигзагом), является одной из ключевых особенностей ее строения. Углерод может объединяться как в открытые цепи, так и в замкнутые (циклические) цепочки.
Важно и то, что строение химических веществ прямо влияет на их химические свойства. Значительную роль играет и то, как атомы и группы атомов в молекуле влияют друг на друга.
Благодаря особенностям строения, счет однотипным соединениям углерода идет на десятки и сотни. Для примера можно рассмотреть водородные соединения углерода: метан, этан, пропан, бутан и т.п.
Например, метан – СН4. Такое соединение водорода с углеродом в нормальных условиях пребывает в газообразном агрегатном состоянии. Когда же в составе появляется кислород, образуется жидкость – метиловый спирт СН3ОН.
Не только вещества с разным качественным составом (как в примере выше) проявляют разные свойства, но и вещества одинакового качественного состава тоже на такое способны. Примером могут служить различная способность метана СН4 и этилена С2Н4 реагировать с бромом и хлором. Метан способен на такие реакции только при нагревании или под ультрафиолетом. А этилен реагирует даже без освещения и нагревания.
Рассмотрим и такой вариант: качественный состав химических соединений одинаков, количественный – отличается. Тогда и химические свойства соединений различны. Как в случае с ацетиленом С2Н2 и бензолом С6Н6.
Не последнюю роль в этом многообразии играют такие свойства органических веществ, «завязанные» на их строении, как изомерия и гомология.
Представьте, что у вас есть два на первый взгляд идентичных вещества – одинаковый состав и одна и та же молекулярная формула, чтобы описать их. Но строение этих веществ принципиально различно, откуда вытекает и различие химических и физических свойств. К примеру, молекулярной формулой С4Н10 можно записать два различных вещества: бутан и изобутан.
Речь идет об изомерах – соединениях, которые имеют одинаковый состав и молекулярную массу. Но атомы в их молекулах расположены в различном порядке (разветвленное и неразветвленное строение).
Что касается гомологии – это характеристика такой углеродной цепи, в которой каждый следующий член может быть получен прибавлением к предыдущему одной группы СН2. Каждый гомологический ряд можно выразить одной общей формулой. А зная формулу, несложно определить состав любого из членов ряда. Например, гомологи метана описываются формулой CnH2n+2.
По мере прибавления «гомологической разницы» СН2, усиливается связь между атомами вещества. Возьмем гомологический ряд метана: четыре первых его члена – газы (метан, этан, пропан, бутан), следующие шесть – жидкости (пентан, гексан, гептан, октан, нонан, декан), а дальше следуют вещества в твердом агрегатном состоянии (пентадекан, эйкозан и т.д.). И чем прочнее связь между атомами углерода, тем выше молекулярный вес, температуры кипения и плавления веществ.
Какие классы органических веществ существуют?
К органическим веществам биологического происхождения относятся:
- белки;
- углеводы;
- нуклеиновые кислоты;
- липиды.
Три первых пункта можно еще назвать биологическими полимерами.
Более подробная классификация органических химических веществ охватывает вещества не только биологического происхождения.
К углеводородам относятся:
- ациклические соединения:
- предельные углеводороды (алканы);
- непредельные углеводороды:
- алкены;
- алкины;
- алкадиены.
- циклические соединения:
- соединения карбоциклические:
- алициклические;
- ароматические.
- соединения гетероциклические.
- соединения карбоциклические:
Есть также иные классы органических соединений, в составе которых углерод соединяется с другими веществами, кроме водорода:
- спирты и фенолы;
- альдегиды и кетоны;
- карбоновые кислоты;
- сложные эфиры;
- липиды;
- углеводы:
- моносахариды;
- олигосахариды;
- полисахариды.
- мукополисахариды.
- амины;
- аминокислоты;
- белки;
- нуклеиновые кислоты.
Формулы органических веществ по классам
Примеры органических веществ
Как вы помните, в человеческом организме различного рода органические вещества – основа основ. Это наши ткани и жидкости, гормоны и пигменты, ферменты и АТФ, а также многое другое.
В телах людей и животных приоритет за белками и жирами (половина сухой массы клетки животных это белки). У растений (примерно 80% сухой массы клетки) – за углеводами, в первую очередь сложными – полисахаридами. В том числе за целлюлозой (без которой не было бы бумаги), крахмалом.
Давайте поговорим про некоторые из них подробнее.
Например, про углеводы. Если бы можно было взять и измерить массы всех органических веществ на планете, именно углеводы победили бы в этом соревновании.
Они служат в организме источником энергии, являются строительными материалами для клеток, а также осуществляют запас веществ. Растениям для этой цели служит крахмал, животным – гликоген.
Кроме того, углеводы очень разнообразны. Например, простые углеводы. Самые распространенные в природе моносахариды – это пентозы (в том числе входящая в состав ДНК дезоксирибоза) и гексозы (хорошо знакомая вам глюкоза).
Как из кирпичиков, на большой стройке природы выстраиваются из тысяч и тысяч моносахаридов полисахариды. Без них, точнее, без целлюлозы, крахмала, не было бы растений. Да и животным без гликогена, лактозы и хитина пришлось бы трудно.
Посмотрим внимательно и на белки. Природа самый великий мастер мозаик и пазлов: всего из 20 аминокислот в человеческом организме образуется 5 миллионов типов белков. На белках тоже лежит немало жизненно важных функций. Например, строительство, регуляция процессов в организме, свертывание крови (для этого существуют отдельные белки), движение, транспорт некоторых веществ в организме, они также являются источником энергии, в виде ферментов выступают катализатором реакций, обеспечивают защиту. В деле защиты организма от негативных внешних воздействий важную роль играют антитела. И если в тонкой настройке организма происходит разлад, антитела вместо уничтожения внешних врагов могут выступать агрессорами к собственным органам и тканям организма.
Белки также делятся на простые (протеины) и сложные (протеиды). И обладают присущими только им свойствами: денатурацией (разрушением, которое вы не раз замечали, когда варили яйцо вкрутую) и ренатурацией (это свойство нашло широкое применение в изготовлении антибиотиков, пищевых концентратов и др.).
Не обойдем вниманием и липиды (жиры). В нашем организме они служат запасным источником энергии. В качестве растворителей помогают протеканию биохимических реакций. Участвуют в строительстве организма – например, в формировании клеточных мембран.
И еще пару слов о таких любопытных органических соединениях, как гормоны. Они участвуют в биохимических реакциях и обмене веществ. Такие маленькие, гормоны делают мужчин мужчинами (тестостерон) и женщин женщинами (эстроген). Заставляют нас радоваться или печалиться (не последнюю роль в перепадах настроения играют гормоны щитовидной железы, а эндорфин дарит ощущение счастья). И даже определяют, «совы» мы или «жаворонки». Готовы вы учиться допоздна или предпочитаете встать пораньше и сделать домашнюю работу перед школой, решает не только ваш распорядок дня, но и некоторые гормоны надпочечников.
Заключение
Мир органических веществ по-настоящему удивительный. Достаточно углубиться в его изучение лишь немного, чтобы у вас захватило дух от ощущения родства со всем живым на Земле. Две ноги, четыре или корни вместо ног – всех нас объединяет волшебство химической лаборатории матушки-природы. Оно заставляет атомы углерода объединяться в цепочки, вступать в реакции и создавать тысячи таких разнообразных химических соединений.
Теперь у вас есть краткий путеводитель по органической химии. Конечно, здесь представлена далеко не вся возможная информация. Какие-то моменты вам, быть может, придется уточнить самостоятельно. Но вы всегда можете использовать намеченный нами маршрут для своих самостоятельных изысканий.
Вы также можете использовать приведенное в статье определение органического вещества, классификацию и общие формулы органических соединений и общие сведения о них, чтобы подготовиться к урокам химии в школе.
Расскажите нам в комментариях, какой раздел химии (органическая или неорганическая) нравится вам больше и почему. Не забудьте «расшарить» статью в социальных сетях, чтобы ваши одноклассники тоже смогли ею воспользоваться.
Пожалуйста, сообщите, если обнаружите в статье какую-то неточность или ошибку. Все мы люди и все мы иногда ошибаемся.
© blog.tutoronline.ru,
при полном или частичном копировании материала ссылка на первоисточник обязательна.
Источник
Какие вещества называют
органическими?
Органическими веществами
(соединениями) называются такие вещества
или соединения, в состав которых входит
углерод.
Ядро наиболее стабильного
изотопа углерода массой 12 (распространенность
98,9%) имеет 6 протонов и 6 нейтронов (12
нуклонов), расположенных тремя квартетами,
каждый содержит 2 протона и два нейтрона
аналогично ядру гелия.
В основном состоянии 6
электронов углерода образуют электронную
конфигурацию 1s22s22px12py12pz0.
Четыре электрона второго уровня являются
валентными, что соответствует положению
углерода в IV группе периодической
системы. Углерод имеет 2 электронных
уровня. На внешнем электронном уровне
4 электрона.
Электронная структура
невозбужденного атома углерода может
быть выражена формулой 1s22s22p2,
т. е. во втором (внешнем) электронном
слое у него два спареных (с противоположными
спинами) s-электрона и только два
неспареных р-электрона,
которые могут участвовать в образовании
ковалентных связей. Следовательно,
углерод должен был бы проявлять
валентность, равную двум; однако в
большинстве своих соединений он
четырехвалентен — образует четыре
ковалентные связи. Это объясняется тем,
что при затрате некоторой энергии
происходит «распаривание» 2p-электронов:
один из них переводится на свободную
орбиту подуровня 2р,
и атом переходит в возбужденное состояние
2s2p2
→ 2sp3
или графически
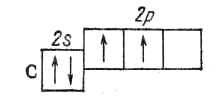 →
→ 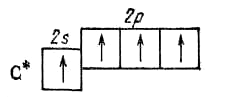
нормальное состояние возбужденное
состояние
Органические вещества.
Углеводы
( сахариды ). Молекулы
этих веществ построены всего из трёх
элементов –
углерода, кислорода и водорода. Углероды
являются основным источником энергии
для живых организмов. Кроме того, они
обеспечивают организмы соединениями,
которые используются в дальнейшем для
синтеза других соединений.
Наиболее известными и
распространёнными углеводами являются
растворённые в воде моно–
и дисахариды. Они кристаллизуются,
сладкие на вкус.
Моносахариды (
монозы ) –
соединения, которые не могут гидролизоваться.
Сахариды могут полимеризоваться, образуя
более высокомолекулярные соединения
–
ди–,
три–
, и полисахариды.
Олигосахариды.
Молекулы этих соединений построены из
2 –
4 молекул моносахаридов. Эти соединения
также могут кристаллизоваться, легко
растворимы в воде, сладкие на вкус и
имеют постоянную молекулярную массу.
Примером олигосахаридов могут быть
дисахариды сахароза, мальтоза, лактоза,
тетрасахарид стахиоза и др.
Полисахариды ( полиозы )
–
нерастворимые в воде соединения (
образуют коллоидный раствор ), не имеющие
сладкого вкуса, Как и предыдущая группа
углеводов способны гидролизоваться (
арабаны, ксиланы, крахмал, гликоген).
Основная функция этих соединений –
связывание, склеивание клеток
соединительной ткани, защита клеток от
неблагоприятных факторов.
Липиды
–
группа соединений, которые содержатся
во всех живых клетках, они нерастворимы
в воде. Структурными единицами молекул
липидов могут быть либо простые
углеводородные цепи, либо остатки
сложных циклических молекул.
В зависимости от химической
природы липиды разделяют на жиры и
липоиды.
Жиры ( триглицериды,
нейтральные жиры )
являются основной группой липидов. Они
представляют собой сложные эфиры
трёхатомного спирта глицерина и жирных
кислот или смесь свободных жирных кислот
и триглицеридов.
Встречаются в живых клетках
и свободные жирные кислоты : пальмитиновая,
стеариновая, рициновая.
Липоиды
–
жироподобные вещества. Имеют большое
значение, так как благодаря своему
строению образуют чётко ориентированные
молекулярные слои, а упорядочённое
расположение гидрофильных и гидрофобных
концов молекул имеет первоочередное
значение для формирования мембранных
структур с избирательной проницаемостью.
Ферменты. Это
биологические катализаторы белковой
природы, способные ускорять биохимические
реакции. Ферменты не разрушаются в
процессе биохимических превращений,
поэтому сравнительно небольшое их
количества катализируют реакции большого
количества вещества. Характерным
отличием ферментов от химических
катализаторов является их способность
ускорять реакции при обычных условиях.
По химической природе
ферменты делятся на две группы –
однокомпонентные ( состоящие только из
белка, их активность обусловлена активным
центром –
специфической группы аминокислот в
белковой молекуле ( пепсин, трипсин )) и
двухкомпонентные ( состоящие из белка
( апофермента –
носителя белка ) и белкового компонента
( коферментом ), причём химическая природа
коферментов бывает разной, так как они
могут состоять из органических ( многие
витамины, НАД, НАДФ ) или неорганических
( атомы металлов : железа, магния, цинка
)).
Функция ферментов заключается
в снижении энергии активации, т.е. в
снижении уровня энергии, необходимой
для придания реакционной способности
молекуле.
Современная классификация
ферментов основывается на типах
катализируемых ими химических реакций.
Ферменты гидролазы
ускоряют реакцию
расщепления сложных соединений на
мономеры ( амилаза ( гидролизует крахмал
), целлюлаза ( разлагает целлюлозу до
моносахаридов ), протеаза ( гидролизует
белки до аминокислот )).
Ферменты оксидоредуктазы
катализируют окислительно–восстановительные
реакции.
Трансферазы
переносят альдегидные, кетонные и
азотистые группы от одной молекулы к
другой.
Лиазы
отщепляют отдельные радикалы с
образованием двойных связей или
катализируют присоединение групп к
двойным связям.
Изомеразы
осуществляют изомеризацию.
Лигазы
катализируют реакции соединения двух
молекул, используя энергию АТФ или
другого триофасфата.
Пигменты
–
высокомолекулярные природные окрашенные
соединения. Из нескольких сотен соединений
этого типа важнейшими являются
металлопорфириновые и флавиновые
пигменты.
Металлопорфирин, в состав
которого входит атом магния, образует
основание молекулы зелёных растительных
пигментов –
хлорофиллов. Если на месте магния стоит
атом железа, то такой металлопорфирин
называют гемом.
В состав гемоглобина
эритроцитов крови человека, всех других
позвоночных и некоторых беспозвоночных
входит окисное железо, которое и придаёт
крови красный цвет. Гемеритрин
придаёт крови розовый цвет ( некоторые
многощетинковые черви ). Хлорокруорин
окрашивает кровь,
тканевую жидкость в зелёный цвет.
Наиболее распространенными
дыхательными пигментами крови являются
гемоглобин и гемоциан
( дыхательный пигмент
высших ракообразных, паукообразных,
некоторых моллюсков спрутов ).
К хромопротеидам относятся
также цитохромы,
каталаза, пероксидаза, миоглобин
( содержится в мышцах и создаёт запас
кислорода, что позволяет морским
млекопитающим длительное время пребывать
под водой ).
Энергию в клетках и организмах
переносят два флавиновых
пигмента : флавинмононуклеотид
( ФМН ) и флавинадениндинуклотид
( ФАД ). По химической природе они не
относятся к металлопорфиринам, однако
по своим функциям аналогичны им.
Металлопорфирины и флавины
играют роль коферментов, или простетических
групп ферментов, которые участвуют в
транспорте электронов и кислорода в
живых организмах.
В хлоропластах содержится
относительно большое количество жёлтых
пластидных пигментов –
каротиноидов.
Чаще всего встречаются каротин,
ксантофилл, ликопин, лютеин.
Витамины
имеют высокую физиологическую активность,
сложное и разнообразное химическое
строение. Они необходимы для нормального
роста и развития организма. Витамины
регулируют окисление углеводов,
органических кислот, аминокислот,
некоторые из которых входят в состав
НАД, НАДФ.
Биосинтез витаминов
свойственен преимущественно зелёным
растениям. В животных организмах
самостоятельно синтезируются только
витамины D
и E.
Витамины делятся на две группы :
водо–растворимые
( C,
B1,
B2,
фолиевая кислота, B5,
B12,
B6,
PP)
и жирорастворимые ( A,
D,
E,
K
).
Гормоны
–
специфические биологически активные
вещества белкового или стероидного
типа, которые образуются и выделяются
железами внутренней секреции животных
и участвуют в регуляции жизненных
функций их организмов. Известно до 30
гормонов и много гормоноподобных
веществ, в том числе гормон щитовидной
железы – тироксин, гормоны надпочечников
– адреналин, норадреналин, гидрокортизон,
гормоны гипофиза – вазопрессин, окситоцин,
гормоны половых желёз – фолликулин,
тестостерон.
Недостаточное
или чрезмерное образование гормонов
вызывает тяжёлые расстройства в
деятельности организма.
Органические
кислоты – к
этой группе относятся органические
вешества, способные образовывать при
диссоциации в водных растворах катионы
водорода. Содержатся в значительном
количестве в клетках животных и особенно
растительных организмов. Органические
кислоты являются продуктами превращения
углсврдов; при синтезе белков они
обрязуют углеродную основу аминокислот.
Самую
многочисленную группу органических
кислот составляют карбоновые
кислоты. В составе их молекул обязательно
содержится хотя бы одня карбоксильная
группа – СООН. По количеству карбоксильных
групп различают одноосновные (мураньиная,
уксусная, пропионовая, магляная, молочная,
гликолевая), двухосновные (щавелевая,
яблочная, янтарная, нинная) и многоосновные
(лимонная, аконитовая).
По
своим свойствам кислоты делятся на
летучие и нелетучие. К летучим относятся
уксусная, пропионовая, масляная и
некоторые другие кислоты. Они легко
испаряются, имеют резкий запах.
Все
другие органические кислоты – нелетучие.
Большую группу органических кислот
составляют карбоновые кетокислоты,
которые кроме группы – СООH содержат
карбонильную группу (кетогруппу).
К
некарбоновым
органическим кислотам относятся также
гетероциклические соединения с кислыми
свойствами. Органические кислоты играют
исключительно большую рольв
обмене веществ живых организмов. Они
обусловливают необходимое соотношение
катионов и анионов (ионное равновесие)
при поступлении питательных веществ в
корни растений, создают в клетках
буферные смеси с заданными значениями
рН, являются начальными, промежуточными
или конечными продуктами биохимических
превращений. В заметных количествах
накапливаются эти кислоты в свободном
состоянии или в виде солей в сочных
плодах (яблоках, лимонах, чернике), в
листьях и стеблях растений (щавеля,
ревеня).
Содержатся они также в крови и выделениях
(мочевая кислота) животных организмов.
Получают
органические кислоты из природных
веществ в результлте брожения сахаристых
веществ (молочнокислое, маслянокислое,
уксуснокислое), а также при окислении
альдегидов, спиртов, некоторых углеводов.
Широко используются в кулинарии, пищевой
промышленности, технике, научных
исследованниях.
Большое
значение в процессах жизнедеятельности
организмов имеют также соли органических
кислот, в частности соли калия, натрия,
кальция.
Продукты
выделенияделятся
на экскреты, секреты, рекреты и инкреты.
Экскреты
– продукты диссимиляции, неиспользованные,
ненужные или вредные вещества. Бывают
газообразные, жидкие и твёрдые. К этой
группе относятся углекислый газ, вода,
этилен, эфирные масла. К секретам
относягся продукты ассимиляции.
Вещества,
способные реутилизироваться называются
рекретами.
Инкреты
–
биологически активные соединения
внутреннего назначения. Это фитогормоны
и гормоны эндокринных желёз животных.
Летучие,
ароматические, пахучие вещества.
Значительные
количества таких веществ биогенного
происхождения выделяются в окружающую
среду как животными, так и растениями.
Большинство этих естественных метаболитов,
выделяемых наружу (экзометаболиты),
проявляют высокую биологическую
активность, поэтому они представляют
интерес для научных исследований и для
практики.
Экзометаболиты
разделяются на метаболиты, которые
влияют на рецепторы и проявляют
информационную, запаховую, сенсорную
функции. С их помощью морские млекопитающие
делают «пахучие метки» в толще воды,
рыбы и млекопитающие объединяются встада, хищники
отыскивают добычу. Очень высокая
чувствитсльность млекопитающих к запаху
самок:
метаболиты
с трофической функцией, которые включаются
н пищевые цепи: метаболиты лишайников;
метаболиты,
которые прямым иликосвенным
образом влияют на размножение, рост и
развитие организмов в биоценозах:
специальные выделения матки пчелиной
семьи;
метаболиты
токсического действия (биологическое
оружие живых организмов): токсические
выделения синезелёных водорослей,
простейших и других животных, летучие
соедииения зелёной массы высших растений.
Фитогормоны.
Это
регуляторы роста рястений гормонального
типа, соединения, способные влиять на
ростовые процессы растительных клеток,
органов и целых рястений. Фигогормоны
играют важиую роль в регенерации
утраченных органов. Существует несколько
групп фитогормонов.
Углерод
6
C
Углерод
Carbon
(He)2s22p2
Атомный номер
6
Атомная масса
12,011
Плотность, кг/м?
2260
Температура плавления, °С
3700 (возг.)
Температура кипения, °С
Теплоемкость, кДж/(кг·°С)
0,69
Электроотрицательность
2,5
Ковалентный радиус, A
0,77
1-й ионизац. потенциал, эв
11,26
Углерод (лат. Carboneum), С,
химический элемент IV группы периодической
системы Менделеева, атомный номер 6,
атомная масса 12,011. Известны два стабильных
изотопа: 12С (98,892%) и 13С (1,108%). Из радиоактивных
изотопов наиболее важен 14С с периодом
полураспада(Т? = 5,6·103 лет).
Соседние файлы в предмете [НЕСОРТИРОВАННОЕ]
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
Источник
