Какие свойства у металлической связи

Металлическая связь — химическая связь, обусловленная наличием относительно свободных электронов. Характерна как для чистых металлов, так и их сплавов и интерметаллических соединений.
Механизм металлической связи
Во всех узлах кристаллической решётки расположены положительные ионы металла. Между ними беспорядочно, подобно молекулам газа движутся валентные электроны, отцепившиеся от атомов при образовании ионов. Эти электроны играют роль цемента, удерживая вместе положительные ионы; в противном случае решётка распалась бы под действием сил отталкивания между ионами. Вместе с тем и электроны удерживаются ионами в пределах кристаллической решётки и не могут её покинуть. Силы связи не локализованы и не направлены.
Поэтому в большинстве случаев проявляются высокие координационные числа (например, 12 или 8). Когда два атома металла сближаются, орбитали их внешних оболочек перекрываются, образуя молекулярные орбитали. Если подходит третий атом, его орбиталь перекрывается с орбиталями первых двух атомов, что дает еще одну молекулярную орбиталь. Когда атомов много, возникает огромное число трехмерных молекулярных орбиталей, простирающихся во всех направлениях. Вследствие многократного перекрывания орбиталей валентные электроны каждого атома испытывают влияние многих атомов.
Характерные кристаллические решётки
Большинство металлов образует одну из следующих высокосимметричных решёток с плотной упаковкой атомов: кубическую объемно центрированную, кубическую гранецентрированную и гексагональную.
В кубической объемно центрированной решётке (ОЦК) атомы расположены в вершинах куба и один атом в центре объёма куба. Кубическую объемно центрированную решётку имеют металлы: Pb, K, Na, Li, β-Ti, β-Zr, Ta, W, V, α-Fe, Cr, Nb, Ba и др.
В кубической гранецентрированной решётке (ГЦК) атомы расположены в вершинах куба и в центре каждой грани. Решётку такого типа имеют металлы: α-Ca, Ce, α-Sr, Pb, Ni, Ag, Au, Pd, Pt,Rh, γ-Fe, Cu, α-Co и др.
В гексагональной решётке атомы расположены в вершинах и центре шестигранных оснований призмы, а три атома — в средней плоскости призмы. Такую упаковку атомов имеют металлы: Mg, α-Ti, Cd, Re, Os, Ru, Zn, β-Co, Be, β-Ca и др.
Другие свойства
Свободно движущиеся электроны обусловливают высокую электро- и теплопроводность. Вещества, обладающие металлической связью, часто сочетают прочность с пластичностью, так как при смещении атомов друг относительно друга не происходит разрыв связей. Также важным свойством является металлическая ароматичность.
Металлы хорошо проводят тепло и электричество, они достаточно прочны, их можно деформировать без разрушения. Некоторые металлы ковкие (их можно ковать), некоторые тягучие (из них можно вытягивать проволоку). Эти уникальные свойства объясняются особым типом химической связи, соединяющей атомы металлов между собой – металлической связью.
Металлы в твердом состоянии существуют в виде кристаллов из положительных ионов, как бы “плавающих” в море свободно движущихся между ними электронов.
Металлическая связь объясняет свойства металлов, в частности, их прочность. Под действием деформирующей силы решетка металла может изменять свою форму, не давая трещин, в отличие от ионных кристаллов.
Высокая теплопроводность металлов объясняется тем, что если нагреть кусок металла с одной стороны, то кинетическая энергия электронов увеличится. Это увеличение энергии распространится в “ электронном море” по всему образцу с большой скоростью.
Становится понятной и электрическая проводимость металлов. Если к концам металлического образца приложить разность потенциалов, то облако делокализованных электронов будет сдвигаться в направлении положительного потенциала: этот поток электронов, движущихся в одном направлении, и представляет собой всем знакомый электрический ток.
Источник
Металлическая химическая связь характерна для металлов и их сплавов в кристаллическом состоянии. Образуется за счет обобществления валентных электронов. Для этого типа строения вещества не характерно образование направленных структурированных связей.
Следует отличать различные типы связи элементов кристаллов – металлическую, ионную и водородную, свойственную кристаллам льда.
Механизм создания металлической связи предусматривает отрыв частично свободных электронов от атома с образованием катионов с положительным зарядом, формирующих “остов” кристаллической решетки и электронного облака. При этом металлический кристалл не приобретает положительного или отрицательного заряда.
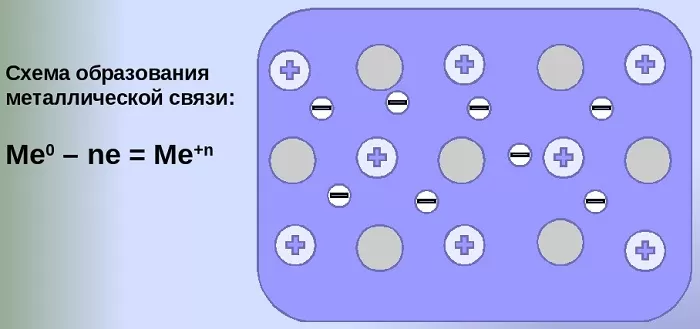
Общий случай формирования связывания металлических атомов в химии, соответствующий данному выше определению:
Me – ne⁻ ⇆ Me,
здесь n – число электронов, участвующих в образовании связи, как правило, от 1 до 3.
В левой части уравнения – атом металла, отдающий электроны, в правой – образовавшийся в результате ион.
Формула показывает, что в кристалле постоянно происходит присоединение и отдача электронов.
Схемы формирования связи на примере атомов различной валентности:
- K – e⁻ ⇆ K;
- Cu – 2e⁻ ⇆ Cu;
- Al – 3e⁻ ⇆ Al.
Отделяющиеся от атома электроны перемещаются на свободные валентные орбитали, которые обобществляются и позволяют всем электронам перемещаться в пределах кристалла. Отделение электронов выгодно атому с точки зрения энергетического баланса, так как позволяет сформировать электронно-стабильную оболочку.
Характерные кристаллические решетки
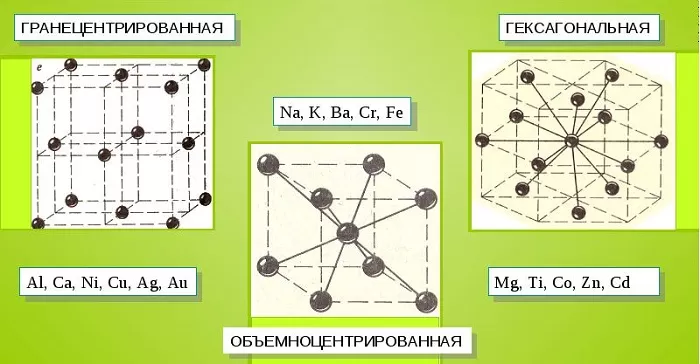
Металлические кристаллы подразделяются на 3 основных типа:
- Объемно-центрированную кубическую решетку, в которой, помимо размещения атомов в четырех вершинах куба, один из них размещается в центре объемной фигуры. Такой тип организации твердого вещества характерен для ряда металлов, включая K, Na и Li, вольфрам, хром, ниобий и др.
- Гранецентрированная кубическая решетка характеризуется расположением атомов в центре граней. Всего в ячейке задействовано 10 атомов, 4 в вершинах и 6 на гранях. Такая решетка встречается у меди, драгметаллов (серебра и золота) и металлов платиновой группы: Pd, Pt.
- Гексагональное строение решетки предполагает размещение атомов в углах и внутри 6-гранной призмы. Ячейка состоит из 15 атомов и свойственна магнию, кальцию, осмию, бериллию и ряду других металлических элементов.
Общими свойствами всех решеток являются высокая симметрия и плотная упаковка составляющих их атомов. Некоторые элементы периодической таблицы формируют уникальную структуру, например, элементарная ячейка In имеет тетрагональное строение.
Для сплавов, являющихся химическими соединениями, также характерно образование кристаллов перечисленных видов, при этом атомы каждого металла занимают определенное место в структуре.
Например, в сплаве никеля и алюминия атомы Al размещаются по углам, а атом Ni – в центре ОЦК ячейки. Свойства сплава и его структура влияют на класс прочности изделия, изготовленного из этого материала.
Физические характеристики металлических кристаллов обусловлены способностью обобществленных электронов свободно перемещаться внутри кристалла.

Характеристики, отличающие подобные вещества:
хорошая электропроводность, благодаря наличию условно свободного электронного облака;
высокая проводимость тепла;
низкая реакционная способность или инертность;
пластичность – большинство металлов можно гнуть и ковать.
Высокий уровень организации вещества обусловливает металлический блеск. Следует иметь в виду, что повышение прочности при пластической деформации и легировании приводит к образованию частично ковалентной связи.
При деформации могут возникать области повышенной прочности и низкими пластическими свойствами, похожие на вещества с ковалентной связью (например, алмаз).
Сходства и отличия металлической химической связи от ионной
Помимо рассматриваемой, металлы могут образовывать другие виды связи, включая простую ионную.
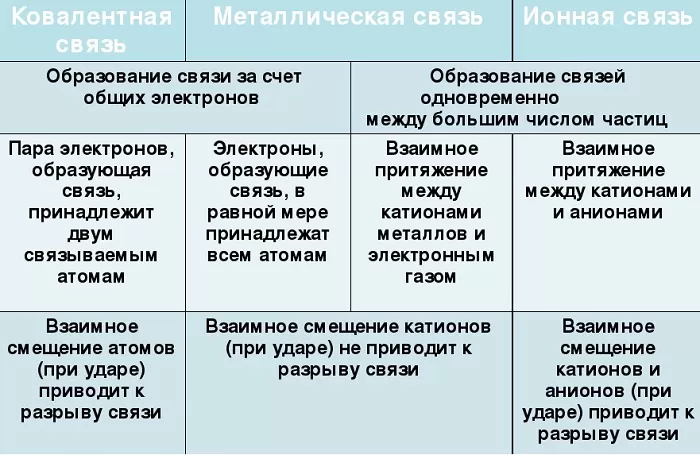
Их общие черты:
участие металлов, при этом металлическая связь формируется исключительно атомами металла, а ионная образуется между металлическим и неметаллическим элементами;
металл высвобождает электроны и становится катионом;
соединения могут существовать в кристаллической форме.
Кристаллы с ионным характером соединения отличают следующие параметры:
- В узлах размещаются как положительно, так и отрицательно заряженные ионы. Каркас металлической решетки формируют исключительно катионы.
- Узлы удерживаются за счет электростатического взаимодействия.
- При низких температурах кристаллические вещества, образованные за счет ионного взаимодействия, проявляют свойства диэлектриков (не проводят ток).
- Переход электронов с атома металла происходит на орбиты атома неметалла.
Характерный пример кристалла с ионной связью – поваренная соль, решетка которой сформирована из ионов Na⁺ и Cl⁻. Такие кристаллические вещества не обладают пластичностью и блеском.
Источник
Атомы в молекуле удерживаются посредством химической связи. Если молекула состоит из разных атомов (KF, Na2S, CO2, H2O), то речь идёт о ковалентной полярной (случай, когда в молекулу входят атомы неметаллов) или ионной связи (случай, когда молекула состоит из атома металла и атома неметалла). Если мы имеем дело с молекулой, состоящей из атомов неметалла одного вида (О2, N2, Br2), то в этом случае имеет место ковалентная неполярная связь. А как же связаны атомы в металлах, например, в натрии Na, кальции Са или алюминии Al?
Фото: livemaster.ru
Металлическая связь
Составляющие металл атомы удерживаются в единой структуре посредством химической связи. Не будь её, не существовало бы кристаллов. И эта связь носит название металлическая.
Металлическая связь – это связь, возникающая в результате обобществления электронов, находящихся на внешних электронных слоях атомов.
Чтобы понять это довольно сложно определение, посмотрим пример. Но для начала вспомним, как построены атомы металлов. В таблице Менделеева элементы-металлы располагаются в левом нижнем углу (мы говорим о главных подгруппах). У атомов металлов на внешнем электронном слое мало электронов. Кроме того, чем ниже мы опускаемся по группе в периодической таблице, тем больше становится радиус атома. Это означает, что на внешний слой всё дальше от ядра (напомню, что ядро атома имеет положительный заряд). Из-за этого электроны на внешнем уровне все меньше притягиваются к ядру. Малое число электронов и их удалённость от ядра позволяют им с лёгкостью отрываться от атома. При этом, как вы помните, атом превращается в ион, в данном случае в катион:
Me – 1e- → Me+1
Здесь Me – произвольный металл, с одним электроном на внешнем электронном уровне. В случае, если на внешнем электронном уровне несколько электронов, схема выглядит так:
Me – ne- → Me+n
Здесь n – число валентных электронов. Например, для кальция, стоящего во второй группе таблицы Менделеева и имеющего 2 электрона не внешнем уровне, схема такова:
Са – 2e- → Са+2
Для алюминия, стоящего в третьей и группе и имеющего 3 электрона на внешнем уровне, мы можем записать такую схему:
Al – 3e- → Al+3
Тут уместно задаться вопросом, а куда же деваются эти самые оторвавшиеся от атомов электроны? Они никуда не исчезают, а просто перемещаются от одного атома к другому. «Найдя» катион, электрон просто временно присоединяется к нему, чтобы тут же оторваться и отправиться в новое путешествие между атомами в поисках нового катиона. Фактически образуется эдакая динамическая система, в которой есть атомы и катионы металлов и курсирующие между ними электроны, которые то и дело присоединяются и отрываются, превращая катионы в атомы и атомы в катионы:
Me – ne- ⇄ Me+n
За счёт чего удерживается эта структура? За счёт электростатического взаимодействия, то есть притяжения отрицательно и положительно заряженных частиц.
Чтобы представить себе это более чётко, вообразите структуру из катионов, которая погружена в своеобразный «газ» из электронов. Это и есть металлическая связь. Подобным образом построены все металлы и их сплавы, когда они находятся в твёрдом или расплавленном состоянии.
Пишите, пожалуйста, в комментариях, что осталось непонятным, и я обязательно дам дополнительные пояснения. Жалуйтесь на сложности в изучении школьного курса и говорите, что вас испугало в учебнике химии. И тогда следующая статья будет рассказывать именно об этой проблеме.
Источник
Вещества с металлической связью: схема механизма образования, отличие от других видов связи, примеры

В одноатомном состоянии при обычных условиях находятся только благородные газы. Остальные же элементы не существуют в виде индивидуальном, так как имеют возможность взаимодействовать между собой или с другими атомами. При этом образуются более сложные частицы.
- Типы химического взаимодействия
- Металлическая химическая связь
- Отличия от других видов
- Схема связи и примеры
- Свойства металлов
Совокупность атомов может образовать следующие частицы:
- молекулы;
- молекулярные ионы;
- свободные радикалы.
Типы химического взаимодействия
Взаимодействие между атомами называют химической связью. Основой являются электростатические силы (силы взаимодействия электрических зарядов), которые действуют между атомами, носителями этих сил являются ядро атома и электроны.
: полярная и неполярная ковалентная связь – что это?
Электронам, находящимся на внешнем энергетическом уровне, отведена основная роль в образовании химических связей между атомами. Они наиболее удалены от ядра, а, следовательно, связаны с ним наименее прочно. Их называют валентными электронами.
Частицы взаимодействуют между собой различными способами, что приводит к образованию молекул (и веществ) разного строения. Различают следующие типы химической связи:
- ионная;
- ковалентная;
- водородная;
- вандерваальсова;
- металлическая.
Говоря о различных типах химического взаимодействия между атомами, стоит помнить о том, что все типы одинаково основаны на электростатическом взаимодействии частиц.
: алканы – химические свойства предельных углеводородов.
Металлическая химическая связь
Как видно из положения металлов в таблице химических элементов, они, в большинстве своём, обладают небольшим числом валентных электронов. Электроны связаны со своими ядрами достаточно слабо и легко отрываются от них. В результате этого образуются положительно заряженные ионы металла и свободные электроны.
Эти электроны, свободно перемещающиеся в кристаллической решётке, называют «электронным газом».
На рисунке схематично изображено строение вещества металла.
То есть в объёме металла атомы постоянно превращаются в ионы (их называют атом-ионами) и наоборот ионы постоянно принимают электроны из «электронного газа».
: как расставлять коэффициенты в химических уравнениях?
Механизм образования металлической связи можно записать в виде формулы:
атом M0 — ne ↔ ион Mn+
Таким образом, металлы представляют собой положительные ионы, которые расположены в кристаллической решётке в определённых положениях, и электроны, которые могут достаточно свободно перемещаться между атом-ионами.
Кристаллическая решётка представляет «скелет», остов вещества, а электроны перемещаются между её узлами. Формы кристаллических решёток металлов могут быть различными, например:
- объёмно-центрическая кубическая решётка характерна для щелочных металлов;
- гранецентрическую кубическую решётку имеют, например, цинк, алюминий, медь, другие переходные элементы;
- гексагональная форма типична для щёлочноземельных элементов (исключением является барий);
- тетрагональная структура — у индия;
- ромбоэдрическая — у ртути.
Пример кристаллической решётки металла показан на картинке ниже.
Отличия от других видов
Отличается металлическая связь от ковалентной по прочности. Энергия металлических связей меньше, чем ковалентных в 3−4 раза и меньше энергии ионной связи.
В случае с металлической связью, нельзя говорить и о направленности, ковалентная связь строго направлена в пространстве.
Такая характеристика, как насыщаемость также не характерна для взаимодействия между атомами металлов. В то время как ковалентные связи являются насыщаемыми, то есть количество атомов, с которыми может произойти взаимодействие, строго ограничено количеством валентных электронов.
Схема связи и примеры
Процесс, происходящий в металле можно записать с помощью формулы:
К — е К +
Al — 3e Al3+
Na — e Na+
Zn — 2e Zn2+
Fe — 3e Fe3+
Если описывать более подробно, металлическую связь, как образуется этот тип связи, необходимо рассматривать строение внешних энергетических уровней элемента.
В качестве примера можно рассмотреть натрий. Имеющийся на внешнем уровне единственный валентный 3s электрон может свободно перемещаться по свободным орбиталям третьего энергетического уровня. При сближении атомов натрия, происходит перекрывание орбиталей. Теперь уже все электроны могут перемещаться между атом-ионами в пределах всех пререкрывшихся орбиталей.
У цинка на 2 валентных электрона приходится целых 15 свободных орбиталей на четвёртом энергетическом уровне. При взаимодействии атомов эти свободные орбитали будут перекрываться, как бы обобществляя электроны, которые по ним перемещаются.
У атомов хрома валентных электронов 6 и все они будут участвовать в образовании электронного газа и связывать атом-ионы.
Свойства металлов
Особый вид взаимодействия, который характерен для атомов металлов, определяет ряд объединяющих их свойств и отличающих металлы от других веществ. Примерами таких свойств являются высокие температуры плавления, высокие температуры кипения, ковкость, способность отражать свет, высокая электропроводность и теплопроводность.
Высокие температуры плавления и кипения объясняются тем, что катионы металла прочно связаны электронным газом.
При этом прослеживается закономерность, что прочность связи увеличивается с увеличением количества валентных электронов.
Например, рубидий и калий являются легкоплавкими веществами (температуры плавления 39 и 63 градуса Цельсия, соответственно), по сравнению с, например, хромом (1615 градусов Цельсия).
Равномерностью распределения валентных электронов по кристаллу объясняется, например, такое свойство металлов, как пластичность — смещение ионов и атомов в любых направлениях без разрушения взаимодействия между ними.
Свободное перемещение электронов по атомным орбиталям объясняет и электропроводность металлов. Электронный газ при наложении разности потенциалов переходит из хаотического движения к движению направленному.
В промышленности часто используют не чистые металлы, а их смеси, называемые сплавами. В сплаве свойства одного компонента обычно удачно дополняют свойства другого.
Металлический тип взаимодействия характерен как для чистых металлов, так и для их смесей — сплавов, находящихся в твёрдом и жидком состояниях. Однако, если металл перевести в газообразное состояние, то связь между его атомами будет ковалентная. Металл в виде пара состоит и отдельных молекул (одно- или двухатомных).
Металлическая химическая связь. Полные уроки — Гипермаркет знаний

Гипермаркет знаний>>Химия>>Химия 8 класс. Полные уроки>>Химия: Металлическая химическая связь. Полные уроки
Тема. Металлическая химическая связь
Цель урока
- Дать представление о металлической химической связи.
- Научится записывать схемы образования металлической связи.
- Ознакомится с физическими свойствами металлов.
- Научится четко разделять виды химических связей.
Задачи урока
- Узнать, как взаимодействуют между собой атомы металлов
- Определить, каким образом влияет металлическая связь на свойства образованных ею веществ
Основные термины:
- Электроотрицательность — химическое свойство атома, которое является количественной характеристикой способности атома в молекуле притягивать к себе общие электронные пары.
- Химическая связь —явление взаимодействия атомов, из-за перекрытия электронных облаков взаимодействующих атомов.
- Металическая связь — это связь в металлах между атомами и ионами, образованная за счет обобществления электронов.
- Ковалентная связь — химическая связь, образуется с помощью перекрытия пары валентных электроннов. Обеспечивающие связь электроны называются общей электронной парой. Бывает 2-х видов: полярная и не полярная.
- Ионная связь — химическая связь,которая образуется между атомами неметалов, при которой общая электронная пара переходит к атому с большей электроотрицательностью. В итоге атомы притягиваются, как разноименно заряженные тела.
- Водородная связь — химическая связь между электроотрицательным атомом и атомом водорода H, связанным ковалентно с другим электроотрицательным атомом. В качестве электроотрицательных атомов могут выступать N, O или F. Водородные связи могут быть межмолекулярными или внутримолекулярными.
ХОД УРОКА
Металлическая химическая связь
Определите элементы ставшие не в ту «очередь».Почему?Ca Fe P K Al Mg Na
Какие элементы из таблицы Менделеева называются металлами?
Сегодня мы узнаем какие свойства есть у металлов, и как они зависят от связи которая образуется между йонами металов.Для начала вспомним месторасполажения металлов в периодической системе?Металлы как мы все знаем обычно существуют не в виде изолированных атомов, а в форме куска, слитка или металлического изделия. Выясним, что собирает атомы металла в целостном объеме.
Рис. 1.
Золото.На примере мы видим кусок золота. И кстати уникальным металлом является золото. С помощью ковки из чистого золота можно сделать фольгу толщиной 0,002 мм! такой нончайший лист фольги почти прозрачный и имеет зелёный оттенок просвете. В итоге из слитка золота размером со спичечный коробок можно получить тонкую фольгу, которая покроет площадь тенисного корта.
В химическом отношении все металы характеризуются легкостью отдачи валентных электронов, и как следствие образование положительно заряженных ионов и проявлять только положительную окисленность. Именно поэтому металы в свободном состоянии являются востановителями. Общей особенностью атомов металов являются большие размеры по отношению к неметалам.
Внешние эллектроны находятся на больших расстояниях от ядра и поэтому слабо с ним связаны, следовательно легко отрываются.Атомы большего колличества металлов на внешнем уровне имеют маленькое колличество электронов – 1,2,3. Эти электроны легко отрываются и атомы металлов становятся ионами. Ме0 – n ē ⇆ Men+ атомы метала – електроны внешн.
орбиты ⇆ ионы металаТаким образом оторвавшиеся электроны могут перемещатся от одного иона к другому тоесть становятся свободными, и как бы связывая их в единое целое.Поэтому получается, что все оторвавшиеся электроны евляются общими, так как нельзя понять какой эллектрон принадлежит какому из атомов металла.
Электроны могут обьединятся с катионами, тогда временно образуются атомы, от которых сопять потом отрываются электроны. Этот процесс происходит постоянно и без остановки. Получается, что в объеме металла атомы непрерывно превращаются в ионы и наоборот. При этом небольшое число общих электронов связывает большое число атомов и ионов металла.
Но важно, что число электронов в металле равно общему заряду положительных ионов, тоесть получается, что в целом металл остается электронейтральным. Такой процесс представляют как модель — ионы металла находятся в облаке из электронов. Такое электронное облако называют «электронным газом».
Вот например на данной картинке мы видим как электрончики двигаются среди неподвижныхйонов внутри кристалической решетки метала.
Рис. 2. Движение электроннов
Для того чтоб лучше понять, что такое Электронный газ и как он ведет себя в химических реакциях разных металлов посмотрим интересное видео. (золото в этом видео упоминается исключительно как цвет!)
Теперь мы можем записать определение: металлическая связь — это связь в металлах между атомами и ионами, образованная за счет обобществления электронов.
Давайте сравним все виды связей которые мы знаем И закрепим, чтобы лучше различать их, для этого посмотрим видео.
Металлическая связь бывает не только в чистых металах но также характерна для смесей разных металов, сплавов в разных агрегатных состояниях. Металлическая связь имеет важное значение и обуславливает основные свойства металлов- электропроводность – беспорядочное движение електронов в объеме металла. Но при небольшой разности потенциалов , чтобы электроны двигались упорядоченно. Металами с лучшей проводимостью являются Ag, Cu, Au, Al. — пластичность Связи между слоями металла не очень значительны, это позволяет перемещать слои под нагрузкой (деформировать металл не ломая его). Наилучше деформирующиеся металы (мягкие)Au, Ag, Cu. — металлический блеск
Электронный газ отражает почти все световые лучи. Вот почему чистые металлы так сильно блестят и чаще всего имеют сенрый или белый цвет. Металы являющиеся наилучшими отражателями Ag, Cu, Al, Pd, Hg
Упражнение 1
Выбрать формулы веществ которые имеют а) ковалентную полярную связь: Cl2, KCl, NH3, O2, MgO, CCl4, SO2; б) с ионную связь: HCl, KBr, P4, H2S, Na2O, CO2, CaS.
Упражнение 2
Вычеркните лишнее: а) CuCl2, Al, MgS б) N2, HCl, O2 в) Ca, CO2, Fe
г) MgCl2, NH3, H2
Интересно знать что…
Металлический натрий, металлический литий, и остальные щелочные металлы меняют цвет пламени. Металлический литий и его соли придают огню —красный цвет, металлический натрий и соли натрия — жёлтый, металлический калий и его соли — фиолетовый, а рубидия и цезия — тоже фиолетовый, но более светлый.
Рис. 4. Кусок металического лития
Рис. 5.
Окрашивание пламени металами
Литий (Li). Металлический литий, как и металлический натрий, относится к щелочным металлам. Оба растворяются в воде. Натрий, растворяясь в воде образует едкий натр –очень сильную кислоту. При растворении щелочных металов в воде выделяется много тепла и газа (водорода).
Такие металы желательно не трогать руками, так как можно обжечся.
Список литературы
1. Урок по теме «Металлическая химическая связь», учителя химии Тухта Валентины Анатольевны МОУ «Есеновичская СОШ»2. Ф. А. Деркач «Химия», — научно-методическое пособие. – Киев, 2008.3. Л. Б.
Цветкова «Неорганическая химия» – 2-е издание, исправленное и дополненное. – Львов, 2006.4. В. В. Малиновский, П. Г. Нагорный «Неорганическая химия» — Киев, 2009.
5. Глинка Н.Л. Общая химия. – 27 изд./ Под. ред. В.А. Рабиновича.
– Л.: Химия, 2008. – 704 с.ил.
Отредактировано и выслано Лисняк А.В.
Над уроком работали:
Тухта В.А.
Лисняк А.В.
Поставить вопрос о современном образовании, выразить идею или решить назревшую проблему Вы можете на Образовательном форуме, где на международном уровне собирается образовательный совет свежей мысли и действия.
Создав блог, Вы не только повысите свой статус, как компетентного преподавателя, а и сделаете весомый вклад в развитие школы будущего.
Гильдия Лидеров Образования открывает двери для специалистов высшего ранга и приглашает к сотрудничеству в направлении создания лучших в мире школ.
Предмети > Химия > Химия 8 класс
Источник
