Какие свойства растворов называются коллигативными приведите примеры
Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 7 июля 2017;
проверки требуют 4 правки.
Коллигативные свойства растворов — это свойства растворов, обусловленные только самопроизвольным движением молекул, то есть они определяются не химическим составом, а числом кинетических единиц — молекул в единице объёма или массы[1]. К таким коллигативным свойствам относятся:
- Понижение упругости растворителя над раствором,
- Повышение температуры кипения растворов (в сравнении с чистыми растворителями),
- Понижение температуры замерзания растворов (в сравнении с чистыми растворителями),
- Возникновение осмотического давления,
- Диффузия.
Законы Рауля[править | править код]
Первый закон Рауля[править | править код]
Пар, находящийся в равновесии с жидкостью, называют насыщенным. Давление такого пара над чистым растворителем (p0) называют давлением или упругостью насыщенного пара чистого растворителя.
В 1886 (1887) году Ф. М. Рауль сформулировал закон:
Давление насыщенного пара раствора, содержащего нелетучее растворенное вещество, прямо пропорционально мольной доле растворителя в данном растворе:
p = p0 · χр-ль, где
p — давление пара над раствором, Па;
p0 — давление пара над чистым растворителем;
χр-ль —— мольная доля растворителя.
Для растворов электролитов используют несколько другую форму уравнения, позволяющую добавить в неё изотонический коэффициент:
Δp = i · p0 · χв-ва, где
Δp — собственно изменение давления по сравнению с чистым растворителем;
χв-ва — мольная доля вещества в растворе.
Второй закон Рауля[править | править код]
Также Рауль экспериментально доказал, что
повышение температуры кипения раствора по сравнению с температурой кипения растворителя равно и понижение температуры замерзания раствора по сравнению с аналогичным характеризующей величиной для растворителя прямо пропорциональна моляльности раствора, то есть,
ΔTкип/зам= Kэб/кр · mв-ва, где
Kэб/кр — соответственно эбуллиоскопическая (от лат. ebullire — «кипеть» и др.-греч. σκοπέω — «наблюдаю») и криоскопическая (относится к замерзанию) константы, характерные для данного растворителя;
mв-ва — моляльность вещества в растворе.
Осмотическое давление[править | править код]
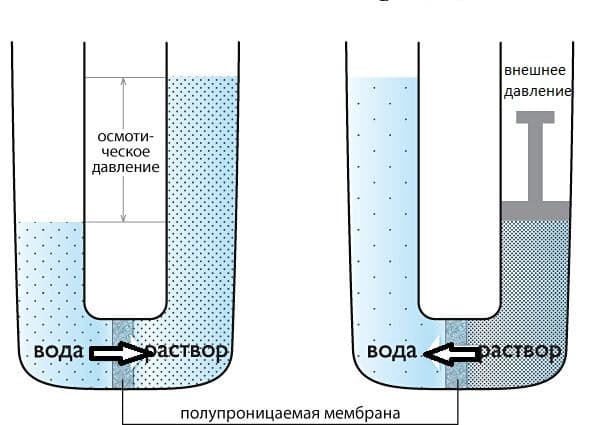
Рассмотрим ситуацию, при которой частично проницаемая мембрана (то есть, такая, через которую могут проходить лишь мелкие объекты, например, молекулы растворителя, но не крупные — например, молекулы растворённого вещества) разделяет чистый растворитель и раствор (или два раствора с разными концентрациями). Тогда молекулы растворителя находятся практически в равных физических условиях по обе стороны мембраны, однако в более насыщенном растворе некоего вещества их концентрация, разумеется, меньше, чем в более разбавленном (в котором меньше места в растворе занимают молекулы растворённого вещества). Следовательно, со стороны менее насыщенного раствора через мембрану диффундирует большее число молекул, чем с противоположной стороны. А это значит, что растворитель попросту переходит из менее насыщенного раствора в более насыщенный, разбавляя его (выравнивая концентрации обоих растворов) и создавая давление на мембрану. Процесс этот (он называется осмосом) можно прекратить, оказав определённое давление на более насыщенный раствор (например, при помощи поршня) —— это давление и называется осмотическим давлением.
Растворы с одинаковым осмотическим давлением называются изотоническими.
Определить осмотическое давление раствора можно по формуле, полученной в 1886 году Я. Х. Вант-Гоффом:
π = CMв-ва · R · T, где
CMв-ва — молярная концентрация раствора, выраженная в , а не в , как обычно;
R — универсальная газовая постоянная;
T — термодинамическая температура системы.
См. также[править | править код]
- Осмос
Примечания[править | править код]
- ↑ Д.А.Фридрихсберг. Курс коллоидной химии. — Ленинград “Химия”, 1984. — С. 368.
Литература[править | править код]
- Ершов Ю.А. Общая химия.Биофизическая химия.Химия биогенных элементов. — Издание восьмое,стериотипное. — Москва: Высшая школа, 2010. — 559 с.
Источник
После изучения этой темы вы должны:
– иметь представления о следующих понятиях и явлениях:
– осмос, осмотическое давление (закон Вант-Гоффа), его роль.
– закон Рауля о давлении паров растворителя над раствором и изменении температур кипения и замерзания растворов (следствия закона Рауля).
Коллигативные свойства – это свойства, которые не зависят от природы частиц растворенного вещества, а зависят только от концентрации частиц в растворе.
Коллигативными свойствами разбавленных растворов являются:
– скорость диффузии
– осмотическое давление (Закон Вант-Гоффа)
– давление насыщенного пара растворителя над раствором (Закон Рауля)
– температура кипения раствора (1следствие из закона Рауля)
– температура кристаллизации раствора (2 следствие из закона Рауля)
Свойства неэлектролитов
Осмосом называется самопроизвольное перемещение молекул растворителя через полупроницаемую мембрану из раствора меньшей концентрации в раствор большей концентрации. В результате протекания осмоса возникает осмотическое давление раствора. Гипертоническим раствором называют тот раствор, у которого осмотическое давление больше. Гипотоническим раствором – раствор с меньшим осмотическим давлением. Изотоничные растворы – это растворы с одинаковой величиной осмотического давления.
Растительная клетка (С >) (внутриклеточный раствор)
Внешняя среда (С <) (межклеточный раствор)
Н2О Н2О
Вант-Гофф, изучая зависимость осмотического давления от внешних факторов установил, что оно не зависит от природы растворенного вещества, а зависит только от числа частиц в растворе и от температуры:
Росм = СмRT, где Росм [кПа], T [K] – абсолютная температура, R = 8,32 кДж/моль – универсальная газовая постоянная, См – молярная концентрация раствора [моль/л].
Осмотическое давление раствора, содержащего несколько веществ, равно сумме осмотических давлений, вызываемых каждым из них.
Давление насыщенного пара растворителя над раствором (Закон Рауля):
Относительное понижение давления насыщенного пара над раствором прямо пропорционально мольной доле растворенного вещества: где – давление насыщенного пара над чистым растворителем; РА-давление насыщенного пара растворителя над раствором; NB – мольная доля растворенного вещества: , где na, nb – число молей растворителя (а) и растворенного вещества (b).
Набольшее практическое значение получили I, II следствие закона Рауля.
I следствие закона Рауля: Повышение температуры кипения раствора прямо пропорционально молярной концентрации растворенного вещества: Dtкип = Kэб.Сm , где Dtкип = t кип р-ра – t кип н2o, 0С ; Kэб – эбулиоскопическая константа растворителя (Kэб н2о ); Сm- моляльная концентрация растворенного вещества, моль/1000г растворителя.
II следствие закона Рауля: Понижение температуры замерзания раствора прямо пропорционально молярной концентрации растворенного вещества: Dtзам = Kкр.Сm , где Dt = t зам.н2о – t зам р-ра, 0С; Kкр – криоскопическая константа растворителя (Ккр н2о =1,86); Сm- моляльная концентрация растворенного вещества, моль/1000г растворителя.
| Росм = См R T Dtкип = Кэб Cm Dtзам = Ккр Cm | ß | Коллигативные свойства для молекулярных растворов |
Примечание: см. приложение 7 – «Криоскопические константы некоторых растворителей», приложение 8 – «Эбулиоскопические константы некоторых растворителей».
Эти уравнения справедливы только для растворов, в которых отсутствует взаимодействие частиц, т.е. для идеальных растворов. В реальных растворах имеют место межмолекулярные взаимодействия между молекулами вещества и растворителя, которые могут приводить либо к процессам диссоциации, либо к процессам ассоциации молекул. Диссоциация молекул вещества в водном растворе характерна для сильных электролитов. В результате диссоциации число частиц увеличивается.
Доля (i) образовавшихся частиц определяется как отношение общего числа частиц к первоначальному числу молекул. Она зависит от степени диссоциации электролита и от числа частиц, на которые распадается молекула:
i = (n -1)a + 1, i – получил название изотонический коэффициент, n – число частиц (ионов), на которые распадается молекула, a – степень диссоциации (в долях).
| Росм = iСМ R Т Dt кип = i Кэб Сm Dtзам = i Ккр Сm | ß | Коллигативные свойства для растворов электролитов |
Примеры расчетов температур кипения, замерзания, осмотического давления растворов различных концентраций.
Пример 1. Вычислить температуру замерзания, кипения раствора этилового спирта с процентной концентрацией (w), равной 40 %.
Решение: Вычислим температуру замерзания раствора исходя из II следствия закона Рауля: Dtзам = Kкр.Сm, однако для решения необходимо перейти от одного вида концентрации к другому:
w [m в-ва, г 100г р-ра] ® Сm[ n молей 1000 г р-ля ]
1. Перейдем от массы вещ-ва (m) к молям (n) через пропорцию:
1 моль С2Н5ОН содержит ——- 46 г
х моль //——//——-//——-//——40 г
или по формуле х(n) = = моль/100р-ра,
где m(с2н5он) = 40г, M(с2н5он) = 46г/моль
2. Перейдем от массы раствора к массе растворителя:
m р-ля = m р-ра – m в-ва = 100 – 40 = 60г р-ля
2. Через пропорцию выразим Сm :
0,87 молей С2Н5ОН содержит в 60 г растворителя
х (Сm) -//—–//—–//—–//——/- 1000 г
х (Сm) = = 14,5 молей/1000г р-ля
4. По формуле Dtзам = Kкр.Сm найдем Dt: Dt = 1,86.14,5 = 26,97 0C
5. Dt = tзам н2о – tзамр-ра Þ tзам р-ра = tзам н2о – Dt = 0 – 26,97 = -26,97 0C – температура замерзания 40 % раствора этилового спирта.
Вычислим температуру кипения раствора исходя из I следствия закона Рауля: Dtкип = Kэб. Сm, Сm = 14,5 моль/1000р-ля (см. выше)
Из формулы найдем Dt: Dt = 0,516 . 14,5 = 7,48 0C
Dt = tкипр-ра – tкип н2о Þ tкип р-ра = tкип н2о + Dtкип = 100 + 7,48 = 107,48 0C- температура кипения 40% раствора этилового спирта.
Пример 2. Вычислить концентрацию физиологического раствора (NaCl) изотоничного с осмотическим давлением крови равное » 800 Кпа. Степень диссоциации NaCl принять за 90%.
Решение: Для растворов электролитов Росм(NaCl ) = i·См·R·T Þ
См = (1)
Условие изотоничности означает, что Росм(NaCl ) = Росм крови = 800 кПа,
i = (n-1)·a + 1= (2 – 1) ·0,9 = 1,9
NaCl Û Na++Cl-, где n = 2, a = 0,9
Подставим найденные значения в формулу (1) См = 0,17 моль/л – концентрация хлорида натрия, которая создает осмотическое давление 800 кПа.
Источник
Любому раствору характерны те или иные физические свойства, к которым относятся и коллигативные свойства растворов. Это такие свойства, на которые не оказывает влияние природа растворенного вещества, а зависят они исключительно от количества частиц этого растворенного вещества.
К их числу относятся:
- Понижение давление паров
- Повышение температуры кипения
- Понижение температуры затвердевания (кристаллизации)
- Осмотическое давление раствора.
Рассмотрим подробнее каждое из перечисленных свойств.
Понижение давление паров
Давление насыщенного пара (т.е. пара, который пребывает в состоянии равновесия с жидкостью) над чистым растворителем называется давлением или упругостью насыщенного пара чистого растворителя.
Если в некотором растворителе растворить нелетучее вещество, то равновесное давление паров растворителя при этом понижается, т.к. присутствие какого – либо вещества, растворенного в этом растворителе, затрудняет переход частиц растворителя в паровую фазу. Экспериментально доказано, что такое понижение давления паров напрямую зависит от количества растворенного вещества. В 1887 г. Ф.М. Рауль описал количественные закономерности коллигативных свойств растворов.
Первый закон Рауля
Первый закон Рауля заключается в следующем:
Давление пара раствора, содержащего нелетучее растворенное вещество, прямо пропорционально мольной доле растворителя в данном растворе:
p = p0 · χр-ль
p = p0 · nр-ля/(nв-ва + nр-ля), где
p — давление пара над раствором, Па;
p0 — давление пара над чистым растворителем, Па;
χр-ль — мольная доля растворителя.
nв-ва и nр-ля – соответственно количество растворенного вещества и растворителя, моль.
Иногда Первому закону Рауля дают другую формулировку: относительное понижение давления насыщенного пара растворителя над раствором равно мольной доле растворенного вещества:
(p – p)/p = χв-ва
(p – p)/p = nв-ва/(nв-ва + nр-ля)
При этом принимаем, что χв-ва + χр-ль= 1
Для растворов электролитов данное уравнение приобретает несколько иной вид, в его состав входит изотонический коэффициент i:
p – p = Δр
Δp = i · p0 · χв-ва, где
Δp — изменение давления паров раствора по сравнению с чистым растворителем;
χв-ва — мольная доля вещества в растворе
i – изотонический коэффициент.
Изотонический коэффициент (или фактор Вант-Гоффа) — это параметр, не имеющий размерности, который характеризует поведение какого – либо вещества в растворе. То есть, изотонический коэффициент показывает, разницу содержания частиц в растворе электролита по сравнению с раствором неэлектролита такой же концентрации. Он тесно связан связан с процессом диссоциации, точнее, со степенью диссоциации и выражается следующим выражением:
i = 1+α(n—1), где
n – количество ионов, на которые диссоциирует вещество.
α – степень диссоциации.
Повышение температуры кипения или понижение температуры затвердевания (кристаллизации)
Равновесное давление паров жидкости имеет тенденцию к увеличению с ростом температуры, жидкость начинает кипеть, при уравнивании давления ее паров и внешнего давления. При наличии нелетучего вещества, давление паров раствора снижается, и раствор будет закипать при более высокой температуре, по сравнению с температурой кипения чистого растворителя. Температура замерзания жидкости также определяется той температурой, при которой давления паров жидкой и твердой фаз уравниваются.
Ф.М. Рауль доказал, что повышение температуры кипения, так же как и понижение температуры замерзания разбавленных растворов нелетучих веществ, прямо пропорционально моляльной концентрации раствора и не зависит от природы растворённого вещества. Это правило известно как II закон Рауля:
ΔTкип = E· mв-ва,
ΔTкрист = K·mв-ва, где
E—эбулиоскопическая константа,
K — криоскопическая константа,
mв-ва — моляльность вещества в растворе.
Растворы электролитов не подчиняются Законам Рауля. Но для учёта всех несоответствий Вант-Гофф предложил ввести в приведённые уравнения поправку в виде изотонического коэффициента i, учитывающего процесс распада на ионы молекул растворённого вещества:
ΔTкип = i·E·mв-ва
ΔTкрист = i·К·mв-ва
Осмотическое давление раствора
Некоторые материалы имеют способность к полупроницаемости, т.е. им свойственно пропускать частицы определенного вида и не пропускать частицы другого вида. Так, перемещение молекул растворителя (но не растворенного, в нем вещества), через полупроницаемую мембрану в раствор с большей концентрацией из более разбавленного представляет собой такое явление как осмос.
 ОСМОС
ОСМОС
Представим два таких раствора, которые разделены полупроницаемой мембраной, как показано на рисунке выше. Растворы стремятся к выравниванию концентраций, поэтому вода будет проникать в раствор, тем самым уменьшая его концентрацию. Для того, чтобы осмос приостановить, необходимо приложить внешнее давление к раствору. Такое давление, которое требуется приложить, называется осмотическим давлением. Осмотическое давление и концентрацию раствора позволяет связать уравнение Вант — Гоффа, которое напоминает уравнение идеального газа Клапейрона – Менделеева:
π = C·R·T,
где C — молярная концентрация раствора, моль/м3,
R — универсальная газовая постоянная (8,314 Дж/моль·К);
T — абсолютная температура раствора.
Преобразуем уравнение следующим образом:
C = n/V = m/(M·V)
π = т·R·T / M·V или
π·V = m·R·T /M
Для растворов электролитов осмотическое давление определяется уравнением, в которое входит изотонический коэффициент:
π` = i·C·R·T ,
где i — изотонический коэффициент раствора.
Для растворов электролитов i > 1, а для растворов неэлектролитов i = 1.
Если полупроницаемой перегородкой разделены два раствора, имеющие одинаковое осмотическое давление, то перемещение растворителя через перегородку отсутствует. Такие растворы называются изотоническими. Раствор, с меньшим осмотическим давлением, по сравнению с более концентрированным раствором, называют гипотоническим, а раствор с большей концентрацией – гипертоническим.
Источник
РАСТВОРЫ И ИХ КОЛЛИГАТИВНЫЕ СВОЙСТВА
Растворы представляют для биологии, физиологии и медицины особый интерес, так как все важнейшие биологические системы (цитоплазма, кровь, лимфа, слюна, моча, пот и др.) являются водными растворами солей, белков, углеводов, липидов. Усвоение пищи, транспорт метаболитов, большинство биохимических реакций в живых организмах протекают в растворах.
Понятие “растворы” включает истинные растворы и коллоидные растворы. Различие между ними заключается прежде всего в размерах частиц и однородности систем.
Истинные растворы – это однородные гомогенные системы с размером частиц на уровне 10–10 – 10–9 м.
Коллоидные растворы – это неоднородные гетерогенные системы с размером частиц 10–9 – 10–6 м. Рассмотрим сначала истинные растворы.
Истинным раствором называется термодинамически устойчивая гомогенная система переменного состава, состоящая из двух и более компонентов, между которыми существуют достаточно сильные взаимодействия.
Компонент, агрегатное состояние которого не изменяется при образовании раствора, принято называть растворителем, а другой компонент – растворенным веществом. При одинаковом агрегатном состоянии компонентов растворителем считают обычно то вещество, которое преобладает в растворе. С позиции живых систем наибольший интерес представляют растворы, в которых растворителем является вода.
ВОДА КАК РАСТВОРИТЕЛЬ И ЕЁ
КОЛЛИГАТИВНЫЕ СВОЙСТВА РАСТВОРОВ
Разбавленные растворы характеризуются отсутствием взаимодействия между частицами растворённого вещества. Поэтому свойства разбавленных растворов не зависят от природы растворённого вещества, а зависят только от числа частиц в единице объема раствора, то есть от их концентрации.
Коллигативными свойствами называются свойства растворов, не зависящих от природы частиц растворённого вещества, а зависящие только от концентрации частиц в растворе.
Коллигативными свойства разбавленных растворов являются:
– скорость диффузии;
– осмотическое давление;
– давление насыщенного пара растворителя над раствором;
– температура кристаллизации раствора;
– температура кипения раствора.
ДИФФУЗИЯ
Очевидно, что если на концентрированный водный раствор какого-нибудь вещества осторожно налить воду так, чтобы не произошло перемешивания, то через некоторое время обязательно произойдёт выравнивание концентрации вещества по всему объему системы вследствие диффузии.
Диффузией в растворе называется самопроизвольный направленный процесс переноса частиц растворенного вещества и растворителя, который осуществляется при наличии градиента концентрации растворённого вещества и приводит к выравниванию концентрации этого вещества по всему объёму раствора.
Причиной диффузии, с позиции термодинамики, является стремление системы к максимуму энтропии. Несмотря на хаотический характер теплового движения частиц в системе, диффузия частиц как результат этого движения всегда направлена от большей концентрации к меньшей. Направленный характер диффузия имеет только до тех пор, пока есть различия в концентрации частиц в отдельных частях системы. После выравнивания концентрации частиц происходит выравнивание и скоростей их диффузии в разных направлениях.
Количество вещества, переносимого за счёт диффузии через единичную площадь поверхности в единицу времени, называется скоростью диффузии. Скорость диффузии прямо пропорциональна температуре и разности концентраций по обе стороны поверхности, через которую осуществляется диффузия. В то же время скорость диффузии обратно пропорциональна вязкости среды и размеру частиц.
Таблица 2.
Осмотическое давление p 1 % водных растворов некоторых веществ
| Природа и состояние раствора | Растворённое вещество | Молекулярная масса | π, кПа | |
| Р—р электролита (диссоциация) | i>1 | Al2(SO4)3 | ||
| Р—р неэлектролита | i=1 | Сахар | 79,5 | |
| Каллоидный р—р (ассоциация) | i<1 | As2S3 | 34*10-4 |
| Раствор электролита, (диссоциация)i > 1Al2(SO4)3342390 | |||
| Раствор неэлектролита,i=1Сахар34279,5 | |||
| Коллоидный раствор, (ассоциация)i < 1As2S32460,0 | |||
При осмосе молекулы растворителя преимущественно движутся через мембрану в том направлении, где концентрация частиц растворённого вещества больше, а концентрация растворителя меньше. Другими словами, в результате осмоса происходит всасывание растворителя в ту часть системы, где концентрация частиц вещества больше. Если осмотическое давление у растворов одинаковое, то они называются изотоническими и между ними происходит подлинно равновесный обмен растворителем. В случае контакта двух растворов с разным осмотическим давлением гипертоническим раствором называется тот, у которого осмотическое давление больше, а гипотоническим — раствор с меньшим осмотическим давлением. Гипертонический раствор всасывает растворитель из гипотонического раствора, стремясь выровнять концентрации вещества путём перераспределения растворителя между контактирующими растворами.
Осмотическая ячейка – это система, отделенная от окружающей среды мембраной с избирательной проницаемостью. Все клетки живых существ являются осмотическими ячейками, которые способны всасывать растворитель из окружающей среды или, наоборот, его отдавать, в зависимости от концентраций растворов, разделенных мембраной.
Эндоосмос – движение растворителя в осмотическую ячейку из окружающей среды..
Условие эндоосмоса: стр < свн (πнар < πвн)
где сар и свн – концентрации вещества в наружном растворе и во внутреннем растворе ячейки; pнар и pвн – осмотические давления соответствующих растворов
В результате эндоосмоса вода диффундирует в клетку, происходит набухание клетки с появлением напряжённого состояния клетки, называемого тургор. В растительном мире тургор помогает растению сохранять вертикальное положение и определённую форму.
Если разница в концентрациях наружного и внутреннего раствора достаточно велика, а прочность оболочки клетки небольшая, то эндоосмос приводит к разрушению клеточной мембраны илизисуклетки. Именно эндоосмос является причиной гемолизаэритроцитов крови с выделением гемоглобина в плазму (см. рис. 3). Эндоосмос происходит, если клетка оказывается в гипотоническом растворе.
Экзоосмос – движение растворителя из осмотической ячейки в окружающую среду.
Условие экзоосмоса: снар > свн (pнар > pвн).
В результате экзоосмоса вода диффундирует из клетки в плазму и происходит сжатие и сморщивание оболочки клетки, называемое плазмолизом. Экзоосмос имеет место, если клетка оказывается в гипертонической среде. Явление экзоосмоса наблюдается, например, при посыпании ягод или фруктов сахаром, а овощей, мяса или рыбы = солью. При этом происходит консервирование продуктов питания благодаря уничтожению микроорганизмов вследствие их плазмолиза.
При приготовлении физиологических растворов необходимо учитывать их осмотические свойства, поэтому их концентрацию выражают через осмолярную концентрацию (осмолярность) (см. Приложение 1).
Осмолярная концентрация – суммарное молярное количество всех кинетически активных, то есть способных к самостоятельному движению, частиц, содержащихся в 1 литре раствора, независимо от их формы, размера и природы.
Осмолярная концентрация раствора связана с его молярной концентрацией через изотонический коэффициент сосм= ic(X).
4.3 Роль осмоса в биологии и медицине.
Осмос является одной из причин, обуславливающих поступление воды и растворенных в ней веществ из почвы по стеблю или стволу растения к листьям, так как pпочвы < pкорней < pлистьев. Осмотическое давление растительных клеток колеблется от 5 до 20 атм, а у растений пустынь достигает даже 70 атм.
Особенностью высших животных и человека является постоянство осмотического давления во многих физиологических системах, и прежде всего в системе кровообращения. Постоянство осмотического давления называется изоосмией. Осмотическое давление человека довольно постоянно и составляет 740 — 780 кПа (7,4 — 7,8 ат) при 37 °С. Оно обусловлено главным образом присутствием в крови катионов и анионов неорганических солей и в меньшей степени — наличием коллоидных частиц и белков. Присутствие в плазме крови форменных элементов (эритроцитов, лейкоцитов, тромбоцитов и кровяных пластинок) почти не влияет на осмотическое давление. Постоянство осмотического давления в крови регулируется выделением паров воды при дыхании, работой почек, выделением пота и т. д.
Осмотическое давление крови, создаваемое за счёт белков плазмы крови, называемое онкотическим давлением, хотя и составляет величину порядка 2,5-4,0 кПа, но играет исключительно важную роль в обмене водой между кровью и тканями, в распределении её между сосудистым руслом и внесосудистым пространством.
Рис. 2.8. Роль онкотического давления крови в капиллярном обмене воды.
Онкотическое давление — это осмотичекое давление, создаваемое за счет наличия белков в биожидкостях организма.
Онкотическое давление крови составляет 0,5 % суммарного осмотического давления плазмы крови, но его величина соизмерима с гидростатическим давлением в кровеносной системе (рис. 2).
Гидростатическое давление крови падает от артериальной части кровеносной системы к венозной. Если в артериальной части капилляров гидростатическое давление больше онкотического давления, то в венозной — меньше. Это обеспечивает перемещение воды из артериальных капилляров в межклеточную жидкость тканей, а венозные капилляры, наоборот, втягивают межклеточную жидкость. Причём интенсивность такого переноса воды прямо пропорциональна разности между ргидри pонк.
При понижении онкотического давления крови, которое наблюдается при гипопротеинемии (понижение содержания белка в плазме), вызванной голоданием, нарушением пищеварения или выделением белка с мочой при болезни почек, указанное соотношение давлений ргидри πонк нарушается. Это приводит к перераспределению жидкости в сторону тканей, и в результате возникают онкотические отёки (“голодные” или “почечные”).
Осмотическому давлению крови человека соответствует осмолярная концентрация частиц от 290 до 300 мОсм/л. В медицинской и фармацевтической практике изотоническими (физиологическими) растворами называют растворы, характеризующиеся таким же осмотическим давлением, как и плазма крови (рис. 3, а). Такими растворами являются 0,9% раствор NaCl (0,15 моль/л), в котором i = 2, и 5 % раствор глюкозы (0,3 моль/л). Во всех случаях, когда в кровяное русло, мышечную ткань, спинномозговой канал и т. д. с терапевтическими целями вводят растворы, необходимо помнить о том, чтобы эта процедура не привела к “осмотическому конфликту” из-за различия осмотических давлений вводимого раствора и данной системы организма. Если, например, внутривенно ввести раствор, гипертонический по отношению к крови, то вследствие экзоосмоса эритроциты будут обезвоживаться и сморщиваться — плазмолиз (рис. 3, б). Если же вводимый раствор гипотоничен по отношению к крови, то наблюдается “осмотический шок” и вследствие эндоосмоса может произойти разрыв эритроцитарных оболочек — гемолиз (рис. 2.9, в). Начальная стадия гемолиза происходит при местном снижении осмотического давления до 360 — 400 кПа (3,5-3,9 атм), а полный гемолиз — при 260 — 300 кПа (2,5 — 3,0 атм).
Изменение осмотического равновесия в биосистемах организма может быть вызвано нарушением обмена веществ, секреторными процессами и поступлением пищи. Кроме того, всякое физическое напряжение, усиливающее обмен веществ, может способствовать повышению осмотического давления крови. Несмотря на эти нарушения, осмотическое давление крови поддерживается постоянным, хотя химический состав крови может значительно изменяться. При возникновении осмотической гипертонии крови соединительная ткань, находящаяся в месте нарушения, отдаёт в кровь воду и забирает из неё соли почти сразу и до тех пор, пока осмотическое давление крови или тканевой жидкости не возвратится к нормальному значению. После этой быстрой реакции включаются почки, которые отвечают на увеличение количества каких-либо солей повышенным их выделением, пока не будет восстановлен нормальный состав соединительной ткани и крови. Осмотическое давление мочи, сохраняя норму, может изменяться в пределах от 7,0 до 25 атм (690 — 2400 кПа). Подобная регуляция имеет определенные границы, и поэтому для её усиления может потребоваться поступление воды или солей извне. Здесь вступает в действие вегетативная нервная система. Чувство жажды после физической работы (повышенный обмен веществ) или при почечной недостаточности (накопление веществ в крови из-за недостаточного их выделения) — это проявление осмотической гипертонии. Обратное явление наблюдается в случае солевого голода, вызывающего осмотическую гипотонию.
Воспаление возникает в результате резкого местного усиления обмена веществ. Причиной воспаления могут быть различные воздействия — химические, механические, термические, инфекционные и радиационные. Вследствие повышенного местного обмена веществ усиливается распад макромолекул на более мелкие молекулы, что увеличивает концентрацию частиц в очаге воспаления. Это приводит к местному повышению осмотического давления, выделению в очаг воспаления большого количества жидкости из окружающих тканей и образованию экссудата. В медицинской практике используют гипертонические растворы или марлевые повязки, смоченные гипертоническим раствором NaCl, который в соответствии с закономерностями осмоса всасывает жидкость в себя, что способствует постоянному очищению раны от гноя или устранению отёка. В некоторых случаях для этих же целей используют этиловый спирт или его концентрированные водные растворы, которые гипертоничны относительно живых тканей. На этом основано их дезинфицирующее действие, так как они способствуют плазмолизу бактерий и микроорганизмов.
Действие слабительных средств — горькой соли MgSO4 • 7Н2О и глауберовой соли Na2SO4 • 10Н2О также основано на явлении осмоса. Эти соли плохо всасываются через стенки кишечника, поэтому они создают в нём гипертоническую среду и вызывают поступление в кишечник большого количества воды через его стенки, что приводит к послабляющему действию. Следует иметь в виду, что распределение и перераспределение воды в организме происходит и по другим более специфическим механизмам, но осмос играет в этих процессах ведущую роль, а значит, он играет ведущую роль и в поддержании гомеостаза.
РАСТВОРЫ И ИХ КОЛЛИГАТИВНЫЕ СВОЙСТВА
Растворы представляют для биологии, физиологии и медицины особый интерес, так как все важнейшие биологические системы (цитоплазма, кровь, лимфа, слюна, моча, пот и др.) являются водными растворами солей, белков, углеводов, липидов. Усвоение пищи, транспорт метаболитов, большинство биохимических реакций в живых организмах протекают в растворах.
Понятие “растворы” включает истинные растворы и коллоидные растворы. Различие между ними заключается прежде всего в размерах частиц и однородности систем.
Истинные растворы – это однородные гомогенные системы с размером частиц на уровне 10–10 – 10–9 м.
Коллоидные растворы – это неоднородные гетерогенные системы с размером частиц 10–9 – 10–6 м. Рассмотрим сначала истинные растворы.
Источник
