Какие свойства проявляют аминокислоты кислотные основные
Аминокислоты являются амфотерными соединениями, для них характерны кислотно-основные свойства. Это обусловлено наличием в их молекулах функциональных групп кислотного (-СООН) и основного (-NH2) характера.
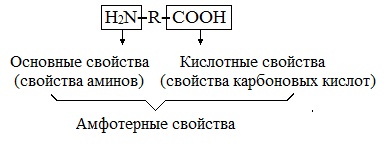
Кислотно-основное равновесие в водных растворах
В водных растворах и твердом состоянии аминокислоты существуют в виде внутренних солей.
Ионизация молекул аминокислот в водных растворах зависит от кислотного или щелочного характера среды:
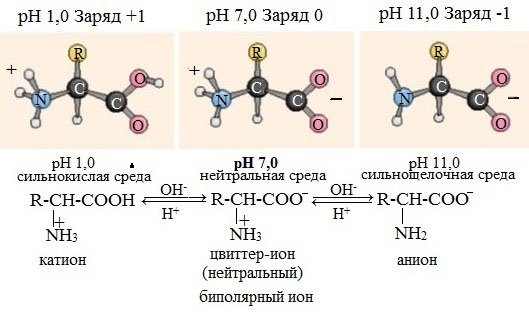
В кислой среде молекулы аминокислот представляю собой катион. В щелочной среде молекулы аминокислот представляют собой анион. В нейтральной среде аминокислоты представляют собой цвиттер-ион или биполярный ион.
Аминокислоты в твердом состоянии всегда существуют в виде биполярного, двухзарядного иона — цвиттер-иона.
Водные растворы аминокислот в кислой и щелочной среде проводят электрический ток.
1. Взаимодействие внутри молекулы – образование внутренних солей (биполярных ионов)
Молекулы аминокислот существуют в виде внутренних солей, которые образуются за счет переноса протона от карбоксила к аминогруппе.
Карбоксильная группа аминокислоты отщепляет ион водорода, который затем присоединяется к аминогруппе той же молекулы по месту неподеленной электронной пары азота. В результате действие функциональных групп нейтрализуется, образуется так называемая внутренняя соль.
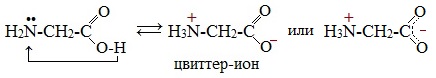
Водные растворы аминокислот в зависимости от количества функциональных групп имеют нейтральную, кислую или щелочную среду.
Аминокислоты с одной карбоксильной группой и одной аминогруппой имеют нейтральную реакцию.
Видеоопыт «Свойства аминоуксусной кислоты»
а) моноаминомонокарбоновые кислоты (нейтральные кислоты)
Внутримолекулярная нейтрализация — образуется биполярный цвиттер-ион.
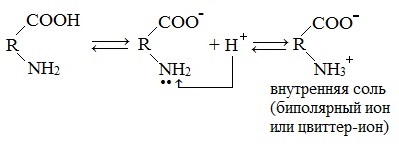
Водные растворы моноаминомонокарбоновых кислот нейтральны (рН≈7).
б) моноаминодикарбоновые кислоты (кислые аминокислоты)
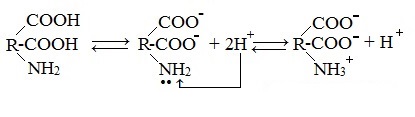
Водные растворы моноаминодикарбоновых кислот имеют рН<7 (кислая среда), так как в результате образования внутренних солей этих кислот в растворе появляется избыток ионов водорода Н+.
в) диаминомонокарбоновые кислоты (основные аминокислоты)
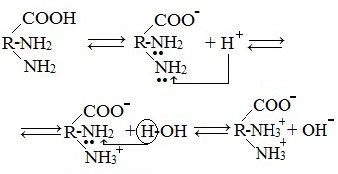
Водные растворы диаминомонокарбоновых кислот имеют рН>7 (щелочная среда), так как в результате образования внутренних солей этих кислот в растворе появляется избыток гидроксид-ионов ОН— .
2. Взаимодействие с основаниями и кислотами
Аминокислоты как амфотерные соединения образуют соли как с кислотами (по группе NH2), так и со щелочами (по группе СООН).
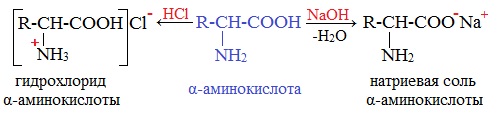
Как кислота (участвует карбоксильная группа)
Как карбоновые кислоты α-аминокислоты образуют функциональные производные: соли, сложные эфиры, амиды.
а) взаимодействие с основаниями
Образуются соли:
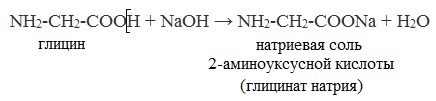
б) взаимодействие со спиртами (р. этерификации)
Аминокислоты могут реагировать со спиртами в присутствии газообразного хлороводорода, превращаясь в сложный эфир. Сложные эфиры аминокислот не имеют биполярной структуры и являются летучими соединениями.
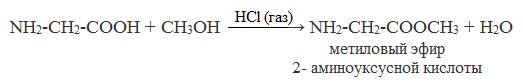
в) взаимодействие с аммиаком
Образуются амиды:
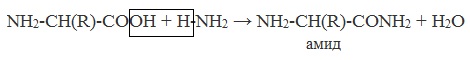
Как основание (участвует аминогруппа)
а) взаимодействие с сильными кислотами
Подобно аминам, аминокислоты реагируют с сильными кислотами с образованием солей аммония:
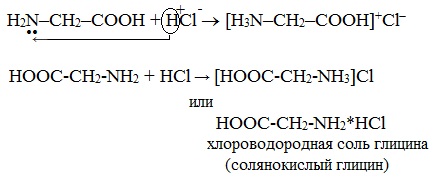
б) взаимодействие с азотистой кислотой (р. дезаминирования)
Подобно первичным аминам, аминокислоты реагируют с азотистой кислотой, при этом аминогруппа превращается в гидроксогруппу, а аминокислота – в гидроксикислоту:
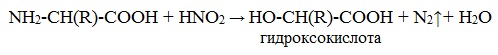
Измерение объёма выделившегося азота позволяет определить количество аминокислоты (метод Ван-Слайка).
3. Внутримолекулярное взаимодействие функциональных групп ε-аминокапроновой кислоты, в результате которого образуется ε-капролактам (полупродукт для получения капрона).
4. Межмолекулярное взаимодействие α-аминокислот – образование пептидов (р. поликонденсации)
При взаимодействии карбоксильной группы одной молекулы аминокислоты и аминогруппы другой молекулы аминокислоты образуются пептиды. При взаимодействии двух α-аминокислот образуется дипептид.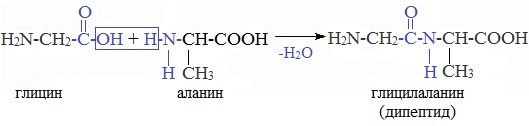
Межмолекулярная реакция с участием трех α-аминокислот приводит к образованию трипептида и т.д.
Важнейшие природные полимеры – белки (протеины) – относятся к полипептидам, т.е представляют собой продукт поликонденсации a-аминокислот.
5. Качественные реакции!
а) нингидриновая реакция
Все аминокислоты окисляются нингидрином с образованием продуктов сине-фиолетового цвета:
Иминокислота пролин дает с нингидрином желтое окрашивание.
б) с ионами тяжелых металлов α-аминокислоты образуют внутрикомплексные соли. Комплексы меди (II), имеющие глубокую синюю окраску, используются для обнаружения α-аминокислот.
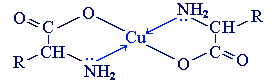
Видеоопыт «Образование медной соли аминоуксусной кислоты»
Аминокислоты
Источник
α-Аминокислоты в силу своего химического строения проявляют кислотно-основные (амфотерные) свойства, которые определяют многие физико-химические и биологические свойства белков. На этих свойствах основаны, почти все методы выделения и идентификации аминокислот и белков.
При нейтральном значении рН аминокислоты в растворах находятся в виде биполярного иона (цвиттер-иона), при этом аминогруппа протонирована (-NH3+), а карбоксильная группа – диссоциирована (-СОО-):
| (рН ≈7) |
Ионизация аминокислоты зависит от рН среды: в кислых растворах ионизирована аминогруппа, а в щелочных – карбоксильная группа:
В кислой среде α-аминокислоты выступают как основания (по аминогруппе), а в щелочной – как кислоты (по карбоксильной группе). У некоторых аминокислот может ионизироваться также радикал (R), в связи, с чем все аминокислоты можно разделить на заряженные и незаряженные (при физиологическом значении рН=6,0 – 8,0) (см. табл. 4). В качестве примера первых можно привести аспарагиновую кислоту и лизин:
Если радикалы аминокислот нейтральные, то они не оказывают влияния на диссоциацию α-карбоксильной или α-аминогруппы, и величинырК (отрицательный логарифм, показывающий значение рН, при котором эти группы наполовину диссоциированы) остаются относительно постоянными.
Величины рК для α-карбоксилыюй (pK1) и α-аминогруппы (рК2) сильно различаются. При рН < pK1 почти все молекулы аминокислоты протежированы и заряжены положительно. Напротив, при рН > рК2 практически все молекулы аминокислоты являются отрицательно заряженными, так как α-карбоксильная группа находится в диссоциированном состоянии.
Следовательно, в зависимости от рН среды аминокислоты имеют суммарный нулевой положительный или отрицательный заряд. Значение рН, при котором суммарный заряд молекулы равен нулю, и она не перемещается в электрическом поле ни к катоду, ни к аноду, называется изоэлектрической точкой и обозначается pI.
Для нейтральных α-аминокислот значение pI находят как среднее арифметическое между двумя значениями рК:
При рН раствора меньше pI аминокислоты протонируются и, заряжаясь положительно, перемещаются в электрическом поле к катоду. Обратная картина наблюдается при рН > pI.
Для аминокислот, содержащих заряженные (кислотные или основные) радикалы, изоэлектрическая точка зависит от кислотности или основности этих радикалов и их рК (рК3). Значение pI для них находят по следующим формулам:
для кислых аминокислот:
для основных аминокислот:
В клетках и межклеточной жидкости организма человека и животных рН среды близко к нейтральному, поэтому основные аминокислоты (лизин, аргинин) имеют положительный заряд (катионы), кислые аминокислоты (аспарагиновая, глутаминовая) имеют отрицательный заряд (анионы), а остальные существуют в виде биполярного цвиттер-иона.
Стереохимия аминокислот
Важной особенностью белковых α-аминокислот является их оптическая активность. За исключением глицина все они построены асимметрично, в связи с чем, будучи растворены в воде или в соляной кислоте, способны вращать плоскость поляризации света. Аминокислоты существуют в виде пространственных изомеров, относящихся к D- или L-ряду. L- или D-конфигурация определяется типом строения соединения относительно асимметрического атома углерода (атом углерода, связанный с четырьмя различными атомами или группами атомов). В формулах асимметрический атом углерода обозначают звездочкой. На рис.3 показаны проекционные модели L- и D- конфигураций аминокислот, которые являются как бы зеркальным отображением друг друга. Все 18 оптически активных белковых аминокислот относятся к L -ряду. Однако в клетках многих микроорганизмов и в антибиотиках, продуцируемых некоторыми из них, обнаружены D-аминокислоты.
Рис. 3. Конфигурация L- и D- аминокислот
Строение белков
Исходя из результатов изучения продуктов гидролиза белков и выдвинутых А.Я. Данилевским идей о роли пептидных связей -CO-NH- в построении белковой молекулы, немецкий ученый Э.Фишер предложил в начале XX века пептидную теорию строения белков. Согласно этой теории, белки представляют собой линейные полимеры α-аминокислот, связанных пептиднойсвязью – полипептиды:
В каждом пептиде один концевой аминокислотный остаток имеет свободную α-аминогруппу (N-конец), а другой – свободную α-карбоксильную группу (С-конец). Структуру пептидов принято изображать, начиная с N-концевой аминокислоты. При этом аминокислотные остатки обозначаются символами. Например: Ala-Tyr-Leu-Ser-Tyr- •••–Cys. Этой записью обозначен пептид, в котором N-концевой α-аминокислотой является аланин, а С-концевой – цистеин. При чтении такой записи окончания названий всех кислот, кроме последних меняются на – “ил”: аланил-тирозил-лейцил-серил-тирозил-••• -цистеин. Длина пептидной цепи в пептидах и белках, встречающихся в организме, колеблется от двух до сотен и тысяч аминокислотных остатков.
Для определения аминокислотного состава белки (пептиды) подвергают гидролизу:
В нейтральной среде эта реакция протекает очень медленно, но ускоряется в присутствии кислот или щелочей. Обычно гидролиз белков проводят в запаянной ампуле в 6М растворе соляной кислоты при 105 °С; в таких условиях полный распад происходит примерно за сутки. В некоторых случаях белок гидролизуют в более мягких условиях (при температуре 37-40 °С) под действием биологических катализаторов-ферментов в течение нескольких часов.
Затем аминокислоты гидролизата разделяют методом хроматографии на ионообменных смолах (сульфополистирольный катионит), выделяя отдельно фракцию каждой аминокислоты. Для вымывания аминокислот с ионнообменной колонки используют буферы с возрастающим значением рН. Первым снимается аспартат, имеющий кислотную боковую цепь; аргинин с основной боковой цепью вымывается последним. Последовательность снятия аминокислот с колонки определяют по профилю вымывания стандартных аминокислот. Фракционированные аминокислоты определяют по окраске, образующейся при нагревании с нингидрином:
В этой реакции бесцветный нингидрин превращается; в синефиолетовый продукт, интенсивность окраски которого (при 570 нм) пропорциональна количеству аминокислоты (только пролин дает желтое окрашивание). Измерив, интенсивность окрашивания, можно рассчитать концентрацию каждой аминокислоты в гидролизате и число остатков каждой из них в исследуемом белке.
В настоящее время такой анализ проводят с помощью автоматических приборов – аминокислотных анализаторов (см. ниже рис. Схемы прибора). Результат анализа прибор выдаёт в виде графика концентраций отдельных аминокислот. Этот метод нашел широкое применение в исследовании состава пищевых веществ , клинической практике; с его помощью за 2-3 часа можно получить полную картину качественного состава аминокислот продуктов и биологических жидкостей.
Рис. Схема аминокислотного анализатора: 1 – вымывающий раствор (буфер с переменным рН); 2 – хроматогрифическая колонка (в верхнюю часть колонки вносят гидролизат белка, затем начинают вымывание); 3 – раствор нингидрина; 4 – водяная баня (подогревание необходимо для ускорения реакции нингидрина с аминокислотами); 5 – спектрофотометр и записывающее устройство; 6 – хроматограмма, каждый пик которой соответствует одной аминокислоте, а площадь пика пропорциональна концентрации аминокислоты в гидролизате.
Дата добавления: 2016-11-12; просмотров: 4341 | Нарушение авторских прав | Изречения для студентов
Читайте также:
Рекомендуемый контект:
Поиск на сайте:
© 2015-2020 lektsii.org – Контакты – Последнее добавление
Источник
Аминокислоты – органические бифункциональные соединения, в состав которых входят карбоксильные группы –СООН и аминогруппы –NH2.
Природные аминокислоты можно разделить на следующие основные группы:
| 1) Алифатические предельные аминокислоты (глицин, аланин) | NH2-CH2-COOH глицин NH2-CH(CH3)-COOH аланин |
| 2) Серосодержащие аминокислоты (цистеин) |  цистеин |
| 3) Аминокислоты с алифатической гидроксильной группой (серин) | NH2-CH(CH2OH)-COOH серин |
| 4) Ароматические аминокислоты (фенилаланин, тирозин) |  фенилаланин
тирозин |
| 5) Аминокислоты с двумя карбоксильными группами (глутаминовая кислота) | HOOC-CH(NH2)-CH2-CH2-COOH глутаминовая кислота |
| 6) Аминокислоты с двумя аминогруппами (лизин) | CH2(NH2)-CH2-CH2-CH2-CH(NH2)-COOH лизин |
- Для природных α-аминокислот R-CH(NH2)COOH применяются тривиальные названия: глицин, аланин, серин и т. д.
- По систематической номенклатуре названия аминокислот образуются из названий соответствующих кислот прибавлением приставки амино- и указанием места расположения аминогруппы по отношению к карбоксильной группе:
- Часто используется также другой способ построения названий аминокислот, согласно которому к тривиальному названию карбоновой кислоты добавляется приставка амино- с указанием положения аминогруппы буквой греческого алфавита.
Аминокислоты – твердые кристаллические вещества с высокой температурой плавления. Хорошо растворимы в воде, водные растворы хорошо проводят электрический ток.
- Замещение галогена на аминогруппу в соответствующих галогензамещенных кислотах:

- Восстановление нитрозамещенных карбоновых кислот (применяется для получения ароматических аминокислот):

При растворении аминокислот в воде карбоксильная группа отщепляет ион водорода, который может присоединиться к аминогруппе. При этом образуется внутренняя соль, молекула которой представляет собой биполярный ион:
![]()
1. Кислотно-основные свойства аминокислот
Аминокислоты — это амфотерные соединения.
Они содержат в составе молекулы две функциональные группы противоположного характера: аминогруппу с основными свойствами и карбоксильную группу с кислотными свойствами.
Водные растворы аминокислот имеют нейтральную, щелочную или кислую среду в зависимости от количества функциональных групп.
Так, глутаминовая кислота образует кислый раствор (две группы -СООН, одна -NH2), лизин — щелочной (одна группа -СООН, две -NH2).
1.1. Взаимодействие с металлами и щелочами
Как кислоты (по карбоксильной группе), аминокислоты могут реагировать с металлами, щелочами, образуя соли:

1.2. Взаимодействие с кислотами
По аминогруппе аминокислоты реагируют с основаниями:

2. Взаимодействие с азотистой кислотой
Аминокислоты способны реагировать с азотистой кислотой.
Например, глицин взаимодействует с азотистой кислотой:
![]()
3. Взаимодействие с аминами
Аминокислоты способны реагировать с аминами, образуя соли или амиды.
![]()
4. Этерификация
Аминокислоты могут реагировать со спиртами в присутствии газообразного хлороводорода, превращаясь в сложный эфир:
Например, глицин взаимодействует с этиловым спиртом:
![]()
5. Декарбоксилирование
Протекает при нагревании аминокислот с щелочами или при нагревании.
Например, глицин взаимодействует с гидроксидом бария при нагревании:
![]()
Например, глицин разлагается при нагревании:
![]()
6. Межмолекулярное взаимодействие аминокислот
При взаимодействии аминокислот образуются пептиды. При взаимодействии двух α-аминокислот образуется дипептид.
Например, глицин реагирует с аланином с образованием дипептида (глицилаланин):

Фрагменты молекул аминокислот, образующие пептидную цепь, называются аминокислотными остатками, а связь CO–NH — пептидной связью.
Источник
Среди
азотсодержащих органических веществ имеются соединения с двойственной функцией.
Особенно важными из них являются аминокислоты.
В клетках и тканях живых организмов
встречается около 300 различных аминокислот, но только 20 (α-аминокислоты) из них служат звеньями (мономерами), из которых построены пептиды и
белки всех организмов (поэтому их называют белковыми аминокислотами).
Последовательность расположения этих аминокислот в белках закодирована в
последовательности нуклеотидов соответствующих генов. Остальные аминокислоты
встречаются как в виде свободных молекул, так и в связанном виде. Многие из
аминокислот встречаются лишь в определенных организмах, а есть и такие, которые
обнаруживаются только в одном из великого множества описанных организмов.
Большинство микроорганизмов и растения синтезируют необходимые им аминокислоты;
животные и человек не способны к образованию так называемых незаменимых
аминокислот, получаемых с пищей. Аминокислоты участвуют в обмене белков и
углеводов, в образовании важных для организмов соединений (например, пуриновых
и пиримидиновых оснований, являющихся неотъемлемой частью нуклеиновых кислот),
входят в состав гормонов, витаминов, алкалоидов, пигментов, токсинов,
антибиотиков и т. д.; некоторые аминокислоты служат посредниками при передаче
нервных импульсов.
Аминокислоты — органические амфотерные соединения, в состав
которых входят карбоксильные группы – СООН и аминогруппы -NH2.
Аминокислоты можно рассматривать как
карбоновые кислоты, в молекулах которых атом водорода в радикале замещен
аминогруппой.
КЛАССИФИКАЦИЯ

Аминокислоты классифицируют по структурным признакам.
1.
В
зависимости от взаимного расположения амино- и карбоксильной групп аминокислоты
подразделяют на α-, β-, γ-, δ-, ε- и
т. д.
2.
В
зависимости от количества функциональных групп различают кислые, нейтральные и
основные.
3.
По
характеру углеводородного радикала различают алифатические (жирные), ароматические,
серосодержащие и гетероциклические
аминокислоты. Приведенные выше аминокислоты относятся к жирному ряду.
Примером
ароматической аминокислоты может служить пара-аминобензойная
кислота:
Примером
гетероциклической аминокислоты может служить триптофан – незаменимая α- аминокислота
НОМЕНКЛАТУРА
По систематической номенклатуре названия
аминокислот образуются из названий соответствующих кислот прибавлением
приставки амино- и указанием места расположения аминогруппы по отношению
к карбоксильной группе. Нумерация углеродной цепи с атома углерода карбоксильной группы.
Например:
Часто используется также другой способ
построения названий аминокислот, согласно которому к тривиальному названию
карбоновой кислоты добавляется приставка амино- с указанием положения
аминогруппы буквой греческого алфавита.
Пример:
Для α-аминокислот R-CH(NH2)COOH

, которые играют исключительно важную
роль в процессах жизнедеятельности животных и растений, применяются тривиальные
названия.
Таблица. Некоторые важнейшие α-аминокислоты
Аминокислота | Сокращённое обозначение | Строение радикала ( R ) |
Глицин | Gly (Гли) | H – |
Аланин | Ala (Ала) | CH3 – |
Валин | Val (Вал) | (CH3)2CH – |
Лейцин | Leu (Лей) | (CH3)2CH – CH2 – |
Серин | Ser (Сер) | OH- CH2 – |
Тирозин | Tyr (Тир) | HO – C6H4 – CH2 – |
Аспарагиновая кислота | Asp (Асп) | HOOC – CH2 – |
Глутаминовая кислота | Glu (Глу) | HOOC – CH2 – CH2 – |
Цистеин | Cys (Цис) | HS – CH2 – |
Аспарагин | Asn (Асн) | O = C – CH2 – │ NH2 |
Лизин | Lys (Лиз) | NH2 – CH2- CH2 – CH2 – |
Фенилаланин | Phen (Фен) | C6H5 – CH2 – |
Если
в молекуле аминокислоты содержится две аминогруппы, то в ее названии
используется приставка диамино-, три группы NH2 – триамино-
и т.д.
Пример:
Наличие
двух или трех карбоксильных групп отражается в названии суффиксом –диовая
или -триовая кислота:
ИЗОМЕРИЯ
1. Изомерия углеродного скелета
2. Изомерия положения функциональных
групп
3. Оптическая изомерия
α-аминокислоты, кроме глицина NН2-CH2-COOH.
ФИЗИЧЕСКИЕ СВОЙСТВА
Аминокислоты представляют собой
кристаллические вещества с высокими (выше 250°С) температурами плавления,
которые мало отличаются у индивидуальных аминокислот и поэтому нехарактерны.
Плавление сопровождается разложением вещества. Аминокислоты хорошо растворимы в
воде и нерастворимы в органических растворителях, чем они похожи на
неорганические соединения. Многие аминокислоты обладают сладким вкусом.
ПОЛУЧЕНИЕ
3. Микробиологический синтез. Известны микроорганизмы, которые
в процессе жизнедеятельности продуцируют α – аминокислоты белков.
ХИМИЧЕСКИЕ СВОЙСТВА
Аминокислоты
амфотерные органические соединения, для них характерны кислотно-основные
свойства.
I.Общие свойства
1. Внутримолекулярная нейтрализация → образуется биполярный цвиттер-ион:
Водные
растворы электропроводны. Эти свойства объясняются тем, что молекулы
аминокислот существуют в виде внутренних солей, которые образуются за счет
переноса протона от карбоксила к аминогруппе:
цвиттер-ион
Водные растворы аминокислот имеют нейтральную, кислую
или щелочную среду в зависимости от количества функциональных групп.
Видео-опыт «Свойства аминоуксусной кислоты»
2. Поликонденсация→ образуются полипептиды (белки):
При взаимодействии двух
α-аминокислот образуется дипептид.
3. Разложение → Амин +
Углекислый газ:
NH2-CH2-COOH → NH2-CH3 + CO2↑
II. Свойства карбоксильной группы
(кислотность)
1. С основаниями → образуются соли:
NH2-CH2-COOH
+ NaOH → NH2-CH2-COONa + H2O
NH2-CH2-COONa – натриевая соль 2-аминоуксусной кислоты
2. Со спиртами → образуются сложные
эфиры – летучие вещества (р.
этерификации): NH2-CH2-COOH
+ CH3OH HCl(газ)→ NH2-CH2-COOCH3
+ H2O
NH2-CH2-COOCH3 – метиловый эфир 2- аминоуксусной кислоты
3. С аммиаком → образуются
амиды:
NH2-CH(R)-COOH + H-NH2 →
NH2-CH(R)-CONH2 + H2O
4. Практическое значение имеет
внутримолекулярное взаимодействие функциональных групп ε-аминокапроновой
кислоты, в результате которого образуется ε-капролактам (полупродукт для
получения капрона):
III. Свойства аминогруппы (основность)
1. С сильными кислотами → соли:
HOOC-CH2-NH2 + HCl → [HOOC-CH2-NH3]Cl
или HOOC-CH2-NH2*HCl
2. С азотистой кислотой (подобно
первичным аминам):
NH2-CH(R)-COOH +
HNO2 → HO-CH(R)-COOH + N2↑+ H2O
гидроксокислота
Измерение
объёма выделившегося азота позволяет определить количество аминокислоты (метод
Ван-Слайка)
IV.Качественная реакция
1. Все аминокислоты окисляются
нингидрином с образованием продуктов сине-фиолетового цвета!
2. С ионами тяжелых металлов α-аминокислоты
образуют внутрикомплексные соли. Комплексы меди (II), имеющие глубокую
синюю окраску, используются для обнаружения α-аминокислот.
Видео-опыт “Образование медной соли аминоуксусной кислоты”.
Генетическая связь аминокислот с другими классами органических соединений
ПРИМЕНЕНИЕ
1) аминокислоты широко
распространены в природе;
2) молекулы аминокислот – это те
кирпичики, из которых построены все растительные и животные белки;
аминокислоты, необходимые для построения белков организма, человек и животные
получают в составе белков пищи;
3) аминокислоты прописываются при
сильном истощении, после тяжелых операций;
4) их используют для питания
больных;
5) аминокислоты необходимы в
качестве лечебного средства при некоторых болезнях (например, глутаминовая
кислота используется при нервных заболеваниях, гистидин – при язве желудка);
6) некоторые аминокислоты
применяются в сельском хозяйстве для подкормки животных, что положительно
влияет на их рост;
7) имеют техническое значение:
аминокапроновая и аминоэнантовая кислоты образуют синтетические волокна –
капрон и энант.
О РОЛИ АМИНОКИСЛОТ
Нахождение в природе и биологическая роль аминокислот
Источник

