Какие свойства проявляет пероксид водорода
Пероксид водорода
Пероксид водорода (перекись водорода), H2O2 – простейший представитель пероксидов. Бесцветная жидкость с «металлическим» вкусом, неограниченно растворимая в воде, спирте и эфире. Концентрированные водные растворы взрывоопасны. Пероксид водорода является хорошим растворителем. Из воды выделяется в виде неустойчивого кристаллогидрата H2O2 • 2H2O.
Строение молекулы
Молекула Н2O2 содержит в своем составе пероксидный анион O2-2 . Каждый атом кислорода образует 2 ковалентные связи, но имеет степень окисления, равную -1. В упрощенном виде строение молекулы отражает графическая формула:
H+1-O-1-O-1-H+1
Физические свойства
В чистом безводном виде Н2O2 – бесцв. сиропообразная жидкость с плотностью 1,45 г/см3 (т. пл. -0,41°С, т. кип. 150,2°С). Смешивается с водой в любых соотношениях, растворяется также в спирте, эфире. 30%-ный р-р Н2O2 называют пергидролем. Подобно воде, Н2O2 – хороший полярный растворитель, в котором вещества с ионной и полярной ковалентной связью диссоциируют на ионы.
Химические свойства
Разложение Н2O2 (диспропорционирование)
2Н2O2 = 2Н2O + O2↑
2O-1 – 2e- → O20
2O-1 +2e- → 2О-2
При Т > 90° С пероксид водорода разлагается практически полностью. Причиной непрочности молекул Н2O2 является неустойчивость атома кислорода в степепени окисления -1.
Н2O2 – слабая кислота
Молекулы Н2O2 в незначительной степени диссоциируют в водном растворе по схеме:
Н2O2 = Н+ + HO2-
(Кдисс = 1,5 * 10-12 при 20°С)
Кислотные свойства проявляются в реакциях со щелочами с образованием солей – средних (пероксидов) и кислых (гидропероксидов), например:
Н2O2 + Ва(ОН)2 = ВаO2 + 2Н2O
пероксид бария
Гидролиз пероксидов металлов
Хотя по составу пероксиды напоминают оксиды, они на самом деле обладают свойствами солей. В водных растворах полностью гидролизуются с выделением Н2O2:
К2O2 + 2Н2O = 2КОН + Н2O2
Получение Н2O2 из пероксидов металлов
Так как Н2O2 – очень слабая кислота, то она вытесняется из своих солей как сильными кислотами, так и слабыми, например:
ВаO2 + H2SO4 = Н2O2 + BaSO4↓
ВаO2 + СO2 + Н2O = Н2O2 + ВаСO3↓
Н2O2 сильный окислитель
Атомы кислорода, находящиеся в неустойчивой степени окисления -1, стремятся приобрести еще один электрон для перехода в устойчивое состояние. Поэтому пероксид водорода проявляет очень сильные окислительные свойства, особенно в кислой среде:
Н2O-2 + 2H+ + 2e- → 2Н2O-2
Окисление неорганических веществ
Примеры:
ЗН2O2 + 2NH3 = N2 + 6Н2O
4Н2O2 + H2S = H2SO4 + 4Н2O
Н2O2 + 2HI = I2 + 2Н2O
4Н2O2 + PbS = PbSO4 + 4Н2O
ЗН2O2 + 2СrСl3 + 10КОН = 2К2СrO4 + 6KCl + 8Н2O
Н2O2 + 2FeSO4 + H2SO4 = Fe2(SO4)3 + 2Н2O
Окисление органических веществ
Конц. водные растворы Н2O2 в смеси с органическими веществами способны к воспламенению и взрыву при ударе. Например, органические кислоты окисляются до СO2 и Н2О(как при горении в O2):
4Н2O2 + CH3COOH = 2CO2↑ + 6Н2O
Н2O2 + Н2С2O4 = 2СO2↑ + 2Н2O
Пероксиды щел. Me – очень сильные окислители
Окисляют многие неорганические и органические вещества, например:
4Na2O2 + СН3СООН = 2Na2CO3 + 4NaOH
Na2O2 + SO2 = Na2SO4
Важной реакцией является диспропорционирование пероксида Na при взаимодействии с углекислым газом:
2Na2O2 + 2СO2 = 2Na2CO3 + O2↑
На этой реакции основано использование Na2O2 в автономных дыхательных аппаратах и в замкнутых помещениях для поглощения СO2 и образования O2.
Н2O2 – слабый восстановитель (в реакциях с очень сильными окислителями)
Окисление пероксида водорода обычно протекает по схеме:
2Н2O-2 – 2e- → O02↑ + 2H+
Примеры реакций:
5Н2O2 + 2КМnO4 + 3H2SO4 = 5O2↑ + 2MnSO4 + K2SO4 + 8Н2O
ЗН2O2 + К2Сr2O7 + 4H2SO4 = 3O2↑ + Cr2(SO4)3 + K2SO4 + 7Н2O
3Н2O2 + KClO3 = 3O2↑ + KCl + 3Н2O
3Н2O2 + 2AuCl3 = 3O2↑ + 2Au + 6HCl
Источник

Строение молекулы и физические свойства
Перекись водорода относится к простейшим представителям группы пероксидов. Её получают в промышленности и лаборатории несколькими способами. Структурная формула перекиси водорода обозначается H2O2. Степень окисления у атомов кислорода -1.
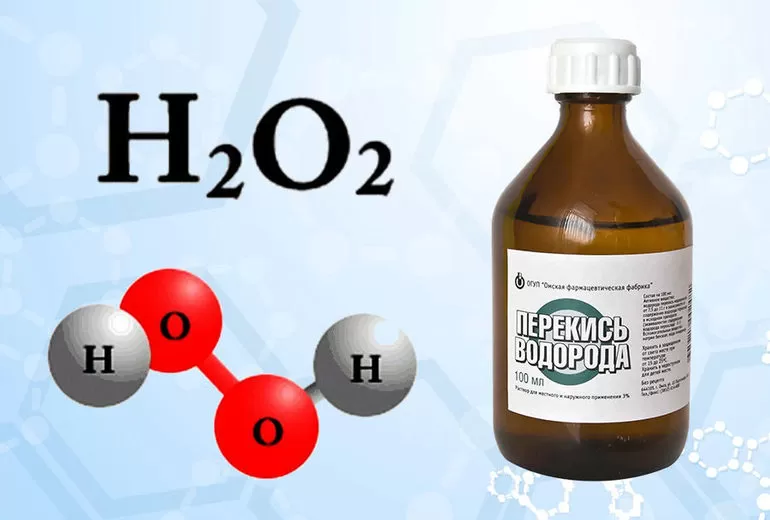
Молекула вещества представлена двумя OH-группами, которые связаны пероксидным -О-О-мостиком и лежат в разных плоскостях. Угол между ними меняется в зависимости от температуры, концентрации раствора и других условий.
Пероксид представлен в виде бесцветной жидкости с «металлическим» вкусом и специфическим запахом. Вязкая консистенция обусловлена развитой системой водородных связей в молекулярной структуре.
Основные физические свойства перекиси водорода:
- Температура кипения: 150,2°C.
- Температура замерзания: -0,432°C.
- Плотность: 1,46 г/см3.
Молекула вещества является полярной, поскольку её строение несимметричное. Соединение может неограниченно растворяться в воде, эфире и спирте. Чистое вещество неустойчиво и способно самопроизвольно разлагаться со взрывом.
Химические особенности
Поскольку оба атома кислорода находятся в промежуточной степени окисления -1, антисептическое средство может проявлять как окислительные, так и восстановительные свойства. Оно участвует в реакциях окисления нитритов до нитратов и выделении иодов из иодидов металлов. Также вещество может расщеплять ненасыщенные соединения.
Перекись обладает слабыми кислотными свойствами, поэтому она диссоциирует по двум ступеням:
- H2O2↔H++OOH−
- OOH−↔H++O22−
Вещество по степени кислотности немного сильнее H2O. Некоторые пероксиды металлов можно рассматривать как его соли. В кислой среде перекись служит окислителем, а в щелочной — восстановителем.
Реагируя с более сильными окислителями, например, с солями серебра и золота, водород служит восстановителем и окисляется до атомарного кислорода. В реакции с нитритом калия вещество выступает окислителем. Если молекула принимает электрон на внешний уровень, тогда степень окисления кислорода меняется на -2; если она его отдаёт, тогда соединение становится восстановителем. Окисление органических веществ пероксидом обычно проводят в уксусной кислоте.
Способы получения вещества
Сначала пероксид водорода получали в промышленности с помощью электролиза серной кислоты или раствора сульфата аммония в H2SO4. В результате реакции получалась надсерная кислота. После гидролиза вещества образовывались пероксид и серная кислота.
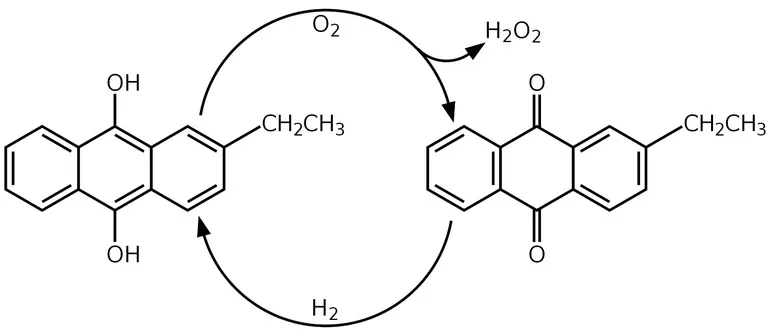
В середине XX века открыли новый способ получения перекиси водорода. Антрахиноновый процесс был разработан компанией BASF. При этом методе водород окисляется кислородом воздуха, после чего образуются антрахиноны и пероксид водорода. Реакцию проводят в растворе алкилантрагидрохинонов в бензоле, который служит катализатором. В него также добавляют вторичные спирты. На завершительной стадии процесса катализатор убирают, а из получившейся смеси продуктов выделяют пероксид водорода путём перегонки при сниженном давлении.

В лабораторных условиях вещество получают с помощью пероксида бария и соляной кислоты. Уравнение взаимодействия соединений: BaO2+2HCl → BaCl2+H2O2. Получившийся хлорид бария осаждают в виде сульфата. Пероксид водорода также можно извлечь при помощи каталитического окисления изопропилового спирта.
В некоторых источниках есть информация, что нужное вещество может образоваться при взаимодействии пероксида бария с серной кислотой, однако такую технологию обычно не используют. Поскольку осадок сульфата бария формируется на зёрнах его пероксида, реагент покрывается нерастворимой оболочкой, которая замедляет реакцию и выход нужного продукта.
Меры предосторожности
Во время работы с концентрированным раствором перекиси необходимо соблюдать меры безопасности. Хотя вещество нетоксично, при попадании в дыхательные пути или на кожный покров и слизистые оно вызывает сильные ожоги. Недостаточно чистый пероксид высокой концентрации может быть взрывоопасен. Всю работу с веществом нужно проводить в «беспылевых» условиях и при отсутствии ионов металлов.
Растворы перекиси водорода относятся к 3-му классу опасности. Вещество может вызывать деструктивные изменения, которые схожи с действием щелочей. Летальная доза пергидроля (название раствора концентрации 30%) составляет 50−100 мл.
Упаковку с аптечным средством необходимо хранить в тёмном месте. При транспортировке нужно избегать встряхивания вещества и других механических воздействий, которые могут привести к его разложению.
Сферы использования
Пероксид водорода может быть разной концентрации. Поскольку растворы обладают различными свойствами, их часто используют в промышленности и быту:
- Вещество применяется при создании бумаги, дезинфицирующих средств и в текстильном производстве в качестве отбеливателя.
- За окислительные свойства пероксид водорода используют как ракетное топливо.
- В аналитической химии при изготовлении пористых материалов средство применяют в качестве пенообразователя.
- В промышленности простейший представитель пероксидов зарекомендовал себя как катализатор и гидрирующий агент.
- В аквариумистике 3%-й раствор помогает очистить резервуары для воды, бороться с паразитами, а также способен оживить задохнувшихся рыб.
- В пищевой промышленности пероксид используется для дезинфекции упаковок для различных напитков и поверхностей оборудования, с которым контактируют продукты.
- В сфере быта средство помогает вывести пятна марганцовки на предметах мебели и текстиле, а также в качестве домашнего антисептика.
Перекись широко используется в области косметологии. Ею обесцвечивают волосы и отбеливают зубы. Поскольку процесс основан на окислении, локоны часто портятся, поэтому вещество не советуют применять обладателям тонких и повреждённых прядей. С зубами не наблюдается дефектов, поскольку с прозрачной эмалью эффект отбеливания достигается за счёт разницы в отражении света дентином.
Применение в области медицины
Широкое применение перекиси водорода нашли в медицине. Средство с бактерицидным механизмом действия предназначено для внешнего использования. Перед применением необходимо тщательно изучить инструкцию к лекарству.
Формы выпуска пероксида водорода:

- Раствор разведённый 1−3%. Применяется для полоскания полости рта и в качестве препарата местного действия.
- Раствор концентрированный 27−31%. Это средство используется редко и только по назначению специалиста. Обычно для обработок его разводят до 3%-го раствора. Лекарство предназначено для лечения заболеваний кожного покрова.
- Гидроперит. Лекарство представлено соединением 35%-го раствора пероксида с карбамидом. Выпускается в форме таблеток. В таком виде препарат легче перевозить и хранить. Чтобы сделать раствор, необходимо растворить в воде 2 таблетки на 100 мл жидкости.
Препаратом лечат гнойные раны и воспалённые слизистые оболочки. Средство используется при носовых и капиллярных кровотечениях, а также для промывки и глубокой очистки ран. Медицинским раствором обрабатывают ротовую полость и горло при ангине, стоматите или тонзиллите. Средство также избавляет кожный покров от пигментных пятен. С помощью лекарства убирают серные пробки при чистке ушей. Препарат применяется в гинекологии для лечения различных женских патологий.
При лёгкой механической очистке ватный тампон смачивают в 3%-м растворе и обрабатывают им поражённые участки кожи. Для компрессов применяют перекись с концентрацией 1 процент. Продолжительность процедуры не должна превышать 30 мин. Для обработки участков кожи с пигментными пятнами используют пергидроль. Ротовую полость или органы половой системы обрабатывают 0,25%-м раствором.
Применение перекиси водорода противопоказано при индивидуальной непереносимости вещества. В редких случаях негативные последствия могут проявиться в жжении во время процедуры и аллергии в виде красных пятен на коже. При длительной терапии после обработок ротовой полости может возникнуть гипертрофия сосочков языка. Если соблюдать дозировку и схему применения перекиси водорода в соответствии с инструкцией, тогда получится избежать побочных действий.
Источник
- Что такое перекись водорода: химическая формула и свойства
- Химическая формула
- Химические свойства
- Основные лечебные свойства
- Способы применения
- В традиционной медицине
- В косметологии
- Применение в быту
- Перекись водорода в народной медицине
- Польза или вред?
- Метод Неумывакина: что это?
Перекись водорода была впервые получена химиком Луисом Тенеро в 1818 году и уже очень скоро стала применяться в промышленности. Сейчас ее повсеместно используют в хозяйстве и быту.
1Что такое перекись водорода: химическая формула и свойства
Перекись водорода это простейший представитель пероксидов. Он представляет собой прозрачную жидкость со своеобразным металлическим вкусом и слабым запахом, способную неограниченно растворяться в спирте, воде и эфире.
Химическая формула
 Химическая формула перекиси водорода – Н2O2. Это означает, что она содержит 2 молекулы водорода и 2 молекулы кислорода.
Химическая формула перекиси водорода – Н2O2. Это означает, что она содержит 2 молекулы водорода и 2 молекулы кислорода.
Химические свойства
- Соединение может распадаться под влиянием некоторых факторов:
- Нагревание;
- Солнечный свет;
- Взаимодействие с окислителями или восстановителями, щелочью.
При взаимодействии с определенными металлами, такими например, как Mn или Fe, происходит активная химическая реакция
Распад вещества быстрее происходит в щелочной среде, кислотная же среда наоборот замедляют процесс. Именно поэтому в раствор часто добавляют фосфорную кислоту. В термических условиях H2O2 быстро разлагается, поэтому не рекомендуется хранить его на свету.
Пероксид водорода хорошо смешивается с C2H5OH (спиртом) и H2O (водой) в любых пропорциях.
Перекись водорода и вода имеют схожий состав, однако температура замерзания гораздо ниже при их взаимодействии, чем если использовать их по отдельности. Смеси, содержащие от 45% пероксида водорода могут значительно переохлаждаться, так есть растворы, температура замерзания которых ниже -55℃.
H2O2- сильный окислитель, отдающий при реакции один атом кислорода. Воздействие крепкого раствора H2O2 на легковоспламеняющиеся вещества, такие как древесина, хлопок, бумага . происходит реакция горения.
Реакция распада перокисда водорода
Кислотная среда более подходящаая среда для распада. Щелочная же более подходит для восстановления
Пример реакции восстановления мы можем наблюдать при взаимодействии H2O2 с серебром
Аналогично, по существу, протекает его взаимодействие с озоном (О3 + Н2О2 = 2 Н2О + 2 О2) и с перманганатом калия в кислой среде:
Последняя реакция применяется для количественного определения пероксида водорода.
Перекись водорода – слабый окислитель, который взаимодействуя с гидроксидами определенных металлов образуют соли H2O2. Например, если рассматривать реакцию с гидроксидом бария:
2 Основные лечебные свойства
Перекись водорода – важное звено в химических процессах живого организма.
- Участвует в процессе метаболизма;
- Выступает в роли антиоксиданта: имеет разрушительное действие на токсины, а также уничтожает любой патологический микроорганизм;
- Обладает восстанавливающим свойством на состав крови и ее кислородное насыщение;
- Нормализует кислотно-щелочной баланс;
- Участвует в регуляции гормонального уровня в щитовидной железе, репродуктивной системе и надпочечниках;
- Не имеет токсического влияния на организм, так как не скапливается при длительном применении;
- Оказывает расширяющее воздействие на сосуды;
- Улучшает функцию желудочно-кишечного тракта;
- Способствует ускорению регенерации в тканях.
3 Способы применения
Уже многие годы перекись водорода используется в различных областях применения благодаря своей эффективности и доступности. Его применение основывается в первую очередь на его окисляющих свойствах.
В традиционной медицине
Соединение назначается при многих заболеваниях. Самыми частыми показаниями к его рекомендации являются:
- Смазывание небольших повреждений кожного покрова: антисептик применяют на раны, царапины и ссадины. К нему чувствительны все инфекционные микробы: вирусы, бактерии, грибки и простейшие.
- Обработка операционного поля перед введением основного антисептика: используют на глубокой гнойной ране, флегмоне. Во время контакта с пероксидазой возникает пена в большом количестве, размягчающая патологические образования. После него вводят лечебный антисептический препарат, с которым легко вымываются некротизированные ткани, гной и кровяные сгустки.
- Очищение слухового прохода от серы: закапывают несколько капель лекарства и ждут около 3 минут. Затем вводят облепиховое масло и засекают 1 минуту. Сера размягчается, и ее нетрудно удалить ватными палочками.
- Полоскание полости рта и горла: при различных воспалениях специалисты рекомендуют готовить раствор из 100 мл дистиллированной воды и 15 мл 3% перекиси водорода. Он устраняет неприятный запах, растворяет пищевые остатки и предупреждает образование налета на зубах и языке.
- Использование при кожных болезнях: в качестве комплексной терапии врач может назначить лекарство для лечения псориаза, экземы, грибка ногтей и бородавок.
В косметологии
Препарат используется на коже, склонной к излишней жирности и появлению акне, черных точек, благодаря способности уничтожать возбудителей инфекции. Для этого 5 капель 3% раствора добавляют к 50 мл тоника. Косметологи советуют его наносить не более 2 раз в неделю.
Людям с веснушками и пигментными пятнами вещество также подойдет за счет его отбеливающего свойства. Чтобы провести процедуру, применяют специальные маски. Взять ст. л. 20% творога, сырой желток и 5 капель перекиси. Все ингредиенты перемешиваются до однородной структуры, а затем кисточкой наносятся на кожный покров. Слегка массируют, оставляя маску на 15 мин. По истечении времени масса смывается, а на лицо накладывают увлажняющий крем.
Применение в быту
Благодаря полезным свойствам Н2О2 можно не только устранить желтые пятна, разводы с белой материи и удалить налет на кафельной плитке, но и избавиться от грибка и плесени.
Чтобы почистить плитку в ванной комнате, взять 40 мл пероксида, ч. л. жидкого мыла и полстакана пищевой соды. Компоненты хорошо перемешать и нанести на влажную губку, которой оттереть проблемные участки. Если загрязнений много, нужно оставить массу на 10 минут, чтобы они растворились.
Для очистки материала берут 3% раствор, который вливают на пятна. Оставляют на 20-30 минут, а затем смывают с поверхности.
Перекись водорода в народной медицине
Перед тем как приготавливать рецепты на основе этого вещества, рекомендуется проконсультироваться с доктором.
- Во время насморка или гайморита берут ст. л. кипяченой воды, в которой разводят 15 капель перекиси. Получившимся лекарством промывают каждый носовой ход пипеткой.
- В период обострения остеохондроза прикладывают компрессы Н2О2. Марлевую салфетку обильно смачивают в веществе и накладывают на проблемную зону позвоночника, оставляя поверх полиэтилен. Не желательно держать компресс свыше 15 минут во избежание образования ожогов.
- При тонзиллите или выраженной зубной боли ч. л. Н2О2 смешивают с четвертью стакана теплой питьевой воды. Полоскают рот до 5-6 раз в сутки.
- Для остановки кровотечения из носа требуется смочить ватный шарик в перекиси и вставить его в ноздрю на 10 минут.
- Чтобы прекратить кровотечение из раны кусок ткани смачивается в Н2О2 и прикладывается на повреждение.
- Для очищения пяток изготавливают ванночки с перекисью водорода. Разогревают 4 л воды, после чего в нее добавляют 3 ст. л. соли и 3 ст. л. препарата. Тщательно размешивают, а затем опускают ноги в таз. Держат около 6 минут, потом очищают пятки пемзой. В завершении смазать ноги кремом.
4 Польза или вред?
Если человек хорошо переносит пероксид и правильно им пользуется, он не должен вызвать каких-либо неблагоприятных последствий.
Попадание на человека крепкого раствора перекиси водорода оставляет на коже белые химические ожоги .
Нельзя употреблять вещество внутрь, это опасно появлением отравления. При полоскании рта иногда теряется чувствительность языка и могут гипертрофироваться его сосочки.
Также не стоит использовать при наличии у человека индивидуальной непереносимости. Это может повлечь за собой развитие аллергической реакции.
5 Форма выпуска и возможные противопоказания препарата
Изготавливается в виде 3% раствора для наружного местного нанесения.
Его крайне нежелательно использовать при следующих состояниях:
- Кровотечения из вен или артерий;
- Индивидуальная непереносимость;
- Период беременности для обработки ротовой полости;
- Детский возраст младше 12 лет.
6 Метод Неумывакина: что это?
Это лечение с успехом применяется в нетрадиционной медицине. Профессор Неумывакин считал перекись панецеей от всех заболеваний. Принцип действия он объяснял укрепляющим эффектом лекарства: при взаимодействии с кровью и ферментом каталазой оно распадается до воды и кислорода, который разжижает кровь, нормализует обменные процессы и улучшает деятельность органов и систем.
Если ожидаемый эффект не достигался, профессор считал, что организм чрезмерно зашлакован. Поэтому он рекомендовал проводить полную очистку.
Метод не признан официальной медициной, так как его противники утверждают, что перекись не только неэффективна, но и может причинить опасность при использовании не по назначению.
В нашей следующей статье мы поговорим об особенностях применения каустической соды.
Источник
