Какие свойства проявляет гидроксид магния

Гидроксид магния, характеристика, свойства и получение, химические реакции.
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
Гидроксид магния – неорганическое вещество, имеет химическую формулу Mg(OH)2.
Краткая характеристика гидроксида магния
Физические свойства гидроксида магния
Получение гидроксида магния
Химические свойства гидроксида магния
Химические реакции гидроксида магния
Применение и использование гидроксида магния
Краткая характеристика гидроксида магния:
Гидроксид магния – неорганическое вещество белого цвета.
Химическая формула гидроксида магния Mg(OH)2.
Практически нерастворим в воде. Является слабым основанием, даже ничтожная его часть, растворившаяся в воде, сообщает раствору слабощелочную реакцию.
Поглощает углекислый газ и воду из воздуха с образованием основного карбоната магния.
Встречается в природе в виде минерала брусита.
Физические свойства гидроксида магния:
| Наименование параметра: | Значение: |
| Химическая формула | Mg(OH)2 |
| Синонимы и названия иностранном языке | magnesium hydroxide (англ.) брусит (рус.) |
| Тип вещества | неорганическое |
| Внешний вид | бесцветные тригональные кристаллы |
| Цвет | белый, бесцветный |
| Вкус | —* |
| Запах | — |
| Агрегатное состояние (при 20 °C и атмосферном давлении 1 атм.) | твердое вещество |
| Плотность (состояние вещества – твердое вещество, при 20 °C), кг/м3 | 2344,6 |
| Плотность (состояние вещества – твердое вещество, при 20 °C), г/см3 | 2,3446 |
| Температура разложения, °C | 350 |
| Молярная масса, г/моль | 58,35 |
* Примечание:
— нет данных.
Получение гидроксида магния:
Гидроксид магния получают в результате следующих химических реакций:
- 1. в результате взаимодействия металлического магния с парами воды:
Mg + 2H2O → Mg(OH)2 + H2.
- 2. в результате взаимодействия оксида магния и воды:
MgO + H2O → Mg(OH)2 (t = 100-125 °C).
- 3. в результате взаимодействия растворимых солей магния с щелочью:
MgCl2 + 2NaOH → Mg(OH)2 + 2NaCl,
Mg(NO3)2 + 2KOH → Mg(OH)2 + 2KNO3.
При этом гидроксид магния выпадает в виде осадка.
- 4. в результате взаимодействия хлорида магния с обожженным доломитом:
MgCl2 + CaO·MgO + 2H2O → 2Mg(OH)2 + CaCl2.
При этом гидроксид магния выпадает в виде осадка.
Химические свойства гидроксида магния. Химические реакции гидроксида магния:
Гидроксид магния является основным основанием, т. е. обладает основными свойствами.
Гидроксид магния – слабое малорастворимое основание.
Химические свойства гидроксида магния аналогичны свойствам гидроксидов других основных металлов. Поэтому для него характерны следующие химические реакции:
1. реакция гидроксида магния с гидроксидом натрия:
Mg(OH)2 + 2NaOH → Na2[Mg(OH)4] (t = 100 °C).
В результате реакции образуется тетрагидроксомагнезиат натрия. В ходе реакции используется насыщенный раствор гидроксида натрия.
2. реакция гидроксида магния с угольной кислотой:
Mg(OH)2 + H2СO3 → MgСO3 + 2H2O.
В результате реакции образуются карбонат магния и вода.
3. реакция гидроксида магния с ортофосфорной кислотой:
Mg(OH)2 + 2H3PO4 → Mg(H2PO4)2 + H2O,
Mg(OH)2 + H3PO4 → MgHPO4 + 2H2O,
3Mg(OH)2 + 2H3PO4 → Mg3(PO4)2 + 6H2O.
В результате реакции образуются в первом случае – дигидроортофосфат магния и вода, во втором – гидроортофосфат магния и вода, в третьем – ортофосфат магния и вода.
4. реакция гидроксида магния с азотной кислотой:
Mg(OH)2 + 2HNO3 → Mg(NO3)2 + 2H2O.
В результате реакции образуются нитрат магния и вода.
Аналогично проходят реакции гидроксида магния и с другими кислотами.
5. реакция гидроксида магния с фтороводородом:
Mg(OH)2 + 2HF → MgF2 + 2H2O.
В результате реакции образуются фторид магния и вода.
6. реакция гидроксида магния с бромоводородом:
Mg(OH)2 + 2HBr → MgBr2 + 2H2O.
В результате реакции образуются бромид магния и вода.
7. реакция гидроксида магния с йодоводородом:
Mg(OH)2 + 2HI → MgI2 + 2H2O.
В результате реакции образуются йодид магния и вода.
8. реакция термического разложения гидроксида магния:
Mg(OH)2 → MgO + H2O (t = 350 °C).
В результате реакции образуются оксид магния и вода.
9. реакция гидроксида магния с пероксидом водорода:
H2O2 + Mg(OH)2 → MgO2 + 2H2O (t < 20 °C).
В результате реакции образуются пероксид магния и вода. В ходе реакции используется концентрированный раствор пероксида водорода.
10. реакция гидроксида магния с оксидом серы:
Mg(OH)2 + SO3 → MgSO4 + 2H2O.
В результате реакции образуются сульфат магния и вода.
11. реакция гидроксида магния с оксидом углерода:
Mg(OH)2 + 2CO2 → Mg(HCO3)2.
В результате реакции образуется гидрокарбонат магния. В ходе реакции гидроксид магния используется в виде суспензии.
12. реакция гидроксида магния с оксидом углерода:
Mg(OH)2 + 2N2O5 → Mg(NO3)2 + 2HNO3 (t = 40-60 °C).
В результате реакции образуются нитрат магния и азотная кислота.
Применение и использование гидроксида магния:
Гидроксид магния используется при очистке воды (как флокулянт), в моющих средствах (как добавка), в качестве наполнителя в зубной пасте, для рафинирования сахара, в качестве пищевой добавки (Е528).
Примечание: © Фото //www.pexels.com, //pixabay.com
карта сайта
гидроксид магния реагирует кислота 1 2 3 4 5 вода
уравнение реакций соединения реакции масса взаимодействие гидроксида магния
Коэффициент востребованности
5 132
Источник
| Гидроксид магния | |
|---|---|
| Систематическое наименование | Гидроксид магния |
| Хим. формула | Mg(OH)2 |
| Рац. формула | Mg(OH)2 |
| Состояние | твёрдое |
| Молярная масса | 58.35 г/моль |
| Плотность | 2,3446 (20 °C) |
| Температура | |
| • плавления | 350 °C |
| • вспышки | невоспламеняющийся °C |
| Энтальпия | |
| • образования | –925 кДж/моль |
| Растворимость | |
| • в воде | 0,0012 г/100 мл |
| Показатель преломления | 1.559 |
| Кристаллическая структура | тригональная |
| Рег. номер CAS | 1309-42-8 |
| PubChem | 73981 |
| Рег. номер EINECS | 215-170-3 |
| SMILES | [OH-].[Mg+2].[OH-] |
| InChI | 1S/Mg.2H2O/h;2*1H2/q+2;;/p-2 VTHJTEIRLNZDEV-UHFFFAOYSA-L |
| Кодекс Алиментариус | E528 |
| RTECS | OM3570000 |
| ChEBI | 6637 |
| ChemSpider | 14107 и 21169899 |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Гидроксид магния (Гидроокись магния) — неорганическое вещество, осно́вный гидроксид металла магния, имеет формулу Mg(OH)2. Слабое малорастворимое основание.

Описание
При стандартных условиях гидроксид магния представляет собой аморфное вещество. При температуре выше 350 °C разлагается на оксид магния и воду. Поглощает углекислый газ и воду из воздуха с образованием основного карбоната магния. Гидроксид магния практически нерастворим в воде, но растворим в солях аммония. Является слабым основанием, даже ничтожная его часть, растворившаяся в воде, сообщает раствору слабощелочную реакцию и окрашивает индикаторы, например, фенолфталеин, в розовый цвет. Встречается в природе в виде минерала брусита.
Получение
- Взаимодействие растворимых солей магния с щелочами:
В общем виде:
Mg2+ + 2 OH− ⟶ Mg(OH)2 ↓
Примеры:
MgCl2 + 2 NaOH ⟶ Mg(OH)2 ↓ + 2 NaCl
Mg(NO3)2 + 2 KOH ⟶ Mg(OH)2 ↓ + 2 KNO3
- Взаимодействие раствора хлорида магния с обожжённым доломитом:
MgCl2 + CaO ⋅ MgO + 2 H2O ⟶ 2 Mg(OH)2 ↓ + CaCl2
- Взаимодействие металлического магния с парами воды:
Mg + 2 H2O ⟶ Mg(OH)2 ↓ + H2 ↑
Химические свойства
- Как и все слабые основания, гидроксид магния термически неустойчив. Разлагается при нагревании до 350 °C:
Mg(OH)2 →ΔT MgO + H2O
- Взаимодействует с кислотами с образованием соли и воды (реакция нейтрализации):
Mg(OH)2 + 2 HCl ⟶ MgCl2 + 2 H2O
Mg(OH)2 + H2SO4 ⟶ MgSO4 + 2 H2O
- Взаимодействие с кислотными оксидами с образованием соли и воды:
Mg(OH)2 + SO3 ⟶ MgSO4 + H2O
- Взаимодействие с горячими концентрированными растворами щелочей с образованием гидроксомагнезатов:
Mg(OH)2 + 2 NaOH ⟶ Na2[Mg(OH)4]
Mg(OH)2 + Sr(OH)2 ⟶ Sr[Mg(OH)4]

В состав Магникора входит – Магния гидроксид.
Применение
Гидроксид магния применяется для связывания диоксида серы, как флокулянт для очистки сточных вод, в качестве огнезащитного средства в термопластических полимерах (полиолефины, ПВХ), как добавка в моющие средства, для получения оксида магния, рафинирования сахара, в качестве компонента зубных паст.
В медицине его применяют в качестве лекарства для нейтрализации кислоты в желудке, а также как очень сильное слабительное.
В Европейском союзе гидроксид магния зарегистрирован в качестве пищевой добавки E528.
Соединения магния | |
|---|---|
| |
Источник
Гидроксид магния – это неорганическое вещество, оно является малорастворимым соединением, из-за чего при его образовании в водных растворах появляется осадок. Формула гидроксида магния – Mg(OH)2, то есть это двухкислотное основание. Более растворим в воде, чем типичные нерастворимые основания, но менее растворим, чем гидроксид кальция. По этой причине его относят к малорастворимым соединениям.
Распространение в природе
Гидроксид магния в природе встречается в виде минерала брусита. Крупные месторождения этой породы – большая редкость. В России его добывают на Кульдурском месторождении, где его запасы оценивают в 14 миллионов тонн. Добыча на нем идет со скоростью примерно в 250 тысяч тонн продукта в год, но с этого года объемы добычи увеличились вдвое. Причиной этому стал хороший спрос на этот минерал за границей. Самым крупным импортером является Япония.

Выглядит брусит как белые, серые или зеленовато-белые кристаллы со стеклянным блеском на изломе. Имеет довольно низкую твердость, поэтому легко режется ножом. Может содержать примеси. В зависимости от их количества и типа выделяют несколько подвидов этого минерала. Так, ферронемалит содержит в себе, помимо гидроксида магния, 5 % железа в виде оксида, а ферробрусит – уже целых 36 %. Оксид железа имеет бурый цвет (цвет ржавчины), поэтому эти минералы приобретают тот же оттенок вместо привычного светло-зеленого. Существует еще и мангобрусит. В качестве примеси здесь выступает марганец. Такой минерал имеет уже медово-желтый цвет. Но при контакте с кислородом воздуха минерал быстро теряет свой красивый цвет и быстро чернеет.
Применяют данный минерал в основном как сырье. Из него получают оксид и другие соединения магния, флюсы, различные огнеупорные материалы. Но брусит можно применять и без какой-либо обработки. Так, этот минерал используют для очистки газов от хлора и для сорбционного фильтрования воды.
Получение
Основная реакция получения нерастворимых гидроксидов – это реакция взаимодействия щелочей с солями магния. Например, при взаимодействии сульфата магния с гидроксидом натрия. Это хорошая иллюстрация. А еще пример – при взаимодействии хлорида магния и гидроксида калия.
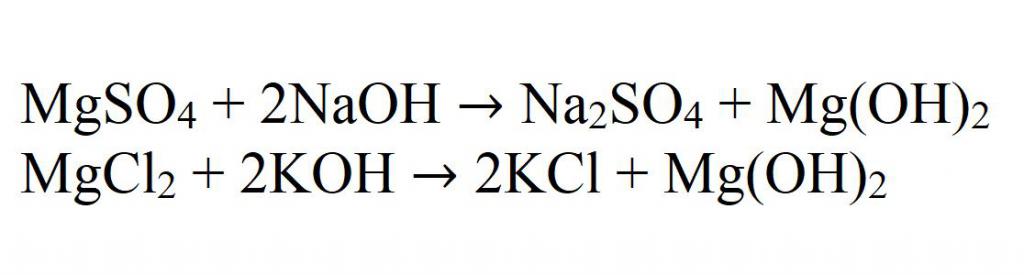
В ионном виде все подобные реакции записываются как:
Mg2+ + OH- → Mg(OH)2
При взаимодействии магния или его оксида с водой может также получаться гидроксид. Данная реакция идет очень медленно и только при нагревании.
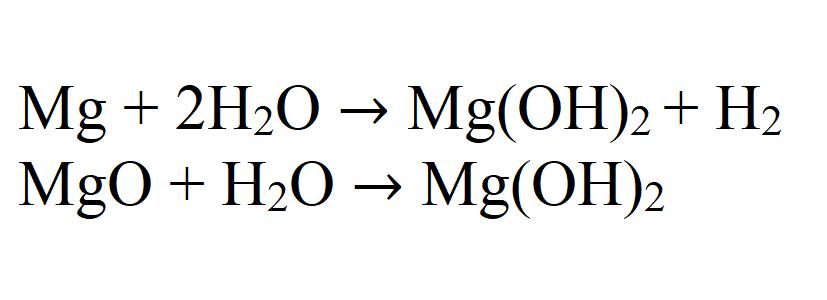
Существует такой достаточно распространенный минерал – доломит. С химической точки зрения он представляет смесь карбоната кальция и магния. При обработке этого минерала водным раствором хлорида магния при нагревании в осадок выпадает нерастворимый гидроксид:
MgCO3·CaCO3 + 2H2O + MgCl2 → Mg(OH)2 + CaCl2 + 2CO2
Физические свойства
В сухом виде гидроксид магния представляет собой белое кристаллическое вещество. Не имеет запаха, но ему присущ вкус щелочи. Он малорастворим в воде (всего 0,6 мг на 100 мл воды). Но даже несмотря на это, его водные растворы имеют слабощелочную среду и окрашивают индикаторы в соответствующие цвета. Зато данное соединение растворяется в растворах солей аммония. Оно не плавится, так как при температуре 480 oC разлагается на оксид магния и воду, как и любое другое нерастворимое основание. Плотность при нормальных условиях: 2,4 г/см3.
Химические свойства
Гидроксид магния – типичное нерастворимое основание. Это и определяет его химические свойства. Так, например, реагирует гидроксид магния с кислотами, кислотными оксидами и неметаллами:
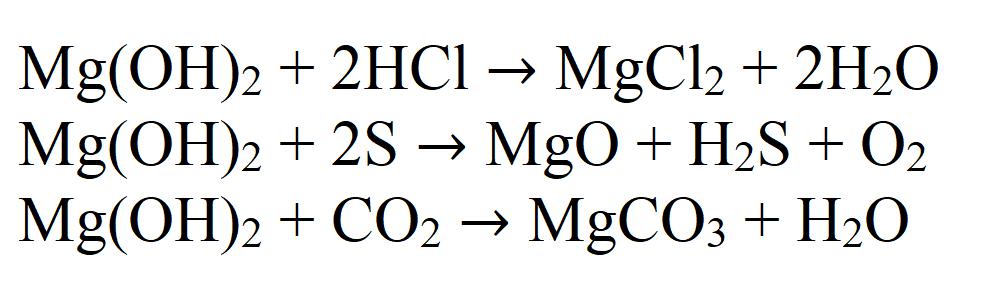
Из-за последней реакции он имеет склонность поглощать углекислый газ прямо из воздуха с образованием карбоната, поэтому хранить данное вещество длительное время открытым не рекомендуется.
Взаимодействует также и с солями, если в результате реакции получается осадок или газ:
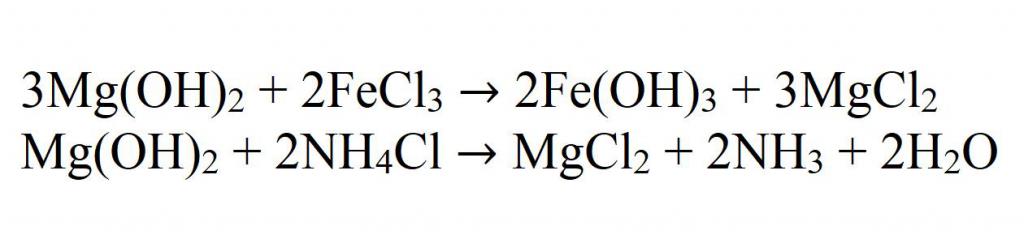
Как уже было указано выше, при нагревании идет разложение гидроксида магния по уравнению:
Mg(OH)2 → H2O + MgO
Что касается образования комплексных соединений, где катион магния выступал бы в качестве лиганда, то на этот счет имеются противоречивые сведения. В одних источниках указывается, что магний не склонен к их образованию, и существуют лишь только неустойчивые соединения с галогенидами магния. В других источниках указывается, что гидроксид магния может реагировать с горячими щелочами с образованием гидромагнезатов:
Mg(OH)2 + 2NaOH → Na2[Mg(OH)4]
Применение в медицине
В медицине суспензии на основе гидроксида магния используются как антацидное средство. Этому способствуют основные свойства. Попадая в желудок, гидроксид магния снижает его кислотность, нейтрализуя соляную кислоту. Применяется при гастритах, язвенной болезни желудка и двенадцатиперстной кишки. Препараты на его основе не снижают кислотно-щелочное равновесие и не нарушают секрецию соляной кислоты. Но даже несмотря на это, препарат имеет ряд ограничений и противопоказан людям с гиперчувствительностью к гидроксиду магния.
Продуктом взаимодействия гидроксида магния и соляной кислоты желудочного сока является хлорид магния. Он является сильным слабительным (действие наступает через 2-6 часов). Поэтому гидроксид магния является активным компонентом некоторых препаратов этой области. Избыток магния в организме легко выводится почками, но если человек страдает какими-либо болезнями этих органов, то он может получить избыток магния в организме при приеме препаратов (гипермагнемия).
Еще одно свойство данного соединения – расслабление мускулатуры. Иногда препараты, содержащие гидроксид магния, прописывают женщинам с угрозой выкидыша.
Применение в других отраслях
Гидроксид магния применяется и в пищевой промышленности как добавка Е528. В продуктах он регулирует кислотность и стабилизирует цвет. Еще применяют гидроксид магния для связывания диоксида серы, появление которого нежелательно в пищевых продуктах. Применяют его при производстве консервированных овощей, соусов, маринада и сыра. Эта добавка считается безвредной, но она запрещена в Австралии, Великобритании и Новой Зеландии.
Также гидроксид магния применяется как огнезащитная добавка в полимеры (ПВХ, полиолефины), как добавка в моющие средства и зубные пасты, для рафинирования сахара и очистки сточных вод.
Получаемый из гидроксида магния оксид – довольно полезное соединение. Оно способно выдерживать температуру около 3000 градусов, поэтому его используют как огнеупор. Так, его добавляют в кирпичи, из которых потом делают доменные печи. Используют оксид магния и как сорбент для очистки нефтепродуктов. Абразивные способности данного соединения также высоки. С помощью него очищают и полируют поверхности деталей в электронной промышленности.
Источник
Гидроксид магния, характеристика, свойства и получение, химические реакции.
Гидроксид магния – неорганическое вещество, имеет химическую формулу Mg(OH)2.
Краткая характеристика гидроксида магния
Физические свойства гидроксида магния
Получение гидроксида магния
Химические свойства гидроксида магния
Химические реакции гидроксида магния
Применение и использование гидроксида магния
Краткая характеристика гидроксида магния:
Гидроксид магния – неорганическое вещество белого цвета.
Химическая формула гидроксида магния Mg(OH)2.
Практически нерастворим в воде. Является слабым основанием, даже ничтожная его часть, растворившаяся в воде, сообщает раствору слабощелочную реакцию.
Поглощает углекислый газ и воду из воздуха с образованием основного карбоната магния.
Встречается в природе в виде минерала брусита.
Физические свойства гидроксида магния:
| Наименование параметра: | Значение: |
| Химическая формула | Mg(OH)2 |
| Синонимы и названия иностранном языке | potassium hydroxide (англ.) magnesium hydroxide (англ.) брусит (рус.) |
| Тип вещества | неорганическое |
| Внешний вид | бесцветные тригональные кристаллы |
| Цвет | белый |
| Вкус | —* |
| Запах | — |
| Агрегатное состояние (при 20 °C и атмосферном давлении 1 атм.) | твердое вещество |
| Плотность (состояние вещества – твердое вещество, при 20 °C), кг/м3 | 2344,6 |
| Плотность (состояние вещества – твердое вещество, при 20 °C), г/см3 | 2,3446 |
| Температура разложения, °C | 350 |
| Молярная масса, г/моль | 58,35 |
* Примечание:
— нет данных.
Получение гидроксида магния:
Гидроксид магния получают в результате следующих химических реакций:
- 1. в результате взаимодействия металлического магния с парами воды:
Mg + 2H2O → Mg(OH)2 + H2.
- 2. в результате взаимодействия оксида магния и воды:
MgO + H2O → Mg(OH)2 (t = 100-125 °C).
- 3. в результате взаимодействия растворимых солей магния с щелочью:
MgCl2 + 2NaOH → Mg(OH)2 + 2NaCl,
Mg(NO3)2 + 2KOH → Mg(OH)2 + 2KNO3.
При этом гидроксид магния выпадает в виде осадка.
- 4. в результате взаимодействия хлорида магния с обожженным доломитом:
MgCl2 + CaO·MgO + 2H2O → 2Mg(OH)2 + CaCl2.
При этом гидроксид магния выпадает в виде осадка.
Химические свойства гидроксида магния. Химические реакции гидроксида магния:
Гидроксид магния является основным основание, т. е. обладает как основными свойствами.
Гидроксид магния — слабое малорастворимое основание.
Химические свойства гидроксида магния аналогичны свойствам гидроксидов других основных металлов. Поэтому для него характерны следующие химические реакции:
1. реакция гидроксида магния с гидроксидом натрия:
Mg(OH)2 + 2NaOH → Na2[Mg(OH)4] (t = 100 °C).
В результате реакции образуется тетрагидроксомагнезиат натрия. В ходе реакции используется насыщенный раствор гидроксида натрия.
2. реакция гидроксида магния с угольной кислотой:
Mg(OH)2 + H2СO3 → MgСO3 + 2H2O.
В результате реакции образуются карбонат магния и вода.
3. реакция гидроксида магния с ортофосфорной кислотой:
Mg(OH)2 + 2H3PO4 → Mg(H2PO4)2 + H2O,
Mg(OH)2 + H3PO4 → MgHPO4 + 2H2O,
3Mg(OH)2 + 2H3PO4 → Mg3(PO4)2 + 6H2O.
В результате реакции образуются в первом случае — дигидроортофосфат магния и вода, во втором – гидроортофосфат магния и вода, в третьем – ортофосфат магния и вода.
4. реакция гидроксида магния с азотной кислотой:
Mg(OH)2 + 2HNO3 → Mg(NO3)2 + 2H2O.
В результате реакции образуются нитрат магния и вода.
Аналогично проходят реакции гидроксида магния и с другими кислотами.
5. реакция гидроксида магния с фтороводородом:
Mg(OH)2 + 2HF → MgF2 + 2H2O.
В результате реакции образуются фторид магния и вода.
6. реакция гидроксида магния с бромоводородом:
Mg(OH)2 + 2HBr → MgBr2 + 2H2O.
В результате реакции образуются бромид магния и вода.
7. реакция гидроксида магния с йодоводородом:
Mg(OH)2 + 2HI → MgI2 + 2H2O.
В результате реакции образуются йодид магния и вода.
8. реакция термического разложения гидроксида магния:
Mg(OH)2 → MgO + H2O (t = 350 °C).
В результате реакции образуются оксид магния и вода.
9. реакция гидроксида магния с пероксидом водорода:
H2O2 + Mg(OH)2 → MgO2 + 2H2O (t < 20 °C).
В результате реакции образуются пероксид магния и вода. В ходе реакции используется концентрированный раствор пероксида водорода.
10. реакция гидроксида магния с оксидом серы:
Mg(OH)2 + SO3 → MgSO4 + 2H2O.
В результате реакции образуются сульфат магния и вода.
11. реакция гидроксида магния с оксидом углерода:
Mg(OH)2 + 2CO2 → Mg(HCO3)2.
В результате реакции образуется гидрокарбонат магния. В ходе реакции гидроксид магния используется в виде суспензии.
12. реакция гидроксида магния с оксидом углерода:
Mg(OH)2 + 2N2O5 → Mg(NO3)2 + 2HNO3 (t = 40-60 °C).
В результате реакции образуются нитрат магния и азотная кислота.
Применение и использование гидроксида магния:
Гидроксид магния используется при очистке воды (как флокулянт), в моющих средствах (как добавка), в качестве наполнителя в зубной пасте, для рафинирования сахара, в качестве пищевой добавки (Е528).
Примечание: © Фото //www.pexels.com, //pixabay.com
карта сайта
гидроксид магния реагирует кислота 1 2 3 4 5 вода
уравнение реакций соединения реакции масса взаимодействие гидроксида магния
Коэффициент востребованности 5
comments powered by HyperComments
Источник публикации ©МИА «Россия сегодня»
Источник
