Какие свойства проявляет азот окислительные или восстановительные

3. Химические свойства соединений азота с точки зрения изменения степеней окисления
Правило 3.1. Аммиак в реакциях, как правило, окисляется до азота:
4NH3 + 3O2 → 2N2 + 6H2O (t)
8NH3 + 3Cl2 → N2 + 6NH4Cl (в атмосфере хлора)
2NH3 + 3CuO → 3Cu + N2 + 6H2O
2NH4Cl + 4CuO → 3Cu + N2 + CuCl2 + 4H2O
2NH3 + 3H2O2 → N2 + 6H2O (t)
2NH3 + 2K2FeO4 + 5H2SO4 → Fe2(SO4)3 + N2 + 2K2SO4 + 8H2O
8NH3 + 3KBrO4 → 3KBr + 4N2 + 12H2O
2NH3 + 3KClO → 3KCl + N2 + 3H2O
4NH3 + 3Ca(ClO)2 → 3CaCl2 + 2N2 + 6H2O
2NH3 + 2NaMnO4 → 2MnO2 + N2 + 2NaOH + 2H2O
2NH3 + 6NaMnO4 + 6NaOH → 6Na2MnO4 + N2 + 6H2O
2NH3×H2O + 2KMnO4 → 2MnO2 + N2 + 2KOH + 4H2O
Исключения:
Чтобы легко запомнить следующие реакции, нужно помнить, что нитрат аммония разлагается при нагревании на оксид азота (I) и воду
(NH4NO3 → N2O + 2H2O):
NH4Cl + KNO3 → N2O + KCl + H2O
А также нужно помнить термическое разложение нитрита аммония на азот и воду (NH4NO2 → N2 + 2H2O):
NH4Cl + NaNO2 → N2 + NaCl + 2H2O
Реакции термического разложения нитрата и нитрита аммония также часто встречаются на экзамене.
В присутствии катализатора аммиак окисляется кислородом до оксида азота (II), а не простого вещества:
4NH3 + 5O2 → 2NO + 6H2O (t, Pt)
Правило 3.2. Нитриды (и для аналогии фосфиды) активных металлов легко реагируют с водой и растворами кислот:
1. Реакции с водой:
Mg3N2 + H2O → 3Mg(OH)2 + 2NH3
Na3N + H2O → NaOH + NH3
Ca3P2 + 6H2O → 3Ca(OH)2 +2PH3
2. В реакциях с кислотами образуются соли (в случае нитридов) или фосфин (в случае фосфидов):
Ca3N2 + HCl → 3CaCl2 + 2NH4Cl
Zn3P2 + 6HCl → 3ZnCl2 + 2PH3
Азотная кислота
Правило 3.3. Чем более разбавленной является кислота, тем более сильным окислителем она является.
Изменение степени окисления азота в реакциях с сильным восстановителем:
N+5 + 8e → N–3 (NH3 или NH4NO3) очень разбавленная HNO3
N+5 + 5e → N0 (N2) разбавленная HNO3
N+5 + 4e → N+1 (N2O) разбавленная HNO3, концентрированная
Изменение степени окисления азота в реакциях со слабым восстановителем:
N+5 + 3e → N+2 (NO) разбавленная HNO3
N+5 + 1e → N+4 (NO2) концентрированная HNO3
Восстановители:
Сильные:
- Металлы от Li до Al
Слабые:
- Металлы, начиная с Fe
- Неметаллы
- Соли (если можем окислить)
- Оксиды (если можем окислить)
- HI и йодиды, H2S и сульфиды
10HNO3(оч. разб.) + 4Mg → 4Mg(NO3)2 + NH4NO3 + 3H2O
10HNO3(разб.) + 4Mg → 4Mg(NO3)2 + N2O + 5H2O (возможно образование N2)
8HNO3(разб.) + 3Cu → 3Cu(NO3)2 + 2NO + 4H2O
4HNO3(конц.) + 3Cu → 3Cu(NO3)2 + 2NO2 + 2H2O
С неметаллами образуются соответствующие кислоты:
10HNO3(конц.) + I2 → 2HIO3 + 10NO2 + 4H2O (t) (из галогенов реакция идет только с йодом)
4HNO3(конц.) + C → CO2 + 4NO2 + 2H2O
5HNO3(конц.) + P → H3PO4 + 5NO2 + H2O
5HNO3(разб.) + 3P +2H2O → 3H3PO4 + 5NO
6HNO3(конц.) + S → H2SO4 + 6NO2 + 2H2O
2HNO3(разб.) + S → H2SO4 + 2NO
Окисляем анион:
8HNO3(к) + H2S → H2SO4 + 8NO2 + 4H2O
8HNO3(к) + Na2S → Na2SO4 + 8NO2 + 4H2O
4HNO3(конц.) + CuS → Cu(NO3)2 + S + 2NO2 + 2H2O
8HNO3(конц.) + CuS → CuSO4 + 8NO2 + 4H2O
8HNO3 + Cu2S → 2Cu(NO3)2 + S + 4NO2 + 4H2O
12HNO3 + Cu2S → CuSO4 + Cu(NO3)2 + 10NO2 + 6H2O
16HNO3(к) + Mg3P2 → Mg3(PO4)2 + 16NO2 + 8H2O
16HNO3(к) + Ca(HS)2 → H2SO4 + CaSO4 + 16NO2 + 8H2O
8HNO3(к) + AlP  → AlPO4 + 8NO2 + 4H2O
В избытке кислоты фосфаты растворяются:
11HNO3(к, изб.) + AlP → H3PO4 + Al(NO3)3 + 8NO2 + 4H2O
Окисляем металл соли или оксида:
10HNO3(к) + Fe3O4 → 3Fe(NO3)3 + NO2 + 5H2O
4HNO3(к) + FeO → Fe(NO3)3 + NO2 + 2H2O
HNO3(к) + FeSO4 → Fe(NO3)3 + NO2 + H2SO4 + H2O
4HNO3(к) + CrCl2 → Cr(NO3)3 + NO2 + 2HCl + H2O (ионы Cl– азотная кислота окислить не может)
Одновременное окисление катиона и аниона:
14HNO3(к) + Cu2S → H2SO4 + 2Cu(NO3)2 + 10NO2 + 6H2O
Нитраты
Правило 3.4. С металлами (Al, Zn, Mg) нитраты восстанавливаются до аммиака:
3NaNO3 + 8Al + 5NaOH +18H2O → 3NH3 + 8Na[Al(OH)4]
NaNO3 + 4Zn + 7NaOH + 6H2O → NH3 + 4Na2[Zn(OH)4]
KNO3 + 4Mg + 6H2O → NH3 + 4Mg(OH)2 + KOH
Правило 3.5. При сплавлении в щелочной среде нитраты восстанавливаются до нитритов:
3NaNO3 + Cr2O3 + 4KOH → 3NaNO2 + 2K2CrO4 + 2H2O
3NaNO3 + Cr2O3 + 2Na2CO3 → 3NaNO2 + 2Na2CrO4 + 2CO2
KNO3 + MnO2 + 2KOH → KNO2 + K2MnO4 + H2O
KNO3 + MnO2 + K2CO3 → KNO2 + K2MnO4 + CO2
2NaNO3 + FeSO4 + 4NaOH → 2NaNO2 + Na2FeO4 + Na2SO4 + 2H2O
3NaNO3 + Fe2O3 + NaOH → 3NaNO2 + 2Na2FeO4 + 2H2O
3KNO3 + Fe + 2KOH → 3KNO2 + K2FeO4 + H2O
Правило 3.6. Неметаллами нитраты восстанавливаются до азота либо нитрита:
2KNO3 + C → 2KNO2 + 2KNO2 + CO2
2KNO3 + S → 2KNO2 + SO2
Правило 3.7. С солями аммония, по сути, идет разложение нитрата аммония:
KNO3 + NH4Cl → N2O + KCl + 2H2O (NH4NO3 → N2O + 2H2O)
Правило 3.8. В случае нитрата слабого металла именно метал будет окислителем, а не азот:
8AgNO3 + PH3 + 4H2O → Ag + H3PO4 + HNO3
Правило 3.9. Термическое разложение нитратов:
MNO3 → MNO2 + O2 M – металл, находящийся в ряду напряжений металлов левее Mg, исключая Li.
MNO3 → MO + NO2 + O2 M – металл, находящийся в ряду напряжений металлов от Mg до Cu (Mg и Cu включительно), а также Li.
MNO3 → M + NO2 + O2 M – металл, находящийся в ряду напряжений металлов правее Cu.
Нитриты
Правило 3.11. Сильными окислителями нитриты окисляются до нитратов:
3KNO2 + 2CrO3 + 3H2SO4 → 3KNO3 + Cr2(SO4)3 + 3H2O
3KNO2 + K2Cr2O7 + 4H2SO4 → 3KNO3 + Cr2(SO4)3 + K2SO4 + 4H2O
NaNO2 + 2KMnO4 + 2KOH → NaNO3 + 2K2MnO4 + H2O
3KNO2 + 2KMnO4 + H2O → 3KNO3 + 2MnO2 + 2KOH
KNO2 + H2O2 → KNO3 + H2O
KNO2 + I2 + H2O → KNO3 + 2HI
Правило 3.12. С восстановителями нитриты восстанавливаются до N2 или NO:
1) С солями аммония, по сути, идет разложение нитрита аммония:
NaNO2 + NH4Cl → N2 + NaCl + 2H2O (NH4NO2 → N2 + 2H2O)
Ca(NO2)2 + (NH4)2SO4 → 2N2 + CaSO4 + 4H2O
2) Соединениями I–, Fe2+ и др. нитриты восстанавливаются до оксида азота (II):
2KNO2 + 2KI + 2H2SO4 → 2NO + I2 + 2K2SO4 + 2H2O
HNO2 + 2HI → 2NO + I2 + 2H2O.
Оксиды азота
Правило 3.14. Оксид азота (IV), как правило, восстанавливается до NO или N2:
2NO2 + P2O3 + 4KOH → 2NO + 2K2HPO4 + H2O
6NO2 + FeI2 → Fe(NO3)3 + I2 + 3NO
10NO2 + 4P → P2O5 + 10NO (возможно образование N2)
NO2 + SO2 → SO3 + NO
2NO2 + 2C → N2+ 2CO2
2NO2 + 2S → N2 + 2SO2
2NO2 + 4Cu → N2 + 4CuO
Правило 3.15. Оксид азота (IV) диспропорционирует в реакциях с водой и растворами щелочей и карбонатов щелочных металлов:
Т.к. оксиду NO2 соответствуют две кислоты, при взаимодействии с щелочью или карбонатами щелочных металлов образуются две соли: нитрат и нитрит соответствующего металла:
2NO2 + 2NaOH → NaNO2 + NaNO3 + H2O 2NO2 + Na2CO3 → NaNO3 + NaNO2 + CO2
4NO2 + 2Ba(OH)2 → Ba(NO2)2 + Ba(NO3)2 + 2H2O
3NO2 + H2O → 2HNO3 + NO (растворение газа в воде в отсутствии кислорода)
В аналогичных реакциях с кислородом образуются только соединения с N+5 :
4NO2 + O2 + 4NaOH → 4NaNO3 + 2H2O
4NO2 + O2 + 2H2O → 4HNO3 (растворение в избытке кислорода)
Правило 3.16. Оксид азота (II), как правило, окисляется до N+5 :
2NO + 3KClO + 2KOH → 2KNO3 + 3KCl + H2O
8NO + 3HClO4 + 4H2O → 8HNO3 + 3HCl
14NO + 6HBrO4 + 4H2O → 14HNO3 + 3Br2
Другие реакции:
2NO + O2 → 2NO2(идет самопроизвольно на воздухе)
2NO + 2SO2 → N2 + 2SO3
2NO + 2Cu → N2 + 2CuO (500-600°C).
Правило 3.17. Как и все оксиды азота, N2O является окислителем, способным окислять металлы:
N2O + Cu → CuO + N2
N2O + Cu2O → 2CuO + N2.
Источник
Азот – неметаллический элемент Va группы периодической таблицы Д.И. Менделеева. Составляет 78% воздуха. Входит в состав
белков, являющихся важной частью живых организмов.
Температура кипения азота составляет -195,8 °C. Однако быстрого замораживания объектов, которое часто демонстрируют в
кинофильмах, не происходит. Даже для заморозки растения нужно продолжительное время, это связано с низкой теплоемкостью
азота.
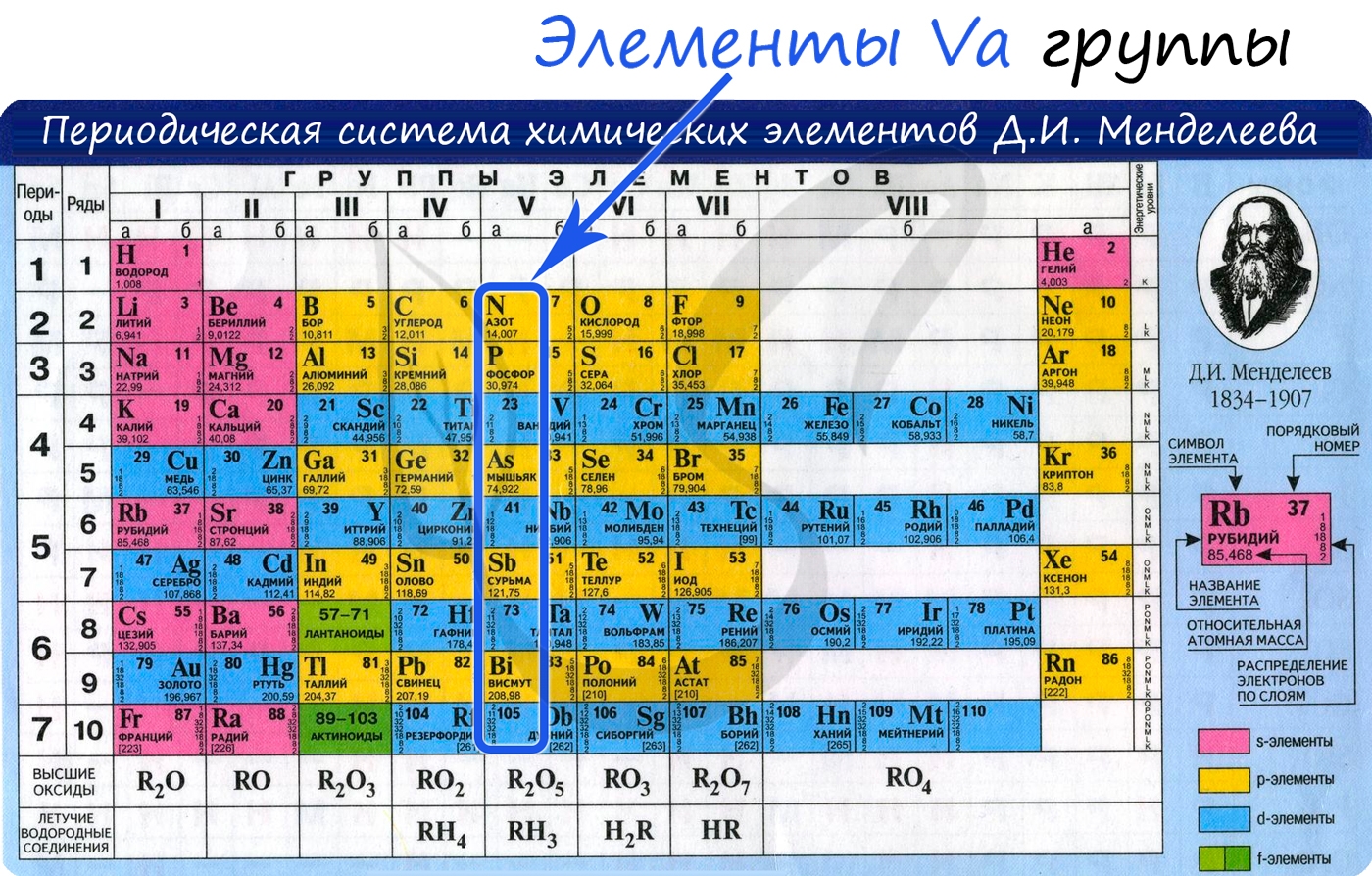
Общая характеристика элементов Va группы
От N к Bi (сверху вниз в периодической таблице) происходит увеличение: атомного радиуса, металлических, основных, восстановительных свойств.
Уменьшается электроотрицательность, энергия ионизация, сродство к электрону.
Азот, фосфор и мышьяк являются неметаллами, сурьма – полуметалл, висмут – металл.
Электронные конфигурации у данных элементов схожи, так как они находятся в одной группе (главной подгруппе!), общая формула ns2np3:
- N – 2s22p3
- P – 3s23p3
- As – 4s24p3
- Sb – 5s25p3
- Bi – 6s26p3
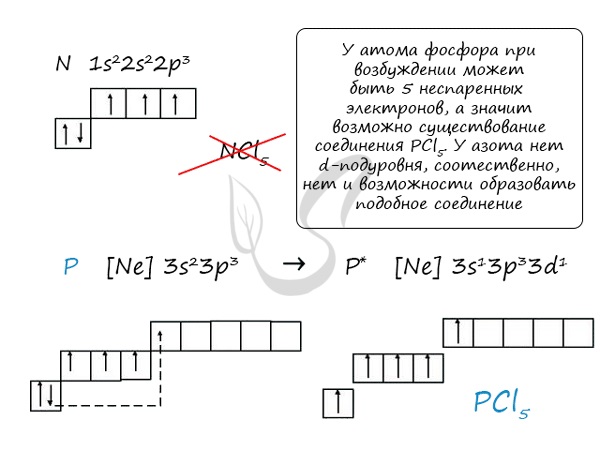
Основное и возбужденное состояние азота
При возбуждении атома азота электроны на s-подуровне распариваются и переходят на p-подуровень. Поскольку азот находится во втором периоде, то
3ий уровень у него отсутствует, что проявляется в особенностях электронной конфигурации возбужденного состояния.
Сравнивая возможности перемещения электронов у азота и фосфора, разница становится очевидна.
Природные соединения
В природе азот встречается в виде следующих соединений:
- Воздух – во вдыхаемом нами воздухе содержится 78% азота
- Азот входит в состав нуклеиновых кислот, белков
- KNO3 – индийская селитра, калиевая селитра
- NaNO3 – чилийская селитра, натриевая селитра
- NH4NO3 – аммиачная селитра (искусственный продукт, в природе не встречается)
Селитры являются распространенными азотными удобрениями, которые обеспечивают быстрый рост и развитие растений, повышают урожайность. Однако,
следует строго соблюдать правила их применения, чтобы не превысить допустимые концентрации.

Получение
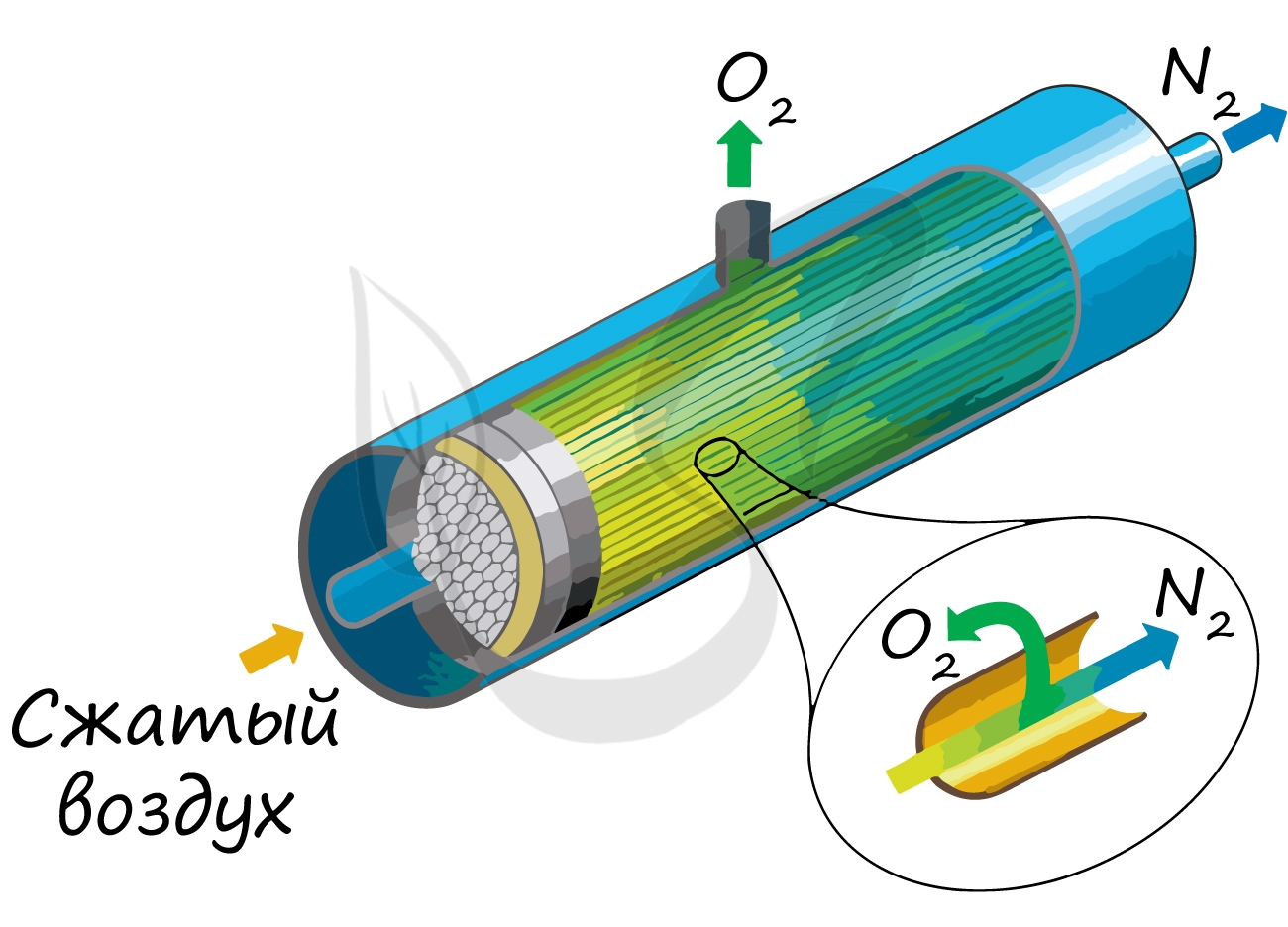
В промышленности азот получают путем сжижения воздуха. В дальнейшем путем испарения их сжиженного воздуха получают азот.
Применяют и метод мембранного разделения, при котором через специальный фильтр из сжатого воздуха удаляют кислород.
В лаборатории методы не столь экзотичны. Чаще всего получают азот разложением нитрита аммония
NH4NO2 → (t) N2 + H2O
Также азот можно получить путем восстановления азотной кислоты активными металлами.
HNO3(разб.) + Zn → Zn(NO3)2 + N2 + H2O

Химические свойства
Азот восхищает – он принимает все возможные для себя степени окисления от -3 до +5.

Молекула азота отличается большой прочностью из-за наличия тройной связи. Вследствие этого многие реакции эндотермичны: даже горение
азота в кислороде сопровождается поглощением тепла, а не выделением, как обычно бывает при горении.

- Реакция с металлами
- Реакция с неметаллами
Без нагревания азот взаимодействует только с литием. При нагревании реагирует и с другими металлами.
N2 + Li → Li3N (нитрид лития)
N2 + Mg → (t) Mg3N2
N2 + Al → (t) AlN
Важное практическое значение имеет синтез аммиака, который применяется в дальнейшим при изготовлении удобрений, красителей, лекарств.
N2 + H2 ⇄ (t, p) NH3
Аммиак
Бесцветный газ с резким едким запахом, раздражающим слизистые оболочки. Раствор концентрацией 10% аммиака применяется в медицинских целях,
называется нашатырным спиртом.
Получение
В промышленности аммиак получают прямым взаимодействием азота и водорода.
N2 + H2 ⇄ (t, p) NH3
В лабораторных условиях сильными щелочами действуют на соли аммония.
NH4Cl + NaOH → NH3 + NaCl + H2O
Химические свойства
Аммиак проявляет основные свойства, окрашивает лакмусовую бумажку в синий цвет.
- Реакция с водой
- Основные свойства
- Восстановительные свойства
Образует нестойкое соединение – гидроксид аммония, слабое основание. Оно сразу же распадается на воду и аммиак.
NH3 + H2O ⇄ NH4OH
Как основание аммиак способен реагировать с кислотами с образованием солей.
NH3 + HCl → NH4Cl (хлорид аммония)
NH3 + HNO3 → NH4NO3 (нитрат аммония)

Поскольку азот в аммиаке находится в минимальной степени окисления -3 и способен только ее повышать, то аммиак проявляет выраженные
восстановительные свойства. Его используют для восстановления металлов из их оксидов.
NH3 + FeO → N2↑ + Fe + H2O
NH3 + CuO → N2↑ + Cu + H2O
Горение аммиака без катализатора приводит к образованию азота в молекулярном виде. Окисление в присутствии катализатора сопровождается
выделением NO.
NH3 + O2 → (t) N2 + H2O
NH3 + O2 → (t, кат) NO + H2O

Соли аммония
Получение
NH3 + H2SO4 → NH4HSO4 (гидросульфат аммония, избыток кислоты)
3NH3 + H3PO4 → (NH4)3PO4
Химические свойства
Помните, что по правилам общей химии, если по итогам реакции выпадает осадок, выделяется газ или образуется вода – реакция идет.
- Реакции с кислотами
- Реакции с щелочами
- Реакции с солями
- Реакция гидролиза
- Реакции разложения
NH4Cl + H2SO4 → (NH4)2SO4 + HCl↑
В реакциях с щелочами образуется гидроксид аммония – NH4OH. Нестойкое основание, которое легко распадается на воду и аммиак.
NH4Cl + KOH → KCl + NH3 + H2O
(NH4)2SO4 + BaCl2 = BaSO4↓ + NH4Cl
В воде ион аммония подвергается гидролизу с образованием нестойкого гидроксида аммония.
NH4+ + H2O ⇄ NH4OH + H+
NH4OH ⇄ NH3 + H2O
NH4Cl → (t) NH3↑ + HCl↑
(NH4)2CO3 → (t) NH3↑ + H2O + CO2↑
NH4NO2 → (t) N2↑ + H2O
NH4NO3 → (t) N2O↑ + H2O
(NH4)3PO4 → (t) NH3↑ + H3PO4

Оксид азота I – N2O
Закись азота, веселящий газ – N2O – обладает опьяняющим эффектом. Несолеобразующий оксид. При н.у. является бесцветным газом с приятным
сладковатым запахом и привкусом. В медицине применяется в больших концентрациях для ингаляционного наркоза.

Получают N2O разложением нитрата аммония при нагревании:
NH4NO3 → N2O + H2O
Оксид азота I разлагается на азот и кислород:
N2O → (t) N2 + O2
Оксид азота II – NO
Окись азота – NO. Несолеобразующий оксид. При н.у. бесцветный газ, на воздухе быстро окисляется до оксида азота IV.
Получение
В промышленных масштабах оксид азота II получают при каталитическом окислении аммиака.
NH3 + O2 → (t, кат) NO + H2O
В лабораторных условиях – в ходе реакции малоактивных металлов с разбавленной азотной кислотой.
Cu + HNO3(разб.) → Cu(NO3)2 + NO + H2O
Химические свойства
На воздухе быстро окисляется с образованием бурого газа – оксида азота IV – NO2.
NO + O2 → NO2

Оксид азота III – N2O3
При н.у. жидкость синего цвета, в газообразной форме бесцветен. Высокотоксичный, приводит к тяжелым ожогам кожи.

Получение
Получают N2O3 в две стадии: сначала реакцией оксида мышьяка III с азотной кислотой, затем
охлаждением полученной смеси газов до температуры – 36 °C.
As2O3 + HNO3 → H3AsO4 + NO↑ + NO2↑
При охлаждении газов образуется оксид азота III.
NO + NO2 → N2O3
Химические свойства
Является кислотным оксидом. соответствует азотистой кислота – HNO2, соли которой называются нитриты (NO2-).
Реагирует с водой, основаниями.
H2O + N2O3 → HNO2
NaOH + N2O3 → NaNO2 + H2O
Оксид азота IV – NO2
Бурый газ, имеет острый запах. Ядовит.

Получение
В лабораторных условиях данный оксид получают в ходе реакции меди с концентрированной азотной кислотой. Также NO2 выделяется при
разложении нитратов.
Cu + HNO3(конц) → Cu(NO3)2 + NO2 + H2O

Cu(NO3)2 → (t) CuO + NO2 + O2
Pb(NO3)2 → (t) PbO + NO2 + O2
Химические свойства
Проявляет высокую химическую активность, кислотный оксид.
- Окислительные свойства
- Реакции с водой и щелочами
Как окислитель NO2 ведет себя в реакциях с фосфором, углеродом и серой, которые сгорают в нем.
NO2 + C → CO2 + N2
NO2 + P → P2O5 + N2
Окисляет SO2 в SO3 – на этой реакции основана одна из стадий получения серной кислоты.
SO2 + NO2 → SO3 + NO
Оксид азота IV соответствует сразу двум кислотам – азотистой HNO2 и азотной HNO3. Реакции с
водой и щелочами протекают по одной схеме.
NO2 + H2O → HNO3 + HNO2
NO2 + LiOH → LiNO3 + LiNO2 + H2O
Если растворение в воде оксида проводить в избытке кислорода, образуется азотная кислота.
NO2 + H2O + O2 → HNO3

© Беллевич Юрий Сергеевич 2018-2020
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение
(в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов
без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования,
обратитесь, пожалуйста, к Беллевичу Юрию.
Источник
Азот находится в V группе главной подгруппе периодической таблицы химических элементов. Ядро атома азота окружено двумя слоями электронов: первый содержит два электрона, второй, внешний, слой – пять электронов. Таким образом, максимальное число электронов, которое может отделиться от атома азота при химических реакциях, составляет пять, а число электронов, которые могут присоединиться, равно трем.
Из всего выше сказанного следует, что неметаллические свойства азота менее выражены, чем у кислорода и серы. Однако он также способен проявлять окислительные и восстановительные свойства. Характерные степени окисления от +1 до +5. Атом азота соединяется одинарными ковалетными связями с одновалентными атомами других элементов (NH3). Для атома азота характерна чаще валентность III, т.е. чаще всего в химических реакциях азот выступает в качестве окислителя.
Молекула азота состоит из двух атомов, между которыми реализуется тройная связь, поэтому молекула очень прочная. По этой причине азот малоактивен.
I. Окислительные свойства
- Он вступает в химические взаимодействия с металлами. В нормальных условиях он реагирует только с литием, с другими металлами при повышенных температурах. Соединения металлов с азотом называются нитридами.
6Li + N2 → 2Li3N
2Fe + N2 → 2FeN - Реагирует с водородом при определенных условиях. Остановимся более подробно на этих условиях.
Давайте пропустим смесь водорода и азота через стеклянную трубку. Теперь положите в трубочку порошок железа и снова пропустите через трубочку смесь водорода и азота. При комнатной температуре мы опять не замечаем образования аммиака. Нагрейте трубку. В присутствии железного порошка теперь образуется аммиак. Это видно по запаху и по изменению цвета фенолфталеина (он становится малиновым) в поглощающей колбе, прикрепленной к выходному отверстию трубки. Железо в этой реакции не расходуется, оно служит катализатором.
Таким образом, необходимыми условиями для реакции соединения азота с водородом являются: катализатор и нагревание.
N2 + 3H2 ⟷2NH3 + Q
Данная реакция относится к равновесным химическим процессам: на примере этой реакции легче всего понять смысл скорости химической реакции и смещения химического равновесия.
II. Восстановительные свойства
При высоких температурах азот вступает в реакцию с кислородом. Пропустим через воздух электрические искры. Появляется желтое «пламя» и образуется газ с резким запахом. При температуре искры азот соединяется с кислородом, с образованием окиси азота (II).
N2 + O2 → 2NO
Азот не взаимодействует с галогенами и серой, но галогениды и сульфиды могут быть получены побочным способом. С водой, кислотами и щелочами азот так же не взаимодействует.
Смотри также:
- Номенклатура неорганических веществ
- Характерные химические свойства простых веществ – металлов: щелочных, щелочноземельных, магния, алюминия; переходных металлов (меди, цинка, хрома, железа)
- Характерные химические свойства простых веществ – неметаллов: водорода, галогенов, кислорода, серы, азота, фосфора, углерода, кремния
- Характерные химические свойства оксидов: оснóвных, амфотерных, кислотных
- Характерные химические свойства оснований и амфотерных гидроксидов
- Характерные химические свойства кислот
- Характерные химические свойства солей: средних, кислых, оснóвных; комплексных ( на примере соединений алюминия и цинка)
- Взаимосвязь различных классов неорганических веществ
Источник
