Какие свойства не характерны для галогенов
Не все знают, что под пугающим названием «галогены» зачастую скрываются распространенные в быту вещества. Не в чистом виде, но все-таки. Отдельными представителями «семейства» ежедневно пользуется каждый человек.
Приведём примеры:
На упаковке любой зубной пасты имеется словосочетание со словом «фтор». Полезен для зубной эмали.
Хлор знаком любой домохозяйке и сотруднику клининговой компании. А уж его запах знают все, кто посещал бассейн или лечебные учреждения России. Не пустой звук для советских школьников. Даже не из курса химии, а из уроков химзащиты в рамках начальной военной подготовки (НВП).
Про «бром» ходили легенды среди военнослужащих СССР. Насколько сведения достоверны – неизвестно.
Темно-коричневая бутылочка с «йодом» – постоянный спутник любителя поиграть с котенком и непоседливого ребенка. Распространенный антисептик.
Что такое галогены
Определяют, как элементы 17-ой группы таблицы Менделеева. Сторонники «старой школы» выразились бы: «главной подгруппы VII группы».
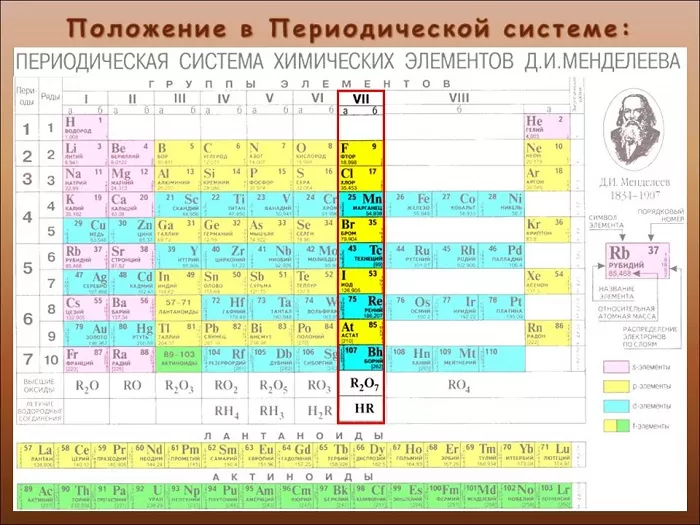
Название представляет собой компиляцию греческих слов. Означает приблизительно «солерождающий». Такое определение было дано в XIX веке британским ученым Гэмфри Дэви.
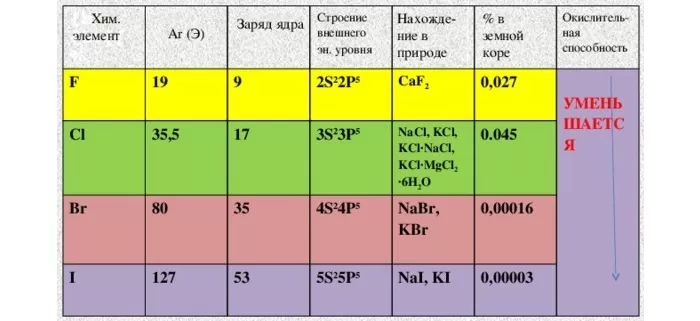
Перечень и общая характеристика галогенов

С первыми четырьмя элементами из списка некоторое знакомство имеется. Надо заметить, что вещества хоть и достаточно распространенные, но в чистом виде в природе не встречаются. Только в составе соединений.
Астат – элемент не просто редкий, а самый редкий из всех встречающихся на планете. Его «запасы» оцениваются в 1 г. Свойства доподлинно не известны. Так как из-за радиоактивности и мизерной «продолжительности жизни» в достаточных количествах выделить не получилось.
Теннессин существует скорее теоретически. На Земле, по крайней мере, не нашли. Рекордное зафиксированное (и признанное) в лаборатории количество – 6 ядер. Включая изотоп.
Зато точно известен общий принцип построения наружного энергетического уровня: ns2np5. Под «n» понимается период расположения элемента.
Легко заметить, что до «идеальных» инертов не хватает всего-то электрончика. А так хочется. Не удивительно, что так агрессивны.
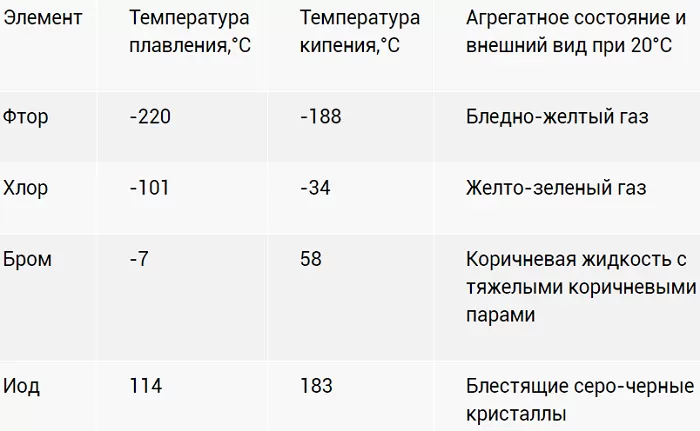
Физические свойства

Галогены – ярко выраженные неметаллы. Летучи, с характерно едким «ароматом». Причем для йода (I2) жидкое агрегатное состояние вообще не характерно. При разогреве просто испаряется фиолетовым дымком.
Хлор – настоящее боевое отравляющее вещество. И применялось в таком качестве. Попадая в незащищенные глаза и органы, образует кислоты. С соответствующими последствиями. Для летального исхода достаточно концентрации в воздухе 2 мг/л.
Насыщенность цветов с «утяжелением» ядер возрастает. Активность, напротив, падает.
В воде растворимость ограничена. Лучше ведёт себя с органическими растворителями. Растворы оригинально окрашены: от слабо желтого до фиолетового.
Химические свойства галогенов
Галогены (Hal) – мощные окислители, а фтор агрессивен настолько, что вступает в реакцию с собратьями. Происходит это при подогреве. Степень окисления «пострадавших» оказывается +1.
Общее уравнение:
![]()
Можно сказать, что F реагирует со всеми простыми субстанциями, кроме отдельных благородных газов. А так (с облучением):
![]()
Остальные элементы ряда не взаимодействуют с:
O;
N;
С (в модификации алмаза);
Pt, Au;
Xe, Kr.
С неметаллами
Водород окисляет фтор при любых условиях, со взрывом. Cl с подсветкой УФ или подогревом. Но тоже громко. Остальные только с нагреванием. Но уравнение едино:
![]()
С фосфором взаимодействуют совершенно по-разному:
∗ F до получения пентафторида. Единственный, без нагревания:
![]()
∗ хлор и бром, в зависимости от концентрации:
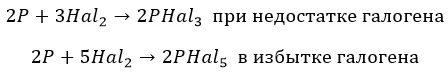
∗ йод – недостаточно мощный окислитель:
![]()
∗ с серой также не все очевидно. Но только не с фтором. Окисление максимально, но с нагревом:
![]()
∗ бром и хлор реагируют нетипично и «неохотно»:
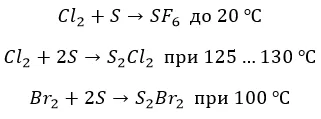
С металлами
Перед фтором ничто не устоит. Даже благородный класс, хоть и с нагревом:
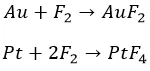
Остальные металлы прочим галогенам по силам. Не без подогрева:
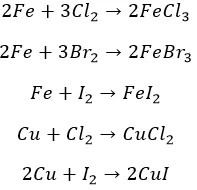
Реакции замещения
Агрессивные вытесняют «тяжелых» соседей по группе:
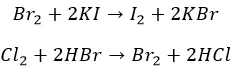
И с неметаллами не церемонятся:
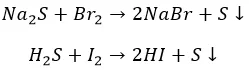
Хлор, как более активный, ведет себя несколько по-другому:
![]()
С водой
Фтор в своем репертуаре. Вода будет пылать синим пламенем и норовить плюнуть плавиковой кислотой:
![]()
Хлор с бромом гораздо спокойнее. Да и процессы нестабильны, обратимы:
![]()
Йод с водой в видимые взаимодействия не вступает.
С растворами щелочей
И в этом случае фтор проявляется как резкий окислитель:
![]()
Остальные ведут себя, как с водой. Но процесс при разных температурах проходит по разным сценариям:
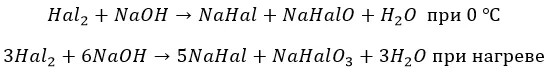
Йод реагирует только по второму варианту.
Получение
Выделить вещество настолько активное, что норовит прореагировать со всем окружающим, не так просто.
Фтор
Обычно получают из сложных солей. При интенсивном нагреве (термолиз) провоцируется распад на более простые и нужный газ.

Или электролизом KF*3HF. Аналогичный метод применяется в промышленности.
Хлор
Из соляной кислоты. Неприятно и опасно даже в условиях лаборатории:
![]()
Индустриально добывают из распространенной поваренной соли при помощи электролиза:
![]()
Бром и йод
«На коленке» – из солей. Окислителями, в кислом же окружении:
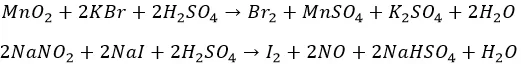
Химзаводам за сырьем ходить не надо. Морская вода, скважные жидкости. Остатки сожженных океанских/морских водорослей – настоящая йодная руда.
Применение галогенов
Как уже упоминалось, фтор применяется в лечебных и профилактических средствах. Соединения необходимы для изготовления алюминия.

Основная часть производимого хлора используется для синтеза соляной кислоты. Необходим в химической индустрии. Для сельскохозяйственных, бытовых ядохимикатов, чистящих средств, отбеливателей. Для очистителей воды.
Бром и йод применяются для медикаментов и в химической отрасли.
Заключение
О свойствах галогенов можно писать бесконечно. В данной статье не затрагивались темы взаимодействий с органическими веществами, например.
А ведь без них невозможен, скажем, фотосинтез. Одна из основ жизни. Без соляной кислоты невозможно пищеварение высших животных. Об этом мы расскажем в следующих публикациях.
Источник
| Группа → | 17 (VIIA) | ||||||
|---|---|---|---|---|---|---|---|
| ↓ Период | |||||||
| 2 |
| ||||||
| 3 |
| ||||||
| 4 |
| ||||||
| 5 |
| ||||||
| 6 |
| ||||||
| 7 |
| ||||||
Галоге́ны (от греч. ἁλός — «соль» и γένος — «рождение, происхождение»; иногда употребляется устаревшее название гало́иды) — химические элементы 17-й группы периодической таблицы химических элементов Д. И. Менделеева (по устаревшей классификации — элементы главной подгруппы VII группы)[1].
Реагируют почти со всеми простыми веществами, кроме некоторых неметаллов. Все галогены — энергичные окислители, поэтому встречаются в природе только в виде соединений. С увеличением порядкового номера химическая активность галогенов уменьшается, химическая активность галогенид-ионов F−, Cl−, Br−, I−, At− уменьшается.
К галогенам относятся фтор F, хлор Cl, бром Br, иод I, астат At, а также (формально) искусственный элемент теннессин Ts.
Все галогены — неметаллы, являются сильными окислителями. На внешнем энергетическом уровне 7 электронов. При взаимодействии с металлами возникает ионная связь, и образуются соли. Галогены (кроме фтора) при взаимодействии с более электроотрицательными элементами могут проявлять и восстановительные свойства вплоть до высшей степени окисления +7.
Этимология[править | править код]
Термин «галогены» в отношении всей группы элементов (на тот момент были известны фтор, хлор, бром и иод) был предложен в 1841 году шведским химиком Й. Берцелиусом. Первоначально слово «галоген» (в буквальном переводе с греческого — «солерод») было предложено в 1811 году немецким учёным И. Швейггером в качестве названия для недавно открытого хлора, однако в химии закрепилось название, которое предложил Г. Дэви[2].
Строение атомов и степени окисления[править | править код]
Электронная конфигурация внешней электронной оболочки атомов галогенов ns2np5: фтор — 2s22p5, хлор — 3s23p5, бром — 4s24p5, иод — 5s25p5, астат — 6s26p5.
Имея на внешней электронной оболочке 7 электронов, атомы всех галогенов легко присоединяют недостающий до завершения оболочки 1 электрон и в своих соединениях проявляют степень окисления −1. Хлор, бром, иод и астат в соединениях с более электроотрицательными элементами проявляют положительные степени окисления: +1, +3, +5, +7. Для фтора характерна постоянная степень окисления −1.
Распространённость элементов и получение простых веществ[править | править код]
Как уже было сказано выше, галогены имеют высокую реакционную способность, поэтому встречаются в природе обычно в виде соединений.
Их распространённость в земной коре уменьшается при увеличении атомного радиуса от фтора к иоду. Количество астата в земной коре измеряется граммами, а теннессин в природе отсутствует. Фтор, хлор, бром и иод производятся в промышленных масштабах, причём объёмы производства хлора значительно выше, чем трёх других стабильных галогенов.
В природе эти элементы встречаются в основном в виде галогенидов (за исключением иода, который также встречается в виде иодата натрия или калия в месторождениях нитратов щелочных металлов). Поскольку многие хлориды, бромиды и иодиды растворимы в воде, то эти анионы присутствуют в океане и природных рассолах. Основным источником фтора является фторид кальция, который очень малорастворим и находится в осадочных породах (как флюорит CaF2).
Основным способом получения простых веществ является окисление галогенидов. Высокие положительные стандартные электродные потенциалы Eo(F2/F−) = +2,87 В и Eo(Cl2/Cl−) = +1,36 В показывают, что окислить ионы F− и Cl− можно только сильными окислителями. В промышленности применяется только электролитическое окисление. При получении фтора нельзя использовать водный раствор, поскольку вода окисляется при значительно более низком потенциале (+1,32 В) и образующийся фтор стал бы быстро реагировать с водой. Впервые фтор был получен в 1886 г. французским химиком Анри Муассаном при электролизе раствора гидрофторида калия KHF2 в безводной плавиковой кислоте.
В промышленности хлор в основном получают электролизом водного раствора хлорида натрия в специальных электролизёрах. При этом протекают следующие реакции:
полуреакция на аноде:
полуреакция на катоде:
Окисление воды на аноде подавляется использованием такого материала электрода, который имеет более высокое перенапряжение по отношению к O2, чем к Cl2 (таким материалом является, в частности, RuO2).
В современных электролизёрах катодное и анодное пространства разделены полимерной ионообменной мембраной. Мембрана позволяет катионам Na+ переходить из анодного пространства в катодное. Переход катионов поддерживает электронейтральность в обеих частях электролизёра, так как в течение электролиза отрицательные ионы удаляются от анода (превращение 2Cl− в Cl2) и накапливаются у катода (образование OH−). Перемещение OH− в противоположную сторону могло бы тоже поддерживать электронейтральность, но ион OH− реагировал бы с Cl2 и сводил на нет весь результат.
Бром получают химическим окислением бромид-иона, находящегося в морской воде. Подобный процесс используется и для получения иода из природных рассолов, богатых I−. В качестве окислителя в обоих случаях используют хлор, обладающий более сильными окислительными свойствами, а образующиеся Br2 и I2 удаляются из раствора потоком воздуха.
Физические свойства галогенов[править | править код]
| Вещество | Агрегатное состояние при обычных условиях | Цвет | Запах |
|---|---|---|---|
| Фтор F2 | Газ, не сжижается при обычной температуре | Светло-жёлтый | Резкий, раздражающий |
| Хлор CI2 | Газ, сжижающийся при обычной температуре под давлением | Жёлто-зелёный | Резкий, удушливый |
| Бром Br2 | Тяжёлая летучая жидкость | Буровато-коричневый | Резкий, зловонный |
| Иод I2 | Твёрдое вещество | Тёмно-серый с металлическим блеском | Резкий |
| Астат At2 | Твёрдое вещество | Сине-чёрный с металлическим блеском | Вероятно, резкий |
| Простое вещество | Температура плавления, °C | Температура кипения, °C |
| F2 | −220 | −188 |
| Cl2 | −101 | −34 |
| Br2 | −7 | 58 |
| I2 | 113,5 | 184,885 |
| At2 | 244 | 309[3] |
Химические свойства галогенов[править | править код]
Все галогены проявляют высокую окислительную активность, которая уменьшается при переходе от фтора к теннессину. Фтор — самый активный из галогенов, реагирует со всеми металлами без исключения, многие из них в атмосфере фтора самовоспламеняются, выделяя большое количество теплоты, например:
Без нагревания фтор реагирует и со многими неметаллами (H2, S, С, Si, Р); все реакции при этом сильно экзотермические и могут протекать со взрывом, например:
При нагревании фтор окисляет все другие галогены по схеме
Hal2 + F2 = 2НalF
причём в соединениях HalF степени окисления хлора, брома, иода и астата равны +1.
Наконец, при облучении фтор реагирует даже с тяжёлыми инертными (благородными) газами:
Взаимодействие фтора со сложными веществами также протекает очень энергично. Так, он окисляет воду, при этом реакция носит взрывной характер:
Свободный хлор также очень реакционноспособен, хотя его активность и меньше, чем у фтора. Он непосредственно реагирует со всеми простыми веществами, за исключением кислорода, азота и благородных газов:
Особый интерес представляет реакция с водородом. Так, при комнатной температуре, без освещения хлор практически не реагирует с водородом, тогда как при нагревании или при освещении (например, на прямом солнечном свету) эта реакция протекает со взрывом по приведенному ниже цепному механизму:
Возбуждение этой реакции происходит под действием фотонов , которые вызывают диссоциацию молекул Cl2 на атомы — при этом возникает цепь последовательных реакций, в каждой из которых появляется частица, инициирующая начало последующей стадии.
Реакция между Н2 и Cl2 послужила одним из первых объектов исследования цепных фотохимических реакций. Наибольший вклад в развитие представлений о цепных реакциях внёс русский учёный, лауреат Нобелевской премии (1956 год) Н. Н. Семёнов.
Хлор вступает в реакцию со многими сложными веществами, например замещения и присоединения с углеводородами:
Хлор способен при нагревании вытеснять бром или иод из их соединений с водородом или металлами:
а также обратимо реагирует с водой, образуя равновесную смесь веществ, называемую хлорной водой:
Хлор может таким же образом реагировать (диспропорционировать) со щелочами:
- на холоде
- при нагревании:
Химическая активность брома меньше, чем у фтора и хлора, но все же достаточно велика в связи с тем, что бром обычно используют в жидком состоянии, и поэтому его исходные концентрации при прочих равных условиях больше, чем у хлора. Он вступает в те же реакции, что и хлор. Являясь более мягким реагентом, бром находит широкое применение в органической химии. Бром, так же как и хлор растворяется в воде и, частично реагируя с ней, образует так называемую «бромную воду».
Растворимость в воде иода — 0,3395 грамма на литр при 25 градусах Цельсия[4], это меньше, чем у брома. Водный раствор иода называется «иодной водой»[5]. Иод способен растворяться в растворах иодидов с образованием комплексных анионов:
Образующийся раствор называется раствором Люголя.
Иод существенно отличается по химической активности от остальных галогенов. Он не реагирует с большинством неметаллов, а с металлами медленно реагирует только при нагревании. Взаимодействие же иода с водородом происходит только при сильном нагревании, реакция является эндотермической и обратимой:
Таким образом, химическая активность галогенов последовательно уменьшается от фтора к астату. Каждый галоген в ряду F — At может вытеснять последующий из его соединений с водородом или металлами, то есть каждый галоген в виде простого вещества способен окислять галогенид-ион любого из последующих галогенов[6].
Астат ещё менее реакционноспособен, чем иод. Но и он реагирует с металлами (например с литием):
При диссоциации образуются не только анионы, но и катионы At+: HAt диссоциирует на:
Применение галогенов и их соединений[править | править код]
Природное соединение фтора — криолит Na3AlF6 — применяется при получении алюминия. Соединения фтора используются в качестве добавок в зубные пасты для предотвращения заболеваний кариесом.
Хлор широко используется для получения соляной кислоты, в органическом синтезе при производстве пластмасс и синтетических волокон, каучуков, красителей, растворителей и др. Многие хлорсодержащие соединения используют для борьбы с вредителями в сельском хозяйстве. Хлор и его соединения применяются для отбеливания льняных и хлопчатобумажных тканей, бумаги, обеззараживания питьевой воды. Правда, применение хлора для обеззараживания воды далеко не безопасно, для этих целей лучше использовать озон.
Простые вещества и соединения брома и иода используются в фармацевтической и химической промышленности.
Токсичность галогенов[править | править код]
Вследствие высокой реакционной способности (особенно это ярко проявляется у фтора) все галогены являются ядовитыми веществами с сильно выраженным удушающим и поражающим ткани воздействиями.
Большую опасность представляют пары и аэрозоль фтора, так как в отличие от других галогенов имеют довольно слабый запах и ощущаются только в больших концентрациях.
Примечания[править | править код]
- ↑ Periodic Table of the Elements (англ.) (недоступная ссылка). IUPAC. — PDF. Дата обращения: 25 октября 2013. Архивировано 22 августа 2015 года.
- ↑ Snelders, H. A. M. J. S. C. Schweigger: His Romanticism and His Crystal Electrical Theory of Matter (англ.) // Isis (англ.)русск. : journal. — 1971. — Vol. 62, no. 3. — P. 328. — doi:10.1086/350763.
- ↑ Бердоносов С.С. Астат // Химическая энциклопедия : в 5 т. / Гл. ред. И. Л. Кнунянц. — М.: Советская энциклопедия, 1988. — Т. 1: А—Дарзана. — 623 с. — 100 000 экз. — ISBN 5-85270-008-8.
- ↑ Стасиневич Д.С. Иод // Краткая химическая энциклопедия / Отв. ред. И. Л. Кнунянц. — М.: Советская Энциклопедия, 1963. — Т. 2. Ж—Малоновый эфир.
- ↑ Ходаков Ю.В., Эпштейн Д.А., Глориозов П.А. § 84. Фтор, бром, иод // Неорганическая химия: Учебник для 7—8 классов средней школы. — 18-е изд. — М.: Просвещение, 1987. — С. 197—199. — 240 с. — 1 630 000 экз.
- ↑ Н. Е. Кузьменко, В. В. Еремин, В. А. Попков. Начала химии. Современный курс для поступающих в вузы: учебник / Кузьменко, Н. Е.. — 16. — 107045, Москва, Луков пер., д. 8.: “Экзамен”, 2013. — С. 343—347. — 831 с. — ISBN 978-5-377-06154-0.
Литература[править | править код]
- Greenwood, Norman N. (англ.)русск.; Earnshaw, Alan. Chemistry of the Elements (неопр.). — 2nd. — Butterworth–Heinemann (англ.)русск., 1997. — ISBN 0080379419.
Источник
