Какие свойства металлов обусловлены металлической связью

Металли́ческая связь — химическая связь между атомами в металлическом кристалле, возникающая за счёт перекрытия (обобществления) их валентных электронов. Металлическая связь описывается многими физическими свойствами металлов, такими как прочность, пластичность, теплопроводность, удельное электрическое сопротивление и проводимость, непрозрачность и блеск[1][2][3][4].
Механизм металлической связи[править | править код]
В узлах кристаллической решётки расположены положительные ионы металла. Между ними беспорядочно, подобно молекулам газа, движутся электроны проводимости, происходящие из атомов металлов при образовании ионов. Эти электроны играют роль «цемента», удерживая вместе положительные ионы; в противном случае решётка распалась бы под действием сил отталкивания между ионами. Вместе с тем и электроны удерживаются ионами в пределах кристаллической решётки и не могут её покинуть. Когда металл принимает какую-либо форму или растягивается, он не разрушается, потому что ионы в его кристаллической структуре довольно легко смещаются относительно друг друга[5]. Силы связи не локализованы и не направлены. В металлах в большинстве случаев проявляются высокие координационные числа (например, 12 или 8).
Рис. 1. Расположение ионов в кристалле щелочного металла
Так, щелочные металлы кристаллизуются в кубической объёмно-центрированной решётке, и каждый положительно заряженный ион щелочного металла имеет в кристалле по восемь ближайших соседей — положительно заряженных ионов щелочного металла (рис. 1). Кулоновское отталкивание одноимённо заряженных частиц (ионов) компенсируется электростатическим притяжением к электронам связывающих звеньев, имеющих форму искажённого сплющенного октаэдра — квадратной бипирамиды, высота которой и рёбра базиса равны величине постоянной решётки aw кристалла щелочного металла (рис. 2).
Связывающие электроны становятся общими для системы из шести положительных ионов щелочных металлов и удерживают последние от кулоновского отталкивания.
Величина постоянной трансляционной решётки aw кристалла щелочного металла значительно превышает длину ковалентной связи молекулы щелочного металла, поэтому принято считать, что электроны в металле находятся в свободном состоянии:
| Щелочной металл | Li | Na | K | Rb | Cs |
|---|---|---|---|---|---|
| Постоянная решётки aw, Å[6] | 3,502 | 4,282 | 5,247 | 5,690 | 6,084 |
| Длина ковалентной связи для Me2, Å[7] | 2,67 | 3,08 | 3,92 | 4,10 | 4,30 |
Математическое построение, связанное со свойствами свободных электронов в металле, обычно отождествляют с «поверхностью Ферми», которую следует рассматривать как геометрическое место в k-пространстве, где пребывают электроны, обеспечивая основное свойство металла — проводить электрический ток[8]. Таким образом, электрический ток в металлах — это движение сорванных с орбитального радиуса электронов в поле положительно заряженных ионов, находящихся в узлах кристаллической решётки металла. Выход и вход свободных электронов в связывающее звено кристалла осуществляется через точки «0», равноудалённые от положительных ионов атомов (рис. 2).
Свободное движение электронов в металле подтверждено в 1916 году опытом Толмена и Стюарта по резкому торможению быстро вращающейся катушки с проводом — свободные электроны продолжали двигаться по инерции, в результате чего гальванометр регистрировал импульс электрического тока. Свободное движение электронов в металле обусловливает высокую теплопроводность металла и склонность металлов к термоэлектронной эмиссии, происходящей при умеренной температуре.
Колебание ионов кристаллической решётки создаёт сопротивление движению электронов по металлу, сопровождающееся разогревом металла. В настоящее время важнейшим признаком металлов считается положительный температурный коэффициент электрической проводимости, то есть понижение проводимости с ростом температуры. С понижением температуры электросопротивление металлов уменьшается, вследствие уменьшения колебаний ионов в кристаллической решётке. В процессе исследования свойств материи при низких температурах Камерлинг-Оннес открывает явление сверхпроводимости. В 1911 году ему удаётся обнаружить уменьшение электросопротивления ртути при температуре кипения жидкого гелия (4,2 К) до нуля. В 1913 году Камерлинг-Оннесу присуждается Нобелевская премия по физике со следующей формулировкой: «За исследование свойств веществ при низких температурах, которые привели к производству жидкого гелия».
Однако теория сверхпроводимости была создана позднее. В её основе лежит концепция куперовской электронной пары — коррелированного состояния связывающих электронов с противоположными спинамии и импульсами, и, следовательно, сверхпроводимость можно рассматривать как сверхтекучесть электронного газа, состоящего из куперовских пар электронов, через ионную кристаллическую решётку. В 1972 году авторам теории БКШ — Бардину, Куперу и Шрифферу присуждена Нобелевская премия по физике «За создание теории сверхпроводимости, обычно называемой БКШ-теорией».
Характерные кристаллические решётки[править | править код]
Большинство металлов образует одну из следующих высокосимметричных решёток с плотной упаковкой атомов: кубическую объемно центрированную, кубическую гранецентрированную и гексагональную.
В кубической объемно центрированной решётке (ОЦК) атомы расположены в вершинах куба и один атом в центре объёма куба. Кубическую объемно центрированную решётку имеют металлы: Pb, K, Na, Li, β-Ti, β-Zr, Ta, W, V, α-Fe, Cr, Nb, Ba и др.
В кубической гранецентрированной решётке (ГЦК) атомы расположены в вершинах куба и в центре каждой грани. Решётку такого типа имеют металлы: α-Ca, Ce, α-Sr, Pb, Ni, Ag, Au, Pd, Pt, Rh, γ-Fe, Cu, α-Co и др.
В гексагональной решётке атомы расположены в вершинах и центре шестигранных оснований призмы, а три атома — в средней плоскости призмы. Такую упаковку атомов имеют металлы: Mg, α-Ti, Cd, Re, Os, Ru, Zn, β-Co, Be, β-Ca и др.
Другие свойства[править | править код]
Свободно движущиеся электроны обусловливают высокую электро- и теплопроводность. Многие металлы обладают высокой твёрдостью, например хром, молибден, тантал, вольфрам и др. Вещества, обладающие металлической связью, часто сочетают прочность с пластичностью, так как при смещении атомов друг относительно друга не происходит разрыв связей.
Примечания[править | править код]
Источник
Металлическая связь — химическая связь, обусловленная наличием относительно свободных электронов. Характерна как для чистых металлов, так и их сплавов и интерметаллических соединений.
Механизм металлической связи
Во всех узлах кристаллической решётки расположены положительные ионы металла. Между ними беспорядочно, подобно молекулам газа движутся валентные электроны, отцепившиеся от атомов при образовании ионов. Эти электроны играют роль цемента, удерживая вместе положительные ионы; в противном случае решётка распалась бы под действием сил отталкивания между ионами. Вместе с тем и электроны удерживаются ионами в пределах кристаллической решётки и не могут её покинуть. Силы связи не локализованы и не направлены.
Поэтому в большинстве случаев проявляются высокие координационные числа (например, 12 или 8). Когда два атома металла сближаются, орбитали их внешних оболочек перекрываются, образуя молекулярные орбитали. Если подходит третий атом, его орбиталь перекрывается с орбиталями первых двух атомов, что дает еще одну молекулярную орбиталь. Когда атомов много, возникает огромное число трехмерных молекулярных орбиталей, простирающихся во всех направлениях. Вследствие многократного перекрывания орбиталей валентные электроны каждого атома испытывают влияние многих атомов.
Характерные кристаллические решётки
Большинство металлов образует одну из следующих высокосимметричных решёток с плотной упаковкой атомов: кубическую объемно центрированную, кубическую гранецентрированную и гексагональную.
В кубической объемно центрированной решётке (ОЦК) атомы расположены в вершинах куба и один атом в центре объёма куба. Кубическую объемно центрированную решётку имеют металлы: Pb, K, Na, Li, β-Ti, β-Zr, Ta, W, V, α-Fe, Cr, Nb, Ba и др.
В кубической гранецентрированной решётке (ГЦК) атомы расположены в вершинах куба и в центре каждой грани. Решётку такого типа имеют металлы: α-Ca, Ce, α-Sr, Pb, Ni, Ag, Au, Pd, Pt,Rh, γ-Fe, Cu, α-Co и др.
В гексагональной решётке атомы расположены в вершинах и центре шестигранных оснований призмы, а три атома — в средней плоскости призмы. Такую упаковку атомов имеют металлы: Mg, α-Ti, Cd, Re, Os, Ru, Zn, β-Co, Be, β-Ca и др.
Другие свойства
Свободно движущиеся электроны обусловливают высокую электро- и теплопроводность. Вещества, обладающие металлической связью, часто сочетают прочность с пластичностью, так как при смещении атомов друг относительно друга не происходит разрыв связей. Также важным свойством является металлическая ароматичность.
Металлы хорошо проводят тепло и электричество, они достаточно прочны, их можно деформировать без разрушения. Некоторые металлы ковкие (их можно ковать), некоторые тягучие (из них можно вытягивать проволоку). Эти уникальные свойства объясняются особым типом химической связи, соединяющей атомы металлов между собой – металлической связью.
Металлы в твердом состоянии существуют в виде кристаллов из положительных ионов, как бы “плавающих” в море свободно движущихся между ними электронов.
Металлическая связь объясняет свойства металлов, в частности, их прочность. Под действием деформирующей силы решетка металла может изменять свою форму, не давая трещин, в отличие от ионных кристаллов.
Высокая теплопроводность металлов объясняется тем, что если нагреть кусок металла с одной стороны, то кинетическая энергия электронов увеличится. Это увеличение энергии распространится в “ электронном море” по всему образцу с большой скоростью.
Становится понятной и электрическая проводимость металлов. Если к концам металлического образца приложить разность потенциалов, то облако делокализованных электронов будет сдвигаться в направлении положительного потенциала: этот поток электронов, движущихся в одном направлении, и представляет собой всем знакомый электрический ток.
Источник
Металлическая химическая связь характерна для металлов и их сплавов в кристаллическом состоянии. Образуется за счет обобществления валентных электронов. Для этого типа строения вещества не характерно образование направленных структурированных связей.
Следует отличать различные типы связи элементов кристаллов – металлическую, ионную и водородную, свойственную кристаллам льда.
Механизм создания металлической связи предусматривает отрыв частично свободных электронов от атома с образованием катионов с положительным зарядом, формирующих “остов” кристаллической решетки и электронного облака. При этом металлический кристалл не приобретает положительного или отрицательного заряда.
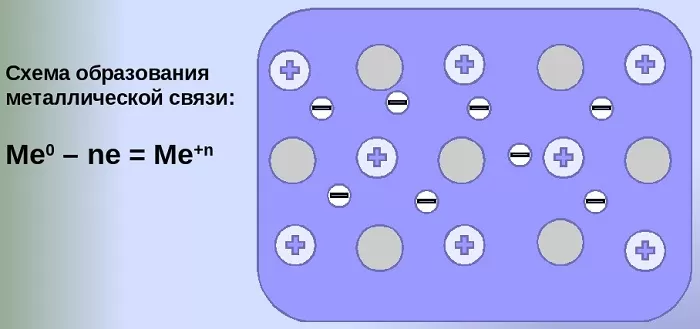
Общий случай формирования связывания металлических атомов в химии, соответствующий данному выше определению:
Me – ne⁻ ⇆ Me,
здесь n – число электронов, участвующих в образовании связи, как правило, от 1 до 3.
В левой части уравнения – атом металла, отдающий электроны, в правой – образовавшийся в результате ион.
Формула показывает, что в кристалле постоянно происходит присоединение и отдача электронов.
Схемы формирования связи на примере атомов различной валентности:
- K – e⁻ ⇆ K;
- Cu – 2e⁻ ⇆ Cu;
- Al – 3e⁻ ⇆ Al.
Отделяющиеся от атома электроны перемещаются на свободные валентные орбитали, которые обобществляются и позволяют всем электронам перемещаться в пределах кристалла. Отделение электронов выгодно атому с точки зрения энергетического баланса, так как позволяет сформировать электронно-стабильную оболочку.
Характерные кристаллические решетки
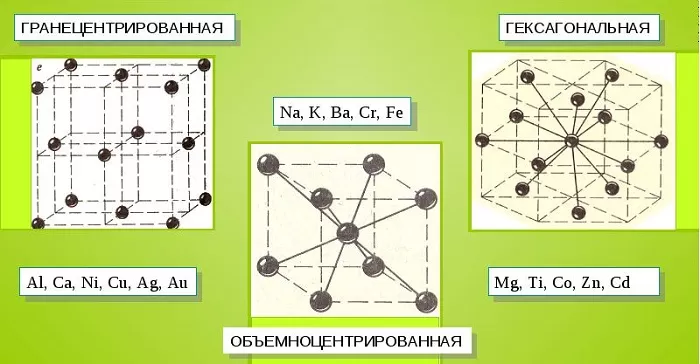
Металлические кристаллы подразделяются на 3 основных типа:
- Объемно-центрированную кубическую решетку, в которой, помимо размещения атомов в четырех вершинах куба, один из них размещается в центре объемной фигуры. Такой тип организации твердого вещества характерен для ряда металлов, включая K, Na и Li, вольфрам, хром, ниобий и др.
- Гранецентрированная кубическая решетка характеризуется расположением атомов в центре граней. Всего в ячейке задействовано 10 атомов, 4 в вершинах и 6 на гранях. Такая решетка встречается у меди, драгметаллов (серебра и золота) и металлов платиновой группы: Pd, Pt.
- Гексагональное строение решетки предполагает размещение атомов в углах и внутри 6-гранной призмы. Ячейка состоит из 15 атомов и свойственна магнию, кальцию, осмию, бериллию и ряду других металлических элементов.
Общими свойствами всех решеток являются высокая симметрия и плотная упаковка составляющих их атомов. Некоторые элементы периодической таблицы формируют уникальную структуру, например, элементарная ячейка In имеет тетрагональное строение.
Для сплавов, являющихся химическими соединениями, также характерно образование кристаллов перечисленных видов, при этом атомы каждого металла занимают определенное место в структуре.
Например, в сплаве никеля и алюминия атомы Al размещаются по углам, а атом Ni – в центре ОЦК ячейки. Свойства сплава и его структура влияют на класс прочности изделия, изготовленного из этого материала.
Физические характеристики металлических кристаллов обусловлены способностью обобществленных электронов свободно перемещаться внутри кристалла.

Характеристики, отличающие подобные вещества:
хорошая электропроводность, благодаря наличию условно свободного электронного облака;
высокая проводимость тепла;
низкая реакционная способность или инертность;
пластичность – большинство металлов можно гнуть и ковать.
Высокий уровень организации вещества обусловливает металлический блеск. Следует иметь в виду, что повышение прочности при пластической деформации и легировании приводит к образованию частично ковалентной связи.
При деформации могут возникать области повышенной прочности и низкими пластическими свойствами, похожие на вещества с ковалентной связью (например, алмаз).
Сходства и отличия металлической химической связи от ионной
Помимо рассматриваемой, металлы могут образовывать другие виды связи, включая простую ионную.
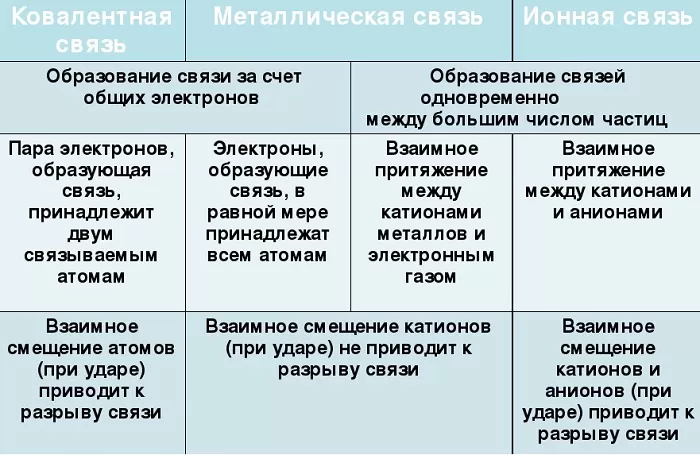
Их общие черты:
участие металлов, при этом металлическая связь формируется исключительно атомами металла, а ионная образуется между металлическим и неметаллическим элементами;
металл высвобождает электроны и становится катионом;
соединения могут существовать в кристаллической форме.
Кристаллы с ионным характером соединения отличают следующие параметры:
- В узлах размещаются как положительно, так и отрицательно заряженные ионы. Каркас металлической решетки формируют исключительно катионы.
- Узлы удерживаются за счет электростатического взаимодействия.
- При низких температурах кристаллические вещества, образованные за счет ионного взаимодействия, проявляют свойства диэлектриков (не проводят ток).
- Переход электронов с атома металла происходит на орбиты атома неметалла.
Характерный пример кристалла с ионной связью – поваренная соль, решетка которой сформирована из ионов Na⁺ и Cl⁻. Такие кристаллические вещества не обладают пластичностью и блеском.
Источник
МЕТАЛЛЫ (от греч. metallon-первоначально, шахта, копи), в-ва, обладающие в обычных условиях характерными, металлическими, свойствами-высокими электрич. проводимостью и теплопроводностью, отрицат. температурным коэф. электрич. проводимости, способностью хорошо отражать световые волны (блеск), пластичностью. К металлам относятся как собственно металлы (простые в-ва), так и их сплавы, металлические соединения, в т.ч. интерметаллиды. Иногда металлами наз. все в-ва, обладающие теми или иными металлич. св-вами, напр. т. наз. “синтетические” металлы (см. Интеркалаты), металлы органические.
Ранее характерными признаками металлов считались блеск, пластичность и ковкость – “светлое тело, которое ковать можно” (М. В. Ломоносов). Но металлич. блеском обладают и нек-рые неметаллы, напр. иод. Известны хрупкие металлы, хотя мн. из них в результате тщательной очистки получены в пластичном состоянии. В настоящее время важнейшим признаком металлов признается отрицат. температурный коэф. электрич. проводимости, т.е. понижение электрич. проводимости с ростом т-ры. Из 109 элементов в периодич. системе 86 относят к металлам. Граница между металлами и неметаллами в периодич. таблице (в ее длинном варианте) проводится по диагонали от В до At. О нек-рых элементах, напр. Ge, Sb, нет единого мнения, все же правильнее считать Ge неметаллом, т.к. он обладает полупроводниковыми св-вами, a Sb-металлом, хотя по физ. св-вам сурьма -полуметалл.
Олово существует как в металлической (b-Sn), в полупроводниковой (a-Sn) модификации. С др. стороны, у Ge, Si, P и нек-рых др. неметаллов при высоких давлениях обнаружены модификации с металлич. проводимостью. Можно предположить, что при достаточно высоких давлениях все в-ва могут приобретать металлич. св-ва. Поэтому вопрос об отнесении того или иного элемента к металлам или неметаллам следует, по-видимому, решать на основании рассмотрения не только физ. св-в простого в-ва, но и его хим. св-в. Иногда для элементов, лежащих на границе между металлами и неметаллами, применяют термин “полуметаллы”, хотя этот термин в химии теперь не рекомендуется.
В металлах существует металлическая связь, характеризующаяся тем, что кристаллич. решетка образована положит. ионами, тогда как валентные электроны делокализованы по всему пространству решетки. Металлы можно представить в виде остова из положит. ионов, погруженного в “электронный газ”, к-рый компенсирует силы взаимного отталкивания положит. ионов. Энергия этих делокализованных электронов-электронов проводимости – отвечает зоне проводимости. Согласно зонной теории, у металлов отсутствует запрещенная зона между валентной зоной и зоной проводимости (см. Твердое тело).
В кристаллах металлов атомы ионизированы лишь частично и часть валентных электронов остается связанной, в результате возможно появление частично ковалентных связей между соседними атомами. Прочность связи в кристаллич. структуре металлов характеризуется энтальпией атомизации, к-рая меняется от 61,4 кДж/молъ у Hg до 850 кДж/моль у W. Макс. энтальпия атомизации характерна для металлов рядов Nb-Ru и Hf-Ir. Относящиеся к ним металлы отличаются макс. т-рами плавления и высокой мех. прочностью.
Классификация металлов.Все металлы делятся на четыре группы (см. форзац): s-металлы (все s-элементы, кроме Н и Не), р-металлы (элементы гр. IIIа, кроме В, а также Sn, Рb, Sb, Bi, Ро), d-металлы и f-металлы, к-рые объединяются под назв. “переходных” (см. Переходные элементы). Металлы первых двух групп иногда наз. “простыми”. Из этих групп выделяются нек-рые более узкие группы: из s-металлов- щелочные металлы и щелочноземельные элементы, из d-металлов- платиновые металлы. Группа редкоземельных элементов включает как d-, так и f-металлы (подгруппа Sc и лантаноиды).
Существует также, хотя и не общепринятая, техн. классификация металлов. В известной мере она перекликается с геохимическими классификациями элементов. Обычно выделяют след. группы: черные металлы (Fe); тяжелые цветные металлы – Сu, Pb, Zn, Ni и Sn (к этой группе примыкают т.наз. малые, или младшие, металлы – Со, Sb, Bi, Hg, Cd, нек-рые из них иногда относят к редким металлам); легкие металлы (с плотностью менее 5 г/см3)-Аl, Mg, Ca и т.д.; драгоценные металлы-Au, Ag и платиновые металлы; легирующие (или ферросплавные) металлы – Mn, Cr, W, Mo, Nb, V и др.; редкие металлы (см. Редкие элементы), разбиваемые в свою очередь на неск. групп; радиоактивные металлы-U, Th, Pu и др.
Кристаллическая структура.Большинство металлов кристаллизуется в одном из трех структурных типов (см. Металлические кристаллы), а именно-в кубич. и гексагoн. плот-нейших упаковках (см. Плотная упаковка)или в объем-ноцентрированной кубич. решетке. В плотнейших упаковках каждый атом на равных расстояниях имеет 12 ближайших соседей. В объемноцентрированной кубич. решетке у каждого атома 8 равноудаленных соседей, еще 6 соседей расположены на большем (на 15%) расстоянии. Поэтому ко-ординац. число в этой структуре считают равным 14 (8 + 6). Межатомные расстояния в кристаллич. структуре металлов характеризуются металлич. радиусом (см. Атомные радиусы).
При обычных условиях щелочные металлы, а также Ва, Ra, элементы подгрупп V и Сr кристаллизуются в объемно-центрированной кубич. решетке типа a-Fe. Плотнейшая кубич. упаковка (гранецентрированная кубич. решетка) типа Си характерна для Al, Ni, металлов подгруппы Сu, платиновых металлов (кроме Ru и Os) и т. д. В гексагoн. плотнейшей упаковке типа Mg кристаллизуются Be, Са, Sr, Zn, Cd, Co, Ru, Os, элементы подгрупп Ti и Sc, мн. РЗЭ. Более сложными являются структуры разл. модификаций Мn, Ра, U, трансурановых элементов.
Многие металлы претерпевают при изменении т-ры или давления полиморфные превращения. Металлы, к-рые при низких т-рах образуют плотнейшие упаковки, напр. Са, La, Zr,часто имеют высокотемпературные модификации с объемноцентрированной кубич. структурой.
При плавлении металлы сохраняют свои электрич., тепловые и оптич. св-ва. Вблизи т-ры плавления в жидких металлах наблюдается примерно такой же ближний порядок, как и в кристаллических металлах. С повышением т-ры ближний порядок нарушается вплоть до полного разупорядочения.
Физические свойства.Физ. св-ва металлов меняются в очень широких пределах. Так, т-ра плавления изменяется от – 38,87 °С (Hg) до 3380 °С (W), плотность – от 0,531 г/см3 (Li) до 22,5 г/см3 (Os). Уд. электрич. сопротивление р при 25 °С имеет значения от 1,63 (Ag) до 140 (Мn) мкОм.см. Сопротивление движению электронов (рассеяние электронов) возникает вследствие нарушения кристаллич. решетки из-за теплового движения атомов, а также дефектов (вакансий, дислокаций, примесных атомов). Мерой его является длина своб. пробега электрона. При комнатной т-ре она равна ~ 10-6 см у металлов обычной чистоты и ~ 10-2 см у высокочистых. Температурный коэф. р (в интервале 0-100°С) меняется в пределах 1,0.10-3 (Hg)-9,0.10-3 К-1 (Be). При гелиевых т-рах (4,2 К) р практически не зависит от т-ры (rост). Его измерение используют для характеристики чистоты и совершенства кристаллов металла. Чем больше отношение r273/r4,2, тем чище металл. В монокристаллах высокой чистоты оно достигает 104-105. Нек-рые металлы при низких т-рах становятся сверхпроводниками, при этом критич. т-ра у чистых металлов от сотых долей до 9 К.
У металлов наблюдается термоэлектронная эмиссия (способность испускать электроны при высокой т-ре). Эмиссия электронов возникает также под действием электромагн. излучения в видимой и УФ областях спектра (фотоэлектронная эмиссия), внеш. электрич. поля высокой напряженности (туннельная, или автоэлектронная, эмиссия), при бомбардировке пов-сти металлов электронами (вторичная электронная эмиссия) или ионами (ионно-электронная эмиссия), при взаимод. пов-сти металла с плазмой (взрывная электронная эмиссия). Перепад т-ры вызывает в металлах появление электрич. тока (термоэдс).
Теплопроводность металлов обусловлена в осн. движением электронов, поэтому уд. коэф. теплопроводности ( ) и электрич. проводимости (s) металлов связаны между собой соотношением /(s•Т) = L = 2,45•10 -8 Вт•Ом/К2 (закон Видемана-Франца). Уд. коэф. теплопроводности металлов имеет значения от 425 (для Ag) до 8,41 (для Bi) Вт/(м-К).
Температурный коэф. линейного расширения металлов в интервале 0-100°С имеет значения от 4,57.10-6 (для Os) до 10-4 K-1 (для Sr). Согласно эмпирич. правилу Грюнайзена, относит. увеличение объема металла в интервале от О К до т-ры плавления приблизительно равно 0,06. Поэтому температурный коэф. объемного расширения у тугоплавких металлов меньше, чем у легкоплавких.
У большинства металлов магн. восприимчивость по абс. величине сравнительно мала (~ 10-9) и слабо зависит от т-ры. Среди металлов есть диамагнетики, напр. Bi ( = — 1,34.10-9), и парамагнетики, причем все переходные металлы, кроме металлов I и II гр., парамагнитны. Нек-рые из них при т-рах точки Кюри переходят в магнитно-упорядоченное состояние. Металлы триады Fe, а также Gd и нек-рые др. лантаноиды – ферромагнетики, тогда как Сr, Мn, большинство лантаноидов-антиферромагнетики.
Излучения оптич. диапазона почти полностью отражаются пов-стью металлов, вследствие чего они непрозрачны и обладают характерным металлическим блеском (порошки мн. металлов матовые). Нек-рые металлы, например Аu в виде тонкой фольги, просвечивают. Отраженный от поверхности металлов плоскополяризованный свет становится эллиптически поляризованным.
Для использования металлов в качестве конструкц. материалов важнейшее значение имеет сочетание мех. св-в – пластичности и вязкости с значит. прочностью, твердостью и упругостью. Эти св-ва зависят не только от состава (чистоты металла), но и от совершенства кристаллич. решетки (наличия дефектов) и структуры, определяемых предварительной термич. и мех. обработкой образца.
Мех. св-ва реальных металлов определяются наличием дефектов, в первую очередь дислокаций, т. к. перемещение дислокаций по плоскостям кристаллич. решетки с наиб. плотной упаковкой является осн. механизмом пластич. деформации металлов. Взаимод. дислокаций с др. дефектами увеличивает сопротивление пластич. деформации. В процессе деформации число дислокаций растет, соотв. растет и сопротивление деформации (деформац. упрочнение, или наклеп). Напряженное состояние и наклеп после деформации ликвидируются при отжиге. Рост напряжений в местах “сгущения” дислокаций вызывает зарождение трещин – очагов разрушения. Важнейшая характеристика мех. св-в металлов-модуль упругости Е (модуль Юнга). Предел текучести, т. е. сопротивление пластич. деформации, 10-3-10-4 Е.
Химические свойства.Металлы обладают низкими значениями первого потенциала ионизации и сродства к электрону. Вследствие этого в хим. р-циях они выступают как доноры электронов (восстановители), а в соед. и их р-рах образуют положительно заряженные ионы (в большинстве случаев аквакатионы). Электроотрицательности атомов металлов ниже электроотрицательностей атомов неметаллов. Металлы могут входить в состав сложных анионов, напр. МnО-4, или ацидокомплексов, напр. [Fe(CN)6]4-, однако в них атомы металлов всегда являются центрами положит. заряда. Только для нек-рых металлов, находящихся на границе с неметаллами, таких, как Sn, Po, Sb и т.п., известны соед., напр. гидриды, в к-рых металлы имеют формально отрицат. степень окисления. Но во всех этих соед. хим. связь ковалентная.
Способность металлов к окислению меняется в очень широких пределах. Большинство металлов окисляется кислородом воздуха уже при обычной т-ре, однако скорость и механизм р-ции очень сильно зависят от природы металлов. В большинстве случаев при этом образуются оксиды, а у щелочных металлов, кроме Li,-пepоксиды. Устойчивость металлов на воздухе определяется св-вами образующегося оксида, в частности отношением молярных объемов Vокс/VM.. Если Vокс/VМ > 1, на металлах образуется защитная пленка, предохраняющая металлы от дальнейшего окисления. Такая пленка характерна, напр., для Al, Ti, Сr, к-рые устойчивы на воздухе, хотя и обладают высокой активностью. Металлы, для к-рых это отношение меньше 1 (напр., щелочные), на воздухе неустойчивы.
С N2 реагирует ряд металлов, напр. Li при обычной т-ре , a Mg, Zr, Hf, Ti-при нагревании. Мн. металлы активно взаимод. с Н2, галогенами, халькогенами. Все металлы, чьи стандартные электродные потенциалы отрицательнее, чем —0,413 В, окисляются водой с выделением Н2. Щелочные и щел.-зем. металлы реагируют с водой при обычных т-рах, а такие металлы, как Zn или Fe, реагируют с водяным паром при высоких т-рах. С р-рами щелочей взаимод. металлы, образующие р-римые анионные гидроксокомплексы (Be, Zn, Al, Ga, Sn).
Большинство металлов окисляется теми или иными к-тами. Металлы, имеющие отрицат. стандартные электродные потенциалы, т.е. стоящие в электрохимическом ряду напряжений до водорода, окисляются ионами Н+ и растворяются поэтому при действии неокисляющих к-т (соляная или разб. H2SO4), если не образуются нер-римые продукты. Р-ции способствует образование анионных комплексов. Азотная к-та, даже разбавленная, окисляет мн. металлы. При этом, если ионы металлов устойчивы в низших степенях окисления, образуются ка-тионные комплексы, если в высших, как в случае, напр., Re,-анионные (ReO-4 ). Нек-рые металлы реагируют с разб. HNO3 и H2SO4 с образованием катионных комплексов и пас-сивируются в конц. р-рах этих к-т. Для растворения малоактивных металлв, напр. Аu или Pt, используют смеси, содержащие окислитель и поставщик лигандов для образования р-римых комплексов, таких, как, напр., царская водка или смесь HNO3 с HF.
О взаимод, металлов со средой, ведущем к разрушению металлов, см. в ст. Коррозия металлов.
Важная характеристика металлич. элементов-их способность образовывать основные оксиды и соотв. гидроксиды. У металлов главных подгрупп периодич. системы основность оксидов и гидроксидов растет сверху вниз, в побочных подгруппах (кроме I – III) – обратная зависимость. По периодам и рядам с ростом порядкового номера элемента основность убывает. У металлов, имеющих неск. степеней окисления, как d- и f-металлы, с ростом степени окисления основность оксидов уменьшается и высшие оксиды имеют кислотный характер.
Получение металлов.Извлечение металлов из прир. сырья и др. источников – область металлургии. Можно отметить двоякий характер технологии металлов. Технология железа, тяжелых цветных металлов, а также малых металлов и большинства рассеянных элементов (халькофильных элементов) имеет “металлур-гич.” характер. Это означает, что конечный продукт получают без предварит. выделения к.-л. чистого соединения, что обусловлено сравнит. легкостью восстановления до металлов как пирометаллургич. (см. Пирометаллургия), так и гидроме-таллургич. (электролиз р-ров, цементация и т.п.; см. Гидрометаллургия)путем.
Иной характер имеет технология легких, а также редких металлы (литофильных элементов). Это связано с трудностями их получения в своб. состоянии. Для этих металлов технология разбивается четко на два этапа – получение чистого соед., напр. Аl2О3, и получение металла из этого соединения. Сами металлы в произ-ве их соед. обычно не используют. Поэтому можно сказать, что технология этих металлов имеет более “химический” характер.
Способность металлов к взаимному растворению с образованием при кристаллизации твердых растворов и интерметал-лидов, разнообразным фазовым превращениям дает возможность получения большого числа сплавов, отличающихся разл. структурой и самыми разнообразными сочетаниями св-в. В совр. технике применяют св. 30 000 разл. сплавов – легкоплавких и тугоплавких, очень твердых и пластичных, с большой и малой электрич. проводимостью, ферромагнитных и др. В сплавах ныне используют практически все известные металлы (кроме искусственно полученных трансплутониевых элементов). Мера использования в значит. степени определяется доступностью металла-содержанием в земной коре, а также степенью концентрирования в месторождениях и трудностью получения. Использование сплавов (бронзовый век) было одним из важнейших этапов становления человеческой цивилизации. И в настоящее время сплавы-важнейшие конструкционные материалы. В последние годы наблюдается тенденция нек-рого снижения роли железа и увеличение использования легких металлов (Al, Mg) и наиб. доступных редких металлов (Ti, Nb, Zr).
МЕТАЛЛИЧЕСКАЯ СВЯЗЬ, хим. связь, обусловленная взаимод. электронного газа (валентные электроны) в металлах с остовом положительно заряженных ионов кристаллич. решетки. Идеальная модель металлической связи отвечает образованию частично заполненных валентными электронами металла зон энергетич. уровней (см. Твердое тело), наз. зонами проводимости. При сближении атомов, образующих металл, атомные орбитали валентных электронов переходят в орбитали, делокализованные по кристаллич. решетке аналогично делокализованным p-орбиталям сопряженных соединений. Количественно описать металлическая связь можно только в рамках квантовой механики, качественно образование металлической связи можно понять исходя из представлений о ковалентной связи.
При сближении двух атомов металла, напр. Li, образуется ковалентная связь, при этом происходит расщепление каждого энергетич. уровня валентного электрона на два. Когда N атомов Li образуют кристаллич. решетку, перекрывание электронных облаков соседних атомов приводит к тому, что каждый энергетич. уровень валентного электрона расщепляется на N уровней, расстояния между к-рыми из-за большой величины N настолько малы, что их совокупность может считаться практически непрерывной зоной энергетич. уровней, имеющей конечную ширину. Поскольку каждый атом участвует в образовании большего числа связей, чем, напр., в двухатомной молекуле при том же числе валентных электронов, то минимум энергии системы (или максимум энергии связи) достигается при расстояниях больших, чем в случае двухцентровой связи в молекуле. Межатомные расстояния в металлах заметно больше, чем в соед. с ковалентной связью (металлич. радиус атомов всегда больше ковалентного радиуса), а координац. число (число ближайших соседей) в кристаллич. решетках металлов обычно 8 или больше 8. Для наиб. часто встречающихся кристаллич. структур координац. числа равны 8 (объемноцентрир. кубич.), 12 (гранецентрир. кубическая и гексаген. плотно-упакованная). Расчеты параметров металлич. решеток с использованием ковалентных радиусов дают заниженные результаты. Так, расстояние между атомами Li в молекуле Li2 (ковалентная связь) равно 0,267 нм, в металле Li-0,304 нм. Каждый атом Li в металле имеет 8 ближайших соседей, а на расстоянии, в раз большем,-еще 6. Энергия связи в расчете на один атом Li в результате увеличения числа ближайших соседей увеличивается с 0,96.10-19 Дж для Li2 до 2,9.10-19 Дж для кристаллич. Li.
Во мн. металлах металлическая связь между атомами включает вклады ионной или ковалентной составляющей. Особенности металлической связи у каждого металла м. б. связаны, напр., с электростатич. отталкиванием ионов друг от друга с учетом распределения электрич. зарядовое них, с вкладом в образование связи электронов внутр. незаполненных оболочек переходных металлов, с корреляцией движения электронов в электронном газе и нек-рыми др. причинами.
Металлическая связь характерна не только для металл
