Какие свойства глюкозы позволяют делать выводы о строении ее молекулы

Строение глюкозы
Название «углеводы» сохранилось с тех времен, когда строение этих соединений еще не было известно, но был установлен их состав, которому соответствует формула Cn(H2O)m. Поэтому углеводы относили к гидратам углерода, т.е. к соединениям углерода и воды – «углеводам». В наше время большинство углеводов выражают формулой CnH2nOn.
1. Углеводы используются с глубокой древности – самым первым углеводом (точнее смесью углеводов), с которой познакомился человек, был мёд.
2. Родиной сахарного тростника является северо-западная Индия-Бенгалия. Европейцы познакомились с тростниковым сахаром благодаря походам Александра Македонского в 327 г. до н.э.
3. Свекловичный сахар в чистом виде был открыт лишь в 1747 г. немецким химиком А. Маргграфом.
4. Крахмал был известен ещё древним грекам.
5. Целлюлоза, как составная часть древесины, используется с глубокой древности.
6. Термин слова “сладкий” и окончание – оза- для сахаристых веществ было предложено французским химиком Ж. Дюла в 1838 г. Исторически сладость была главным признаком, по которому то или иное вещество относили к углеводам.
7. В 1811 г. русский химик Кирхгоф впервые получил глюкозу гидролизом крахмала, а впервые правильную эмпирическую формулу глюкозы предложил шведский химик Я. Берцемус в 1837 г. С6Н12О6
8. Синтез углеводов из формальдегида в присутствии Са(ОН)2 был произведён А.М. Бутлеровым в 1861 г.
Глюкоза является бифункциональным соединением, т.к. содержит функциональные группы – одну альдегидную и 5 гидроксильных. Таким образом, глюкоза – многоатомный альдегидоспирт.
Структурная формула глюкозы имеет вид:
Сокращённая формула имеет вид:
Молекула глюкозы может существовать в трех изомерных формах, причем две из них являются циклическими, одна – линейной.
Все три изомерных формы находятся в динамическом равновесии между собой:
циклическая [(альфа-форма) (37%)] <–> линейная (0,0026%) <–> циклическая [(бета-форма) (63%)]
Циклические альфа- и бета- формы глюкозы представляют собой пространственные изомеры, отличающиеся положением полуацетального гидроксила относительно плоскости кольца. В альфа-глюкозе этот гидроксил находится в транс-положении к гидроксиметильной группе -СН2ОН, в бета-глюкозе – в цис-положении.
Химические свойства глюкозы:
Свойства, обусловленные наличием альдегидной группы:
1. Реакции окисления:
а) с Cu(OH)2:
C6H12O6 + Cu(OH)2↓ ——> ярко-синий раствор
2.Реакция восстановления:
c водородом H2:
В этой реакции может принимать участие лишь линейная форма глюкозы.
Свойства обусловленные наличием нескольких гидроксильных групп (ОН):
1. Реагирует с карбоновыми кислотами с образованием сложных эфиров (пять гидроксильных групп глюкозы вступают в реакцию с кислотами):
2. Как многоатомный спирт реагирует с гидроксидом меди (II) c образованием алкоголя-та меди (II):
Специфические свойства
Большое значение имеют процессы брожения глюкозы, происходящие под действием органических катализаторов-ферментов (они вырабатываются микроорганизмами).
а) спиртовое брожение (под действием дрожжей):
б) молочнокислое брожение (под действием молочнокислых бактерий):
в) уксуснокислое брожение:
г) лимоннокислое брожение:
д) ацетон-бутанольное брожение:
Получение глюкозы
1.Синтез глюкозы из формальдегида в присутствии гидроксида кальция (ре-акция Бутлерова):
2. Гидролиз крахмала (реакция Киргофа):
Биологическое значение глюкозы, её применение
Глюкоза – необходимый компонент пищи, один из главных участников обмена веществ в организме, очень питательна и легко усваивается. При её окислении выделяется больше трети используемой в организме энергий ресурс – жиры, но роль жиров и глюкозы в энергетике разных органов различна. Сердце в качестве топлива используется жирные кислоты. Скелетным мышцам глюкоза нужна для “запуска”, а вот нервные клетки, в том числе и клетки головного мозга работают только на глюкозе. Их потребность составляет 20-30% вырабатываемой энергии. Нервным клеткам энергия нужна каждую секунду, а глюкозу организм получает при приёме пищи. Глюкоза легко усваивается организмом, поэтому ее используют в медицине в качестве укрепляющего лечебного средства. Специфические олигосахариды определяют группу крови. В кондитерском деле для изготовления мармелада, карамели, пряников и т.д. Большое значение имеют процессы брожения глюкозы. Так, например, при квашении капусты, огурцов, молока происходит молочнокислое брожение глюкозы, также как и при силосовании кормов. На практике используется и спиртовое брожение глюкозы, например, при производстве пива.
Углеводы действительно самые распространенные органические вещества на Земле, без которых невозможно существование живых организмов. В живом организме в процессе метаболизма глюкоза окисляется с выделением большого количества энергии:
Источник
План-конспект урока по химии в 10 классе:
«Глюкоза, её строение и свойства, значение, применение»
УМК Габриеляна О.С.
Бондаренко Геннадий Михайлович, учитель химии МБОУ «СОШ с. Малокурильское» Южно-Курильского р-на Сахалинской обл.
Тема урока: «Глюкоза, её строение и свойства, значение, применение»
Цели урока:
Образовательные:
Сформировать у учащихся знания об углеводах, их составе и классификации. Рассмотреть зависимость химических свойств углеводов от строения молекул. Качественные реакции на глюкозу. Дать представление о биологической роли углеводов, их значении в жизни человека.
Развивающие:
Продолжить развивать у учащихся мыслительные операции: умение связывать уже имеющиеся знания с вновь приобретенными, умение выделять главное в изученном материале, обобщать изученный материал и делать выводы.
Воспитательные:
Воспитание ответственного отношения к учебе, стремления к творческой, познавательной деятельности
Тип урока: комбинированный урок усвоения знаний, умений и навыков и творческого применения их на практике.
Оборудование и материалы: периодическая система химических элементов Д.И. Менделеева, таблица « Классификация углеводов», штатив с пробирками, раствор глюкозы, раствор сульфата меди, щелочи, карточки с заданиями.
Предварительная подготовка: Некоторым учащимся учитель дает задание подготовить электронные презентации по истории открытия углеводов.
Ход урока:
I. Организационный момент урока.
II. Актуализация знаний, проверка домашнего задания.
Беседа
1.Какие вещества называются углеводами?
2.Что вы знаете о составе углеводов? Презентация.
3.Какова их классификация?
4.Что вы знаете о физических свойствах углеводов?
5..Как углеводы образуются в растениях? (процесс)
6.Что такое функциональная группа, какая функциональная группа у спиртов, у альдегидов?
III. Изучение нового материала.
Сегодня мы продолжаем изучение углеводов, и ознакомимся подробнее со свойствами и строением простейшего из представителей углеводов- с глюкозой. ( Тема урока)
1.Стоение молекулы глюкозы
Глюкоза имеет молекулярную формулу C6H12O6
Структурная формула: СН2ОН-(СНОН)4-СОН
Кроме молекул с открытой цепью, для глюкозы характерны молекулы циклического строения: а- форма, в-форма. Работа с учебником стр.148.
Изучив структурную формулу глюкозы можно сделать вывод о том , что это многофункциональное вещество, содержащее пять гидроксильных групп, и одну альдегидную группу. Наличие этих функциональных групп позволяет сделать вывод, что глюкоза – альдегидоспирт. Чтобы доказать это- проведём опыты.
2.Химические свойства глюкозы.
Качественные реакции
Опыт № 1 Реакция с гидроксидом меди II.
В раствор глюкозы добавить раствор сульфата меди( II) и гидроксид натрия, наблюдается ярко- синее окрашивание. У каких известных ранее вам веществ вы встречали такую реакцию?
Это качественная реакция на многоатомные спирты. Следовательно, глюкоза также имеет несколько гидроксильных групп – ОН (5 групп)
СН2ОН-(СНОН)4-СОН
Подогреем данный раствор, наблюдаем изменение цвета. Образование морковного осадка. Такая реакция происходит у альдегидов, реакция окисления при температуре. Следовательно ,у глюкозы так же есть альдегидная группа.
Опыт №2 Реакция серебряного зеркала
Взаимодействие с аммиачным раствором оксида серебра. Также доказывает наличие альдегидной группы. (эту реакцию используют для получения зеркал и новогодних игрушек)
СН2ОН-(СНОН)4-СОН
Вывод: глюкоза- это альдегидоспирт .
Специфические свойства глюкозы:
3. Брожение (ферментация) моносахаридов
а) Спиртовое брожение
С6Н12О6 → 2С2Н5ОН + 2СО2
б) Маслянокислое брожение
С6Н12О6 → СН3 ─СН2 ─СН2 ─СООН + 2Н2↑ + 2СО2↑
в) Молочнокислое брожение
С6Н12О6 → 2СН3 ─ СНОН ─ СООН
Работа с учебником , Таблица 13, стр 150.
3.Применение.
А) получение этилового спирта, посеребрение новогодних игрушек, зеркал
2) в кондитерском производстве для получения карамели, напитков, пряников
3) она легко усваивается организмом, поэтому ее используют в медицине в качестве укрепляющего средства ослабленным больным, послеоперационным больным, входит в состав кровозаменяющих и противошоковых жидкостей.
Только глюкоза основной источник энергии для головного мозга, поэтому, когда предстоит решить трудную задачу или сдать экзамен, рекомендуют съесть кусочек сахара или шоколад
4) реакции брожения используются для квашения капусты. Получения молочнокислых продуктов.
IV. Закрепление знаний.
Тестовые задания:
1 вариант 1.Укажите признак, характерный для глюкозы:
А) при обычных условиях легко реагирует с натрий гидроксидом;
Б) имеет молекулярную кристаллическую решётку;
В) при нормальных условиях – жидкость;
2.Укажите группу углеводов, к которой относят глюкозу:
А) моносахариды; Б) олигосахариды; В) полисахариды.
3.Обозначте функциональные группы, которые содержит глюкоза:
А) Карбоксильная и карбонильная Б) Альдегидная и гидроксильная
В) Карбоксильная и аминогруппа
4.Какие реакции характерны для глюкозы:
А) Реакция «серебряного зеркала» Б) Гидратация
В) Взаимодействие с гидроксидом меди(II)
5.Газообразным продуктом спиртового брожения глюкозы является
А) СО; Б) О2; В) СО2; Г) Н2.
6. Написать уравнение реакции фотосинтеза, указать сумму коэффициентов.
2 вариант 1.Какие формы молекул глюкозы существуют в растворе:
А) только а-форма; Б) только в-форма; В) и а- и в-формы;
2.Укажите группу углеводов, к которой относят сахарозу:
А) моносахариды; Б) олигосахариды; В) Полисахариды.
3. Какая из формул отражает состав насыщенных одноатомных спиртов?
а) СnH2n +1 OH б) СnH2n +1 CHО в) СnH2n +1 СООН г) СnH2n +2
4.В процессе жизнедеятельности животных и человека глюкоза:
А) является источником энергии; Б) является катализатором;
В) Участвует в процессе фотосинтеза.
5. Укажите неорганический продукт в « реакции серебряного зеркала»
А) СО; Б) О2; В) СО2; Г) Аg
6. Написать уравнение реакции глюкозы с гидроксидом меди, указать сумму коэффициентов.
V. Рефлексия.
Составить рассказ в логической последовательности по основным понятиям, которые представлены на доске: углеводы, простые углеводы, сложные углеводы, моносахариды, глюкоза, фруктоза, альдегидоспирт, функциональные группы, качественные реакции глюкозы, брожение, источник энергии.
VI. Домашнее задание
Параграф 31, Упражнение № 1-7 стр.152.
Источник
Химические свойства глюкозы, как и других альдоз, обусловлены присутствием в ее молекуле: а)альдегидной группы; б) спиртовых гидроксилов; в) полуацетального (гликозидного) гидроксила.
Глюкоза
Специфические свойства
1. Брожение (ферментация) моносахаридов
Важнейшим свойством моносахаридов является их ферментативное брожение, т.е. распад молекул на осколки под действием различных ферментов. Брожению подвергаются в основном гексозы в присутствии ферментов, выделяемых дрожжевыми грибками, бактериями или плесневыми грибками. В зависимости от природы действующего фермента различают реакции следующих видов:
1) Спиртовое брожение
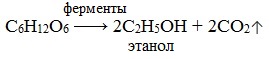
2) Молочнокислое брожение
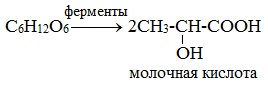 (образуется в организмах высших животных при мышечных сокращениях).
(образуется в организмах высших животных при мышечных сокращениях).
3) Маслянокислое брожение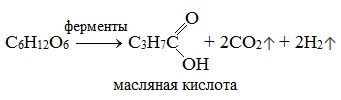
4) Лимоннокислое брожение
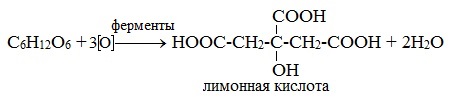
Реакции с участием альдегидной группы глюкозы (свойства глюкозы как альдегида)
1. Восстановление (гидрирование) с образованием многоатомного спирта
В ходе этой реакции карбонильная группа восстанавливается и образуется новая спиртовая группа:
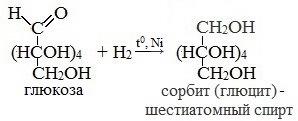
Cорбит содержится во многих ягодах и фруктах, особенно много сорбита в плодах рябины.
2. Окисление
1) Окисление бромной водой
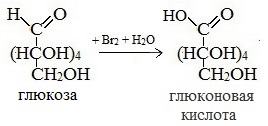
Качественные реакции на глюкозу как альдегид!
Протекающие в щелочной среде при нагревании реакции с аммиачным раствором Ag2O (реакция серебряного зеркала») и с гидроксидом меди (II) Cu (OH)2 приводят к образованию смеси продуктов окисления глюкозы.
2) Реакция серебряного зеркала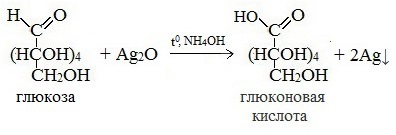
Соль этой кислоты – глюконат кальция – известное лекарственное средство.
Видеоопыт «Качественная реакция глюкозы с аммиачным раствором оксида серебра (I)»
3) Окисление гидроксидом меди (II)
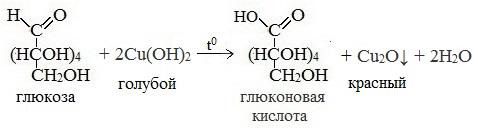
В ходе этих реакций альдегидная группа – СНО окисляется до карбоксильной группы – СООН.
Реакции глюкозы с участием гидроксильных групп (свойства глюкозы как многоатомного спирта)
1. Взаимодействие с Cu (ОН)2с образованием глюконата меди (II)
Качественная реакция на глюкозу как многоатомный спирт!
Подобно этиленгликолю и глицерину, глюкоза способна растворять гидроксид меди (II), образуя растворимое комплексное соединение синего цвета:
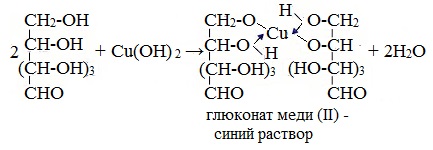
Прильём к раствору глюкозы несколько капель раствора сульфата меди (II) и раствор щелочи. Осадка гидроксида меди не образуется. Раствор окрашивается в ярко-синий цвет.
В данном случае глюкоза растворяет гидроксид меди (II) и ведет себя как многоатомный спирт, образуя комплексное соединение.
Видеоопыт «Качественная реакция глюкозы с гидроксидом меди (II)»
2. Взаимодействие с галогеналканами с образованием простых эфиров
Являясь многоатомным спиртом, глюкоза образует простые эфиры:
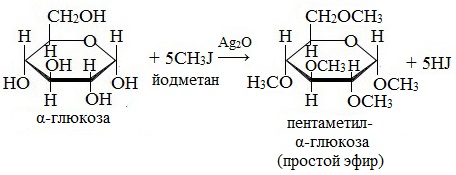
Реакция происходит в присутствии Ag2O для связывания выделяющегося при реакции НI.
3. Взаимодействие с карбоновыми кислотами или их ангидридами с образованием сложных эфиров.
Например, с ангидридом уксусной кислоты: 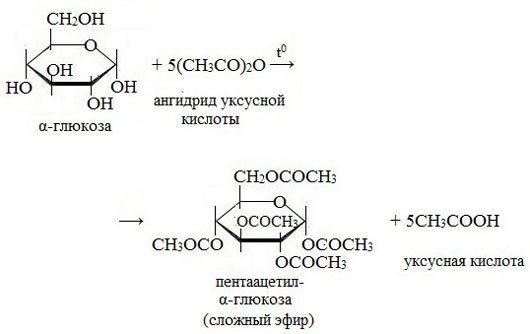
Реакции с участием полуацетального гидроксила
1. Взаимодействие со спиртами с образованием гликозидов
Гликозиды – это производные углеводов, у которых гликозидный гидроксил замещен на остаток какого-либо органического соединения.
Содержащийся в циклических формах глюкозы полуацетальный (гликозидный) гидроксил является очень реакционноспособным и легко замещается на остатки различных органических соединений.
В случае глюкозы гликозиды называются глюкозидами. Связь между углеводным остатком и остатком другого компонента называется гликозидной.
Гликозиды построены по типу простых эфиров.
При действии метилового спирта в присутствии газообразного хлористого водорода атом водорода гликозидного гидроксила замещается на метильную группу:
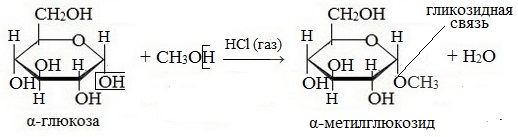
В данных условиях в реакцию вступает только гликозидный гидроксил, спиртовые гидроксильные группы в реакции не участвуют.
Гликозиды играют чрезвычайно важную роль в растительном и животном мире. Существует огромное число природных гликозидов, в молекулах которых с атомом С (1) глюкозы остатки самых различных соединений.
Реакции окисления
Более сильный окислитель – азотная кислота НNO3 – окисляет глюкозу до двухосновной глюкаровой (сахарной) кислоты:
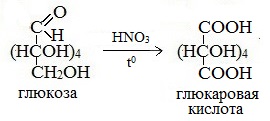
В ходе этой реакции и альдегидная группа – СНО и первичная спиртовая группа — СН2ОН окисляются до карбоксильных – СООН.
Видеоопыт «Окисление глюкозы кислородом воздуха в присутствии метеленового голубого»
Углеводы
Моносахариды
Источник
О строении молекулы глюкозы можно судить на основании опытных данных. Она реагирует с карбоновыми кислотами, образуя сложные эфиры, содержащие от 1 до 5 остатков кислоты. Если раствор глюкозы прилить к свежеполученному гидроксиду меди(II), то осадок растворяется и образуется ярко-синий раствор соединения меди, т.е. происходит качественная реакция на многоатомные спирты. Следовательно, глюкоза является многоатомным спиртом. Если же подогреть полученный раствор, то вновь выпадает осадок, но уже красноватого цвета, т.е. произойдет качественная реакция на альдегиды. Аналогично если раствор глюкозы нагреть с аммиачным раствором оксида серебра, то произойдет реакция «серебряного зеркала». Следовательно, глюкоза является одновременно многоатомным спиртом и альдегидом – альдегидо-спиртом. Попробуем вывести структурную формулу глюкозы. Всего атомов углерода в молекуле шесть C6H12O6.
Один атом входит в состав альдегидной группы:

Остальные пять атомов углерода связываются с пятью гидроксильными группами. И наконец, атомы водорода в молекуле распределим с учетом того, что углерод четырехвалентен:

Однако установлено, что в растворе глюкозы, помимо линейных (альдегидных) молекул, существуют молекулы циклического строения, из которых состоит кристаллическая глюкоза. Превращение молекул линейной формы циклическую можно объяснить, если вспомнить, что атомы углерода могут свободно вращаться вокруг у-связей, расположенных под углом 109 градусов 28 минут. При этом альдегидная группа (1-й атом углерода) может приблизиться к гидроксильной группе пятого атома углерода. В первой под влиянием гидроксильной группы разрывается р-связь: к атому кислорода присоединяется атом водорода и «потерявшийся» этот атом кислород гидроксидной группы замыкает цикл:

глюкоза физический химический соединение
В результате такой перегруппировки атомов образуется циклическая молекула. Циклическая формула показывает не только порядок связи атомов, но и их пространственное расположение. В результате взаимодействия первого и пятого атомов углерода появляется новая гидроксильная группа у первого атома, которая может занять в пространстве два положения: над и под плоскостью цикла, а потому возможны две циклические формы глюкозы: а) альфа форма глюкозы – гидроксильная группы при первом и втором атомах углерода расположены по одну сторону кольца молекулы и б) бета-форма глюкозы – гидроксильной группы находятся по разные стороны кольца молекулы:

В водном растворе глюкозы в динамическом равновесии находятся три ее изомерные формы – циклическая альфа-форма, линейная (альдегидная) форма и циклическая бета-форма:

В установившемся динамическом равновесии преобладает бета – форма (около 63%), так как она энергетически предпочтительнее – у нее OH – группы у первого и второго углеродных атомов по разные стороны цикла. У б – формы (около 37%) OH-группы у тех же углеродных атомов расположенных по одну сторону плоскости, поэтому она энергетически менее устойчива, чем в – форма. Доля же линейной формы в равновесии очень мала (всего около 0,0026%).
Динамическое равновесие можно сместить. Например, при действии на глюкозу аммиачного раствора оксида серебра количество ее линейной (альдегидной) формы, которой в растворе очень мало, пополняется все время за счет циклических форм, и глюкоза полностью подвергается окислению до глюконовой кислоты:
Изомером альдегидоспирта глюкозы является кетоноспирт – фруктоза:
Источник
