Какие свойства фермента характеризуются константой михаэлиса
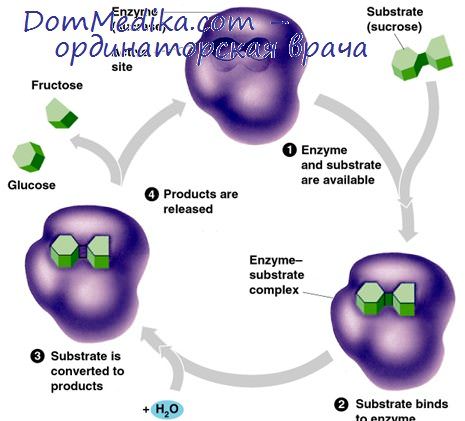
Константа Михаэлиса Км — весьма удобный количественный параметр, помогающий установить, каким образом данный фермент будет реагировать при тех условиях, которые имеются в живой клетке.
Иными словами, Км представляет собой концентрацию субстрата, при которой скорость реакции равна половине максимальной. Если фермент характеризуется высоким значением Км, то это означает, что потребуется много субстрата для того, чтобы увеличить скорость катализируемой этим ферментом реакции до половины максимальной; низкая величина Км указывает на то, что для насыщения фермента достаточно небольшого количества субстрата. Из этих положений следует также, что фермент-субстратные пары с низким значением Км характеризуются высоким сродством друг к другу и наоборот.
Кроме того, величина Км помогает решить вопрос о том, какие из групп субстратов будут наиболее эффективно связываться с данным ферментом. Если фермент не обладает строгой специфич ностью, то в присутствии обычных концентраций реагентов, имею щихся в клетке, он будет предпочтительно катализировать реакцию, протекающую при участии того субстрата, для которого характерна наиболее низкая величина /См при взаимодействии с данным ферментом. Знание концентраций различных субстратов в клетке и величин /См при взаимодействии этих субстратов с ферментами позволяет оценить вклад отдельных реакций в процесс обмена веществ в организме в целом, а также установить, какая из этих реакций лимитирует скорость всего процесса. Выяснение этих вопросов совершенно необходимо для понимания воздействия физиологических регуляторных факторов, таких, как гормоны, на скорость метаболических реакций.

Влияние концентрации фермента на реакцию
Хотя величина Км характерна и постоянна для каждой фермент-субстратной пары, величина Vmax прямо пропорциональна количеству имеющегося в системе фермента. Действительно, можно показать алгебраически, что Vmаx=k [Е], где [Е] — концентрация фермента, a k — константа скорости для реакций, описанных выше при рассмотрении этапов (3) и (4). Измерение Vmax» или скорости ферментативной реакции в присутствии насыщающей концентрации субстрата, фактически служит мерой числа имеющихся в клетке молекул фермента. Хотя не всегда удается выразить [Е] в молях на литр, поскольку величина k не всегда известна, можно допустить, что измерение активности фермента при оптимальных условиях дает истинное представление об относительных количествах фермента.
В число условий, оптимальных для действия фермента, включают, кроме обеспечения достаточной для насыщения фермента концентрации субстрата, соответствующие физические параметры (температура, рН среды, степень ионизации), а также наличие любых дополнительных факторов, которые могли бы способствовать каталитическому процессу.
– Читать “Влияние температуры на реакцию. Оптимальная температура ферментной реакции”
Оглавление темы “Ферментативные реакции в организме”:
1. Ферментный катализ. Механизмы ферментного катализа
2. Соединение субстрата с ферментом. Конкурентное торможение
3. Концентрация субстрата. Влияние концентрации субстрата на ферментативную реакцию
4. Константа Михаэлиса. Влияние концентрации фермента на реакцию
5. Влияние температуры на реакцию. Оптимальная температура ферментной реакции
6. Оптимальная температура человека. Влияние pH на реакции в организме
7. Влияние ионов на химические реакции. Кофакторы и коферменты
8. Ингибиторы ферментов. Механизмы действия ингибиторов ферментов
9. Аллостерические модификаторы. Механизм действия модификаторов
10. Положительные модификаторы. Активация зимогенов
Источник
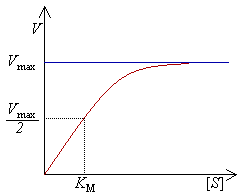
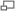
Диаграмvа скорости реакции V как функции от концентрации [S].
Уравне́ние Михаэ́лиса — Ме́нтен — основное уравнение ферментативной кинетики, описывает зависимость скорости реакции, катализируемой ферментом, от концентрации субстрата и фермента. Простейшая кинетическая схема, для которой справедливо уравнение Михаэлиса:
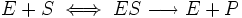
Уравнение имеет вид:
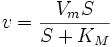 ,
,
где
· 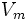 — максимальная скорость реакции, равная
— максимальная скорость реакции, равная 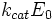 ;
;
· 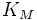 — константа Михаэлиса, равная концентрации субстрата, при которой скорость реакции составляет половину от максимальной;
— константа Михаэлиса, равная концентрации субстрата, при которой скорость реакции составляет половину от максимальной;
· 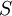 — концентрация субстрата.
— концентрация субстрата.
Вывод уравнения
Вывод уравнения был впервые предложен Бриггсом и Холдейном. Вывод уравнения скорости ферментативной реакции, описываемой схемой Михаэлиса-Ментен.
Обозначения констант скоростей:
k1 — константа скорости реакции образования фермент-субстратного комплекса из фермента и субстрата
k-1 — константа скорости реакции диссоциации фермент-субстратного комплекса на фермент и субстрат
k2 — константа скорости реакции превращения фермент-субстратного комплекса в фермент и продукт
Для фермент-субстратного комплекса применим метод квазистационарности, так как в подавляющем большинстве реакций константа скорости превращения фермент-субстратного комплекса в фермент и продукт много больше, чем константа скорости образования ферменто-субстратного комплекса из фермента и субстрата. Иными словами:
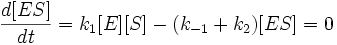
Учтем тот факт, что фермент, изначально находившийся только в свободной форме, в процессе реакции находится как в виде фермент-субстратного комплекса, так и в виде молекул свободного фермента. Таким образом:
[E]0 = [E] + [ES]
Преобразуем это к виду:
[E] = [E]0 − [ES]
И подставим в первое уравнение. После раскрытия скобок и группировки слагаемых получим следующее:
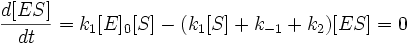
Выразим отсюда концентрацию фермент-субстратного комплекса:
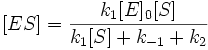
Скорость ферментативной реакции в целом (то есть скорость образования продукта) представляет собой скорость распада фермент-субстратного комплекса по реакции первого порядка с константой k2:
v = k2[ES]
Подставим в эту формулу выражение, которое мы получили для концентрации ES. Получим:
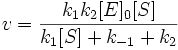
Разделим числитель и знаменатель на k1. В результате:
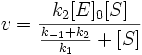
Выражение в знаменателе — (k-1+k2)/k1 — называется константой Михаэлиса (Km). Это кинетическая константа (с размерностью концентрации), которая равняется такой концентрации субстрата, при которой скорость ферментативной реакции составляет половину от максимального значения.
Для начальной стадии реакции можно пренебречь уменьшением концентрации субстрата. Тогда выражение для начальной скорости реакции будет выглядеть так:
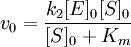
Если k-1>k2, то на первой стадии ферментативной реакции с течением времени устанавливается равновесие (квазиравновесный режим протекания реакции), и в выражение для скорости ферментативной реакции входит уже не константа Михаэлиса, а субстратная константа KS, характеризующая взаимодействие фермента с субстратом в равновесных условиях:
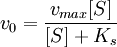 ;
; 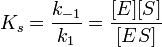
По значению KS можно судить о химическом сродстве субстрата к ферменту.
Металлоферменты и ферменты, активируемые металлами
Металлоферменты содержат определенное количество ионов металлов, имеющих функциональное значение и остающихся связанными с молекулой фермента в ходе его очистки. Ферменты, активируемые металлами, связывают последние менее прочно, но для своей активности требуют добавления металлов в среду. Таким образом, разграничение между металлоферментами и ферментами, активируемыми металлами, основано на сродстве данного фермента к иону «своего» металла. Механизмы, основанные на участии ионов металлов в катализе, в обоих случаях, по-видимому, сходны.
Тройные комплексы фермент—металл — субстрат
Для тройных (трехкомпонентных) комплексов, включающих каталитический центр (Enz), ион металла (М) и субстрат (S) со стехиометрией 1:1:1, возможны четыре различных схемы образования:
Enz—S—М М —Enz—S
Комплекс с мостиковым Комплекс с мостиковым субстратом ферментом
М
Enz—M—S Enz|
S
Простой комплекс с Циклический комплекс
мостиковым металлом с мостиковым металлом
В случае ферментов, активируемых металлами, реализуются все четыре схемы. Для металлофермен-тов образование комплекса Enz—S—М невозможно, иначе они не могли бы удерживать металл в процессе очистки (они находятся в форме Enz — — М). Можно сформулировать три общих правила.
1. Большинство (но не все) киназ (АТР:фосфо-трансферазы) образуют комплексы с мостиковым субстратом типа Enz—нуклеозид—М.
2. Фосфотрансферазы, использующие в качестве субстрата пируват или фосфоенолпируват, другие ферменты, катализирующие реакции с участием фосфоенолпирувата, а также карбоксилазы образуют комплексы с мостиковым металлом.
3. Данный фермент может быть способен к образованию мостикового комплекса одного типа с одним субстратом и другого типа — с другим.
Комплексы с мостиковым ферментом(М —Enz—S)
Металлы в комплексах с мостиковым ферментом, по-видимому, выполняют структурную роль, поддерживая активную конформацию (примером служит глутаминсинтаза), или образуют мостик с другим субстратом (как в пируваткиназе). В пиру-ваткиназе ион металла играет не только структурную роль, но и удерживает один из субстратов (АТР) и активирует его:
А
Пируваткиназа—АТР
Креатин.
Комплексы с мостиковым субстратом
Образование тройных комплексов с мостиковым субстратом, которое наблюдается при взаимодействии ферментов с нуклеозидтрифосфатами, по-видимому, связано с выстеснением Н20 из координационной сферы металла, место которой занимает АТР:
АТР- + M(H20)2+fi г± АТР—М(Н20)2 + ЗН20.
Затем субстрат связывается с ферментом, образуя тройной комплекс:
АТР—М(Н20)2:, + Enz <± *± Enz —ATP—M(H20)2:v
В фосфотрансферазных реакциях ионы металлов, как полагают, активируют атомы фосфора и образуют жесткий полифосфат-адениновый комплекс в соответствующей конформации, который включается в состав активного четырехкомпонентного комплекса.
Комплексы с мостиковым металлом
м
Enz-M-SnnnEnz |
S
Кристаллографические данные, а также анализ первичной структуры показывают, что в активных центрах многих белков в связывании металла участвует остаток гистидина (примерами служат кар-боксипептидаза А, цитохром с, рубредоксин, мет-миоглобин и метгемоглобин; см. гл. 6). Лимитирующей стадией образования бинарных (двухкомпо-нентных) комплексов Enz—М во многих случаях является вытеснение воды из координационной сферы иона металла. Активация многих пептидаз ионами металла является медленным процессом, длящимся несколько часов. Среди таких металлоферментов особое значение в живых системах имеют цитохромы и гемсодержащие ферменты, активными группировками которых служат железопорфириновые комплексы ( см. стр. [1]
Во многих металлоферментах, особенно катализирующих окислительно-восстановительные реакции, присутствуют именно металлы с переменной валентностью, действующие как акцепторы водорода, например железо, медь, марганец, молибден. Известно, что для активации таких ферментов, как ксантиноксидаза или нитроредуктаза, молибден должен быть в шестивалентном состоянии. [2]
Карбоксипептидаза – это металлофермент, содержащий один атом цинка на молекулу белка. Карбоксипептидаза катализирует гидролиз С-концевой пептидной связи в белках и олигопеп-тидах и сложных эфиров а-оксикислот. По данным рентгеноструктурного анализа Карбоксипептидаза представляет собой глобулярный белок, в котором содержится один атом цинка, координированный двумя остатками гистидина. Кроме того, в состав активного центра входят карбоксильная ( Glu-270), фенольная ( Туг-248) и гуанидиновая ( Arg-145) группы. [3]
Ингибирует широкий набор металлоферментов, включая гидроге-назу и гемоглобины ( при низких конц. СО-инги-бирование, обратимое под действием света, характерно для цитохромокси-дазы и др. гемсодержащих белков. Карбонилы Си и др. металлов не чувствительны к свету. Моноксид углерода сильно токсичен для многих живых тканей и микроорганизмов. [4]
СОД относится к металлоферментам, у которых в активном центре происходит восстановление и окисление иона металла. [5]
| Трехмерная структура химотрипсина. |
Карбоксипептидаза А – это металлофермент, который, будучи экзопепти-дазой, гидролитически отщепляет С-концевые, прежде всего ароматические, остатки аминокислот. Для работы фермента необходим ион Zn2, который с некоторыми ограничениями может быть замещен на ионы других переходных металлов. [6]
Сравнительное изучение каталитических свойств различных металлоферментов в начале было главным образом ограничено оценкой их относительной каталитической активности. Однако детальное изучение катализа и связывания лиганда для серии металлоферментов может пролить свет на роль иона металла, если при отсутствии каталитической активности сохраняется связывание металла. [7]
Прочность связи фосфата с металлоферментом удивительно велика. Константа устойчивости комплекса, равная около 106 М 1 [51, 63, 76], выше, чем можно было бы ожидать для взаимодействия НРО f – и иона двухвалентного металла. Вероятно, вблизи иона цинка находится еще один катионный центр связывания, например протон аминогруппы боковой цепи аминокислоты, взаимодействующий с кислородными атомами фосфата. Образование фосфорилфермента при реакции с субстратом и НРО можно считать твердо установленным. После разрушения белка фосфат оказывается присоединенным к серину. Отсюда делается вывод о том, что в активном центре вблизи иона цинка находится остаток серина, ориентация которого делает возможной его атаку по фосфорильному атому присоединенного производного фосфата. Вполне вероятно, что фосфорильная группа, присоединенная к серину, сохраняет связь с ионом цинка. [8]
ЭКВ отчетливо проявляются в свойствах металлоферментов. Металлы служат кофакторами многих ферментов – в большинстве классов ферментов имеются металлозависимые. [9]
В части IV рассмотрены структуры металлоферментов и механизмы, посредством которых ионы металлов принимают участие в ферментативной активности, в частности, в разрыве связей. [10]
Малер [8] подчеркивает различия между металлоферментами, в которых металл прочно связан с белком ( по существу необратимо), и ферментами, активированными металлами, в которых связь металла с белком слаба и легкообратима. [11]
В настоящее время известно более 100 истинных металлоферментов, участвующих в большинстве реакций клеточного метаболизма. Многие из них передают электроны за счет металлов с переменной валентностью. В этом случае можно постулировать, что металл принимает непосредственное участие в осуществлении каталитического акта. [12]
Ферменты окислительно-восстановительного действия являются чаще всего металлоферментами, так как в качестве компонентов каталитически активных центров этих ферментов служат металлы. В истинных металлоферментах металл прочно связан в строго определенных стехиометрических соотношениях с теми или иными химическими группировками апофермента или со специальной группой небелковой природы. [13]
В этих же органах и тканях находятся соответствующие металлоферменты или ферменты, активируемые тем или иным металлом. Так, для меди, цинка, молибдена, селена, марганца критическим органом является печень; для марганца, кобальта – также и щитовидная железа; для кадмия и цинка – мужские половые железы и почки; для бериллия – костная ткань. Полагают также, что распределение металлов внутри клетки коррелирует с содержанием в ней металлосодержащих ферментов
Источник
Большая Советская энциклопедия
один из важнейших параметров кинетики ферментативных реакций, введённый немецкими учёными Л. Михаэлисом (L. Michaelis) и М. Ментен в 1913; характеризует зависимость скорости ферментативного процесса от концентрации субстрата. Согласно теории Михаэлиса — Ментен, первым этапом любого ферментативного процесса является обратимая реакция между ферментом (Е) и субстратом (S), приводящая к образованию промежуточного фермент-субстратного комплекса (ES), который затем подвергается практически необратимому расщеплению на продукт реакции (Р) и исходный фермент:
Реакции образования и распада комплекса ES характеризуются константами скорости k1, k-1, k2. Если концентрация субстрата значительно превышает концентрацию фермента ([S] >> [E]) и, следовательно, концентрация ES становится постоянной, скорость ферментативной реакции (υ) выражается уравнением:
где V — максимальная скорость реакции, достигаемая при полном насыщении фермента субстратом. Соотношение констант скорости
также является константой (Кm), получившей название М. к. Подставляя в уравнение (2) М. к., получаем уравнение Михаэлиса — Ментен:
Из уравнения (3) следует, что М. к. численно равна концентрации субстрата, при которой скорость реакции составляет половину максимально возможной (см. рис.). В ряде случаев, когда величина k1 мала и ею можно пренебречь, М. к. становится равной
и может служить мерой сродства субстрата к ферменту. М. к. имеет размерность концентрации. Практически величину М. к. находят различными графическими методами, исследуя зависимость скорости ферментативной реакции от концентрации субстрата. См. также Ферментативный катализ.
Лит.: Яковлев В. А., Кинетика ферментативного катализа, М., 1965; Уэбб Л., Ингибиторы ферментов и метаболизма, пер. с англ., М., 1966. Д.
Д. М. Беленький.
Зависимость скорости ферментативной реакции (υ)от концентрации субстрата [S].
- константа Михаэлиса — Michaelis constant, Km – .Kинетический параметр ферментативной реакции, численно равный концентрации субстрата, при которой скорость реакции составляет половину максимальной…
Молекулярная биология и генетика. Толковый словарь
- Константа — постоянная величина. Постоянство величины х обозначается символически записью х = const…
Начала современного Естествознания
- Михаэлиса синдром — Наблюдается при патологии промежуточного мозга и включает в себя явления депрессии, повышенной сонливости и прожорливости либо мании, осложненной дисфориями и параноидными эпизодами…
Толковый словарь психиатрических терминов
- Прибор Михаэлиса — лабораторный прибор рычажного типа для определения предела прочности при изгибе образцов-балочек из цементного раствора с нагружением образца ведерком с дробью из бункера прибора…
Строительный словарь
- КОНСТАНТА — в математике и других науках – величина или коэффициент, не подвергающийся изменению. Константа может быть универсальной, как число , или конкретной, как коэффициенты, введенные в алгебраическое уравнение…
Научно-технический энциклопедический словарь
- КОНСТАНТА — остающееся неизменным при всех изменениях и расчетах…
Философская энциклопедия
- КОНСТАНТА — постоянная величина. Постоянство величины х символически записывают х = const…
Естествознание. Энциклопедический словарь
- аппарат Михаэлиса — см. Михаэлиса аппарат…
Большой медицинский словарь
- Михаэлиса аппарат — комплект для определения концентрации водородных ионов колориметрическим методом, состоящий из простейшего колориметра и набора эталонов – пробирок с жидкостью, окрашенной индикаторами…
Большой медицинский словарь
- Михаэлиса ромб — см. Крестцовый…
Большой медицинский словарь
- Фульда-Гросса-Михаэлиса метод — метод измерения активности трипсина в панкреатическом соке, основанный на определении максимальной степени разведения, при которой он способен переварить определенное количество казеина…
Большой медицинский словарь
- КОНСТАНТА — пост. величина. Постоянство величины х записывают: х = const…
Большой энциклопедический политехнический словарь
- Константа — постоянная величина в математике, физике, химии и других отраслях науки и техники, часто обозначаемая буквами С или К. К физическим константам относятся: c ≈ 3 • 108 м/с — скорость света в вакууме…
Энциклопедический словарь по металлургии
- Константа — I Конста́нта постоянная величина в математических, физических и химических исследованиях. Постоянство величины х символически записывают х = const…
Большая Советская энциклопедия
- Михаэлиса константа — один из важнейших параметров кинетики ферментативных реакций, введённый немецкими учёными Л. Михаэлисом и М. Ментен в 1913…
Большая Советская энциклопедия
- КОНСТАНТА — постоянная величина. Постоянство величины х символически записывают х=const…
Большой энциклопедический словарь
“Михаэлиса константа” в книгах
7. КОНСТАНТА ЛИВАНОВА
Существует множество эмпирических зависимостей, называемых законами. В качестве примеров можно назвать основной психофизический закон, устанавливающий зависимость силы ощущения от физической интенсивности стимула, закон постоянства скорости
7. КОНСТАНТА ЛИВАНОВА
Существует множество эмпирических зависимостей, называемых законами. В качестве примеров можно назвать основной психофизический закон, устанавливающий зависимость силы ощущения от физической интенсивности стимула, закон постоянства скорости
Константа разума
— Ну, хорошо, — согласился Скептик. — Не получается — подсмотрим у соседей. А они где берут? Где подсмотреть самое первое — то, что нет ни у кого? Ведь должно же быть что-нибудь самое первое?!Нас губит «одна, но пламенная страсть» — к упрощению. Упрощаем
Сакральная константа
Что-то здесь должно свидетельствовать об универсальной константе, геометрической модели. Хорошо известно, что Vesica Piscis создавалась с помощью сакральной геометрии, а сейчас современная наука обнаружила такую же удивительную форму в коррелированных
12. КОНСТАНТА ЖИЗНИ
Августин Блаженный невесело пошутил: «Я прекрасно знаю, что такое время, пока меня об этом не спросят». За полторы тысячи лет ничего не изменилось: о природе времени мы знаем не больше, чем рыба о воде. Время может тянуться, идти и лететь, — но мы
«Образец веры» Константа II
Церковная политика после смерти Ираклия, при Константе II, сводилась к следующему: после потери Египта, перешедшего в сороковых годах VII века к арабам, император, оставаясь сторонником монофелитства, несмотря на то, что этот вопрос потерял уже
«Образец веры» Константа II
Церковная политика после смерти Ираклия, при Константе II, сводилась к следующему: после потери Египта, перешедшего в сороковых годах VII века к арабам, император, оставаясь сторонником монофелитства, несмотря на то, что этот вопрос потерял уже
Некая константа
«Кто был в Италии, тот скажет «прощай» другим землям. Кто был на небе, тот не захочет на землю». Эти слова принадлежат классику русской литературы Николаю Гоголю.Когда солнечная Италия стала для обитателей снежной Московии земным воплощением рая,
Константа RES_USE_INET6
Поскольку функция gethostbyname не имеет аргумента для указания нужного семейства адресов (подобного hints.ai_family для getaddrinfo), в первом варианте API использовалась константа RES_USE_INET6, которая должна была добавляться к флагам распознавателя посредством внутреннего
14.2.2. Константа ARGF
Глобальная константа ARGF представляет псевдофайл, получающийся в результате конкатенации всех имен файлов, заданных в командной строке. Во многих отношениях она ведет себя так же, как объект IO.Когда в программе встречается «голый» метод ввода (без
Психическая константа
Вот есть мозг. Центральная нервная система. Кора и подкорка. Нейроны и сосуды.И вот есть мощность человеческого организма. Которую в сущности можно измерить. Надо взять потребляемую энергию на килограмм веса – и суммарную производимую работу на
Константа правды
Людям вообще трудно что-то предвидеть. В частности, то, что стало происходить с нашим телевидением, его федеральными каналами. Вот две цитаты, первая из статьи 2008 года “Суверенный экран” («ЛГ», № 36): «Вопрос о создании хотя бы одного телеканала, который
Источник
