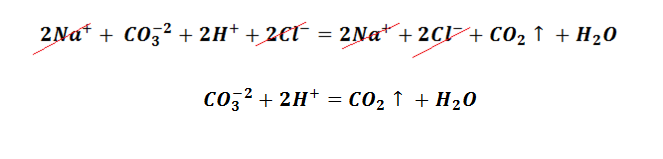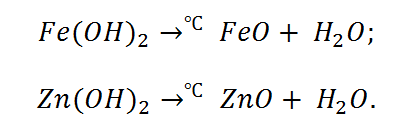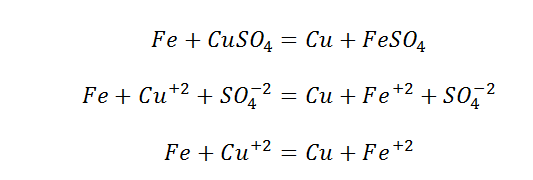Какие продукты будут находиться а растворе
Электролиз (греч. elektron – янтарь + lysis — разложение) – химическая реакция, происходящая при прохождении постоянного тока через
электролит. Это разложение веществ на их составные части под действием электрического тока.
Процесс электролиза заключается в перемещении катионов (положительно заряженных ионов) к катоду (заряжен отрицательно), и отрицательно
заряженных ионов (анионов) к аноду (заряжен положительно).
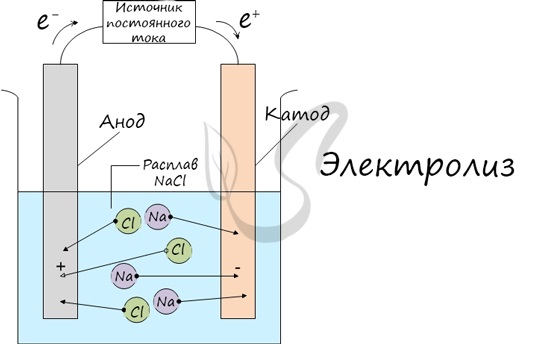
Итак, анионы и катионы устремляются соответственно к аноду и катоду. Здесь и происходит химическая реакция. Чтобы успешно решать задания
по этой теме и писать реакции, необходимо разделять процессы на катоде и аноде. Именно так и будет построена эта статья.
Катод
К катоду притягиваются катионы – положительно заряженные ионы: Na+, K+, Cu2+, Fe3+,
Ag+ и т.д.
Чтобы установить, какая реакция идет на катоде, прежде всего, нужно определиться с активностью металла: его положением в электрохимическом
ряду напряжений металлов.
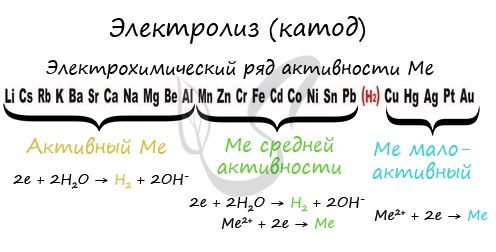
Если на катоде появился активный металл (Li, Na, K) то вместо него восстанавливаются молекулы воды, из которых выделяется водород. Если металл средней
активности (Cr, Fe, Cd) – на катоде выделяется и водород, и сам металл. Малоактивные металлы выделяются на катоде в чистом виде (Cu, Ag).
Замечу, что границей между металлами активными и средней активности в ряду напряжений считается алюминий. При электролизе на катоде металлы
до алюминия (включительно!) не восстанавливаются, вместо них восстанавливаются молекулы воды – выделяется водород.
В случае, если на катод поступают ионы водорода – H+ (например при электролизе кислот HCl, H2SO4) восстанавливается
водород из молекул кислоты: 2H+ – 2e = H2
Анод
К аноду притягиваются анионы – отрицательно заряженные ионы: SO42-, PO43-, Cl-, Br-,
I-, F-, S2-, CH3COO-.

При электролизе кислородсодержащих анионов: SO42-, PO43- – на аноде окисляются не анионы, а молекулы
воды, из которых выделяется кислород.
Бескислородные анионы окисляются и выделяют соответствующие галогены. Сульфид-ион при оксилении окислении серу. Исключением является фтор – если он
попадает анод, то разряжается молекула воды и выделяется кислород. Фтор – самый электроотрицательный элемент, поэтому и является исключением.
Анионы органических кислот окисляются особым образом: радикал, примыкающий к карбоксильной группе, удваивается, а сама карбоксильная группа (COO)
превращается в углекислый газ – CO2.
Примеры решения
В процессе тренировки вам могут попадаться металлы, которые пропущены в ряду активности. На этапе обучения вы можете пользоваться расширенным рядом
активности металлов.
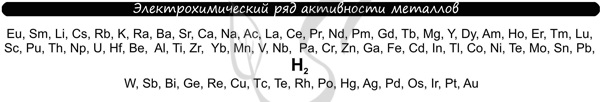
Теперь вы точно будете знать, что выделяется на катоде 😉
Итак, потренируемся. Выясним, что образуется на катоде и аноде при электролизе растворов AgCl, Cu(NO3)2, AlBr3,
NaF, FeI2, CH3COOLi.

Иногда в заданиях требуется записать реакцию электролиза. Сообщаю: если вы понимаете, что образуется на катоде, а что на аноде,
то написать реакцию не составляет никакого труда. Возьмем, например, электролиз NaCl и запишем реакцию:
NaCl + H2O → H2 + Cl2 + NaOH
Натрий – активный металл, поэтому на катоде выделяется водород. Анион не содержит кислорода, выделяется галоген – хлор. Мы пишем уравнение, так
что не можем заставить натрий испариться бесследно 🙂 Натрий вступает в реакцию с водой, образуется NaOH.
Запишем реакцию электролиза для CuSO4:
CuSO4 + H2O → Cu + O2 + H2SO4
Медь относится к малоактивным металлам, поэтому сама в чистом виде выделяется на катоде. Анион кислородсодержащий, поэтому в реакции выделяется
кислород. Сульфат-ион никуда не исчезает, он соединяется с водородом воды и превращается в серую кислоту.
Электролиз расплавов
Все, что мы обсуждали до этого момента, касалось электролиза растворов, где растворителем является вода.
Перед промышленной химией стоит важная задача – получить металлы (вещества) в чистом виде. Малоактивные металлы (Ag, Cu) можно легко получать
методом электролиза растворов.
Но как быть с активными металлами: Na, K, Li? Ведь при электролизе их растворов они не выделяются на катоде в чистом виде, вместо них восстанавливаются
молекулы воды и выделяется водород. Тут нам как раз пригодятся расплавы, которые не содержат воды.
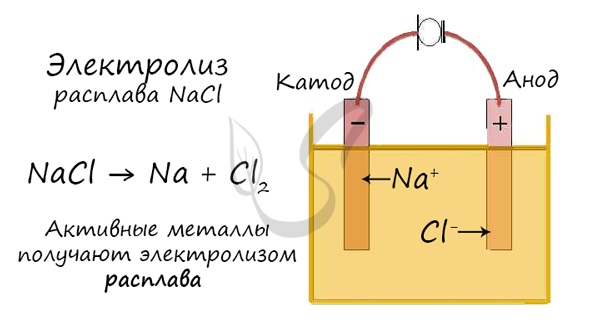
В безводных расплавах реакции записываются еще проще: вещества распадаются на составные части:
AlCl3 → Al + Cl2
LiBr → Li + Br2
© Беллевич Юрий Сергеевич 2018-2020
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение
(в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов
без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования,
обратитесь, пожалуйста, к Беллевичу Юрию.
Источник
Цели первого урока: научить писать схемы
электролиза растворов и расплавов солей и
применять полученные знания для решения
расчетных задач; продолжить формирование
навыков работы с учебником, тестовыми
материалами; обсудить применение электролиза в
народном хозяйстве.
П л а н п е р в о г о у р о к а
1. Повторение изученных способов получения
металлов.
2. Объяснение нового материала.
3. Решение задач из учебника Г.Е.Рудзитиса,
Ф.Г.Фельдмана «Химия-9» (М.: Просвещение, 2002), с. 120,
№ 1, 2.
4. Проверка усвоения знаний на тестовых
заданиях.
5. Сообщение о применении электролиза.
Цели первого урока: научить писать схемы
электролиза растворов и расплавов солей и
применять полученные знания для решения
расчетных задач; продолжить формирование
навыков работы с учебником, тестовыми
материалами; обсудить применение электролиза в
народном хозяйстве.
ХОД ПЕРВОГО УРОКА
Повторение изученных
способов получения металлов на примере
получения меди из оксида меди(II).
Запись уравнений соответствующих реакций:
Еще один способ
получения металлов из растворов и расплавов их
солей – электрохимический, или электролиз.
Электролиз – это
окислительно-восстановительный процесс,
происходящий на электродах при пропускании
электрического тока через расплав или раствор
электролита.
Электролиз расплава хлорида натрия:
NaCl Na+ + Cl–;
катод (–) (Na+): Na+ + е = Na0,
анод (–) (Cl–): Cl– – е = Cl0, 2Cl0
= Cl2;
2NaCl = 2Na + Cl2.
Электролиз раствора хлорида натрия:
NaCl Na+ + Cl–,
H2O Н+
+ ОН–;
катод (–) (Na+; Н+): H+ + е = H0,
2H0 = H2
(2H2O + 2е = H2 + 2OH–),
анод (+) (Cl–; OН–): Cl– – е = Cl0,
2Cl0 = Cl2;
2NaCl + 2H2O = 2NaOH + Cl2 + H2.
Электролиз раствора нитрата меди(II):
Cu(NO3)2 Cu2+ +
Н2O H+
+ OH–;
катод (–) (Cu2+; Н+): Cu2+ + 2е = Cu0,
анод (+) ( OН–): OH– – е = OH0,
4H0 = O2 + 2H2O;
2Cu(NO3)2 + 2H2O = 2Cu + O2 + 4HNO3.
Эти три примера показывают, почему электролиз
проводить выгоднее, чем осуществлять другие
способы получения металлов: получаются металлы,
гидроксиды, кислоты, газы.
Мы писали схемы электролиза, а теперь попробуем
написать сразу уравнения электролиза, не
обращаясь к схемам, а только используя шкалу
активности ионов:
Примеры уравнений электролиза:
2HgSO4 + 2H2O = 2Hg + O2 + 2H2SO4;
Na2SO4 + 2H2O = Na2SO4
+ 2H2 + O2;
2LiCl + 2H2O = 2LiOH + H2 + Cl2.
Решение задач из
учебника Г.Е.Рудзитиса и Ф.Г.Фельдмана (9-й класс,
с. 120, № 1, 2).
Задача 1. При электролизе раствора хлорида
меди(II) масса катода увеличилась на 8 г. Какой газ
выделился, какова его масса?
Решение
CuCl2 + H2O = Cu + Cl2 + H2O,
(Cu) = 8/64 = 0,125
моль,
(Cu) = (Сl2) = 0,125 моль,
m(Cl2) = 0,125•71 = 8,875 г.
Ответ. Газ – хлор массой 8,875 г.
Задача 2. При электролизе водного раствора
нитрата серебра выделилось 5,6 л газа. Сколько
граммов металла отложилось на катоде?
Решение
4AgNO3 + 2H2O = 4Ag + O2 + 4HNO3,
(O2) = 5,6/22,4 =
0,25 моль,
(Ag) = 4(O2) = 4•25 = 1 моль,
m(Ag) = 1•107 = 107 г.
Ответ. 107 г серебра.
Тестирование
Вариант 1
1. При электролизе раствора гидроксида
калия на катоде выделяется:
а) водород; б) кислород; в) калий.
2. При электролизе раствора сульфата меди(II)
в растворе образуется:
а) гидроксид меди(II);
б) серная кислота;
в) вода.
3. При электролизе раствора хлорида бария на
аноде выделяется:
а) водород; б) хлор; в) кислород.
4. При электролизе расплава хлорида
алюминия на катоде выделяется:
а) алюминий; б) хлор;
в) электролиз невозможен.
5. Электролиз раствора нитрата серебра
протекает по следующей схеме:
а) AgNO3 + H2O Ag + Н2 + HNO3;
б) AgNO3 + H2O Ag + О2 + HNO3;
в) AgNO3 + H2O AgNO3
+ Н2 + О2.
Вариант 2
1. При электролизе раствора гидроксида
натрия на аноде выделяется:
а) натрий; б) кислород; в) водород.
2. При электролизе раствора сульфида натрия
в растворе образуется:
а) сероводородная кислота;
б) гидроксид натрия;
в) вода.
3. При электролизе расплава хлорида ртути(II)
на катоде выделяется:
а) ртуть; б) хлор; в) электролиз невозможен.
4. При электролизе раствора нитрата серебра
на катоде выделяется:
а) серебро; б) водород; в) кислород.
5. Электролиз раствора нитрата ртути(II)
протекает по следующей схеме:
а) Hg(NO3)2 + H2O Hg + Н2 + HNO3;
б) Hg(NO3)2 + H2O Hg + О2 + HNO3;
в) Hg(NO3)2 + H2O Hg(NO3)2 + Н2 + О2.
Вариант 3
1. При электролизе раствора нитрата меди(II)
на катоде выделяется:
а) медь; б) кислород; в) водород.
2. При электролизе раствора бромида лития в
растворе образуется:
а) вода;
б) бромоводородная кислота;
в) гидроксид лития.
3. При электролизе расплава хлорида серебра
на катоде выделяется:
а) серебро; б) хлор; в) электролиз невозможен.
4. При электролизе раствора хлорида
алюминия алюминий выделяется на:
а) катоде; б) аноде; в) остается в растворе.
5. Электролиз раствора бромида бария
протекает по следующей схеме:
а) BaBr2 + H2O Br2
+ Н2 + Ba(OH)2;
б) BaBr2 + H2O Br2
+ Ba + H2O;
в) BaBr2 + H2O Br2
+ О2 + Ba(OH)2.
Вариант 4
1. При электролизе раствора гидроксида
бария на аноде выделяется:
а) водород; б) кислород; в) барий.
2. При электролизе раствора йодида калия в
растворе образуется:
а) йодоводородная кислота;
б) вода; в) гидроксид калия.
3. При электролизе расплава хлорида
свинца(II) на катоде выделяется:
а) свинец; б) хлор; в) электролиз невозможен.
4. При электролизе раствора нитрата серебра
на катоде выделяется:
а) серебро; б) водород; в) кислород.
5. Электролиз раствора сульфида натрия
протекает по следующей схеме:
а) Na2S + H2O S + Н2 + NaOH;
б) Na2S + H2O Н2 + O2 + Na2S;
в) Na2S + H2O Н2 + Na2S + NaOH.
Ответы
| Вариант | Вопрос 1 | Вопрос 2 | Вопрос 3 | Вопрос 4 | Вопрос 5 |
| 1 | а | б | б | а | б |
| 2 | б | б | а | а | б |
| 3 | а | в | а | в | а |
| 4 | б | в | а | а | а |
Применение
электролиза в народном хозяйстве
1. Для защиты металлических изделий от
коррозии на их поверхность наносят тончайший
слой другого металла: хрома, серебра, золота,
никеля и т.д. Иногда, чтобы не расходовать дорогие
металлы, производят многослойное покрытие.
Например, внешние детали автомобиля сначала
покрывают тонким слоем меди, на медь наносят
тонкий слой никеля, а на него – слой хрома.
При нанесении покрытий на металл электролизом
они получаются ровными по толщине, прочными.
Таким способом можно покрывать изделия любой
формы. Эту отрасль прикладной электрохимии
называют гальваностегией.
2. Кроме защиты от коррозии гальванические
покрытия придают красивый декоративный вид
изделиям.
3. Другая отрасль электрохимии, близкая по
принципу к гальваностегии, названа
гальванопластикой. Это процесс получения точных
копий различных предметов. Для этого предмет
покрывают воском и получают матрицу. Все
углубления копируемого предмета на матрице
будут выпуклостями. Поверхность восковой
матрицы покрывают тонким слоем графита, делая ее
проводящей электрический ток.
Полученный графитовый электрод опускают в
ванну с раствором сульфата меди. Анодом служит
медь. При электролизе медный анод растворяется, а
на графитовом катоде осаждается медь. Таким
образом получается точная медная копия.
С помощью гальванопластики изготавливают
клише для печати, грампластинки, металлизируют
различные предметы. Гальванопластика открыта
русским ученым Б.С.Якоби (1838).
Изготовление штампов для грампластинок
включает нанесение тончайшего серебряного
покрытия на пластмассовую пластинку, чтобы она
стала электропроводной. Затем на пластинку
наносят электролитическое никелевое покрытие.
Чем следует сделать пластинку в
электролитической ванне – анодом или катодом?
(О т в е т. Катодом.)
4. Электролиз используют для получения
многих металлов: щелочных, щелочно-земельных,
алюминия, лантаноидов и др.
5. Для очистки некоторых металлов от
примесей металл с примесями подключают к аноду.
Металл растворяется в процессе электролиза и
выделяется на металлическом катоде, а примесь
остается в растворе.
6. Электролиз находит широкое применение
для получения сложных веществ (щелочей,
кислородсодержащих кислот), галогенов.
Схема электролиза воды |
Практическая работа
(второй урок)
Цели урока. Провести электролиз воды,
показать гальваностегию на практике, закрепить
знания, полученные на первом уроке.
Оборудование. На столах учащихся:
плоская батарейка, два провода с клеммами, два
графитовых электрода, химический стакан,
пробирки, штатив с двумя лапками, 3%-й раствор
сульфата натрия, спиртовка, спички, лучина.
На столе учителя: то же + раствор медного
купороса, латунный ключ, медная трубка (кусок
меди).
Инструктаж учащихся
1. Прикрепить провода клеммами к электродам.
2. Электроды поставить в стакан, чтобы они не
соприкасались.
3. Налить в стакан раствор электролита (сульфата
натрия).
4. В пробирки налить воды и, опустив их в стакан с
электролитом кверху дном, надеть их на
графитовые электроды поочередно, закрепив
верхний край пробирки в лапке штатива.
5. После того как прибор будет смонтирован,
концы проводов прикрепить к батарейке.
6. Наблюдать выделение пузырьков газов: на аноде
их выделяется меньше, чем на катоде. После того
как в одной пробирке почти вся вода вытеснится
выделяющимся газом, а в другой – наполовину,
отсоединить провода от батарейки.
7. Зажечь спиртовку, осторожно снять пробирку,
где вода почти полностью вытеснилась, и поднести
к спиртовке – раздастся характерный хлопок газа.
8. Зажечь лучину. Снять вторую пробирку,
проверить тлеющей лучиной газ.
Задания для учащихся
1. Зарисовать прибор.
2. Написать уравнение электролиза воды и
пояснить, почему надо было проводить электролиз
в растворе сульфата натрия.
3. Написать уравнения реакций, отражающие
выделение газов на электродах.
Учительский демонстрационный
эксперимент
(могут выполнять лучшие ученики класса
при наличии соответствующего оборудования)
1. Подсоединить клеммы проводов к медной трубке
и латунному ключу.
2. Опустить трубку и ключ в стакан с раствором
сульфата меди(II).
3. Подсоединить вторые концы проводов к
батарейке: «минус» батарейки к медной трубке,
«плюс» к ключу!
4. Наблюдать выделение меди на поверхности
ключа.
5. После выполнения эксперимента вначале
отсоединить клеммы от батарейки, затем вынуть
ключ из раствора.
6. Разобрать схему электролиза с растворимым
электродом:
CuSО4 = Сu2+ +
анод (+): Сu0 – 2e = Cu2+,
катод (–): Cu2+ + 2e = Сu0.
Суммарное уравнение электролиза с растворимым
анодом написать нельзя.
Электролиз проводился в растворе сульфата
меди(II), поскольку:
а) нужен раствор электролита, чтобы протекал
электрический ток, т.к. вода является слабым
электролитом;
б) не будут выделяться какие-либо побочные
продукты реакций, а только медь на катоде.
Ученик 9-го класса проводит |
7. Для закрепления пройденного написать
схему электролиза хлорида цинка с угольными
электродами:
ZnCl2 = Zn2+ + 2Cl–,
катод (–): Zn2+ + 2e = Zn0,
2H2O + 2e = H2 + 2OH–,
анод (+): 2Cl– – 2e = Cl2.
Суммарное уравнение реакции в данном случае
написать нельзя, т.к. неизвестно, какая часть
общего количества электричества идет на
восстановление воды, а какая – на восстановление
ионов цинка.
Схема демонстрационного |
Домашнее задание
1. Написать уравнение электролиза раствора,
содержащего смесь нитрата меди(II) и нитрата
серебра, с инертными электродами.
2. Написать уравнение электролиза раствора
гидроксида натрия.
3. Чтобы очистить медную монету, ее надо
подвесить на медной проволоке, присоединенной к
отрицательному полюсу батареи, и опустить в 2,5%-й
раствор NаОН, куда следует погрузить также
графитовый электрод, присоединенный к
положительному полюсу батареи. Объясните, каким
образом монета становится чистой. (Ответ. На
катоде идет восстановление ионов водорода:
2Н+ + 2е = Н2.
Водород вступает в реакцию с оксидом меди,
находящимся на поверхности монеты:
СuО + Н2 = Сu + Н2О.
Этот способ лучше, чем чистка порошком, т.к. не
стирается монета.)
М.А.АЛЕКСАНДРОВА,
учитель химии школы № 81
(Москва)
Источник
План урока:
Особенности протекания реакций в растворе
Кислоты и их свойства
Основания и их свойства
Соли и их свойства
Особенности протекания реакций в растворе
Химические реакции, в отличие от физических, характеризуются образованием новых веществ. Судить об их получении, мы можем, наблюдая изменение окраски, либо выделение газа или осадка.
Вспомним, что происходит с веществом, когда оно попадает в воду. Оно распадается на ионы. Тем не менее, этот процесс характерен не для всех веществ, а только для сильных электролитов, к которым относятся растворимые соли и кислоты, а также щёлочи.

Также необходимо вспомнить, какие реакции относятся к типу обмена.
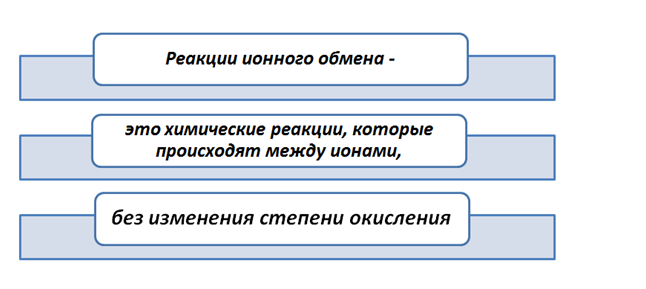
Судить произошла реакция или нет, мы можем, если будет выполняться хотя бы одно из условий.
Условия протекания реакций между ионами сложных веществ.
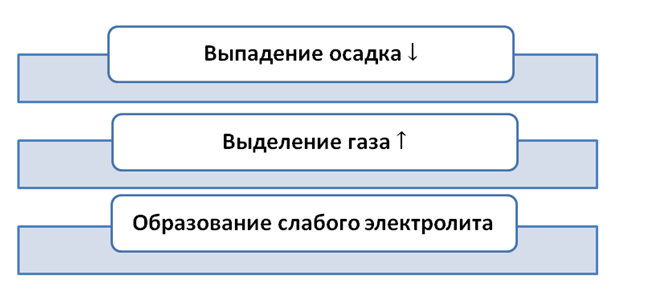
Рассмотрим подробно каждое условие и составим алгоритм написания уравнений.
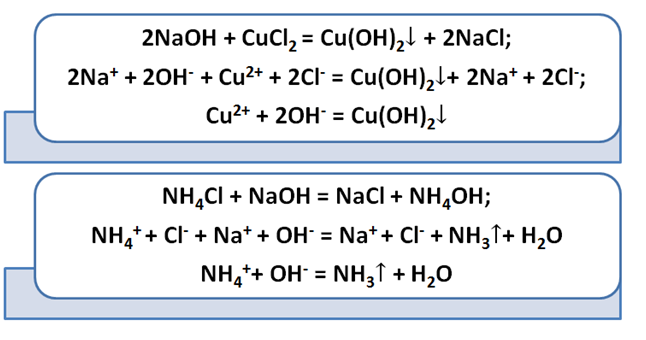
Выпадение осадка является подтверждением того, мы визуально видим, что реакция произошла. Составим уравнение между щёлочью – гидроксидом калия и солью – сульфатом меди (II). Запишем молекулярное уравнение.

Выполняя данный опыт, Вы могли бы наблюдать образование осадка голубого цвета.

Чтобы понять, какое вещество выпало в осадок, воспользуемся таблицей растворимости, а также составим полное ионно-молекулярное уравнение, которое отображает все частицы, находящиеся в растворе, с учётом коэффициентов.

Таким образом, KOH, K2SO4 и CuSO4 – это сильные электролиты, которые запишем в ионном виде. Cu(OH)2 – нерастворимое вещество, будет в молекулярном виде со стрелкой ↓. Также обращаем внимание, что перед щёлочью КОН находится коэффициент 2. Значит, образуется по два моля ионов К+ и ОН−.
При написании уравнений реакций, не забываем о законе сохранения вещества. Поэтому количество атомов, а также ионов, до реакции и после должны быть равны.
Следует отметить, что в полном ионно-молекулярном уравнении, слева и справа, имеются одинаковые частицы, их можно сократить.
Эти ионы при взаимодействии не образуют вещества, поэтому находятся в растворе в свободном виде как K+и SO4−2.
Сокращённая реакция ионного обмена отображает суть химического процесса, а именно, между какими частицами происходит реакция.
Следственно, Cu(OH)2 будет осадком в растворе состоящем из ионов SO42−и К+.
Вторым из условий является выделение газа. Эту реакцию Вы наблюдаете, когда гасите соду кислотой, не важно, какой уксусной, лимонной, яблочной, или же при добавлении к ней кефира, результат будет один и тот же, образование пузырьков углекислого газа. Для примера возьмём взаимодействие соды и соляной кислоты. Составим молекулярное уравнение.
Возникает закономерный вопрос, в уравнении отсутствует газ, однако раствор «шипит». Чтобы разобраться в этой проблеме, следует вспомнить, что угольная кислота относится к слабым электролитам и происходит выделение углекислого газа, а также образование молекулы воды. Поэтому полное молекулярно-ионное уравнение приобретает вид.
После сокращение одинаковых частиц левой и правой части, получаем сокращённое ионное уравнение.
Именно по причине наличия ионов водорода, сода «шипит» во всех кислотах.
И к третьему условию относится образование слабого электролита, зачастую это молекула воды, однако могут получаться и другие вещества. Ярким примером является реакция нейтрализации.

Почему этот тип реакции носит такое название? Рассмотрим на примере взаимодействия оснований КОН и Cu(OH)2 с раствором соляной кислоты.

В каждом случае происходит образование воды. В случае нерастворимых оснований, реакция идёт с образованием растворимой соли.
Уравнение реакции нейтрализации показывает, как два противоположных по свойствам класса неорганических соединений, отдавая по своей частице (Н+ и ОН-), образуют нейтральное вещество Н2О.
Кислоты и их свойства
Если посмотреть на состав этого класса соединений, то абсолютно во всех содержаться ионы водорода.

Следует заметить, что уравнение диссоциации кислот похожи, но отличие будет по кислотному остатку.Рассмотрим на примерах следующих многоосновных кислот –сернойН2SО4 и фосфорной Н3РО4.Характерной особенностью диссоциации многоосновных кислот – это ступенчатая диссоциация. Это означает, что ионы водорода будут отрываться не сразу все (2 или 3), а по одному.

Следствием этого является способность многоосновных кислот образовывать кислые соли.
Рассмотрим химические свойства кислот, за которые отвечают ионы Н+.
Каким образом можно доказать, что неизвестное вещество относится к кислотам. Для этих целей создали индикаторы, которые как настоящие сыщики, ищут ионы Н+ или ОН- (в основаниях). Найдя их, они моментально меняют свою окраску. Кислая среда обусловлена наличием Н+.

Источник
В реакциях обмена на их место могут стать только ионы металла, поэтому кислоты реагируют со следующими веществами.

Следственно, при реакции кислот с основными оксидами образуется соль и вода.
Атомы металла входят в состав оснований, в результате реакции нейтрализации, аналогично, как и основными оксидами, продуктом реакции является соль (может быть и кислая, и средняя) и вода.
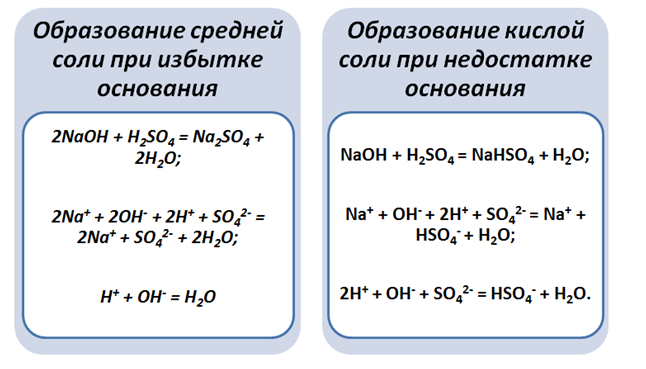
Исходя из этого, кислая соль образуется, если «не хватает» атомов металла, чтобы обменять их на атомы водорода.
Взаимодействие кислот с солями возможно только в случае, когда соль образована слабой или летучей кислотой, а также в продукте будет газ или осадок.

Источник

Особенно хочется отметить взаимодействие металлов с кислотами, поскольку это будет реакция замещения со сменой степени окисления. Не все металлы способны реагировать с кислотами, а только те, что стоят в ряду напряжения до водорода и способны его вытеснить.
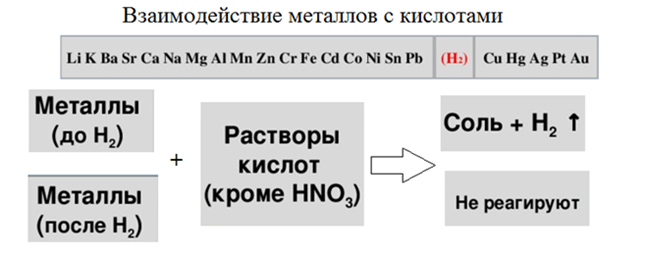
Действие концентрированных серной и азотной кислот на металлы отличается от их растворов, при этом происходит образование не водорода, а воды и других продуктов. Детально со свойствами азотной кислоты Вы познакомитесь чуть позже, однако сейчас необходимо запомнить, что при реакции с раствором этой кислоты водород не выделяется.

Основания и их свойства
Данный класс веществ характеризуется наличием функциональной группы, которая отвечает за химические свойства, а именно группы ОН-. По растворимости основания делятся на щёлочи (растворимые) и нерастворимые основания. Соответственно они будут отличаться по химическим свойствам. Щелочная среда образуется, если есть свободные ОН-, которые образуются при диссоциации щелочей.
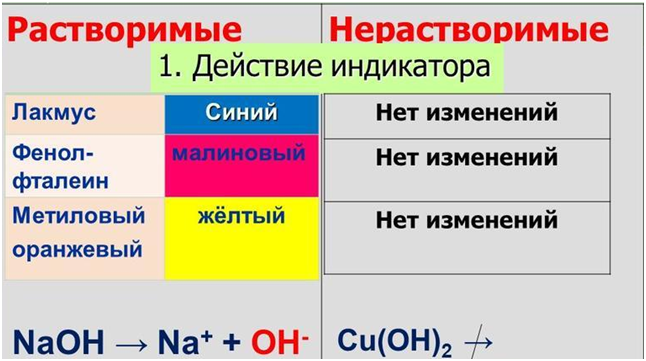
Для щелочей, подобно многоосновным кислотам, характерна ступенчатая диссоциация.

Тем не менее, будет происходить не только взаимодействие щелочей с кислотами, но и нерастворимых оснований. Объяснением этому служит, то, что кислоты практически все растворимы, за исключением силикатной H2SiO3, которая реагирует только со щелочами. Продуктом будет соль (в зависимости от соотношения реагентов средняя, основная или кислая) и вода.

Кислотные оксиды со щелочами образуют соль и воду.

Для нерастворимых оснований эта реакция не характерна, поскольку именно гидроксильная группа реагирует с оксидами.
Амфотерные основания реагируют также с щелочами. Результатом данного взаимодействия будет соль, зачастую комплексная, и вода.

Взаимодействие солей с щелочами приводит к образованию соли либо основания. Также не забываем об условии, что в продукте должен быть либо газ, либо осадок.
Отличительной способностью обладают нерастворимые, а также амфотерные основания. Они при нагревании распадаются на оксиды.
Соли и их свойства
Этот класс веществ состоит из частичек кислоты – кислотного остатка и основания – катионов металла (либо иона аммония NH4+). Диссоциация солей всегда идёт в одну стадию.

Если посмотреть на состав соли, то смело можно предположить, что их растворы будут нейтральными. Поскольку нет ионов, которые отвечают за реакцию среды. Однако на деле совсем не так. Лакмус в водном растворе солей может иметь как красную, так и синюю окраску, а также не изменять её. Объяснением этого явления служит их взаимодействие с водой, которое имеет название гидролиз солей. Возьмём, к примеру, три пробирки, в которых содержатся растворы NaCl, ZnCl2 и Na2CO3. И в каждую добавим лакмус. Результаты эксперимента отображены на рисунке.
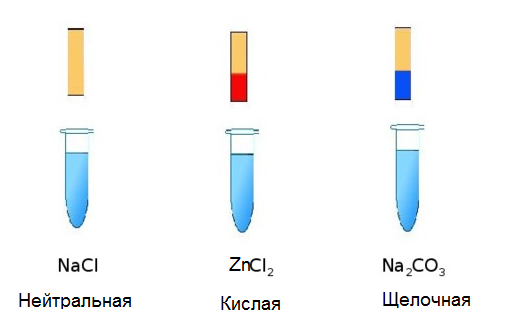
Запишем суть реакции соли с водой (молекулу Н2О распишем как НОН), с помощью ионно-молекулярных уравнений.

Сокращённое уравнение хорошо иллюстрирует, почему происходит изменение окраски индикатора. Теперь давайте разберёмся, какие соли подвергаются гидролизу.

Именно наличием ионов Н+ в растворе соли ZnCl2, а также группы ОН- в солевом растворе карбоната натрия, объясняется изменение окраски индикатора.

Источник
Рассмотрим взаимодействие металлов с солями. Чтобы понять принцип их взаимодействия, вспомним ряд активностей металлов.

Данный вид взаимодействия Вы можете наблюдать, выполнив дома опыт (не забываем о разрешении родителей). Вам понадобится раствор медного купороса и скрепка, либо гвоздь.
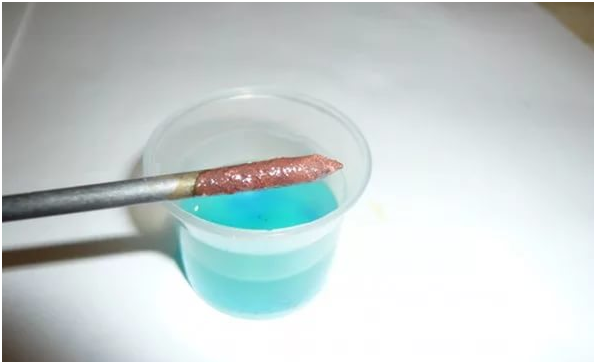
Источник
На поверхности гвоздя выделилась медь в чистом виде. Это окислительно-восстановительная реакция.
Более сильный металл, вытесняет слабый с раствора его соли. Если промоделировать обратную реакцию, а именно положить медную проволоку в раствор соли железа, то не будет никакого взаимодействия. «Силы» у меди не хватит, потеснить железо.
Взаимодействие солей между собой возможно только, если реагенты растворимы, а в продукте будет осадок.

Свойства солей, кислот и оснований, рассмотренных выше, можно объединить в схематическом виде.

Источник
Источник