Какие оксиды обладают кислотными свойствами

Оксиды – сложные вещества, состоящие из двух элементов, один из которых кислород. В названиях оксидов сначала указывают слово оксид, затем название второго элемента, которым он образован. Какие особенности имеют кислотные оксиды, и чем они отличаются от других видов оксидов?

Классификация оксидов
Оксиды делятся на солеобразующие и несолеобразующие. Уже по названию ясно, что несолеобразующие не образуют солей. Таких оксидов немного : это вода H2 O, фторид кислорода OF2 (если условно его считать оксидом), угарный газ, или оксид углерода (II), монооксид углерода CO; оксиды азота (I) и (II): N2 O (оксид диазота, веселящий газ) и NO (монооксид азота).
Солеобразующие оксиды образуют соли при взаимодействии с кислотами или щелочами. В качестве гидроксидов им соответствуют основания, амфотерные основания и кислородосодержащие кислоты. Соответственно они называются основными оксидами (например, CaO), амфотерными оксидами (Al2 O3 ) и кислотными оксидами, или ангидридами кислот (CO2).
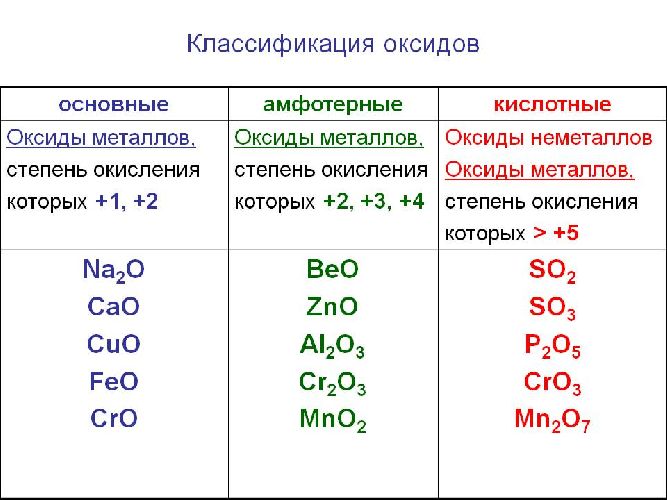
Рис. 1. Виды оксидов.
Часто перед учащимися встает вопрос, как отличить основной оксид от кислотного. Прежде всего необходимо обратить внимание на второй элемент рядом с кислородом. Кислотные оксиды – содержат неметалл или переходный металл (CO2 , SO3 , P2 O5 ) основные оксиды – содержат металл (Na2 O, FeO, CuO).
Основные свойства кислотных оксидов
Кислотные оксиды (ангидриды) – вещества, которые проявляют кислотные свойства и образуют кислородосодержащие кислоты. Следовательно, кислотным оксидам соответствуют кислоты. Например, кислотным оксидам SO2 ,SO3 соответствуют кислоты H2 SO3 и H2 SO4 .
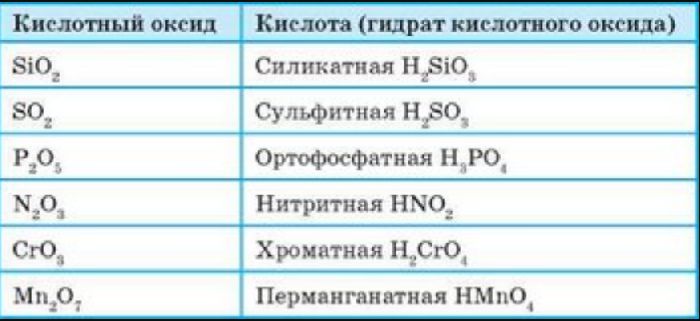
Рис. 2. Кислотные оксиды с соответствующими кислотами.
Кислотные оксиды, образуемые неметаллами и металлами с переменной валентностью в высшей степени окисления (например, SO3 , Мn2 O7 ), реагируют с основными оксидами и щелочами, образуя соли:
SO3 (кислотный оксид)+CaO (основной оксид)=СaSO4 (соль);
Типичными реакциями являются взаимодействие кислотных оксидов с основаниями в результате чего образуется соль и вода:
Mn2 O7 (кислотный оксид)+2KOH (щелочь)=2KMnO4 (соль)+H2O (вода)
Все кислотные оксиды, кроме диоксида кремния SiO2 (кремниевый ангидрид, кремнезем), реагируют с водой, образуя кислоты:
SO3 (кислотный оксид)+H2O (вода)=H2SO4 (кислота)
Кислотные оксиды образуются при взаимодействии с кислородом простых и сложных веществ (S+O2 =SO2 ), либо при разложении в результате нагревания сложных веществ, содержащих кислород, – кислот, нерастворимых оснований, солей (H2 SiO3 =SiO2 +H2 O).
Список кислотных оксидов:
| Название кислотного оксида | Формула кислотного оксида | Свойства кислотного оксида |
| Оксид серы (IV) | SO2 | бесцветный токсичный газ с резким запахом |
| Оксид серы (VI) | SO3 | легколетучая безцветная токсичная жидкость |
| Оксид углерода (IV) | CO2 | бесцветный газ без запаха |
| Оксид кремния (IV) | SiO2 | бесцветные кристаллы, обладающие прочностью |
| Оксид фосфора (V) | P2 O5 | белый легковозгораемый порошок с неприятным запахом |
| Оксид азота (V) | N2 O5 | вещество, состоящее из бесцветных летучих кристаллов |
| Оксид хлора (VII) | Cl2 O7 | бесцветная маслянистая токсичная жидкость |
| Оксид марганца (VII) | Mn2 O7 | жидкость с металлическим блеском, являющаяся сильным окислителем. |

Рис. 3. Примеры кислотные оксиды.
Что мы узнали?
Кислотные оксиды относятся к солеобразующим оксидам и образуются с помощью кислот. Кислотные оксиды вступают в реакции с основаниями и водой, а их образование происходит при нагревании и разложении сложных веществ.
Тест по теме
Оценка доклада
Средняя оценка: 4.5. Всего получено оценок: 876.
Источник
Оксиды — это сложные вещества, состоящие из атомов двух элементов, один из которых — кислород со степенью окисления -2. При этом кислород связан только с менее электроотрицательным элементом.
В зависимости от второго элемента оксиды проявляют разные химические свойства. В школьном курсе оксиды традиционно делят на солеобразующие и несолеобразующие. Некоторые оксиды относят к солеобразным (двойным).
Двойные оксиды — это некоторые оксиды , образованные элементом с разными степенями окисления.
Солеобразующие оксиды делят на основные, амфотерные и кислотные.
Основные оксиды — это оксиды, обладающие характерными основными свойствами. К ним относят оксиды, образованные атомами металлов со степень окисления +1 и +2.
Кислотные оксиды — это оксиды, характеризующиеся кислотными свойствами. К ним относят оксиды, образованные атомами металлов со степенью окисления +5, +6 и +7, а также атомами неметаллов.
Амфотерные оксиды — это оксиды, характеризующиеся и основными, и кислотными свойствами. Это оксиды металлов со степенью окисления +3 и +4, а также четыре оксида со степенью окисления +2: ZnO, PbO, SnO и BeO.
Несолеобразующие оксиды не проявляют характерных основных или кислотных свойств, им не соответствуют гидроксиды. К несолеобразующим относят четыре оксида: CO, NO, N2O и SiO.
Классификация оксидов

Тренировочные тесты по теме Классификация оксидов.
Получение оксидов
Общие способы получения оксидов:
1. Взаимодействие простых веществ с кислородом:
1.1. Окисление металлов: большинство металлов окисляются кислородом до оксидов с устойчивыми степенями окисления.
Например, алюминий взаимодействует с кислородом с образованием оксида:
4Al + 3O2 → 2Al2O3
Не взаимодействуют с кислородом золото, платина, палладий.
Натрий при окислении кислородом воздуха образует преимущественно пероксид Na2O2,
2Na + O2 → 2Na2O2
Калий, цезий, рубидий образуют преимущественно пероксиды состава MeO2:
K + O2 → KO2
Примечания: металлы с переменной степенью окисления окисляются кислородом воздуха, как правило, до промежуточной степени окисления (+3):
4Fe + 3O2 → 2Fe2O3
4Cr + 3O2 → 2Cr2O3
Железо также горит с образованием железной окалины — оксида железа (II, III):
3Fe + 2O2 → Fe3O4
1.2. Окисление простых веществ-неметаллов.
Как правило, при окислении неметаллов образуется оксид неметалла с высшей степенью окисления, если кислород в избытке, или оксид неметалла с промежуточной степенью окисления, если кислород в недостатке.
Например, фосфор окисляется избытком кислорода до оксида фосфора (V), а под действием недостатка кислорода до оксида фосфора (III):
4P + 5O2(изб.) → 2P2O5
4P + 3O2(нед.) → 2P2O3
Но есть некоторые исключения.
Например, сера сгорает только до оксида серы (IV):
S + O2 → SO2
Оксид серы (VI) можно получить только окислением оксида серы (IV) в жестких условиях в присутствии катализатора:
2SO2 + O2 = 2SO3
Азот окисляется кислородом только при очень высокой температуре (около 2000оС), либо под действием электрического разряда, и только до оксида азота (II):
N2 + O2 = 2NO
Не окисляется кислородом фтор F2 (сам фтор окисляет кислород). Не взаимодействуют с кислородом прочие галогены (хлор Cl2, бром и др.), инертные газы (гелий He, неон, аргон, криптон).
2. Окисление сложных веществ (бинарных соединений): сульфидов, гидридов, фосфидов и т.д.
При окислении кислородом сложных веществ, состоящих, как правило, из двух элементов, образуется смесь оксидов этих элементов в устойчивых степенях окисления.
Например, при сжигании пирита FeS2 образуются оксид железа (III) и оксид серы (IV):
4FeS2 + 11O2 → 2Fe2O3 + 8SO2
Сероводород горит с образованием оксида серы (IV) при избытке кислорода и с образованием серы при недостатке кислорода:
2H2S + 3O2(изб.) → 2H2O + 2SO2
2H2S + O2(нед.) → 2H2O + 2S
А вот аммиак горит с образованием простого вещества N2, т.к. азот реагирует с кислородом только в жестких условиях:
4NH3 + 3O2 →2N2 + 6H2O
А вот в присутствии катализатора аммиак окисляется кислородом до оксида азота (II):
4NH3 + 5O2 → 4NO + 6H2O
3. Разложение гидроксидов. Оксиды можно получить также из гидроксидов — кислот или оснований. Некоторые гидроксиды неустойчивы, и самопроизвольную распадаются на оксид и воду; для разложения некоторых других (как правило, нерастворимых в воде) гидроксидов необходимо их нагревать (прокаливать).
гидроксид → оксид + вода
Самопроизвольно разлагаются в водном растворе угольная кислота, сернистая кислота, гидроксид аммония, гидроксиды серебра (I), меди (I):
H2CO3 → H2O + CO2
H2SO3 → H2O + SO2
NH4OH → NH3 + H2O
2AgOH → Ag2O + H2O
2CuOH → Cu2O + H2O
При нагревании разлагаются на оксиды большинство нерастворимых гидроксидов — кремниевая кислота, гидроксиды тяжелых металлов — гидроксид железа (III) и др.:
H2SiO3 → H2O + SiO2
2Fe(OH)3 → Fe2O3 + 3H2O
4. Еще один способ получения оксидов — разложение сложных соединений — солей.
Например, нерастворимые карбонаты и карбонат лития при нагревании разлагаются на оксиды:
Li2CO3 → CO2 + Li2O
CaCO3 → CaO + CO2
Соли, образованные сильными кислотами-окислителями (нитраты, сульфаты, перхлораты и др.), при нагревании, как правило, разлагаются с с изменением степени окисления:
2Zn(NO3)2 → 2ZnO + 4NO2 + O2
Более подробно про разложение нитратов можно прочитать в статье Окислительно-восстановительные реакции.
Химические свойства оксидов
Значительная часть химических свойств оксидов описывается схемой взаимосвязи основных классов неорганических веществ.
Химические свойства основных оксидов
Подробно про химические свойства оксидов можно прочитать в соответствующих статьях:
Химические свойства основных оксидов.
Химические свойства кислотных оксидов.
Химические свойства амфотерных оксидов.
Источник
Определение
Оксиды – бинарные соединения, в состав которых входит кислород в степени окисления -2.
Номенклатура оксидов
Названия оксидов строятся по следующим правилам систематической номенклатуры:
Сначала указывают слово оксид, после него, в родительном падеже, – название второго элемента.
Если элемент, образующий оксид, имеет единственную валентность, то её в названии оксида можно не указывать. Если же элемент имеет переменную валентность и образует несколько оксидов, то валентность элемента обязательно указывается римскими цифрами в скобках в конце записи названия оксида.
При записи химической формулы оксида кислород записывается на последнем месте.
Примеры:
$Na_2O$ – оксид натрия
$CaO$ – оксид кальция
$Al_2O_3$ – оксид алюминия
$overset{+7}{Mn_2}O_7$ – оксид марганца (VII)
$overset{+2}{Cr}O$ – оксид хрома (II)
$overset{+3}{Cr_2}O_3$ – оксид хрома (III)
В настоящее время при формировании названий оксидов пользуются правилами систематической номенклатуры. Однако до её появления, пока число известных соединений было не столь велико, широко использовалась тривиальная номенклатура, в которой названия веществ основаны не на особенностях их строения, а на внешнем виде или каких-то специфических свойствах именуемых объектов. Многие тривиальные названия распространены и в наше время.
На смену тривиальной номенклатуре пришла полусистематическая номенклатура. В полусистематических названиях веществ с помощью использования морфем пытались отразить особенности химического строения соединений. Применительно к оксидам вводились следующие названия: закись – для оксидов элементов в низких степенях окисления, окись – для более высоких степеней окисления. Кислотные оксиды часто рассматривали как продукты дегидратации соответствующих кислот и отражали это в виде названия ангидрид: $P_2O_5$ – фосфорный ангидрид, $SO_3$ – серный ангидрид и т.д.
Таблица 1
Формулы и названия некоторых оксидов в соответствии с тривиальной, полусистематической и систематической номенклатурой
| Формула | Тривиальное название | Устаревшее название | Систематическое название |
| $N_2O$ | веселящий газ | закись азота | оксид азота (I) |
| $NO$ | окись азота | оксид азота (II) | |
| $N_2O_3$ | трёхокись азота, азотистый ангидрид | оксид азота (III) | |
| $NO_2$ | бурый газ | двуокись азота | оксид азота (IV) |
| $N_2O_5$ | пятиокись азота, азотный ангидрид | оксид азота (V) | |
| $SO_2$ | сернистый газ | двуокись серы, сернистый ангидрид | оксид серы (IV) |
| $SO_3$ | трёхокись серы, серный ангидрид | оксид серы (VI) | |
| $CO$ | угарный газ | окись углерода | оксид углерода (II) |
| $CO_2$ | углекислый газ | двуокись углерода | оксид углерода (IV) |
| $Na_2O$ | натр | окись натрия | оксид натрия |
| $MgO$ | жжёная магнезия | окись магния | оксид магния |
| $CaO$ | жжёная известь, негашёная известь | окись кальция | оксид кальция |
| $Al_2O_3$ | глинозём | окись алюминия | оксид алюминия |
| $SiO_2$ | кремнезём | двуокись кремния | оксид кремния (IV) |
| $Fe_3O_4$ | железная окалина | закись-окись железа | оксид железа (II, III) |
| $H_2O$ | вода | окись водорода | оксид водорода |
КЛАССИФИКАЦИЯ ОКСИДОВ
Оксиды делятся на две большие группы: солеобразующие и несолеобразующие. Последние, как вытекает из названия, не образуют солей.
Несолеобразующими называют оксиды, которые не вступают во взаимодействие ни с щелочами, ни с кислотами и не образуют солей. Эти оксиды образованы неметаллами.
Несолеобразующих оксидов немного, их необходимо запомнить: $N_2O$, $NO$, $CO$, $SiO$.
Солеобразующими называют оксиды, способные взаимодействовать с кислотами или с основаниями с образованием солей.
Солеобразующие оксиды делятся на основные, кислотные и амфотерные оксиды.
Основные оксиды – оксиды, которым соответствуют основные гидроксиды (основания).
Основные оксиды образованы типичными металлами (щелочными, щелочноземельными, магнием), а также переходными металлами в низких степенях окисления (кроме $ZnO$).
Примеры основных оксидов: $Li_2O$, $Na_2O$, $K_2O$, $MgO$, $CaO$, $BaO$, $overset{+2}{Fe}O$, $overset{+2}{Cr}O$, $overset{+1}{Cu_2}O$, $overset{+2}{Cu}O$, $overset{+2}{Mn}O$ и др.
Кислотные оксиды – оксиды, которым соответствуют кислотные гидроксиды (кислоты).
Кислотные оксиды образованы неметаллами (за исключением несолеобразующих оксидов $CO$, $SiO$, $NO$, $N_2O$), а также переходными металлами в высоких степенях окисления.
Примеры кислотных оксидов: $Cl_2O_7$, $SO_3$, $SO_2$, $N_2O_5$, $NO_2$, $N_2O_3$, $P_2O_5$, $P_2O_3$, $CO_2$, $SiO_2$, $B_2O_3$, $overset{+6}{Cr}O_3$, $overset{+7}{Mn_2}O_7$ и др.
Амфотерными называются оксиды, которые в зависимости от условий проявляют основные или кислотные свойства. Им соответствуют амфотерные гидроксиды.
К амфотерным оксидам относятся оксид бериллия $BeO$, оксид алюминия $Al_2O_3$, оксид цинка $ZnO$, а также оксиды переходных металлов в промежуточных степенях окисления.
Примеры амфотерных оксидов: $Al_2O_3$, $overset{+3}{Fe_2}O_3$, $overset{+3}{Cr_2}O_3$, $overset{+4}{Mn}O_2$, $overset{+2}{Sn}O$, $overset{+4}{Sn}O_2$, $overset{+5}{V_2}O_5$, $ZnO$, $BeO$ и др.

Основные оксиды взаимодействуют с кислотами с образованием соли и воды. Это оксиды металлов (кроме некоторых переходных металлов в высших степенях окисления), твердые вещества.
Основным оксидам соответствуют основания, в которых металл имеет такую же степень окисления, как в оксиде, при этом степень окисления равна числу гидроксильных групп.
Например, оксиду натрия $overset{+1}{Na}_2O$ соответствует гидроксид натрия $overset{+1}{Na}OH$;
оксиду кальция $overset{+2}{Ca}O$ соответствует гидроксид кальция $overset{+2}{Ca}(OH)_2$;
оксиду железа (II) $overset{+2}{Fe}O$ соответствует гидроксид железа (II) $overset{+2}{Fe}(OH)_2$.
Кислотные оксиды взаимодействуют с щелочами с образованием соли и воды, им соответствуют кислоты. Это оксиды неметаллов ($mathrm{CO_2, SO_2, SO_3, N_2O_5}$) или переходных металлов в высших степенях окисления ($mathrm{CrO_3, Mn_2O_7}$).
Оксиду соответствует кислота в случае, если степень окисления элемента в обоих соединениях одинакова, при этом степень окисления кислотного остатка равна количеству атомов водорода.
Например, оксиду углерода (IV) $overset{+4}{C}O_2$ соответствует угольная кислота $H_2overset{+4}{C}O_3$;
оксиду серы (IV) $overset{+4}{S}O_2$ соответствует сернистая кислота $H_2overset{+4}{S}O_3$;
оксиду серы (VI) $overset{+6}{S}O_3$ соответствует серная кислота $H_2overset{+6}{S}O_4$;
оксиду азота (V) $overset{+3}{N}_2O_3$ соответствует азотистая кислота $Hoverset{+3}{N}O_2$;
оксиду азота (V) $overset{+5}{N}_2O_5$ соответствует азотная кислота $Hoverset{+5}{N}O_3$;
оксиду азота (IV) $overset{+4}{N}O_2$ соответствует сразу две кислоты: азотная — $Hoverset{+5}{N}O_3$ и азотистая — $Hoverset{+3}{N}O_2$;
оксиду хлора (IV) $Cloverset{+4}O_2$ соответствует хлорноватая $Hoverset{+3}{Cl}O_2$ и хлористая $Hoverset{+5}{Cl}O_3$ кислоты.
Обратите внимание: если элемент в оксиде проявляет степень окисления, отличную от той, которую он проявляет в кислоте, такой оксид является несолеобразующим!
Например: углерод в угарном газе $overset{+2}{C}O$ проявляет степень окисления +2, в то время как в единственной кислоте, содержащей углерод, $H_2overset{+4}{C}O_3$ его степень окисления равна +4. Поэтому оксид углерода (II) относится к несолеобразующим оксидам.
Амфотерные оксиды проявляют в зависимости от условий свойства основных или кислотных оксидов.
Им соответствуют амфотерные основания.
Например, оксиду железа (III) $overset{+3}{Fe}_2O_3$ соответствует гидроксид железа (III) $overset{+3}{Fe}(OH)_3$
оксиду алюминия $overset{+3}{Al}_2O_3$ соответствует гидроксид алюминия $overset{+3}{Al}(OH)_3$
оксиду хрома (III) $overset{+3}{Cr}_2O_3$ соответствует гидроксид хрома (III) $overset{+3}{Cr}(OH)_3$
В таблице представлены основные свойства кислотных, основных и амфотерных оксидов.
| основные | амфотерные | кислотные |
|---|---|---|
Взаимодействуют с кислотами с образованием соли и воды. Это оксиды металлов (кроме некоторых переходных металлов в высших степенях окисления), твердые вещества CaO, FeO, Cu$_2$O | оксиды, проявляющие в зависимости от условий свойства основных или кислотных оксидов. Им соответствуют амфотерные основания Это твердые вещества. Al$_2$O$_3$, ZnO, Fe$_2$O$_3$, $Cr_2O_3$, BeO | взаимодействуют с щелочами с образованием соли и воды, им соответствуют кислоты. Это оксиды неметаллов (CO$_2$, SO$_2$, SO$_3$, N$_2$O$_5$) или переходных металлов в высших степенях окисления (CrO$_3$, Mn$_2$O$_7$) Газы, жидкости, твердые тела Прим. Некоторые (NO$_2$, ClO$_2$) образуют сразу две кислоты |
ФИЗИЧЕСКИЕ СВОЙСТВА ОКСИДОВ
Основные и амфотерные оксиды при комнатной температуре – твердые вещества ($CaO$, $Fe_2O_3$ и др.); кислотные оксиды – твёрдые вещества ($P_2O_5$, $SiO_2$), жидкости ($SO_3$, $Сl_2О_7$ и др.) или газы ($NO_2$, $SO_2$ и др.). Все несолеообразующие оксиды являются газами, кроме $SiO$, который является твердым веществом. Однако, нужно помнить, что кремниевую кислоту $H_2SiO_3$ нельзя получить непосредственно из оксида кремния, добавляя воду! Эту кислоту можно получить косвенным путем из солей кремния – силикатов.
Оксиды металлов могут быть окрашены в разные цвета: оксиды щелочных и щелочно-земельных металлов обычно белого цвета, оксиды переходных металлов $Cr_2O_3$ – зеленый; $HgO$ – красно-оранжевый; $CuO$ – черный, а $Cu_2O$ – красный.
Оксид кремния $SiO_2$ – самое распространенное твердое вещество на Земле. Он входит в состав почвы (песок), горных пород и минералов. Драгоценные камни, такие как изумруд, сапфир, горный хрусталь имеют в своей структуре молекулы оксида кремния, при этом атомы кремния и кислорода образуют атомную кристаллическую решетку, и, поэтому представляют собой тугоплавкие, твердые, но хрупкие кристаллы правильной формы:



Бурый газ (оксид азота(IV)) Оксид железа (III) Оксид кремния
ХИМИЧЕСКИЕ СВОЙСТВА ОКСИДОВ
ХИМИЧЕСКИЕ СВОЙСТВА ОСНОВНЫХ ОКСИДОВ
| Исходное вещество | Реагент | Продукты реакции | Уравнение реакции |
|---|---|---|---|
| $K_2O$ | вода | растворимое основание (щелочь)* | $K_2O + H_2O = 2KOH$ |
| MgO | кислота | соль и вода | $MgO + 2HCl = MgCl_2 + H_2O$ |
| CaO | кислотный оксид | соль | $ CaO + CO_2 = CaCO_3$ |
| $Na_2O$ | амфотерный оксид | соль | $Na_2O + ZnO = Na_2ZnO_2$ |
* Взаимодействие основного оксида с водой протекает только в случае, если образуется растворимое основание, т.е. щелочь. В случае возможного образования нерастворимого основания реакция не идет, например:
$MgO + H_2O not = Mg(OH)_2 downarrow$
ХИМИЧЕСКИЕ СВОЙСТВА КИСЛОТНЫХ ОКСИДОВ
| Исходное вещество | Реагент | Продукты реакции | Уравнение реакции |
|---|---|---|---|
$SO_3$ $N_2O_5$ | вода | соответствующая растворимая* кислота | $SO_3 + H_2O = H_2SO_4$ $N_2O_5 + H_2O = 2HNO_3$ $SiO_2 + H_2O not = H_2SiO_3 downarrow$ |
| $SO_2$ | щелочь | соль и вода | $SO_2 + 2NaOH = Na_2SO_3 + H_2O$ |
| $P_2O_5$ | основный оксид | соль | $P_2O_5 + 3Na_2O = 2Na_3PO_4 $ |
| $SO_3$ | амфотерный оксид | соль | $ZnO + SO_3= ZnSO_4 $ |
*Реакция не протекает в случае,если образуется нерастворимая кислота, например: $SiO_2 + H_2O not = H_2SiO_3 downarrow$
Кислотные оксиды образуют соли, соответствующие определенной кислоте. Если у элемента может быть две или более кислот, то следует ориентироваться на степень окисления этого элемента в оксиде и кислоте: она должна быть одинаковой. Для лучшего понимания превращений кислотных оксидов в соли советуем воспользоваться следующим алгоритмом (на примере взаимодействия оксида азота(V) с гидроксидом кальция): $N_2O_5 + Ca(OH)_2 rightarrow$
1) Определим степень окисления азота в оксиде: $overset{X}{N}_2 overset{-2}{O_5} $ X=10/2=+5
2) Вспомним, какие кислоты образует азот и определим в каждой его степень окисления:
$hspace{2cm} overset{+1}{H}overset{x}{N}overset{-2}{O_2}hspace{3cm} overset{+1}{H}overset{x}{N}overset{-2}{O_3}hspace{2cm} $
$1cdot (+1) +1 cdot x + 2cdot(−2) = 0 hspace{0.5cm} 1cdot (+1) +1 cdot x + 3cdot(−2) = 0 $
$hspace{2cm} x = +3 hspace{3.2cm} x = +5$
Значит оксиду азота (V) соответствует азотная кислота, и $N_2O_5$ при взаимодействии с щелочами образует ее соли – нитраты ($NO_3^ – $):
$N_2O_5 + Ca(OH)_2 = Ca(NO_3)_2 + H_2O$
Воспользовавшись этим алгоритмом, можно составить следующие логические ряды:
$N_2O_5 rightarrow HNO_3$ ст.ок=+5 образует соли нитраты $NO_3^ – $
$ N_2O_3 rightarrow HNO_2$ ст.ок=+3 образует соли нитриты $NO_2^ –$
$P_2O_5 rightarrow H_3PO_4$ ст.ок=+5 образует соли нитраты $PO_4^{3 -}$
Для наглядного запоминания этого принципа можно воспользоваться таблицей, приведенной ниже.
Таблица. Формулы и названия кислот, кислотных остатков и соответствующих кислотных оксидов
| Формула кислоты | Название кислоты | Формула кислотного остатка | Название кислотного остатка | Соответствующий кислотный оксид |
|---|---|---|---|---|
| HF | Фтороводород, плавиковая | $ F^-$ | Фторид | |
| HCl | Хлороводород, соляная | $ Cl^-$ | Хлорид | |
| HBr | Бромоводород | $Br-$ | Бромид | |
| HI | Йодоводород | $I^-$ | Йодид | |
| $H_2S$ | Сероводород | $S^{2-}$ | Сульфид | |
| HCN | Циановодородная | $CN^-$ | Цианид | |
| $HNO_2$ | Азотистая | $NO^{2-}$ | Нитрит | $N_2O_3$ |
| $HNO_3$ | Азотная | $NO^{3-}$ | Нитрат | $N_2O_5$ |
| $H_3PO_4$ | Ортофосфорная | $mathrm{PO_4^{3-}}$ | Фосфат | $P_2O_5$ |
| $ H_3AsO_4$ | Мышьяковая | $mathrm{AsO_4^{3-}}$ | Арсенат | $As_2O_5$ |
| $ H_2SO_3$ | Сернистая | $mathrm{SO_3^{2-}}$ | Сульфит | $SO_2$ |
| $ H_2SO_4$ | Серная | $mathrm{SO_4^{2-}}$ | Сульфат | $SO_3$ |
| $H_2CO_3$ | Угольная | $mathrm{CO_3^{2-}}$ | Карбонат | $CO_2$ |
| $ H_2SiO_3$ | Кремниевая | $mathrm{SiO_3^{2-}}$ | Силикат | $SiO_2$ |
| $ H_2CrO_4$ | Хромовая | $mathrm{CrO_4^{2-}}$ | Хромат | $CrO_3$ |
| $ H_2Cr_2O_7$ | Дихромовая | $mathrm{Cr_2O_7^{2-}}$ | Дихромат | $CrO_3$ |
| $HMnO_4$ | Марганцовая | $mathrm{MnO_4^{-}}$ | Перманганат | $Mn_2O_7$ |
| $HClO$ | Хлорноватистая | $mathrm{ClO^-}$ | Гипохлорит | $Cl_2O$ |
| $ HClO_2$ | Хлористая | $mathrm{ClO_2^{-}}$ | Хлорит | $Cl_2O_3$ |
| $ HClO_3$ | Хлорноватая | $mathrm{ClO_3^{-}}$ | Хлорат | $Cl_2O_5$ |
| $ HClO_4$ | Хлорная | $mathrm{ClO_4^{-}}$ | Перхлорат | $Cl_2O_7$ |
| $HCOOH$ | Метановая, муравьиная | $mathrm{HCOO^-}$ | Формиат | |
| $CH_3COOH$ | Этановая, уксусная | $mathrm{CH_3COO^-}$ | Ацетат | |
| $ H_2C_2O_4$ | Этандиовая, щавелевая | $mathrm{C_2O_4^-}$ | Оксалат |
ХИМИЧЕСКИЕ СВОЙСТВА АМФОТЕРНЫХ ОКСИДОВ
| Исходное вещество | Реагент | Продукты реакции | Уравнение реакции | |
|---|---|---|---|---|
| $ZnO, Al_2O_3$ | вода | $not = $ | не взаимодействуют | |
| $ZnO$ | кислотный оксид | соль | $ ZnO + SO_3= ZnSO_4 $ | |
| основный оксид | соль | $ZnO + Na_2O = Na_2ZnO_2$ | ||
| $Al_2O_3$ | кислота | соль | $ Al_2O_3 + 6HNO_3 = 2Al(NO_3)_3 + 3H_2O $ | |
| $Al_2O_3$ | щелочь | щелочь в расплаве — соль+вода | $Al_2O_3 + 2NaOH (т)xrightarrow[t, ^circ C]{}$ $ 2NaAlO_2 + H_2O $ | |
| $Al_2O_3$ | щелочь в растворе — комплексная соль | $Al_2O_3 + 6NaOH (p-p) + 3H_2O = $ $=2Na_3[Al(OH)_6]$ |
СПОСОБЫ ПОЛУЧЕНИЯ ОКСИДОВ
1) взаимодействие простых веществ с кислородом
$mathrm{2Ca + O_2 = 2CaO}$
$mathrm{S + O_2 = SO_2}$
2) взаимодействие сложных веществ с кислородом
$mathrm{2ZnS + 3O_2 = 2ZnO + SO_2}$
3) разложение некоторых солей при нагревании
$mathrm{CaCO_3 = CaO + CO_2}$
$mathrm{2CuSO_4 = 2CuO + 2SO_2 + O_2}$
Примечание: соли натрия и калия обычно не разлагаются с образованием оксидов. Подробнее смотрите тему “Разложение солей”
4) дегидратация кислот и нерастворимых оснований
$mathrm{ H_2SO_4 = SO_3 + H_2O}$
(точнее: $mathrm{3H_2SO_4 + P_2O_5 = 3SO_3uparrow + 2H_3PO_4}$)
$mathrm{H_2SiO_3 = SiO_2 + H_2O}$
$mathrm{Cu(OH)_2 = CuO + H_2O}$
5) окисление одних оксидов и восстановление других
$mathrm{MnO_2 + 2H_2 = MnO + 2H_2O}$
$mathrm{2NO + O_2 = 2NO_2}$
$mathrm{Cr_2O_3 + 2Al = Al_2O_3 + 2Cr}$ (алюмотермия)
$mathrm{CuO + C = Cu + CO}$
При этом более активный металл вытесняет менее активный из его оксида. Для сравнения активности металлов следует использовать электрохимический ряд напряжения металлов.
6) вытеснение летучих оксидов из солей менее летучими
$mathrm{Na_2CO_3 + SiO_2 = Na_2SiO_3 + CO_2uparrow}$
Источник
