Какие общие свойства имеют газы

Физические законы и параметры газов являются основополагающими для создания вакуумных систем. Даже при крайне низких значениях давлений, используемых в вакуумной технике, физические процессы, протекающие в газах, подчиняются общим газовым законам. Необходимость создания вакуума обычно связана с потребностью уменьшения концентрации молекул газа или частоты их столкновений с поверхностью сосуда. Газовые процессы в вакуумных системах можно, как правило, рассматривать с точки зрения законов идеального газа, а некоторые общие физические процессы вакуумных систем могут быть описаны с помощью статических и динамических свойств газов. Физические процессы, протекающие в газах при низком давлении, а также различные параметры и свойства газового потока рассмотрены ниже.
Параметры состояния газа
Если взять образец газа, то для описания его состояния достаточно знать три из четырех параметров. Этими параметрами являются давление, объем, температура и количество газа.
Давление – это сила, с которой газ воздействует на единицу площади поверхности сосуда. В СИ единицей измерения давления является паскаль, или ньютон на квадратный метр (Н/м2). В вакуумной технике также используется единица измерения миллиметр ртутного столба, или Торр: 1 мм рт. ст. = 133 Па (1 Па = 7,5 мм рт. ст.).
Объем – мера пространства, которое занимает газ; обычно он задается размерами сосуда. Единицей объема в СИ является кубический метр (м3), однако для обозначения быстроты откачки и потока газа, а также других величин широко используются литры.
Температура газа при давлении ниже 1 Торр главным образом определяется температурой поверхностей, с которыми он соприкасается. Как правило, газ находится при комнатной температуре. При выводе уравнений, описывающих состояние газов, для измерения температуры используют Кельвины (К).
Количество газа в данном объеме измеряется в молях.
Моль – число граммов газа (или любого вещества), равное его молекулярной массе. Моль содержит 6,02 х 1023 молекул. Один моль любого газа при 0 °С и давлении 760 Торр занимает объем, равный 22,4 л. Масса 1 моля газа равна его молекулярной массе в граммах.
Молярный объем является универсальной постоянной. Экспериментально установлено, что он составляет 22,414 л при 760 Торр и 0 °С. Поскольку 1 моль любого газа при температуре 0 °С и давлении 760 Торр занимает объем 22,4 л, из этого соотношения можно рассчитать молекулярную концентрацию любого объема газа, если известны его температура и давление. Например, 1 см3 воздуха при 760 Торр и 0 °С содержит 2,7 x 1019 молекул; в то время как при давлении 1 Торр и температуре 0 °С 1 см3 воздуха содержит 3,54 x 1016 молекул.
Газовые законы
Газовые законы устанавливают соотношения между физическими параметрами состояния газа (давление, объем, температура и количество газа) при постоянном значении одного из параметров. Эти законы справедливы для идеального газа в котором объем всех молекул является незначительным по сравнению с объемом газа, и энергия притяжения между молекулами является незначительной по сравнению с их средней тепловой энергией. Это означает, что данное вещество (в данном случае газ) находится в газообразном состоянии при температуре, которая достаточно высока для его конденсации. К газам, по своим свойствам близким к идеальным при комнатной температуре, относятся 02, Ne, Аг, СО, Н2 и NO.
Ниже приведены общие формулировки газовых законов.
Закон Бойля – произведение давления на объем рУ, где р – давление газа, V – его объем, является постоянной величиной для данной массы газа при постоянной температуре.
Закон Гей-Люссака – величина V/T, где Т- абсолютная температура газа, является постоянной для данной массы газа при постоянном давлении.
Закон Авогадро – равные объемы различных газов при одинаковых температуре и давлении содержат одно и то же количество молекул. Из этого закона можно получить важное соотношение между числом молей газа и давлением, которое создает газ.
Основное уравнение состояния идеального газа (уравнение Клапейрона) устанавливает зависимость между давлением, объемом и температурой для данной массы газа, т. е. теми параметрами, которые необходимы для описания состояния газа:
$$pV=MRT, (1.1)$$
где R – универсальная газовая постоянная данного газа, R = 8,31 ДжДмоль К) (62,4 Торр-л/(моль x К)); М – это число молей в объеме V
Данный закон будет справедлив и для большинства газов, которые при низких давлениях ведут себя как идеальные газы.
Закон парциальных давлений Дальтона – общее давление, создаваемое смесью газов, равняется сумме парциальных давлений, создаваемых отдельными компонентами смеси.
Парциальное давление, создаваемое одним компонентом смеси газов, – это давление, создаваемое этим компонентом, если бы он занимал весь объем.
Закон Авогадро – равные объемы идеального газа при постоянных температуре и давлении содержат одно и то же количество молекул.
Число Авогадро – число молекул в 1 моле газа или любого вещества, является универсальной постоянной и составляет 6,023 • 1023.
Число Лошмидта – число молекул в кубическом сантиметре газа при атмосферном давлении и температуре 0 °С. Это универсальная постоянная, равная 2,637 x 1019.
Для 1 моля газа при атмосферном давлении и температуре 0 °С (273,2 К), занимающего объем V = 22,414 л, R= 8.31 Дж/(моль x К) или в тепловых единицах R/J= 1,99 кал/К (У – механический эквивалент теплоты, J = 4,182 Дж кал). Следовательно, количество теплоты 1,99 кал будет повышать температуру 1 моля любого идеального газа на 1 К, или после повышения температуры 1 моля любого идеального газа на 1 К увеличение энергии газа составит 8,31 Дж.
Неидеальные газы
Примерами некоторых распространенных неидеальных газов являются аммиак, этан, бензол, диоксид углерода (углекислый газ), пары ртути, SO и S02. Газовые законы должны описывать физические процессы, протекающие в любом газе при температуре выше критической. При критической температуре, Тс, газ начинает конденсироваться. Ниже этой критической температуры имеет место давление паров над жидким конденсатом, которое называется давлением пара. Если газ конденсируется (его объем уменьшается), давление изменяться не будет, но большее количество газа будет переходить в жидкую фазу. По мере снижения температуры над жидкостью будет присутствовать меньшее количество молекул, при этом давление паров также будет снижаться.
Источник
На сегодняшний день известно о существовании более чем 3 миллионов различных веществ. И цифра эта с каждым годом растет, так как химиками-синтетиками и другими учеными постоянно производятся опыты по получению новых соединений, обладающих какими-либо полезными свойствами.
Часть веществ – это природные обитатели, формирующиеся естественным путем. Другая половина – искусственные и синтетические. Однако и в первом и во втором случае значительную часть составляют газообразные вещества, примеры и характеристики которых мы и рассмотрим в данной статье.

Агрегатные состояния веществ
С XVII века принято было считать, что все известные соединения способны существовать в трех агрегатных состояниях: твердые, жидкие, газообразные вещества. Однако тщательные исследования последних десятилетий в области астрономии, физики, химии, космической биологии и прочих наук доказали, что есть еще одна форма. Это плазма.
Что она собой представляет? Это частично или полностью ионизированные газы. И оказывается, таких веществ во Вселенной подавляющее большинство. Так, именно в состоянии плазмы находятся:
- межзвездное вещество;
- космическая материя;
- высшие слои атмосферы;
- туманности;
- состав многих планет;
- звезды.
Поэтому сегодня говорят, что существуют твердые, жидкие, газообразные вещества и плазма. Кстати, каждый газ можно искусственно перевести в такое состояние, если подвергнуть его ионизации, то есть заставить превратиться в ионы.
Газообразные вещества: примеры
Примеров рассматриваемых веществ можно привести массу. Ведь газы известны еще с XVII века, когда ван Гельмонт, естествоиспытатель, впервые получил углекислый газ и стал исследовать его свойства. Кстати, название этой группе соединений также дал он, так как, по его мнению, газы – это нечто неупорядоченное, хаотичное, связанное с духами и чем-то невидимым, но ощутимым. Такое имя прижилось и в России.
Можно классифицировать все газообразные вещества, примеры тогда привести будет легче. Ведь охватить все многообразие сложно.
По составу различают:
- простые,
- сложные молекулы.
К первой группе относятся те, что состоят из одинаковых атомов в любом их количестве. Пример: кислород – О2, озон – О3, водород – Н2, хлор – CL2, фтор – F2, азот – N2 и прочие.
Ко второй категории следует относить такие соединения, в состав которых входит несколько атомов. Это и будут газообразные сложные вещества. Примерами служат:
- сероводород – H2S;
- хлороводород – HCL;
- метан – CH4;
- сернистый газ – SO2;
- бурый газ – NO2;
- фреон – CF2CL2;
- аммиак – NH3 и прочие.
Классификация по природе веществ
Также можно классифицировать виды газообразных веществ по принадлежности к органическому и неорганическому миру. То есть по природе входящих в состав атомов. Органическими газами являются:
- первые пять представителей предельных углеводородов (метан, этан, пропан, бутан, пентан). Общая формула CnH2n+2;
- этилен – С2Н4;
- ацетилен или этин – С2Н2;
- метиламин – CH3NH2 и другие.
К категории газов неорганической природы относятся хлор, фтор, аммиак, угарный газ, силан, веселящий газ, инертные или благородные газы и прочие.
Еще одной классификацией, которой можно подвергнуть рассматриваемые соединения, является деление на основе входящих в состав частиц. Именно из атомов состоят не все газообразные вещества. Примеры структур, в которых присутствуют ионы, молекулы, фотоны, электроны, броуновские частицы, плазма, также относятся к соединениям в таком агрегатном состоянии.
Свойства газов
Характеристики веществ в рассматриваемом состоянии отличаются от таковых для твердых или жидких соединений. Все дело в том, что свойства газообразных веществ особенные. Частицы их легко и быстро подвижны, вещество в целом изотропное, то есть свойства не определяются направлением движения входящих в состав структур.
Можно обозначить самые главные физические свойства газообразных веществ, которые и будут отличать их от всех остальных форм существования материи.
- Это такие соединения, которые нельзя увидеть и проконтролировать, ощутить обычными человеческими способами. Чтобы понять свойства и идентифицировать тот или иной газ, опираются на четыре описывающих их все параметра: давление, температура, количество вещества (моль), объем.
- В отличие от жидкостей газы способны занимать все пространство без остатка, ограничиваясь лишь величиной сосуда или помещения.
- Все газы между собой легко смешиваются, при этом у этих соединений нет поверхности раздела.
- Существуют более легкие и тяжелые представители, поэтому под действием силы тяжести и времени, возможно увидеть их разделение.
- Диффузия – одно из важнейших свойств этих соединений. Способность проникать в другие вещества и насыщать их изнутри, совершая при этом совершенно неупорядоченные движения внутри своей структуры.
- Реальные газы электрический ток проводить не могут, однако если говорить о разреженных и ионизированный субстанциях, то проводимость резко возрастает.
- Теплоемкость и теплопроводность газов невысока и колеблется у разных видов.
- Вязкость возрастает с увеличением давления и температуры.
- Существует два варианта межфазового перехода: испарение – жидкость превращается в пар, сублимация – твердое вещество, минуя жидкое, становится газообразным.
Отличительная особенность паров от истинных газов в том, что первые при определенных условиях способны перейти в жидкость или твердую фазу, а вторые нет. Также следует заметить способность рассматриваемых соединений сопротивляться деформациям и быть текучими.

Подобные свойства газообразных веществ позволяют широко применять их в самых различных областях науки и техники, промышленности и народном хозяйстве. К тому же конкретные характеристики являются для каждого представителя строго индивидуальными. Мы же рассмотрели лишь общие для всех реальных структур особенности.
Сжимаемость
При разных температурах, а также под влиянием давления газы способны сжиматься, увеличивая свою концентрацию и снижая занимаемый объем. При повышенных температурах они расширяются, при низких – сжимаются.
Под действием давления также происходят изменения. Плотность газообразных веществ увеличивается и, при достижении критической точки, которая для каждого представителя своя, может наступить переход в другое агрегатное состояние.
Основные ученые, внесшие вклад в развитие учения о газах
Таких людей можно назвать множество, ведь изучение газов – процесс трудоемкий и исторически долгий. Остановимся на самых известных личностях, сумевших сделать наиболее значимые открытия.
- Амедео Авогадро в 1811 году сделал открытие. Неважно, какие газы, главное, что при одинаковых условиях их в одном объеме их содержится равное количество по числу молекул. Существует рассчитанная величина, имеющая название по фамилии ученого. Она равна 6,03*1023 молекул для 1 моль любого газа.
- Ферми – создал учение об идеальном квантовом газе.
- Гей-Люссак, Бойль-Мариотт – фамилии ученых, создавших основные кинетические уравнения для расчетов.
- Роберт Бойль.
- Джон Дальтон.
- Жак Шарль и многие другие ученые.
Строение газообразных веществ
Самая главная особенность в построении кристаллической решетки рассматриваемых веществ, это то, что в узлах ее либо атомы, либо молекулы, которые соединяются друг с другом слабыми ковалентными связями. Также присутствуют силы ван-дер-ваальсового взаимодействия, когда речь идет о ионах, электронах и других квантовых системах.
Поэтому основные типы строения решеток для газов, это:
- атомная;
- молекулярная.
Связи внутри легко рвутся, поэтому эти соединения не имеют постоянной формы, а заполняют весь пространственный объем. Это же объясняет отсутствие электропроводности и плохую теплопроводность. А вот теплоизоляция у газов хорошая, ведь, благодаря диффузии, они способны проникать в твердые тела и занимать свободные кластерные пространства внутри них. Воздух при этом не пропускается, тепло удерживается. На этом основано применение газов и твердых тел в совокупности в строительных целях.

Простые вещества среди газов
Какие по строению и структуре газы относятся к данной категории, мы уже оговаривали выше. Это те, что состоят из одинаковых атомов. Примеров можно привести много, ведь значительная часть неметаллов из всей периодической системы при обычных условиях существует именно в таком агрегатном состоянии. Например:
- фосфор белый – одна из аллотропных модификаций данного элемента;
- азот;
- кислород;
- фтор;
- хлор;
- гелий;
- неон;
- аргон;
- криптон;
- ксенон.
Молекулы этих газов могут быть как одноатомными (благородные газы), так и многоатомными (озон – О3). Тип связи – ковалентная неполярная, в большинстве случаев достаточно слабая, но не у всех. Кристаллическая решетка молекулярного типа, что позволяет этим веществам легко переходить из одного агрегатного состояния в другое. Так, например, йод при обычных условиях – темно-фиолетовые кристаллы с металлическим блеском. Однако при нагревании сублимируются в клубы ярко-фиолетового газа – I2.

К слову сказать, любое вещество, в том числе металлы, при определенных условиях могут существовать в газообразном состоянии.
Сложные соединения газообразной природы
Таких газов, конечно, большинство. Различные сочетания атомов в молекулах, объединенные ковалентными связями и ван-дер-ваальсовыми взаимодействиями, позволяют сформироваться сотням различных представителей рассматриваемого агрегатного состояния.
Примерами именно сложных веществ среди газов могут быть все соединения, состоящие из двух и более разных элементов. Сюда можно отнести:
- пропан;
- бутан;
- ацетилен;
- аммиак;
- силан;
- фосфин;
- метан;
- сероуглерод;
- сернистый газ;
- бурый газ;
- фреон;
- этилен и прочие.
Кристаллическая решетка молекулярного типа. Многие из представителей легко растворяются в воде, образуя соответствующие кислоты. Большая часть подобных соединений – важная часть химических синтезов, осуществляемых в промышленности.
Метан и его гомологи
Иногда общим понятием “газ” обозначают природное полезное ископаемое, которое представляет собой целую смесь газообразных продуктов преимущественно органической природы. Именно он содержит такие вещества, как:
- метан;
- этан;
- пропан;
- бутан;
- этилен;
- ацетилен;
- пентан и некоторые другие.
В промышленности они являются очень важными, ведь именно пропан-бутановая смесь – это бытовой газ, на котором люди готовят пищу, который используется в качестве источника энергии и тепла.

Многие из них используются для синтеза спиртов, альдегидов, кислот и прочих органических веществ. Ежегодное потребление природного газа исчисляется триллионами кубометров, и это вполне оправданно.
Кислород и углекислый газ
Какие вещества газообразные можно назвать самыми широко распространенными и известными даже первоклассникам? Ответ очевиден – кислород и углекислый газ. Ведь это они являются непосредственными участниками газообмена, происходящего у всех живых существ на планете.
Известно, что именно благодаря кислороду возможна жизнь, так как без него способны существовать только некоторые виды анаэробных бактерий. А углекислый газ – необходимый продукт “питания” для всех растений, которые поглощают его с целью осуществления процесса фотосинтеза.
С химической точки зрения и кислород, и углекислый газ – важные вещества для проведения синтезов соединений. Первый является сильным окислителем, второй чаще восстановитель.
Галогены
Это такая группа соединений, в которых атомы – это частицы газообразного вещества, соединенные попарно между собой за счет ковалентной неполярной связи. Однако не все галогены – газы. Бром – это жидкость при обычных условиях, а йод – легко возгоняющееся твердое вещество. Фтор и хлор – ядовитые опасные для здоровья живых существ вещества, которые являются сильнейшими окислителями и используются в синтезах очень широко.
Источник
- Химическая энциклопедия
ГАЗЫ
вещества в агрегатном состоянии, характеризующемся слабым взаимод. составляющих вещество частиц (по сравнению с их средней кинетич. энергией), в результате чего Г. заполняют весь предоставленный им объем. Г., как и нормальные (обычные) жидкости, макроскопически однородны и изотропны при отсутствии внеш. воздействий, в отличие от анизотропных состояний вещества — твердого кристаллического и жидких кристаллов. Строго различать жидкое и газообразное состояния вещества на фазовой диаграмме можно лишь при температуре ниже критической Гкр (см. рис.), т. к. выше Ткр газ нельзя превратить в жидкость повышением давления. Ниже Ткр возможно фазовое равновесие жидкость — пар, причем газообразному состоянию отвечает фаза с меньшей плотностью (Г., находящийся в термодинамич. равновесии с жидкой или твердой фазой того же вещества, обычно наз. паром). В критич. точке различие между жидкостью и паром исчезает, поэтому возможен непрерывный (без фазового превращения) переход из газообразного состояния в жидкое. При этом все свойства вещества меняются постепенно (наиб. быстро вблизи критич. точки). В тройной точке Т^ сосуществуют газ, жидкость и твердое тело (кристалл), причем плотность Г. вблизи тройной точки обычно на три порядка меньше плотности жидкости или кристалла. Кривую сосуществования жидкости и Г. наз. кривой парообразования, твердого тела и Г. — кривой сублимации (возгонки).
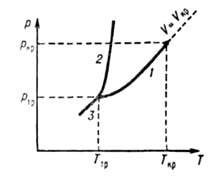
Диаграмма состояния однокомпонентной системы в координатах давление р-температура Т! Линии /, 2 и 3 — кривые парообразования, плавления и возгонки соотв.; 7″кр и ркр-координаты критич. точки; Ттр и ртр-координаты тройной точки; И,—-Критич. объем.
В нормальных условиях (при 0 °C и атм. давлении) в газообразном состоянии находятся элементы гелиевой группы (Не, Ne и т. д.), а также ряд элементов, образующих молекулярные газы: O2, N2, H2, Г2 и Cl2. Атм. воздух состоит из N2 и O2 (соотв. 75,5 и 23,1% по массе), благородных газов, N2O, CO2 и паров H2O (остальные 1,4%). В природе Г. образуются как продукты жизнедеятельности бактерий, при превращениях орг. веществ, восстановлении минер. солей и др. В недрах Земли Г., в основном CH4и др. легкие углеводороды, как правило, сопутствуют нефтям; встречаются газовые месторождения, содержащие до 70% неуглеводородных компонентов (H2S, CO2 и” др.).
При низких давлениях Г. смешиваются друг с другом в любых соотношениях. При высоких давлениях и температурах выше Ткр взаимная растворимость Г. может быть ограниченной и возможно равновесное сосуществование двух газовых фаз; такие системы рассматривают как расслаивающиеся газовые растворы (см. критическое состояние). Растворимость Г. в жидкостях и твердых телах может достигать больших значений (см. табл. 1).
Табл. 1 — РАСТВОРИМОСТЬ ГАЗОВ В ЖИДКОСТЯХ ПРИ 298 К И 10s Па (в мольных долях)

Теория газообразного состояния. Важнейшая теоретич. модель газообразного состояния-ид сальный газ, для которого энергия взаимод. между молекулами пренебрежимо мала по сравнению с кинетической энергией их хаотич. (теплового) движения. Уравнение состояния для n молей идеального Г., занимающего объем V при температуре Т и давлении р, имеет вид: pV = nRT, где R = 8,31 Дж/(моль∙К)-газовая постоянная (см. Клапейрона — Менделеева уравнение). Внутр. энергия 1 моля одноатомного идеального газа ? = 3/2/?Т ДлЯ идеального Г. строго выполняются Бойля-Мариотта закон и Гей-Люссака законы, для реальных Г. эти законы выполняются приближенно-тем лучше, чем дальше р и Т от критич. значений.
Статистич. физика позволяет вычислить макроскопич. свойства идеального Г., рассматривая его как систему из N квазинезависимых молекул и определяя вероятность раз л. состояний отдельной молекулы. В идеальном Г. для каждой из молекул все окружающие частицы представляют термостат, с которым она обменивается энергией. В соответствии с канонич. распределением Гиббса среднее число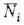 молекул в 1-том состоянии с энергией Е, равно:
молекул в 1-том состоянии с энергией Е, равно:
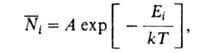
где k — постоянная Больцмана; Л-коэф., зависящий от Т. Применение данной формулы в случае, когда движение молекул идеального Г. подчиняется законам классич. механики, позволяет установить распределение молекул по скоростям, а также их пространств. распределение в поле внеш. сил. В соответствии с распределением Максвелла среднее число dN молекул с массой ш, компоненты скоростей которых лежат в интервалах от vx до vx + dvx, от vy до vy + dvy и от v. до vz + dvz, равно:
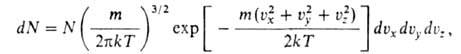
где N — общее число молекул. В любом реальном Г. распределение по скоростям центров инерции молекул представляет собой распределение Максвелла. При наличии внеш. силового поля, в котором потенциальная энергия молекулы идеального Г. зависит от координат ее центра инерции, концентрация молекул устанавливается распределением Больцмана:
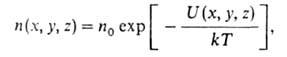
где п0- концентрация молекул в отсутствие поля; U(x, у, z)- потенциальная энергия молекулы во внеш. поле. В частности, в однородном поле тяжести, направленном вдоль оси z, U = mgz, где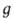 -ускорение своб. падения, и распределение плотности газа определяется т. наз. барометрической формулой:
-ускорение своб. падения, и распределение плотности газа определяется т. наз. барометрической формулой:
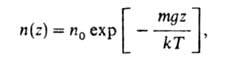
где и0 — плотность газа в точке z = 0.
При низких температурах классич. статистика неприменима к идеальному Г. и заменяется квантовой статистикой Бозе-Эйнштейна или Ферми-Дирака для частиц с целым или полуцелым спином соответственно. Температура, ниже которой отчетливо проявляются квантовые свойства идеального Г., тем выше, чем меньше масса частиц и чем больше плотность числа частиц. Для обычных Г. соответствующая температура очень низка; квантовые эффекты практически существенны лишь для Не, H2 и в некоторой степени для Ne. Квантовую природу системы, проявляющуюся в дискретности энергетич. спектра, необходимо учитывать при описании внутр. состояний молекул (электронных, колебательных, а при низких температурах- и вращательных). Энергетич. спектр молекул Г., соответствующий их постулат, движению, можно считать квазинепрерывным, т. к. расстояния между соседними уровнями энергии малы.
Применение законов классич. статистики с учетом квантовых закономерностей позволяет рассчитать по молекулярным данным термодинамич. функции Г. (энтропию, внутр. энергию, энергии Гельмгольца и Гиббса), константы хим. равновесия газофазных реакций, теплоемкость и кинетич. характеристики, знание которых требуется при проектировании мн. технол. процессов. Так, теплоемкость идеального Г. может быть рассчитана в классич. теории, если известно число i степеней свободы молекулы. Вклад каждой из вра-щат. и постулат, степеней свободы молекулы в молярную теплоемкость Су равен R/2, а каждой из колебат. степеней свободы-JR (т. наз. закон равнораспределения). Частица одноатомного Г. обладает тремя постулат, степенями свободы, соотв. его теплоемкость составляет ЗЯ/2, что хорошо совпадает с эксперим. данными. Молекула двухатомного Г. обладает тремя поступательными, двумя вращательными и одной колебат. степенями свободы, и, согласно закону равнораспределения, Су = 1R/2, однако это значение не совпадает с опытными данными даже при обычных температурах. Наблюдаемое расхождение, а также температурная зависимость теплоемкости Г. объясняются квантовой теорией (подробнее см. в ст. теплоемкость).
Кинетич. свойства Г. — теплопроводность, взаимная диффузия (для газовых смесей), вязкость-определяются столкновениями молекул. В простейшем случае явления переноса рассматриваются для разреженного Г., молекулы которого считаются упругими шарами, взаимодействующими лишь в момент соударения. В первом приближении все коэф. переноса выражаются через среднюю длину своб. пробега молекулы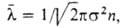 где
где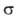 -диаметр молекулы. Так,
-диаметр молекулы. Так, 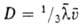 , где
, где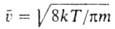 -средняя скорость теплового движения молекул. Более строгая теория учитывает взаимод. молекул на расстоянии, что приводит к появлению в выражениях для коэф. переноса т. наз. интегралов столкновений, которые м. б. рассчитаны, если известен вид потенциала межмолекулярных взаимодействий.
-средняя скорость теплового движения молекул. Более строгая теория учитывает взаимод. молекул на расстоянии, что приводит к появлению в выражениях для коэф. переноса т. наз. интегралов столкновений, которые м. б. рассчитаны, если известен вид потенциала межмолекулярных взаимодействий.
Свойства реальных газов. Неидеальность Г. в молекулярно-кинетич. теории рассматривается как результат взаимод. молекул. В первом приближении ограничиваются рассмотрением парных взаимодействий, во втором-тройных и т. д. Такой подход приводит к вириальному уравнению состояния, коэф. которого м. б. теоретически рассчитаны, если известен потенциал межмол. взаимодействий. Наиб. полезно вириальное уравнение при рассмотрении свойств Г. малой и умеренной плотности. Предложено много эмпирич. и полуэмпирич. уравнений, связывающих р, V и Т, которые либо исходят из некоторой простой модели взаимодействий (напр., Ван-дер-Ваальса уравнение), либо выражают чисто эмпирич. зависимость, справедливую для определенного класса веществ (см. уравнения состояния).
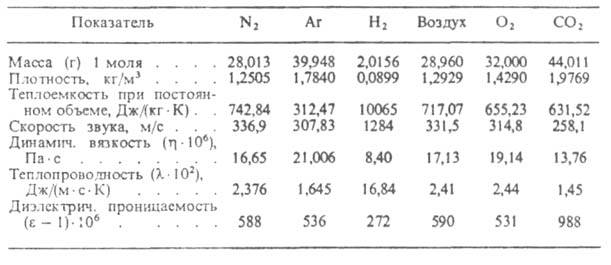
Наличие межмол. взаимодействий оказывает влияние на все свойства реальных Г., в т. ч. приводит и к тому, что их внутр. энергия зависит от плотности. С этим свойством связан эффект Джоуля-Томпсона: изменение температуры газа при его адиабатич. расширении, напр. при протекании с малой постоянной скоростью через пористую перегородку (этот процесс наз. дросселированием). Учет межмол. взаимодействий и внутр. строения молекул необходим при решении мн. теоретич. задач физ.химии. Молекул, которые можно было бы принимать как упругие шары, практически не бывает, и при расчете свойств реальных Г. применяют др. молекулярные модели. Из них наиб. употребительны простые модели гармонич. осциллятора и жесткого ротатора. Физ. свойства некоторых газов приведены в табл. 2 [по данным Автоматизированной информац. системы достоверных данных о теплофиз. свойствах газов и жидкостей (АИСТ)].
Табл. 2 — ФИЗИЧЕСКИЕ СВОЙСТВА НЕКОТОРЫХ ГАЗОВ ПРИ НОРМАЛЬНЫХ УСЛОВИЯХ (Г= 273,15 К, р = 1,01∙105 Па)
Лит.: Гиршфельдер Дж., КертиссЧ., Берд Р., Молекулярная теория газов и жидкостей, пер. с англ., М., 1961; Рид Р., ПраусницДж., Шервуд Т., Свойства газов и жидкостей, пер. с англ., Л., 1982; Смирнова Н. А., Методы статистической термодинамики в физической химии, 2 изд., М, 1982.
М. А. Анисимов
Источник:
Химическая энциклопедия
на Gufo.me
Значения в других словарях
- газы —
см.: Дать по газам; Нажать на газ
Толковый словарь русского арго - газы —
газы мн. Газообразные выделения, образующиеся в кишечнике.
Толковый словарь Ефремовой - Газы —
I Га́зы (французское gaz; название предложено голланским учёным Я. Б. Гельмонтом агрегатное состояние вещества, в котором его частицы не связаны или весьма слабо связаны силами взаимодействия и движутся свободно, заполняя весь предоставленный им объём.
Большая советская энциклопедия - газы —
см. испытательные газы
Строительная терминология - газы —
(иноск.) — скопление ветров в желудке, вызывающее угрюмое настроение (дамы особенно приписывают ипохондрию “вапёрам”) Ср. Gas (нем.). Ср. Geist, geest (нидерл.) — дух (изобрел van Helmont). Ср.
Фразеологический словарь Михельсона - газы —
сущ., кол-во синонимов: 1 ветры 1
Словарь синонимов русского языка

Источник
