Какие из приведенных утверждений о металлах и их свойствах верны
НЕОРГАНИЧЕСКАЯ ХИМИЯ
1. Выбрать правильный ответ
К образованию только кислотных оксидов способен химический
элемент
1) хлор 2) фтор 3) марганец 4) алюминий
2. Выбрать правильный ответ
К образованию амфотерного оксида способен химический элемент
1) фосфор 2) натрий 3) сера 4) хром
3. Выбрать правильный ответ
К образованию оксидов трех видов: основного, амфотерного и
кислотного
способен химический элемент
1) фосфор 2) йод 3) марганец 4) цинк
4. Какие из приведенных утверждений верны?
А. К образованию кислотных оксидов способны только
неметаллы.
Б. Все металлы IIА группы образуют щелочи .
1) верно только А
2) верно только Б
3) верны оба утверждения
4) оба утверждения неверны
5. Установить соответствие между названием вещества и его
принадлежностью к соответствующему классу неорганических
соединений.
НАЗВАНИЕ ВЕЩЕСТВА КЛАСС (ГРУППА)
НЕОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
А) oксид бериллия 1) амфотерный оксид
Б) хлорид железа (III) 2) средняя соль
В) гидросульфит натрия 3) кислая соль
Г) гидроксид хрома (II) 4) основание
6. Расположить оксиды в последовательности кислотный –
основный –
амфотерный – несолеобразующий
1) Cl2O7 оксид хлора(VII) 2) BaО оксид бария 3) MnO2 оксид
марганца(IV)
4) N2O оксид азота(I)
7. Выбрать правильный ответ
Установить последовательность увеличения восстановительных
свойств
металлов
1) Мg 2) Ca 3) K 4)
Rb
8. Выбрать правильный ответ
Наиболее электропроводным металлом из перечисленных является
1) медь 2) ртуть 3) свинец 4) хром
9. Выбрать правильный ответ
С разбавленной серной кислотой взаимодействует
1) медь 2) ртуть 3) цинк 4) кремний
10. Выбрать правильный ответ
Наиболее выраженные основные свойства проявляет оксид
1) бериллия 2) магния 3) калия 4) алюминия
11. Выбрать правильный ответ
Пероксид металла образуется при взаимодействии кислорода с
1) магнием 2) литием 3) натрием 4) алюминием
12. Выбрать правильный ответ
Цинк вытесняет металл из растворов обеих солей, содержащихся
в группе
1) хлорид кальция и сульфат марганца (II)
2) сульфат меди(II) и сульфат алюминия
3) нитрат кобальта(II) и сульфат магния
4) нитрат меди (II) и хлорид никеля(II)
13. Выбрать правильный ответ
С концентрированной азотной кислотой при комнатной
температуре
взаимодействует
1) Аl 2) Cr 3) Au 4) Hg
14. Выбрать правильный ответ
Водород выделяется в результате взаимодействия между
1) концентрированной азотной кислотой и хромом
2) раствором гидроксида натрия и алюминием
3) золотом и концентрированной серной кислотой
4) разбавленной азотной кислотой и железом
15. Выбрать правильный ответ
И медь, и цинк способны вступать во взаимодействие с
1) соляной кислотой
2) разбавленной серной кислотой
3) раствором сульфата железа(II)
4) концентрированной азотной кислотой
16. Выбрать правильные ответы
Какие из приведенных утверждений о металлах и их свойствах
верны?
А. В природе все металлы встречаются в самородном состоянии.
Б. Атомы металлов способны только отдавать валентные электроны.
1) верно только А
2) верно только Б
3) верны оба утверждения
4) оба утверждения неверны
17. Выбрать правильные ответы
Литий взаимодействует с
1) азотом 4) толуолом
2) водородом 5) кислородом
3) метаном 6) гексаном
18. Выбрать правильные ответы
Натрий взаимодействует с
1) бензолом 4) ацетиленом
2) метаном 5) хлорэтаном
3) глицерином 6) гидроксидом калия
19. Выбрать правильные ответы
Хром взаимодействует с
1) гидроксидом меди(II)
2) раствором сульфата никеля(II)
3) разбавленной азотной кислотой
4) этанолом
5) оксидом алюминия
6) соляной кислотой
20. Выбрать правильный ответ
Коррозия детали, изготовленной из железного сплава, будет
наибольшей при
помещении ее в воду
1) насыщенную кислородом
2) насыщенную смесью кислорода и углекислого газа
3) содержащую уротропин
4) дистиллированную
21. Установить соответствие между металлом и способом его
получения
путем электролиза
МЕТАЛЛ ЭЛЕКТРОЛИЗ
А) барий 1) расплава галогенидов
Б) серебро 2) водного раствора солей
В) алюминий 3) раствора глинозема в расплавленном
криолите
22. Выбрать правильные ответы
Электролиз водного раствора соли можно использовать для
получения
1) калия 4) алюминия
2) цинка 5) меди
3) хрома 6) магния
23. Выбрать правильный ответ
И оксид алюминия, и гидроксид калия реагируют с
1) соляной кислотой 3) нитратом кальция
2) оксидом магния 4) водой
24. Выбрать правильный ответ
И оксид хрома(III), и оксид хрома(VI) реагируют с
1) сульфатом магния 3) водой
2) гидроксидом натрия 4) серной кислотой
25. Выбрать правильные утверждения
Какие из приведенных утверждений о марганце и его
соединениях верны?
А. В соединениях марганец проявляет степени окисления от +2
до +7.
Б. Оксид марганца(VII) и соответствующий ему гидроксид
проявляют
кислотные свойства.
1) верно только А
2) верно только Б
3) верны оба утверждения
4) оба утверждения неверны
26. Выбрать правильные утверждения о металлах
1) Щелочные металлы можно получить путем электролиза водных
растворов
их солей
2) Для восстановления активных металлов из их оксидов можно
использовать водород
3) Наиболее устойчивая степень окисления железа равна +3
4) Внешний электронный уровень атома меди в невозбужденном
состоянии
содержит два s-электрона
5) Соединения хрома(VI) являются сильными окислителями
6) Большинство соединений d-элементов окрашено
27. Выбрать правильные ответы
Магний взаимодействует с
1) 1,2-дихлорэтаном
2) бромэтаном в диэтиловом эфире
3) гидроксидом натрия
4) пропаном
5) карбонатом кальция
6) муравьиной кислотой
28. Выбрать правильные ответы
Цинк взаимодействует с
1) раствором гидроксида натрия
2) толуолом
3) 1,2-дибромпропаном
4) серой
5)сульфатом калия
29. Выбрать правильный ответ
При комнатной температуре азот реагирует с
1) кислородом 3) кальцием
2) литием 4) водородом
30. Установить последовательность усиления кислотных свойств
галогеноводородных кислот
1) HF 2) HCl 3) HBr 4) HI
31. Установить последовательность усиления кислотных свойств
кислот
1) селенистая кислота2) сернистая кислота 3) серная кислота4) хлорная кислота
32. Выбрать правильный ответ
Оксид кремния(IV) взаимодействует с каждым из трех веществ
1) H2O, O2, NaOH водой, кислородом, гидроксидом натрия
2) K2CO3, CaO, HNO3 карбонатом калия, оксидом кальция,
азотной кислотой
3) C, KOH, SO2 углеродом, гидроксидом калия, оксидом
серы(IV)
4) HF, Mg, CaCO3 плавиковой кислотой, магнием, карбонатом
кальция
33. Выбрать правильные ответы
Оксид углерода(II) взаимодействует с
1) хлором
2) oксидом железа(III)
3) карбонатом кальция
4) соляной кислотой
5) кислородом
6) раствором гидроксида калия
34. Выбрать правильные ответы
Аммиак взаимодействует с
1) серной кислотой
2) водородом
3) медью
4) оксидом меди(II)
5) гидроксидом меди(II)
6) гидроксидом натрия
35. Выбрать правильные ответы
Оксид серы(IV) взаимодействует с
1) сероводородом
2) концентрированной серной кислотой
3) концентрированной азотной кислотой
4) азотом
5) углекислым газом
6) оксидом азота(IV)
36. Какие из приведенных утверждений о соединениях неметаллов
верны?
А. Летучие водородные соединения, образованные химическими
элементами
IVА группы, проявляют основные свойства.
Б. Оксиды и кислоты, в которых атом неметалла проявляет
промежуточную
степень окисления, обладают окислительно-восстановительной
двойственностью.
1) верно только А
2) верно только Б
3) верны оба утверждения
4) оба утверждения неверны
37. И с хлороводородной, и с серной кислотой взаимодействует
каждое из
трех веществ
1) Ag, BaCl2, NaOH
2) K2CO3, Mg(OH)2, Zn
3) Ca(NO3)2, BaO, H2S
4) Na3PO4, SO2, BaO
Источник
Технологическая карта урока: 11 класс. Обобщение знаний по теме: «Металлы и их соединения»
Оценка УЭ-0
Цель урока: в результате овладения содержанием модуля вы будете знать положение металлов в Периодической системе, строение атомов металлов, физические и химические свойства металлов и их соединений; уметь объяснять зависимость свойств металлов и их соединений от положения в Периодической системе; развивать учебные умения самостоятельно работать с текстом и практические навыки работы с тестами ЕГЭ (части А, В, С) Познакомьтесь с целью урока
УЭ-1 Цель: определить исходный уровень знаний о металлах и их соединениях.
1. Запишите в тетради дату, тему урока и выполните тестовую работу по теме «Металлы и их соединения», используя знания из ранее изученных тем. 1.Выполните задания: 1 уровень. Вставьте пропущенное слово: 1.Атомы металлов легко отдают валентные электроны и превращаются в положительно заряженные ионы, т.е. являются __________________ .
2.В главных подгруппах сверху вниз восстановительная активность атомов металлов _____________________ .
3.В периодах слева направо восстановительная способность атомов металлов __________________________ .
4.Только некоторые металлы ___________ , _____________, находятся в природе в виде простых веществ.
5.При обычных условиях все металлы, за исключением ___________ , находятся в твёрдом состоянии.
6.Самые мягкие металлы ________________ , самый твёрдый _______ , самый тугоплавкий ___________________ .
7. ______________________ , и _________________________ обусловлены наличием в металлических решетках свободных электронов. 2. Оцените свою работу. Правильные ответы найдете на доске. Мотивация урока Работайте самостоятельно За каждый правильный ответ получаете 1 балл. Ваша сумма баллов __________
УЭ-2 Цель: закрепить умения составлять уравнения реакций взаимодействия металлов с простыми и сложными веществами. 1. Закончите уравнения реакций. 1 уровень: а) Na + O2 =________________________________________ Работайте самостоятельно Обсудите вопросы в парах и дайте ответ. Оцените свою работу б) K + H2 =_________________________________________ в) Fe + Cl2 = ________________________________________ г) Fe + I2 =__________________________________________ д) Mg + P =_________________________________________ 2 уровень: е) Be + KOH сплавление ___________________________ ж) Zn + KOH + H2O = _________________________________ з) Fe + H2SO4 ( конц.) = _________________________________ по следующим критериям: а) – д) – 1 балл за уравнение е) – з) – 2 балла за уравнение Ваша сумма баллов __________ УЭ-3 Цель: определить взаимосвязь различных классов неорганических веществ. 1.Выполните задание высокого уровня сложности (С 2) Соль, полученную при растворении меди в разбавленной азотной кислоте, подвергли электролизу, используя графитовые электроды. Вещество, выделившееся на аноде, ввели во взаимодействие с натрием, а полученный продукт реакции поместили в сосуд с углекислым газом. Составьте уравнения четырёх описанных реакций. 1.________________________________________________________________ 2._________________________________________________________________ 3._________________________________________________________________ 4._________________________________________________________________ Работайте самостоятельно Оцените свою работу по следующим критериям: за 1 правильно написанное уравнение реакции – 1 балл Ваша сумма баллов __________ УЭ-4 Цель: отработать навыки решения расчетных задач высокого уровня сложности (С4) 1. Реши задачу: Сплав серебра с медью массой 500 г обработали раствором азотной кислоты. К полученному раствору добавили соляную кислоту. Масса образовавшегося осадка равна 430 г. Определите массовую долю (%) серебра в сплаве. Выполняйте самостоятельно Запишите решение задачи в тетради. УЭ-5 Цель: определить степень усвоения знаний по теме урока. 1.Выполните задания: 1 вариант 1 уровень. Выбери правильные ответы, заполни таблицу: 1 2 3 4 5 6 7 1. В порядке усиления металлических свойств химические элементы расположены в ряду: 1) Na – K – Cu – Rb 3) Mg – Ca – Sr – Rb 2) Al – Мg – Na – Li 4) Ca – K – Rb – Sr 2. Пероксид металла образуется при взаимодействии кислорода с 1) цинком 2) литием 3) натрием 4) алюминием 3. Железо вытесняет металл из растворов обеих солей: Выполняйте самостоятельно Работайте по вариантам: Прочитайте на доске номера правильных ответов. За каждый правильный ответ получаете 1 балл – 1 уровень и 2 балла – 2 уровень, 1)нитрат цинка и сульфат никеля (II); 2)сульфат меди (II) и нитрат серебра; 3)нитрат марганца(II) и сульфат алюминия; 4)хлорид магния и хлорид кобальта(II); 4. С концентрированной азотной кислотой при комнатной температуре взаимодействует металл: 1)алюминий 2) хром 3)золото 4)медь 5. С образованием щелочи с водой взаимодействует: 1) железо 2) хром 3) калий 4) магний 6. Какие из приведённых утверждений о металлах и их свойствах верны? А. В природе все металлы встречаются в самородном состоянии. Б. Атомы металлов способны только отдавать валентные электроны. 1) верно только А 3) верны оба суждения 2) верно только Б 4) оба суждения не верны 7. Какие из приведенных утверждений о щелочных металлах верны? А. Щелочные металлы проявляют во всех соединениях степень окисления + 1 Б. Щелочные металлы получают путём электролиза растворов их хлоридов. 1) верно только А 3) верны оба суждения 2) верно только Б 4) оба суждения не верны 2 уровень. Выбери правильные ответы В1. Магний взаимодействует с 1) 1,2- дихлорэтаном 4) пропаном 2) Хлором 5) карбонатом кальция 3) Гидроксидом натрия 6) муравьиной кислотой В2 А Б В Г Установите соответствие между металлом и способом его электролитического получения Металл Электролиз А) ртуть 1) водного раствора солей Б) алюминий 2) расплава хлорида В) литий 3)водного раствора гидроксида Г) железо 4) расплава нитрата если всё верно, при одной ошибке – 1 балл 5) раствора глинозёма в расплавленном криолите 2 вариант 1 уровень. Выбери правильные ответы, заполни таблицу: 1 2 3 4 5 6 7 1. В порядке уменьшения металлических свойств химические элементы расположены в ряду: 1) Mg – Be – Li 3) Cs – Rb – Sr 2) Sc – Rb – K 4) Li – Na – K 2. Железо окисляется до степени окисления + 2 под действием 1) фтора 2) хлора 3) брома 4) йода 3. Хром вытесняет металл из растворов обеих солей 1) хлорид меди (II) и нитрат никеля (II); 2) нитрат железа (II) и хлорид магния 3) сульфат марганца (II) и сульфат натрия 4) хлорид цинка и хлорид бария 4. Без нагревания с водой взаимодействует 1) натрий 2) марганец 3) хром 4)олово 5. Медь может вступать во взаимодействие с водным раствором 1) гидроксида натрия 3) серной кислоты 2) хлорида цинка 4) нитрата серебра 6. Какие из приведённых утверждений о металлах и их свойствах верны? А. Все металлы при комнатной температуре находятся в твёрдом состоянии Б. Металлы в химических реакциях могут быть как окислителями, так и восстановителями 1) верно только А 3) верны оба суждения 2) верно только Б 4) оба суждения не верны 7. Какие из приведенных утверждений об алюминии и его соединениях верны? А. Алюминий проявляет сильные восстановительные свойства Б. Оксид и гидроксид алюминия обладают амфотерными свойствами 1) верно только А 3) верны оба суждения 2) верно только Б 4) оба суждения не верны 2 уровень. Выбери правильные ответы В1. Цинк взаимодействует с Ваша сумма баллов ________________ 1) 1,2- дибромпропаном 4) кислородом 2) толуолом 5) оксидом алюминия 3) гидроксидом натрия 6) сульфатом калия В2 А Б В Г Установите соответствие между металлом и способом его электролитического получения Металл Электролиз А) барий 1) водного раствора гидроксидов Б) серебро 2) водного раствора солей В) цезий 3) расплава нитрата Г) хром 4) расплава галогенидов 5) раствора глинозёма в расплавленном криолите 2.Оцените себя 1. Суммируйте набранные вами баллы за урок. Критерии оценок: «5»–31-37 баллов «4»– 21-30 баллов «3»– 15 -20 баллов «2»– меньше 15 баллов Спасибо за сотрудниче
Источник
Контрольная работа № 1 по теме «Металлы» Вариант 1
1.Распределение электронов 2é 8é 2é соответствует атому элемента с атомным номером:
а) 11; б) 20; в) 13; г) 12.
Напишите формулу оксида и гидроксида этого элемента и укажите его свойства (основные, кислотные, амфотерные).
2. Химические элементы расположены в ряду в порядке увеличения их атомных радиусов
а) Na, Mg, Al; б) Sr, Ca, Mg; в) Na, Cs, Rb; г) Ca, K, Rb.
3. Наиболее электропроводным металлом из перечисленных является
а) цинк; б) медь; в) свинец; г) хром.
4. Реагирует с водой без нагревания металл:
а) железо; б) кальций; в) магний; г) цинк.
5. С раствором серной кислоты взаимодействует:
а) калий; б) свинец; в) медь; г) цинк.
6. С раствором хлорида меди (II) взаимодействует:
а) серебро; б) ртуть; в) железо; г) кальций.
7. Оксид кальция реагирует с веществами:
а) CO2; б) NaOH; в) Н2O; г) НCl.
8) Натрий в промышленности получают, используя метод:
а) пирометаллургия; б) гидрометаллургия; в) электрометаллургия; г) магниетермия.
9) Качественной реакцией на ион бария Ba2+ является:
а) NO3–; б) OH–; в) SO42-; г) Cl–
10) Какие из приведенных утверждений о металлах и их свойствах верны?
А. В природе большинство металлов встречаются в самородном виде.
Б. Ионы металлов не могут иметь отрицательный заряд.
а) верно только А; б) верно только Б; в) верны оба утверждения; г) неверны оба утверждения.
11) Составьте уравнения реакций, с помощью которых можно осуществить следующие превращения
![]()
![]() 2 и 6 реакцию рассмотрите с точки зрения ТЭД, 1, 4, 5 с точки зрения ОВР.
2 и 6 реакцию рассмотрите с точки зрения ТЭД, 1, 4, 5 с точки зрения ОВР.
12. Магний, содержащий 20 % примесей, массой 9 г взаимодействует с серной кислотой, вычислите объем водорода, если выход реакции составил 95% .
Контрольная работа № 1 по теме «Металлы» Вариант 2
1.Распределение электронов 2é 8é 3é соответствует атому элемента с атомным номером:
а) 11; б) 20; в) 13; г) 12.
Напишите формулу оксида и гидроксида этого элемента и укажите его свойства (основные, кислотные, амфотерные).
2. Химические элементы расположены в ряду в порядке усиления металлических свойств
а) Na, Mg, Al; б) Sr, Ca, Mg; в) Na, Cs, Rb; г) Ca, K, Rb.
3. Самый тугоплавкий металл
а) галлий; б) вольфрам; в) цезий; г) алюминий.
4. Реагирует с водой в раскаленном виде металл:
а) железо; б) кальций; в) магний; г) калий.
5. С раствором соляной кислоты не взаимодействует:
а) магний; б) железо; в) медь; г) цинк.
6. С раствором хлорида ртути (II) взаимодействует:
а) серебро; б) золото; в) барий; г) медь.
7. Оксид алюминия реагирует с веществами:
а) CO2; б) NaOH; в) Н2O; г) Н2SO4.
8) Кальций в промышленности получают, используя метод:
а) пирометаллургия; б) электрометаллургия; в) гидрометаллургия; г) магниетермия.
9) Качественной реакцией на ион бария Са2+ является:
а) NO3–; б) СО32-; в) SO42-; г) Cl–
10) Какие из приведенных утверждений о металлах и их свойствах верны?
А. Металлы IIА группы относятся к щелочноземельным .
Б. У натрия восстановительные свойства выражены сильней, чем у цезия.
а) верно только А; б) верно только Б; в) верны оба утверждения; г) неверны оба утверждения.
11) Составьте уравнения реакций, с помощью которых можно осуществить следующие превращения
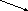
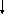
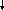
![]()

![]()
![]()
![]()
3, 4 и 6 реакцию рассмотрите с точки зрения ТЭД, 1, 2 с точки зрения ОВР.
12. Технический литий массой 14,375 г, содержащий 20 % примесей, поместили в сосуд с водой. Рассчитайте объем водорода, если выход реакции составил 80% .
Источник
Контрольная работа по теме «Металлы» Вариант1
1. Самым распространенным металлом в земной коре является:
а) натрий; б) алюминий; в) золото; г) кальций.
2.Из приведенного перечня металлов:Na,Cd ,Ca ,Co, Mn, L,i, Au ,Zn, Mg, Cu, Os
к легким относятся:
к тяжелым относятся:
3. Получение металлов из руд при высоких температурах называется:
а) электрометаллургия б) пирометаллургия в) гидрометаллургия г)карботермия
4. В электротехнике для производства ламп накаливания используют металлическую нить:
а) Al б) Ca в) Mo г) W
5. При сгорания натрия в кислороде образуется вещество состава … , а при сгорании железа в кислороде образуется …
6. Сколько молей оксида алюминия образуется из одного моля алюминия по реакции:
а) 0.5 б) 2 в)3 г) 4
7. Сплав никеля и хрома , обладающий большой жаропрочностью называется:
а) латунь б)дюралюминий в)бронза г)нихром
8. Верны ли следующие суждения о металлах: А) В периоде с увеличением заряда ядра металлические свойства ослабевают; Б) Все металлы при комнатной температуре являются твердыми.
а) верно только А б) верно только Б в) верны оба суждения г) оба суждения не верны.
9) Медну пластинку внесли в нагретую до температуры красного каления печь. Какой из графиков отражает изменение массы пластинки приокисления меди до оксида меди
а) б) в) г)
10. Какой из перечисленных металлов способен вытеснять водород из воды при комнатной температуре:
а) медь б) железо в) натрий в) серебро
11. При растворения натрия в воде образуется раствор:
а) пероксид натрия б) оксида натрия в) гидроксида натрия г) гидрида натрия
12.Тип связи, существующий в кристаллах металлов:
1) Ионная 2) Ковалентная полярная 3) Ковалентная неполярная 4) Металлическая
13. Соляной кислотой не будет взаимодействовать:
а) Cu б) Fe в) Al г) Zn
14. С водой не взаимодействует:
а) Сa б) Ni в) Fe г)Na
15. Между какими из попарно взятых веществ, формулы которых даны ниже (электролит берется в виде водного раствора), произойдет химическая реакция:
а) Au и AgNO3 б)ZnиMgCl2 в)Pb и ZnSO4 г)Feи CuCl2
16. Сумма всех коэффициентов в уравнении реакции меди с концентрированной серной кислотой равна:
а) 7; б) 6; в) 5; г) 4
17. Качественным реактивом на катион кальцияCa2+ является:
а) нитрат-ион б) карбонат-ионв) сульфат-ионг) хлорид-ион
Задания с открытым ответом
18. Осуществите превращения:Na→Na2O2 →Na2O→NaOH→Na3PO4→NaNO3.. Укажите типы реакции.
Na2CO3
5 реакцию напишите в сокращенно-ионном виде.
19. Вычислите массу хлорида алюминия, образующегося при взаимодействии 5.4 г алюминия с соляной кислотой, если выход продукта реакции от теоретически возможного составляет 80%?
Контрольная работа по химии по теме «Металлы» Вариант2
1.Самый активный металл первой группы главной подгруппы:
а) цезий б) рубидий в) калийг) натрий
2.Назовите металлы:
а) самый тяжелый… г) самый легкий…
б) самый твердый … д) самый легкоплавкий…
в) самый тугоплавкий… е) самый мягкий…
3. Каким методом в металлургии получают щелочные металлы:
а) пирометаллургией; в) электрометаллургией;
б) гидрометаллургией; г) микробиологическим
4. В электротехнике используют следующее физическое свойство меди и алюминия:
а) теплопроводность б) ковкость в) пластичность г) электропроводность
5. При окисления лития в атмосфере воздуха преимущественно образуется вещество состава … , а при сгорании натрия в кислороде образуется …
6. Сколько молей оксида железа (III) образуется из одного моля железа по реакции
а) 0.5 б) 2 в) 3 г) 4
7. Какие металлы входят в состав бронзы:
а) медь и свинец; б) медь и олово в) медь и железо; г) медь и ртуть.
8. Верны ли следующие суждения о железе:
А) Простое вещество железо, является только восстановителем; Б) В своих соединениях железо проявляет постоянную степень окисления +2.
а) верно только А б) верно только Б в) верны оба суждения г) оба суждения не верны
9. Кусочек кальция внесли в стакан с водой. Какой из графиков отражает изменение массы полученного раствора при взаимодействии кальция с водой:
а) б) в) г)
10. Какой металл не вытесняет водород из разбавленной кислоты:
a) магний б)алюминий в)натрий г)ртуть
11. При взаимодействии калия с разбавленной соляной кислотой преимущественно образуется
а) хлорид калия б) гидроксид калия в) пероксид калия г) оксид калия
12. Металлическая связь имеется в соединении
а) FеО б) FеС13 в) Fе г) Fе(ОН)3
13. С азотной концентрированной кислотой невзаимодействует:
а) медь б) цинкв) кальций г) алюминий.
14. При взаимодействии какого металла с водой образуется щелочь:
а) магний б) алюминий в) медь г) литий
15. Между какими из попарно взятых веществ, формулы которых даны ниже (электролит берется в виде водного раствора), произойдет химическая реакция:
а) Ag и KNO3 б)Zn и CuCl2 в) Pb и FeSO4 г) Fe и MgCl2
16. Сумма всех коэффициентов в уравнении реакции меди с концентрированной азотной кислотой равна:
а) 7 б) 8 в) 9 г) 10
17. Качественным реактивом на катион барияBa2+ является:
а) нитрат-ионб) карбонат-ионв) сульфат-ионг) хлорид-ион
Задания с открытым ответом
18. Осуществите превращения:Fe→FeSO4→Fe(OH)2→FeO→Fe→FeCl3
Fe(OH)3
Укажите типы реакции, 6 реакцию рассмотрите сточки зрения ОВР
19. При взаимодействии 5,4 гAl с соляной кислотой было получено 6,4 л водорода (н.у.).Сколько это составляет процентов от теоретически возможного?
Инструкция по проверке и оценке контрольной работы по химии
За правильный ответ на каждое задание части ставится 1 балл.
1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | 19 | |
В-1 | б | Легкие:Al. Mg. Na. Ca. Li, остальные-тяжелые | б | г | Na2O2 Fe3O4 | а | г | а | в | в | в | г | а | б | г | а | б | 21.36 | |
В-2 | а | Os Cr W Li Hg Cs | в | г | Li3NNa2O2 | а | б | а | б | г | б | в | г | г | б | г | в | 95,2 |
Шкала оценки
27 – 32 балла, оценка «5»
18 – 26 баллов, оценка «4»
9 – 17 баллов, оценка «3»
0 – 8 баллов, оценка «2»
За каждое правильное задание №№1-17 – по 1 баллу.
18 задание – 8 баллов – по 1 за каждое молекулярное уравнение и 1 балл за полное и сокращенное ионные уравненияи ОВР, 1 б за определение типов реакции
19 задание-3 балла-
1 балл за составленное уравнение реакции или схему превращения с учетом молей участвующих веществ
1 балл – за расчет массы и количества вещества чистого вещества
1 балл – за расчет по химическому уравнению
Источник
