Какая функциональная группа придает аминокислоте кислые какая щелочные свойства
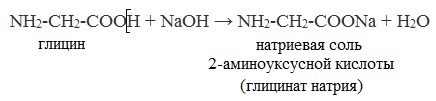
Опубликовано 5 месяцев назад по предмету
Химия
от emailmuhamedx9
Не тот ответ, который вам нужен?
Найди нужный
Самые новые вопросы
![]()
Математика – 5 месяцев назад
Сколько здесь прямоугольников
![]()
История – 1 год назад
Какое управление было в древнейшем риме? как звали первого и последнего из царей рима?
![]()
Литература – 1 год назад
Уроки французского ответе на вопрос : расскажите о герое по следующему примерному плану: 1.почему мальчик оказался в райцентре ? 2.как он чувствовал себя на новом месте? 3.почему он не убежал в деревню? 4.какие отношения сложились у него с товарищами? 5.почему он ввязался в игру за деньги? 6.как характеризуют его отношения с учительницей ? ответе на эти вопросы пожалуйста ! сочините сочинение пожалуйста
![]()
Русский язык – 1 год назад
Помогите решить тест по русскому языку тест по русскому языку «местоимение. разряды местоимений» для 6 класса
1. укажите личное местоимение:
1) некто
2) вас
3) ни с кем
4) собой
2. укажите относительное местоимение:
1) кто-либо
2) некоторый
3) кто
4) нам
3. укажите вопросительное местоимение:
1) кем-нибудь
2) кем
3) себе
4) никакой
4. укажите определительное местоимение:
1) наш
2) который
3) некий
4) каждый
5. укажите возвратное местоимение:
1) свой
2) чей
3) сам
4) себя
6. найдите указательное местоимение:
1) твой
2) какой
3) тот
4) их
7. найдите притяжательное местоимение:
1) самый
2) моего
3) иной
4) ничей
8. укажите неопределённое местоимение:
1) весь
2) какой-нибудь
3) любой
4) этот
9. укажите вопросительное местоимение:
1) сколько
2) кое-что
3) она
4) нами
10. в каком варианте ответа выделенное слово является притяжательным местоимением?
1) увидел их
2) её нет дома
3) её тетрадь
4) их не спросили
![]()
Русский язык – 1 год назад
Переделай союзное предложение в предложение с бессоюзной связью.
1. океан с гулом ходил за стеной чёрными горами, и вьюга крепко свистала в отяжелевших снастях, а пароход весь дрожал.
2. множество темноватых тучек, с неясно обрисованными краями, расползались по бледно-голубому небу, а довольно крепкий ветер мчался сухой непрерывной струёй, не разгоняя зноя
3. поезд ушёл быстро, и его огни скоро исчезли, а через минуту уже не было слышно шума
![]()
Русский язык – 1 год назад
помогите прошу!перепиши предложения, расставляя недостающие знаки препинания. объясни, что соединяет союз и. если в предложении один союз и, то во втором выпадающем списке отметь «прочерк».пример:«я шёл пешком и,/поражённый прелестью природы/, часто останавливался».союз и соединяет однородные члены.ночь уже ложилась на горы (1) и туман сырой (2) и холодный начал бродить по ущельям.союз и соединяет:1) части сложного предложенияоднородные члены,2) однородные членычасти сложного предложения—.поэт — трубач зовущий войско в битву (1) и прежде всех идущий в битву сам (ю. янонис).союз и соединяет:1) части сложного предложенияоднородные члены,2)
![]()
Физика – 1 год назад
Вокруг прямого проводника с током (смотри рисунок) существует магнитное поле. определи направление линий этого магнитного поля в точках a и b.обрати внимание, что точки a и b находятся с разных сторон от проводника (точка a — снизу, а точка b — сверху). рисунок ниже выбери и отметь правильный ответ среди предложенных.1. в точке a — «от нас», в точке b — «к нам» 2. в точке a — «к нам», в точке b — «от нас» 3. в обеих точках «от нас»4. в обеих точках «к нам»контрольная работа по физике.прошу,не наугад важно
Информация
Посетители, находящиеся в группе Гости, не могут оставлять комментарии к данной публикации.
Источник
Аминокислоты являются амфотерными соединениями, для них характерны кислотно-основные свойства. Это обусловлено наличием в их молекулах функциональных групп кислотного (-СООН) и основного (-NH2) характера.
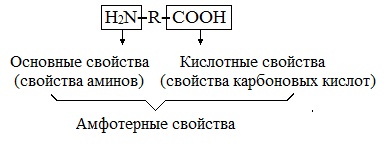
Кислотно-основное равновесие в водных растворах
В водных растворах и твердом состоянии аминокислоты существуют в виде внутренних солей.
Ионизация молекул аминокислот в водных растворах зависит от кислотного или щелочного характера среды:
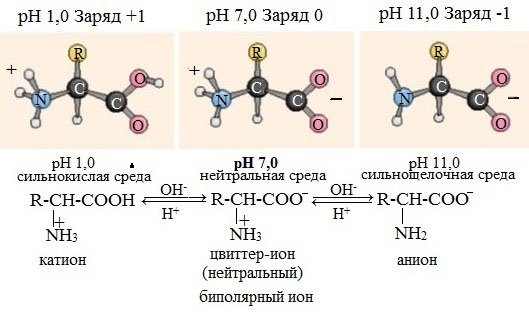
В кислой среде молекулы аминокислот представляю собой катион. В щелочной среде молекулы аминокислот представляют собой анион. В нейтральной среде аминокислоты представляют собой цвиттер-ион или биполярный ион.
Аминокислоты в твердом состоянии всегда существуют в виде биполярного, двухзарядного иона — цвиттер-иона.
Водные растворы аминокислот в кислой и щелочной среде проводят электрический ток.
1. Взаимодействие внутри молекулы – образование внутренних солей (биполярных ионов)
Молекулы аминокислот существуют в виде внутренних солей, которые образуются за счет переноса протона от карбоксила к аминогруппе.
Карбоксильная группа аминокислоты отщепляет ион водорода, который затем присоединяется к аминогруппе той же молекулы по месту неподеленной электронной пары азота. В результате действие функциональных групп нейтрализуется, образуется так называемая внутренняя соль.
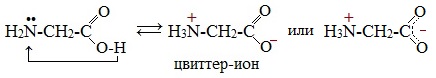
Водные растворы аминокислот в зависимости от количества функциональных групп имеют нейтральную, кислую или щелочную среду.
Аминокислоты с одной карбоксильной группой и одной аминогруппой имеют нейтральную реакцию.
Видеоопыт «Свойства аминоуксусной кислоты»
а) моноаминомонокарбоновые кислоты (нейтральные кислоты)
Внутримолекулярная нейтрализация — образуется биполярный цвиттер-ион.
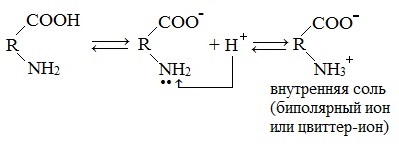
Водные растворы моноаминомонокарбоновых кислот нейтральны (рН≈7).
б) моноаминодикарбоновые кислоты (кислые аминокислоты)
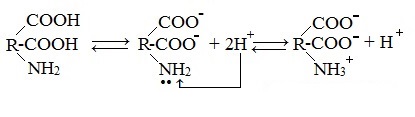
Водные растворы моноаминодикарбоновых кислот имеют рН<7 (кислая среда), так как в результате образования внутренних солей этих кислот в растворе появляется избыток ионов водорода Н+.
в) диаминомонокарбоновые кислоты (основные аминокислоты)
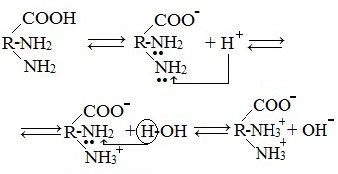
Водные растворы диаминомонокарбоновых кислот имеют рН>7 (щелочная среда), так как в результате образования внутренних солей этих кислот в растворе появляется избыток гидроксид-ионов ОН— .
2. Взаимодействие с основаниями и кислотами
Аминокислоты как амфотерные соединения образуют соли как с кислотами (по группе NH2), так и со щелочами (по группе СООН).
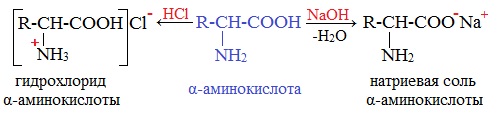
Как кислота (участвует карбоксильная группа)
Как карбоновые кислоты α-аминокислоты образуют функциональные производные: соли, сложные эфиры, амиды.
а) взаимодействие с основаниями
Образуются соли:
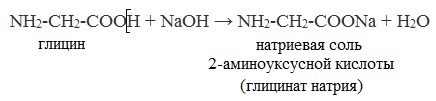
б) взаимодействие со спиртами (р. этерификации)
Аминокислоты могут реагировать со спиртами в присутствии газообразного хлороводорода, превращаясь в сложный эфир. Сложные эфиры аминокислот не имеют биполярной структуры и являются летучими соединениями.
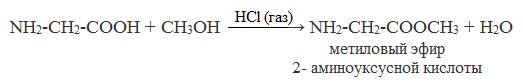
в) взаимодействие с аммиаком
Образуются амиды:
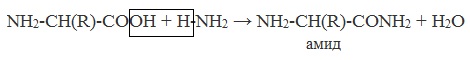
Как основание (участвует аминогруппа)
а) взаимодействие с сильными кислотами
Подобно аминам, аминокислоты реагируют с сильными кислотами с образованием солей аммония:
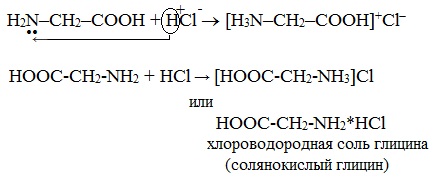
б) взаимодействие с азотистой кислотой (р. дезаминирования)
Подобно первичным аминам, аминокислоты реагируют с азотистой кислотой, при этом аминогруппа превращается в гидроксогруппу, а аминокислота – в гидроксикислоту:
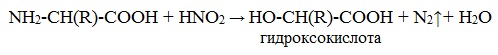
Измерение объёма выделившегося азота позволяет определить количество аминокислоты (метод Ван-Слайка).
3. Внутримолекулярное взаимодействие функциональных групп ε-аминокапроновой кислоты, в результате которого образуется ε-капролактам (полупродукт для получения капрона).
4. Межмолекулярное взаимодействие α-аминокислот – образование пептидов (р. поликонденсации)
При взаимодействии карбоксильной группы одной молекулы аминокислоты и аминогруппы другой молекулы аминокислоты образуются пептиды. При взаимодействии двух α-аминокислот образуется дипептид.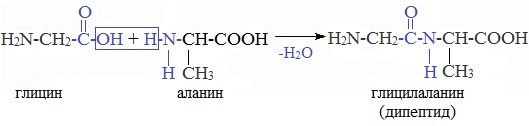
Межмолекулярная реакция с участием трех α-аминокислот приводит к образованию трипептида и т.д.
Важнейшие природные полимеры – белки (протеины) – относятся к полипептидам, т.е представляют собой продукт поликонденсации a-аминокислот.
5. Качественные реакции!
а) нингидриновая реакция
Все аминокислоты окисляются нингидрином с образованием продуктов сине-фиолетового цвета:
Иминокислота пролин дает с нингидрином желтое окрашивание.
б) с ионами тяжелых металлов α-аминокислоты образуют внутрикомплексные соли. Комплексы меди (II), имеющие глубокую синюю окраску, используются для обнаружения α-аминокислот.
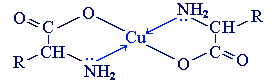
Видеоопыт «Образование медной соли аминоуксусной кислоты»
Аминокислоты
Источник
Цель: расширить знания о функциях белков в живой клетке; научить учащихся выявлять причины происходящих в клетке процессов, используя свои знания о функциях в ней белков.
Оборудование: таблицы по общей биологии, модель первичной структуры белка.
Ход урока
I. Проверка знаний учащихся.
Карточка для работы у доски.
Запишите номера вопросов, против них – правильные ответы.
- Какие органические вещества в клетке на первом месте по массе?
- Какие элементы входят в состав простых белков?
- Сколько аминокислот образует все многообразие белков?
- Сколько аминокислот являются незаменимыми для человека?
- Какие белки называются неполноценными?
- Какая функциональная группировка придает аминокислоте кислые, какое – щелочные свойства?
- В результате какой реакции образуется пептидная связь?
- Между какими группировками аминокислот образуется пептидная связь?
- Какие связи стабилизируют вторичную структуру белков ?
- Какую структуру имеет молекула гемоглобина?
Тесты классу.
Тест 1. Какие органические вещества в клетке на первом месте по массе?
- углеводы.
- белки
- липиды.
- нуклеиновые кислоты.
Тест 2. Какие элементы входят в состав простых белков?
- углерод…
- водород
- кислород
- сера
- фосфор
- азот
- железо
- хлор.
Тест 3. Сколько аминокислот образует все многообразие белков?
- 170
- 26
- 20
- 10
Тест 4. Сколько аминокислот являются незаменимыми для человека?
- таких аминокислот нет.
- 20
- 10
- 7
Тест 5. Какие белки называются неполноценными?
- В которых отсутствуют некоторые аминокислоты.
- В которых отсутствуют некоторые незаменимые аминокислоты.
- В которых отсутствуют некоторые заменимые аминокислоты.
- Все известные белки являются полноценными.
Тест 6. Какая функциональная группировка придает аминокислоте кислые, какое –щелочные свойства?
- Кислые – радикал, щелочные – аминогруппа.
- Кислые – аминогруппа, щелочные – радикал.
- Кислые – карбоксильная группа, щелочные – радикал.
- Кислые – карбоксильная группа, щелочные – аминогруппа.
Тест 7. В результате какой реакции образуется пептидная связь?
- Реакция гидролиза.
- Реакция гидратации.
- Реакции конденсации.
- Все вышеперечисленные реакции могут привести к образованию пептидной связи.
Тест 8. Между какими группировками аминокислот образуется пептидная связь?
- Между карбоксильными группами соседних аминокислот.
- Между аминогруппами соседних аминокислот.
- Между аминогруппой одной аминокислоты и радикалом другой.
- Между аминогруппой одной аминокислоты и карбоксильной группой другой.
Тест 9. Какие связи стабилизируют вторичную структуру белков ?
- ковалентные
- водородные
- ионные
- такие связи отсутствуют
Тест 10. Какую структуру имеют молекула гемоглобина?
- первичную
- вторичную
- третичную
- четвертичную
II. Изучение нового материала.
1. Свойства белков.
У человека более 10 000 видов разных белков.
Свойства белков:
- Денатурация (утрата трехмерной конформации без изменения первичной структуры ). Ренатурация.
- Нерастворимые белки (кератин, фиброин) и растворимые белки (альбумины, фибринген).
- Малоактивные и химически высокоактивные.
- Устойчивые и крайне неустойчивые.
- Фибриаллярные и глобулярные.
- Нейтральные (альбумины, глобулины), основные (гистоны), кислые (казеин)
- Инактивация при замерзании.
2. Функции белков в клетке и организме.
1. Строительная.
2. Каталическая (ферментативная).
Напомним некоторые особенности функционирования ферментов:
а) ферменты ускоряют протекание реакции только одного вида, то есть обладают специфичностью действия;
б) ферменты конкретного организма действуют в узких температурных пределах;
в) ферменты эффективно работают при строго определенных показателях среды. Например, в разных участках пищеварительного тракта она может быть слабощелочной, щелочной или кислой.
Ферментативный белок соединятся реагирующими веществами, ускоряет их превращения ения и выходит из реакции неизменным.
3. Регуляторная.
Осуществляется с помощью гормонов. Многие гормоны являются белками. Рассмотрим их действия на некоторых конкретных примерах.
Пример 1
Пример 2
Ослабленное функционирование поджелудочной железы может привести к нарушению (замедлению) процесса превращения глюкозы в гликоген, вследствие чего возникает серьезное заболевание – сахарный диабет.
4. Двигательная функция белка проявляется при работе мускулатуры человека и животных. В мышечных клетках имеются специальные сократительные белки, обеспечивающие специфическое функционирование этих клеток.
5. Транспортная функция белка проявляется в переносе кислорода и углекислого газа с помощью белка глобина.
6. Защитная функция белка заключается в выработке белков – антител, уничтожающих возбудителей болезней, попавших в организм.
Защитная функция белка приносит… человеку не только пользу. Могут возникнуть серьезные проблемы при пересадке органов и тканей от одного человека другому. Пересаженный орган воспринимается иммунной системой нового «хозяина» этого органа как чужеродный белок. Воздействие антител приводит к отторжению пересаженного органа со всеми вытекающими отсюда последствиями.
Аналогичные проблемы могут возникнуть при беременности, в том случае, если мать будущего ребенка является резус-отрицательной, а отец имеет резус-положительную кровь. В том случае может возникнуть серьёзный конфликт между материнским организмом и организмом развивающего плода.
Напомним, что ген резус-положительности доминирует над геном резус-отрицательности.
Следствием указанного выше конфликта являются задержка и нарушение процесса развития плода, в ряде случаев – его гибель. Связи с ответным воздействием антител плода на чужеродный белок материнского организма женщина испытывает симптомы обостренно протекающего токсикоза беременности.
Защитные функции могут быть могут быть ослаблены либо с помощью медицинских средств (когда это необходимо),либо в результате негативного воздействия природных факторов(ухудшение условий жизни организма, агрессия вируса СПИДа) (см. схему).
7. Энергетическая функция белка проявляется в выделении свободной энергии при последовательном расщеплении полипептидной молекулы
Биологическую роль, которую играют белки в живой клетке и организме, трудно переоценить. Вероятно, жизнь на нашей планете действительно можно рассматривать как способ существования белковых тел, осуществляющих обмен веществом и энергией с внешней средой.
III. Закрепление.
«Свойства и функции белков. »
Тест 1. Что образуется при окислении 1 г белка?
- Вода
- Углекислый газ.
- Аммиак.
- 17,6 кДж энергии.
- Мочевина.
- 38,9 кДж энергии.
Тест 2. В пробирке с пероксидом водорода поместили кусочек варенной колбасы, хлеба, моркови, рубленного яйца. В одной из пробирок выделялся кислород. В какой?
- С кусочком вареной колбасы.
- С кусочком хлебы.
- С кусочком моркови.
- С кусочком рубленного яйца.
Тест 3. Какие суждения верны?
- Ферменты специфичны, каждый фермент обеспечивает раекции одного типа.
- Ферменты универсальны и могут катализировать реакции разных типов.
- Каталическая активность ферментов не зависит от рН и температуры.
- 4. Каталическая активность ферментов напрямую зависит от рН и температуры.
Тест 4. Какие суждения верны?
- Фермент – ключ, субстрат – замок, согласно теории Фишера.
- Фермент – замок, субстрат – ключ, согласно теории Фишера.
- После каталитической реакции фермент и субстрат распадаются, образуя продукты реакции.
- После каталитической реакции фермент остается неизменным, субстрат распадается, образуя продукты реакции.
Тест 5. Какие суждения верны?
- Витамины являются кофакторами ферментов.
- Все белки являются биологическими катализаторами, ферментов.
- При замерзании происходит необратимая денатурация ферментов.
- Ренатурация – утрата трехмерной конфигурации белка без изменения первичной структуры
Тест 6. Какая функциональная группировка придает аминокислоте кислые, какое –щелочные свойства?
- Кислые – радикал, щелочные – аминогруппа.
- Кислые – аминогруппа, щелочные – радикал.
- Кислые – карбоксильная группа, щелочные – радикал.
- Кислые – карбоксильная группа, щелочные – аминогруппа.
Тест 7. В результате какой реакции образуется пептидная связь?
- Реакция гидролиза.
- Реакция гидратации.
- Реакции конденсации.
- Все вышеперечисленные реакции могут привести к образованию пептидной связи.
Тест 8. Между какими группировками аминокислот образуется пептидная связь?
- Между карбоксильными группами соседних аминокислот.
- Между аминогруппами соседних аминокислот.
- Между аминогруппой одной аминокислоты и радикалом другой.
- Между аминогруппой одной аминокислоты и карбоксильной группой другой.
Тест 9. Какие связи стабилизируют вторичную структуру белков?
- ковалентные
- водородные
- ионные
- такие связи отсутствуют.
Тест 10. Какие связи стабилизируют третичную структуру белков?
- ковалентные
- водородные
- ионные
- гидрофильно-гидрофобное взаимодействие.
На дом: стр. 94-99, вопросы в конце параграфа.
Источник
Аминокислоты – органические бифункциональные соединения, в состав которых входят карбоксильные группы –СООН и аминогруппы –NH2.
Природные аминокислоты можно разделить на следующие основные группы:
| 1) Алифатические предельные аминокислоты (глицин, аланин) | NH2-CH2-COOH глицин NH2-CH(CH3)-COOH аланин |
| 2) Серосодержащие аминокислоты (цистеин) |  цистеин |
| 3) Аминокислоты с алифатической гидроксильной группой (серин) | NH2-CH(CH2OH)-COOH серин |
| 4) Ароматические аминокислоты (фенилаланин, тирозин) |  фенилаланин
тирозин |
| 5) Аминокислоты с двумя карбоксильными группами (глутаминовая кислота) | HOOC-CH(NH2)-CH2-CH2-COOH глутаминовая кислота |
| 6) Аминокислоты с двумя аминогруппами (лизин) | CH2(NH2)-CH2-CH2-CH2-CH(NH2)-COOH лизин |
- Для природных α-аминокислот R-CH(NH2)COOH применяются тривиальные названия: глицин, аланин, серин и т. д.
- По систематической номенклатуре названия аминокислот образуются из названий соответствующих кислот прибавлением приставки амино- и указанием места расположения аминогруппы по отношению к карбоксильной группе:
- Часто используется также другой способ построения названий аминокислот, согласно которому к тривиальному названию карбоновой кислоты добавляется приставка амино- с указанием положения аминогруппы буквой греческого алфавита.
Аминокислоты – твердые кристаллические вещества с высокой температурой плавления. Хорошо растворимы в воде, водные растворы хорошо проводят электрический ток.
- Замещение галогена на аминогруппу в соответствующих галогензамещенных кислотах:

- Восстановление нитрозамещенных карбоновых кислот (применяется для получения ароматических аминокислот):

При растворении аминокислот в воде карбоксильная группа отщепляет ион водорода, который может присоединиться к аминогруппе. При этом образуется внутренняя соль, молекула которой представляет собой биполярный ион:
![]()
1. Кислотно-основные свойства аминокислот
Аминокислоты — это амфотерные соединения.
Они содержат в составе молекулы две функциональные группы противоположного характера: аминогруппу с основными свойствами и карбоксильную группу с кислотными свойствами.
Водные растворы аминокислот имеют нейтральную, щелочную или кислую среду в зависимости от количества функциональных групп.
Так, глутаминовая кислота образует кислый раствор (две группы -СООН, одна -NH2), лизин — щелочной (одна группа -СООН, две -NH2).
1.1. Взаимодействие с металлами и щелочами
Как кислоты (по карбоксильной группе), аминокислоты могут реагировать с металлами, щелочами, образуя соли:

1.2. Взаимодействие с кислотами
По аминогруппе аминокислоты реагируют с основаниями:

2. Взаимодействие с азотистой кислотой
Аминокислоты способны реагировать с азотистой кислотой.
Например, глицин взаимодействует с азотистой кислотой:
![]()
3. Взаимодействие с аминами
Аминокислоты способны реагировать с аминами, образуя соли или амиды.
![]()
4. Этерификация
Аминокислоты могут реагировать со спиртами в присутствии газообразного хлороводорода, превращаясь в сложный эфир:
Например, глицин взаимодействует с этиловым спиртом:
![]()
5. Декарбоксилирование
Протекает при нагревании аминокислот с щелочами или при нагревании.
Например, глицин взаимодействует с гидроксидом бария при нагревании:
![]()
Например, глицин разлагается при нагревании:
![]()
6. Межмолекулярное взаимодействие аминокислот
При взаимодействии аминокислот образуются пептиды. При взаимодействии двух α-аминокислот образуется дипептид.
Например, глицин реагирует с аланином с образованием дипептида (глицилаланин):

Фрагменты молекул аминокислот, образующие пептидную цепь, называются аминокислотными остатками, а связь CO–NH — пептидной связью.
Источник


Ответ
Ответ дан
janislav
Правильный вариант ответа : Б)