Как узнать какими свойствами обладает вещество

«Вещества и их свойства. Чистые вещества и смеси»
Ключевые слова конспекта: предмет химии, вещества и их свойства, чистые вещества и смеси, способо разделения смесей.
Химия – это наука о веществах, их свойствах, превращениях веществ и явлениях, сопровождающих эти превращения. Химия является одной из наук, изучающих природу. Вместе с биологией и физикой химия принадлежит к числу естественных наук.
Вещество — это то, из чего состоит физическое тело. Вещество характеризуется определенными физическими свойствами.
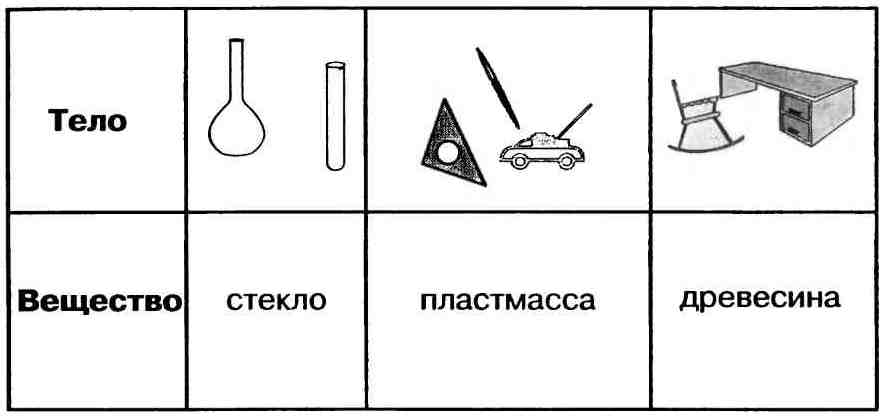
Свойства веществ — это признаки, по которым вещества отличаются друг от друга или сходны между собой, например:
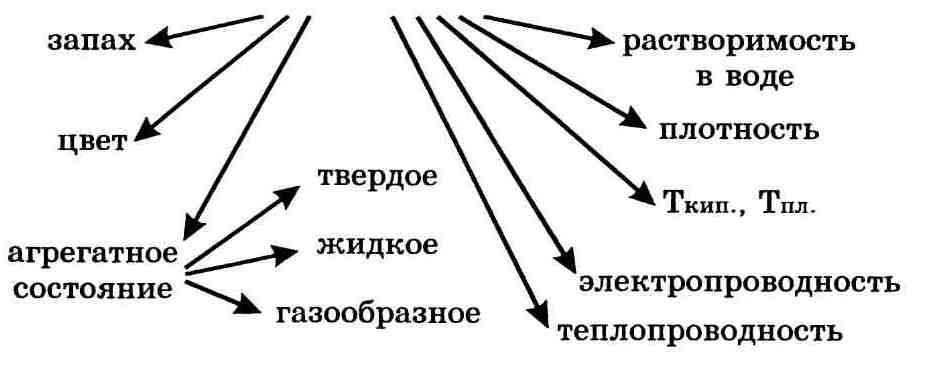
Важнейшие физические свойства вещества следующие: агрегатное состояние, цвет, запах, плотность, растворимость в воде, тепло-и электропроводность, температуры плавления и кипения.
Например, всем известное вещество алюминий можно охарактеризовать так: Алюминий — металл серебристо-белого цвета, сравнительно лёгкий (р = 2,7 г/см3), плавится при температуре 600°С. Алюминий очень пластичен. По электрической проводимости уступает лишь золоту, серебру и меди. Из-за лёгкости алюминий в виде сплавов широко используют в самолёто- и ракетостроении. Его также используют для изготовления электрических проводов и предметов быта.
Чистые вещества и смеси
Чистыми называются вещества, состоящие из одинаковых молекул. Смесь состоит из молекул разных веществ.
Каждое вещество имеет прежде всего свои, характерные именно для него свойства. Они в наибольшей степени проявляются, только если вещество является практически чистым, т. е. содержит мало примесей.
В природе чистых веществ не бывает, они встречаются преимущественно в виде смесей. Во многих случаях смеси нелегко отличить от чистых веществ. Например, сахар, растворяясь в воде, образует однородную по внешнему виду смесь. Даже с помощью микроскопа нельзя обнаружить частицы веществ, входящих в эту смесь. Такие смеси называют гомогенными (однородными).
Молоко на первый взгляд тоже кажется однородным веществом. Однако, если рассмотреть каплю молока под микроскопом, можно увидеть, что в ней плавает множество мельчайших капелек жира. Если дать молоку постоять, то эти капельки соберутся в верхнем слое, образуя сливки. Подобные неоднородные смеси называют гетерогенными смесями.
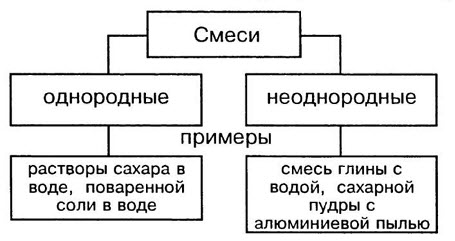
Однородные смеси — это смеси, в которых даже с помощью микроскопа нельзя обнаружить частицы веществ, входящих в смесь. Неоднородные смеси — это смеси, в которых невооруженным глазом или с помощью микроскопа можно заметить частицы веществ,составляющие смесь.
Способ разделения смесей
В смеси сохраняются свойства составляющих их веществ компонентов. На основании этих свойств выбирают рациональный способ разделения смесей.
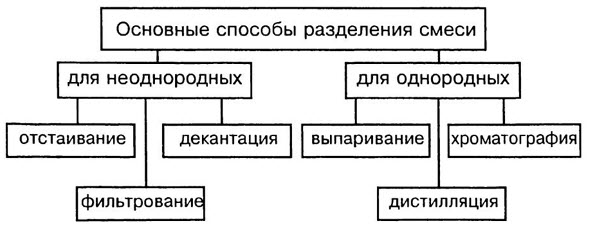
Способы разделения смесей основаны на различии свойств веществ-компонентов, их составляющих: плотности, растворимости в воде и других жидкостях-растворителях, способности плавиться и испаряться.
Способы разделения смесей: неоднородные смеси — отстаивание и фильтрование, действие магнитом; однородные смеси — перегонка, выпаривание, кристаллизация и хроматография.
Отстаивание. Прием разделения смеси твердого и жидкого вещества путем осаждения твердого на дно под действием сил тяжести.
- а) При выдерживании воды, содержащей частички глины, в емкостях глина медленно осаждается на дно, отстаивается. Применяется при очистке питьевой воды.
- б) Чтобы разделить смесь поваренной соли и речного песка, надо поместить ее в колбу и добавить воды. Соль растворится, а песок опустится на дно. Затем осторожно слить раствор, чтобы песок остался в колбе. Соль из раствора получают выпариванием воды.
- в) Для разделения смеси малорастворимых друг в друге жидкостей с различной плотностью используют делительную воронку. Это цилиндрический сосуд с краником внизу. Помещенная в эту воронку смесь бензина с водой или растительного масла с водой быстро расслаивается, причем водный слой оказывается внизу. Открывая кран, сливаем воду, а когда вода заканчивается, закрываем кран. В воронке — бензин или масло.
Фильтрование. Чтобы избавиться от нерастворимых в воде примесей, воду пропускают через фильтр. Материал фильтра — бумага, ткань, пористая керамика. Примеси остаются на фильтре, а вода очищается.
Действие магнитом. Выделение из неоднородной смеси веществ, способных к намагничиванию. К магниту притягиваются железные опилки.
Перегонка. Прием разделения однородных жидких смесей путем испарения летучих жидкостей, различающихся температурами кипения, с последующей конденсацией паров. Так из нефти, представляющей собой смесь жидких, газообразных и твердых углеводородов, получают попутные газы, бензин, керосин, дизельное топливо и другие продукты.
Выпаривание. Способ извлечения растворенного в жидком растворителе твердого или жидкого вещества. Например, упаривая воду из сладкого сиропа, получают сахар.
Кристаллизация. Избирательное извлечение одного из нескольких твердых веществ, содержащихся в растворе. Частичное упаривание воды с последующим охлаждением раствора приводит к осаждению кристаллов главного компонента. Так из морской воды выделяют поваренную соль NaCl, а другие соли, присутствующие в меньшем количестве, остаются в растворе.
Хроматография. Метод разделения смесей, основанный на различиях относительной растворимости веществ в используемом растворителе (жидкая фаза) и прочности связывания этих веществ поверхностью сорбента (твердая фаза).
Бумажная хроматография. Нанесем каплю раствора смеси двух веществ на расстоянии 2 см от края длинной полоски фильтровальной бумаги. Подвесим полоску в стеклянном цилиндре, на дне которого находится растворитель. Нижнюю часть полоски погрузим в растворитель, при этом пятно со смесью находится чуть выше. Верхняя часть полоски удерживается проволокой у отверстия цилиндра. Сверху цилиндр закроем стеклом, чтобы не испарялся растворитель. Боковые стороны полоски не касаются стенок цилиндра. Растворитель смачивает полоску, и жидкий фронт движется вверх за счет капиллярных сил. Вместе с растворителем по бумаге движутся и растворенные вещества. Если они цветные, то за движением можно наблюдать визуально. Вещество, которое лучше растворимо и менее прочно удерживается сорбентом (бумагой), поднимется выше. Когда фронт поднимется достаточно высоко и пятна разделятся, полоску вынимают и разрезают.
Колоночная хроматография — процесс, родственный рассмотренному. В качестве твердой фазы служит силикагель, помещенный в колонку. Только в этом случае смесь наносят равномерно вверху колонки, а потом добавляют растворитель. Разделенные вещества собирают внизу в разные стаканчики.
Конспект урока «Вещества и их свойства. Чистые вещества и смеси».
Следующая тема: «Физические и химические явления».
Источник
Химия – наука о веществах, их свойствах, превращениях и явлениях, сопровождающих эти превращения.
Вещества – это то, из чего состоят предметы (физические тела) окружающего мира. Вещества, существующие в природе, постоянно претерпевают различные изменения.
Явления – различные изменения, которые происходят с веществами.
Физические явления – явления, не сопровождающиеся превращениями одних веществ, в другие (обычно изменяется агрегатное состояние веществ или их форма).
Химические явления – явления, в результате которых из данных веществ образуются другие.
Иначе химические явления называют химическими реакциями.
Каждое вещество обладает строго определёнными свойствами.
Свойства веществ – признаки, позволяющие отличить одни вещества от других, или установить сходство между ними.
Физические свойства:
m – масса, V – объём, ρ – плотность.
Масса может быть выражена в граммах, объем в миллилитрах (если это жидкость) или литрах (если это газ).
1 мл = 1 см3, 1 л = 1 дм3, 1000 л = 1 м3
Поэтому плотность измеряют в г/мл, г/см3 (если это жидкость), или в г/л, г/дм3 (если это газ).
Если принять V = 1, то плотность – это масса единичного объёма вещества.
Химические свойства – это те химические реакции, в которые вступает данное вещество.
Так же можно сказать, что химические свойства – это те химические реакции, которые характеризуют группу веществ (класс веществ). Например, мы будем в дальнейшем изучать свойства воды, свойства класса оксидов, свойства класса алканов и т.д.
ООсновы атомно – молекулярного учения
Идея о том, что вещества состоят из мельчайших частиц возникла в Древней Греции в философских учениях Левкиппа и его ученика Демокрита. Эти частицы они назвали атомами (неделимые).
Существование атомов было доказано эмпирическим путём в конце 16 – начале 17 века Джоном Дальтоном и М. В. Ломоносовым. Ими же были заложены основы атомно – молекулярного учения.
В настоящее время, в связи с открытием делимости атома и появлением теории химической связи, основные положения атомно – молекулярного учения существенно изменились. Его суть можно свести к ряду важных положений, которые необходимо запомнить.
Все вещества, существующие в природе, представляют собой совокупность очень большого числа частиц (атомов, молекул или ионов). В зависимости от типа частиц все вещества условно подразделяют на две группы: вещества молекулярного строения и вещества немолекулярного строения (атомного или ионного).
Вещества молекулярного строения – вещества, основной структурной единицей которых является молекула.
Вещества немолекулярного строения – вещества, основными структурными единицами которых являются атомы или ионы.
Частицы, из которых состоит данное вещество, взаимодействуют между собой посредством электромагнитных (кулоновских) сил и находятся в постоянном движении. Движение частиц ограничено силами взаимодействия между ними.Каждое вещество, в зависимости от условий (температуры, давления) может находиться в определённом агрегатном состоянии.
В твёрдом агрегатном состоянии вещества, составляющие его частицы находятся относительно упорядоченно (кристаллическое состояние), их кинетическая энергия (энергия движения) существенно меньше чем потенциальная (энергия покоя). В газообразном состоянии, частицы свободно движутся в предоставленном им объёме и их кинетическая энергия существенно выше чем потенциальная.
В жидкости же потенциальная энергия частиц примерно равна их кинетической энергии. Это связано с тем, что часть частиц жидкости находится относительно упорядоченно в составе так называемых кластеров(англ. cluster— скопление). Другие же частицы свободно перемещаются по объёму жидкости. Чем ниже температура жидкости, тем больше в ней кластеров и наоборот.
Рис. Кластеры воды, где число молекул 20-220
Следует отметить, что существуют еще два дополнительные “состояния”. Это жидкокристаллическое состояние и состояние плазмы.
Цитоплазматическая мембрана клетки – типичный пример жидкого кристалла. Молекулы фосфолипидов в биологической мембране относительно упорядоченно распределяются в двух слоях, но при этом могут в пределах слоя свободно перемещаться, а также “перескакивать” из одного слоя в другой.
Жидкие кристаллы имеют широкое применение в технике (напр., ЖК-мониторы компьютеров).
Плазма (от греч. πλάσμα «вылепленное», «оформленное») — ионизованный газ.
Плазма в своём составе содержит свободные электроны, катионы (положительно заряженные ионы) и анионы (отрицательно заряженные ионы).
Так как плазма содержит заряженные частицы, то она проводит электрический ток и на неё можно воздействовать внешним магнитным полем. Различают низкотемпературную и высокотемпературную плазму.
Изучает свойства плазмы наука физика.
Вещество из одного агрегатного состояния может переходить в другие агрегатные состояния при изменении внешних условий – температуры (T) и давления (P). Такие переходы принято называть фазовыми переходами.
Так, при повышении температуры, твердое вещество превращается в жидкость, а жидкость при ещё большей температуре превращается в газ. Дальнейшее повышение температуры переводит газ в плазму. При таких переходах вещество в другие вещества не превращается. Напомним, что такие явления мы называем физическими. Поэтому фазовые переходы – это физические явления.
При понижении температуры происходят обратные фазовые переходы – газ превращается в жидкость, а жидкость переходит в твердое состояние.
Фазовые переходы имеют названия.
Твердое —> Жидкое (плавление, обратный переход – кристаллизация)
Жидкое —> Газообразное (испарение, обратный переход – конденсация)
Газообразное —> Плазма (ионизация, обратный переход – деионизация)
Твердое —> Газообразное (сублимация или возгонка, обратный переход – десублимация)
Вещество – совокупность большого числа частиц, находящаяся в определённом агрегатном состоянии в зависимости от условий (температуры и давления).
Поэтому, например, такая фраза как: “Вода – жидкое вещество”, является некорректной. Если мы говорим об агрегатном состоянии вещества, то следует обязательно уточнить условия в которых находится вещество – температуру и давление. Такая фраза как: “При нормальном атмосферном давлении и комнатной температуре, вода – жидкое по агрегатному состоянию вещество”, является правильной.
С точки зрения физики, что более точно, вещество – это форма материи, состоящая из частиц, обладающих массой покоя. Существуют частицы, не обладающие массой покоя, например, фотоны. Материя, состоящая из частиц, не обладающих массой покоя называется поле.
Протоны, нейтроны, электроны – это частицы, обладающие массой покоя, следовательно это частицы вещества. Но химия не изучает вещество, состоящее, к примеру, из электронов (электронный газ), или вещество, состоящее из нейтронов (нейтронный газ). Это удел физики.
Химия изучает вещества, состоящие из атомов, молекул или ионов.
Ввиду этого вещество условно можно подразделить на физическое (электронный газ в проводнике, нейтронный газ и т.д.) и химическое (состоящее из атомов, молекул, ионов, свободных радикалов).
Источник
Гипермаркет знаний>>Химия>>Химия 7 класс>> Вещества и их свойства. Экспериментируем дома. Свойства некоторых продуктов питания
Первоначальные химические понятия
Вещества и их свойства
Материал параграфа поможет вам:
> различать вещества, физические тела и материалы;
> характеризовать вещества по физическим свойствам.
Вещество.
В повседневной жизни мы сталкива емся со многими веществами. Среди них — вода, песок, железо, золото, сахар, соль, крахмал, уголь… Продолжать этот перечень можно очень долго. В сотни раз больше веществ используют и получают ученые.

Рис. 20. Природные вещества
Ныне известно свыше 20 млн веществ. Многие из них существуют в природе (рис. 20). В воздухе есть различные газы; в реках, морях и океанах, кроме воды, — растворенные в ней вещества; в твердом поверхностном слое нашей планеты — многочисленные минералы, горные породы, руды и т. п. Чрезвычайно большое количество веществ находится и в живых организмах.

Рис. 21. Искусственно полученные вещества
Алюминия, цинка, ацетона, извести, мыла, аспирина, полиэтилена, многих других веществ в природе нет. Их выпускает промышленность (рис. 21).
Некоторые вещества, существующие в природе, можно получить и в химической лаборатории. Так, при нагревании марганцовки выделяется кислород, а при нагревании мела — углекислый газ. Ученые при высокой температуре и давлении превращают графит в алмаз, но кристаллики искусственных алмазов очень мелкие и непригодны для изготовления ювелирных украшений. Получить же полудрагоценный камень малахит с помощью химических опытов не удается.
Неотъемлемым признаком вещества является масса. Световые лучи, магнитное поле не имеют массы и к веществам не относятся.
Вещество — это то, из чего состоит физическое тело.
Физическим телом называют все, что имеет массу и объем. Физическими телами являются, например, капля воды, кристаллик минерала, обломок стекла, кусочек пластмассы, зерно пшеницы, яблоко, орех, а также любой предмет, изготовленный человеком, — часы, игрушка, книга, ювелирное украшение и т. д.
► Назовите вещества, из которых состоят такие физические тела: льдина, гвоздь, карандаш.
Вещества, используемые для изготовления предметов, оборудования, а также в строительстве и других отраслях, называют материалами (рис. 22).
Первыми в истории человечества были природные материалы — древесина, камень, глина. Co временем люди научились выплавлять металлы и стекло, получать известь и цемент. В последние десятилетия на замену традиционным материалам приходят новые, в частности различные пластмассы.

Рис. 22. Строительные материалы
► Из каких материалов (пластмасса, стекло, металл, ткань, древесина) могут быть изготовлены ваза, ожерелье, тарелка?
Агрегатные состояния вещества.
Вещество может существовать в трех агрегатных состояниях — твердом, жидком и газообразном.
При нагревании твердые вещества плавятся, а жидкости закипают, превращаясь в пар. Понижение температуры приводит к обратным превращениям. Некоторые газы при высоком давлении сжижаются. При всех этих явлениях мельчайшие частицы вещества не разрушаются. Таким образом, вещество, изменяя агрегатное состояние, не превращается в другое.
Каждый знает о трех агрегатных состояниях воды, в которых она существует в природе: лед, вода, водяной пар. Ho не всякое вещество может быть твердым, жидким и газообразным. Для сахара известны два агрегатных состояния: твердое и жидкое. При нагревании сахар плавится, затем его расплав темнеет, и появляется неприятный запах. Это свидетельствует о превращении сахара в другие вещества. Значит, газообразного состояния для сахара не существует. А такое вещество как графит нельзя расплавить: при температуре 3500 0C он сразу превращается в пар.
Кристаллические и аморфные вещества.
Если рассматривать соль и сахар через увеличительное стекло, то можно заметить, что крупинки соли имеют форму кубиков, а сахара — другую форму, но тоже правильную, симметричную. Каждая такая крупинка является кристаллом. Кристалл — это природное физическое тело, имеющее плоские грани (поверхности) и прямые ребра (стыки граней). Следовательно, соль и сахар — кристаллические вещества. К таким веществам относятся лимонная кислота, глюкоза, алмаз, графит, металлы и др. (рис. 23). Во многих случаях кристаллы веществ настолько мелкие, что их можно увидеть только под микроскопом.
Стекло — не кристаллическое, а аморфное1 вещество. Если его измельчить, то получим бесформенные кусочки, не похожие друг на друга. Аморфными веществами являются также крахмал, мука, полиэтилен и др. (рис. 24).
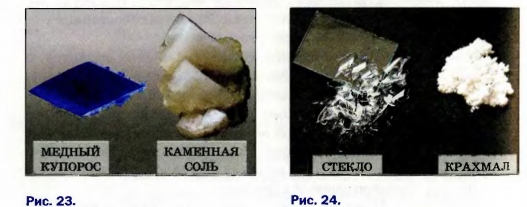
Рис. 23. Кристаллические вещества
Рис. 24. Аморфные вещества
Физические свойства веществ.
Все вещества чрезвычайно разнообразны; каждое обладает совокупностью определенных свойств.
Свойства вещества — это признаки, по которым вещество отличается от другого или подобно ему.
1 Термин происходит от греческих приставки а- и слова morphe — форма.
Железо легко отличить от древесины по цвету, особому блеску, а также на ощупь: металл всегда кажется более холодным, так как лучше проводит теплоту. Особенностью железа является то, что оно притягивается к магниту, а древесина — нет. В отличие от железа древесина в воде не тонет, поскольку ее плотность меньше плотности воды, а плотность железа — больше. Железо выдерживает высокую температуру, а древесина сначала темнеет, затем чернеет и загорается.
Свойства вещества, которые определяют наблюдением или измерением, без превращения его в другое вещество, называют физическими.
Важнейшие физические свойства вещества:
• агрегатное состояние при определенных температуре и давлении;
• цвет, блеск (или их отсутствие);
• запах (или его отсутствие);
• растворимость (или нерастворимость) в воде;
• температура плавления;
• температура кипения;
• плотность;
• теплопроводность;
• электропроводность (или неэлектропроводность).
Перечень физических свойств твердых веществ можно расширить, включив в него твердость, пластичность (или хрупкость), а для кристаллических — еще и форму кристаллов. Характеризуя жидкость, указывают, какая она — подвижная или маслянистая.
Такие физические свойства как цвет, запах, вкус, форма кристаллов можно определить визуально, с помощью органов чувств, а плотность, электропроводность, температуру плавления и кипения определяют измерением. Сведения о физических свойствах многих веществ собраны в специальной литературе, в частности — в справочниках.

Рис. 25. Нагревание иода
Физические свойства вещества зависят от его агрегатного состояния. Например, плотность льда, воды и водяного пара различна. Газообразный кислород бесцветный, а жидкий — голубой.
Знание физических свойств помогает «узнавать» немало веществ. Например, медь — единственный металл красного цвета. Соленый вкус имеет только поваренная соль. Иод — почти черное твердое вещество, которое при нагревании превращается в темно- фиолетовый пар (рис. 25). В большинстве случаев для определения вещества нужно при нимать во внимание несколько его свойств.
Лабораторный опыт№ 1Ознакомление с физическими свойствами веществ
Вам выдано три пробирки, в которых содержатся селитра1, графит и полиэтилен2. В вашем распоряжении есть стакан с водой (или промывалка) и стеклянные палочки.
Опишите вещества. Каков характер частиц каждого вещества (кристаллики, порошок, мелкие кусочки произвольной формы)? Выясните, растворяются ли вещества в воде, легче они или тяжелее ее.
Запишите физические свойства веществ в таблицу:

Какое свойство (свойства) позволяет отличить каждое вещество от двух других?
Назовите свойства, одинаковые для двух (трех) веществ.
Кроме физических свойств, каждое вещество имеет и химические свойства. О них пойдет речь позже.
1 Минеральное удобрение.
2 Учитель может заменить графит серой, медными или железными опилками, а полиэтилен — другим полимером.
Выводы
Вещество — то, из чего состоит физическое тело. Неотъемлемым признаком вещества является его масса.
Вещество может существовать в трех агрегатных состояниях: твердом, жидком и газообразном. Твердые вещества бывают кристаллическими и аморфными.
Свойства вещества — это признаки, по которым оно отличается от другого вещества или подобно ему.
Физические свойства вещества определяют наблюдением или измерением, без превращения его в другое вещество.
?
19. Что такое физическое тело, вещество, материал?
20. Найдите соответствие:
Вещество Физическое тело
1) золото; а) термометр;
2) ртуть; б) кольцо;
3) бумага; в) витрина;
4) стекло; г) тетрадь.
21.. Выберите среди приведенных слов и словосочетаний те, которые от носятся к веществам: стол, медь, лед, пластмассовая бутылка, спирт, газета, водяной пар, серебряная цепочка.
22. Какие из веществ являются строительными материалами: углекислый газ, железобетон, стекло, бумага, капрон, сталь?
23. Приведите примеры: а) нескольких предметов, сделанных из одного материала; б) предмета, сделанного из нескольких материалов; в) двух материалов, из которых изготовляют аналогичные предметы.
24. Опишите физические свойства мела.
25. Какие вещества, имеющиеся у вас дома, можно определить по за паху?
26. В сосудах без этикеток содержатся духи, растительное масло, поваренная соль, кусочки железа, мрамора. По каким свойствам можно определить каждое вещество?
27. Назовите несколько твердых веществ, которые вы легко можете отличить от остальных.
28. Приняв во внимание физические свойства веществ, объясните, почему отвертки и плоскогубцы имеют, как правило, пластмассовые ручки.
Экспериментируем дома
Свойства некоторых продуктов питания
Напишите на отдельных листочках бумаги названия веществ: мука, поваренная соль «Экстра», сахарная пудра, крахмал. Насыпьте на каждый листочек по несколько граммов соответствующего вещества.
Опишите внешний вид веществ.
Разотрите щепотку каждого вещества пальцами (определите, насколько мелкими являются его частички).
Попробуйте вещества на вкус (с веществами, имеющимися в химической лаборатории, это делать категорически запрещено).
Выясните, растворяются ли вещества в воде.
Запишите результаты исследований и наблюдений в таблицу, аналогичную представленной на с. 32.
Можно ли различить эти вещества? Если да, то как именно?
Попель П. П., Крикля Л. С., Хімія: Підруч. для 7 кл. загальноосвіт. навч. закл. — К.: ВЦ «Академія», 2008. — 136 с.: іл.
Содержание урока
![]() конспект урока и опорный каркас
конспект урока и опорный каркас
![]() презентация урока
презентация урока
![]() интерактивные технологии
интерактивные технологии
![]() акселеративные методы обучения
акселеративные методы обучения
Практика
![]() тесты, тестирование онлайн
тесты, тестирование онлайн
![]() задачи и упражнения
задачи и упражнения
![]() домашние задания
домашние задания
![]() практикумы и тренинги
практикумы и тренинги
![]() вопросы для дискуссий в классе
вопросы для дискуссий в классе
Иллюстрации
![]() видео- и аудиоматериалы
видео- и аудиоматериалы
![]() фотографии, картинки
фотографии, картинки
![]() графики, таблицы, схемы
графики, таблицы, схемы
![]() комиксы, притчи, поговорки, кроссворды, анекдоты, приколы, цитаты
комиксы, притчи, поговорки, кроссворды, анекдоты, приколы, цитаты
Дополнения
![]() рефераты
рефераты
![]() шпаргалки
шпаргалки
![]() фишки для любознательных
фишки для любознательных
![]() статьи (МАН)
статьи (МАН)
![]() литература основная и дополнительная
литература основная и дополнительная
![]() словарь терминов
словарь терминов
Совершенствование учебников и уроков
![]() исправление ошибок в учебнике
исправление ошибок в учебнике
![]() замена устаревших знаний новыми
замена устаревших знаний новыми
Только для учителей
![]() календарные планы
календарные планы
![]() учебные программы
учебные программы
![]() методические рекомендации
методические рекомендации
![]() обсуждения
обсуждения
![]() Идеальные уроки-кейсы
Идеальные уроки-кейсы
Если у вас есть исправления или предложения к данному уроку, напишите нам.
Если вы хотите увидеть другие корректировки и пожелания к урокам, смотрите здесь – Образовательный форум.
Авторські права | Privacy Policy |FAQ | Партнери | Контакти | Кейс-уроки
© Автор системы образования 7W и Гипермаркета Знаний – Владимир Спиваковский
При использовании материалов ресурса
ссылка на edufuture.biz обязательна (для интернет ресурсов –
гиперссылка).
edufuture.biz 2008-© Все права защищены.
Сайт edufuture.biz является порталом, в котором не предусмотрены темы политики, наркомании, алкоголизма, курения и других “взрослых” тем.
Разработка – Гипермаркет знаний 2008-
Ждем Ваши замечания и предложения на email: 
По вопросам рекламы и спонсорства пишите на email: 
Источник
